Содержание
- 2. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий, утвержденные решением Совета Евразийской экономической комиссии
- 3. Соглашение о единых принципах и правилах обращения медицинских изделий в рамках Евразийского экономического союза от 23.12.2014
- 4. ПРАВИЛА проведения мониторинга безопасности, качества и эффективности медицинских изделий, утвержденные решением Коллегии Евразийской экономической комиссии от
- 5. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 3: "безопасность медицинских изделий" -
- 6. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 5: До подачи в уполномоченный
- 7. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 18: Уполномоченным органом (экспертной организацией)
- 8. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий, пункт 18 Экспертная организация уведомляет заявителя
- 9. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 20: Ответственность за достоверность предоставленного
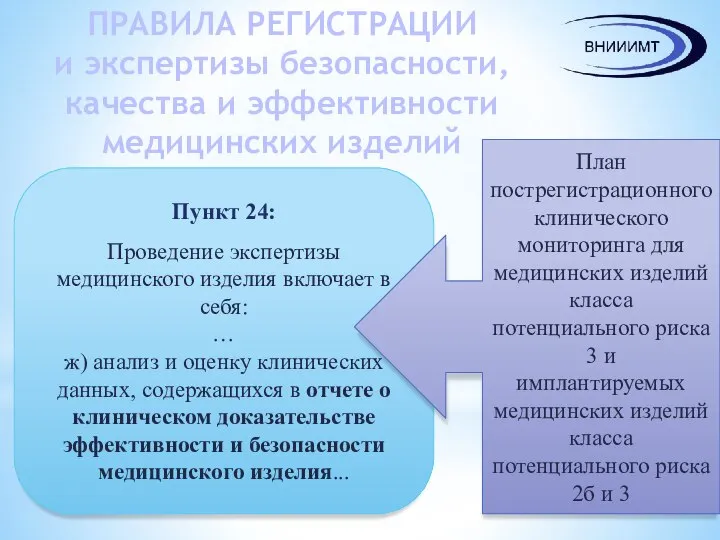
- 10. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 24: Проведение экспертизы медицинского изделия
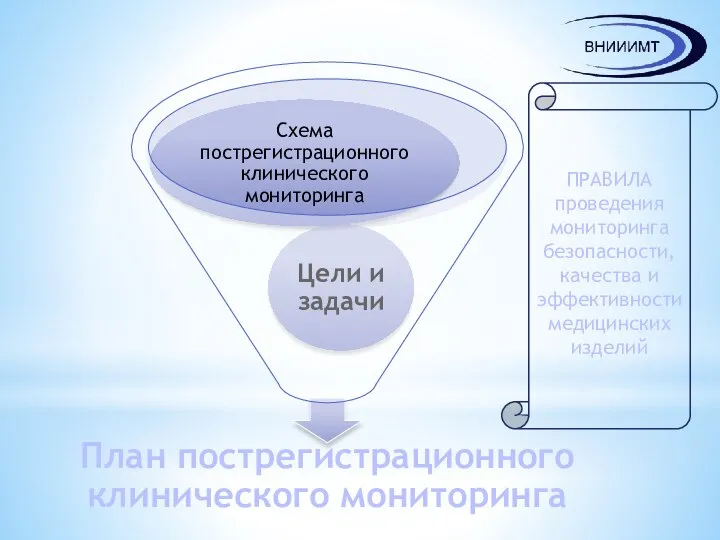
- 11. ПРАВИЛА проведения мониторинга безопасности, качества и эффективности медицинских изделий
- 12. Цели и задачи пострегистрационного клинического мониторинга Имеющиеся клинические данные Специфические особенности, связанные с медицинским изделием Факторы
- 13. Схема плана пострегистрационного клинического мониторинга Методы (способ) получения клинических данных и их обоснование Методы (способы) статистического
- 14. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 24: Проведение экспертизы медицинского изделия
- 15. Требованиями к внедрению, поддержанию и оценке системы менеджмента качества медицинских изделий в зависимости от потенциального риска
- 16. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 24: Проведение экспертизы медицинского изделия
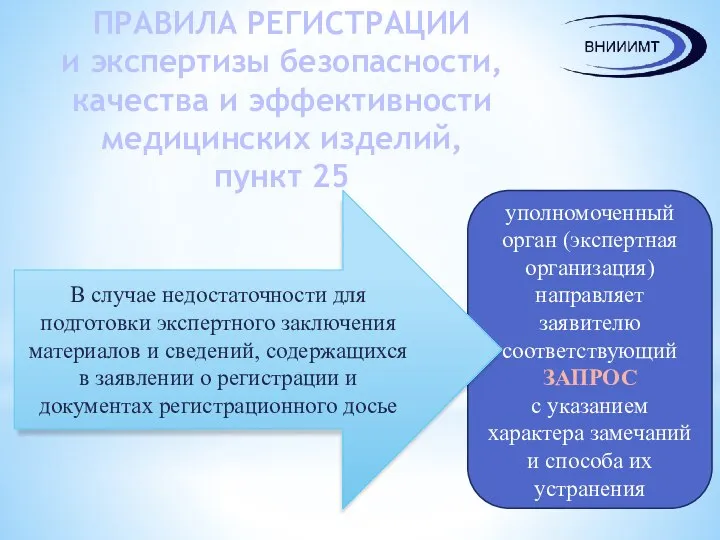
- 17. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий, пункт 25 уполномоченный орган (экспертная организация)
- 18. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 27: Основаниями для вынесения уполномоченным
- 19. План пострегистра-ционного клинического мониторинга Сообщения о НС и ответные корректиру-ющие действия План сбора и анализа данных
- 20. ПРАВИЛА РЕГИСТРАЦИИ и экспертизы безопасности, качества и эффективности медицинских изделий Пункт 17: Заявитель представляет в уполномоченный
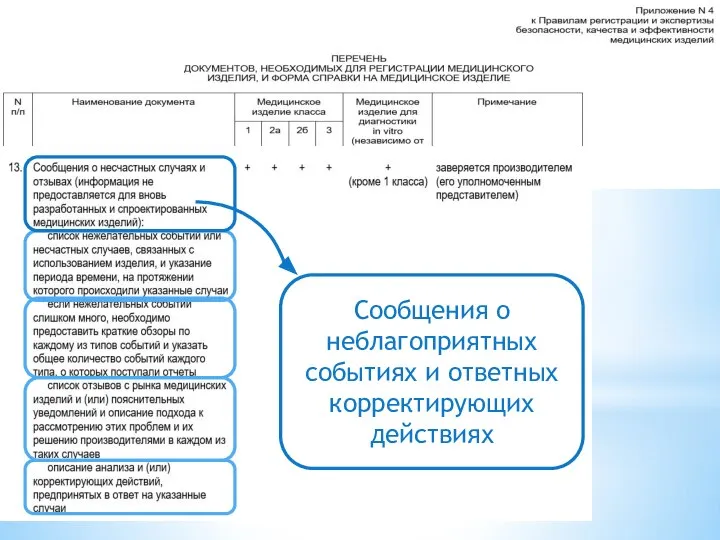
- 21. Сообщения о неблагоприятных событиях и ответных корректирующих действиях
- 22. План постегистрационного клинического мониторинга для медицинских изделий класса потенциального риска 3 и имплантируемых медицинских изделий класса
- 23. План отслеживании и выявлении побочных действий медицинских изделий в процессе их эксплуатации
- 24. «Особые» медицинские изделия Комплекты, наборы МИ, в состав которых входят уже зарегистрированные МИ (аптечка, набор инструментов,
- 25. Источники информации о неблагоприятных событиях ? FDA, США MHRA, Великобритания Health Canada, Канада Swiss medic, Швейцария
- 26. Источники информации о неблагоприятных событиях
- 28. Скачать презентацию





















 Официальный Сайт О.С. Сухарева Подготовила : Сушкова Н.
Официальный Сайт О.С. Сухарева Подготовила : Сушкова Н. Понятие уголовного права, предмет, метод, система и задача Григоров Георгий Т095
Понятие уголовного права, предмет, метод, система и задача Григоров Георгий Т095 Разработка и реализация программ спортивной подготовки на основе федеральных стандартов спортивной подготовки по видам спорта
Разработка и реализация программ спортивной подготовки на основе федеральных стандартов спортивной подготовки по видам спорта Анализ международной деятельности компании Apple
Анализ международной деятельности компании Apple Функциональные элементы САР ЭПС: исполнительные и управляющие элементы
Функциональные элементы САР ЭПС: исполнительные и управляющие элементы Политические партии и движения, их классификация
Политические партии и движения, их классификация День Матери в разных странах мира
День Матери в разных странах мира Создание 3D модели втулки нажимной
Создание 3D модели втулки нажимной Лентивирусы
Лентивирусы C# перечисления
C# перечисления Своеобразие архитектурных традиций Особенности храмового зодчества
Своеобразие архитектурных традиций Особенности храмового зодчества Городские сети водопровода запитаны от трех водоисточников
Городские сети водопровода запитаны от трех водоисточников «Тайный покупатель» (пример реализованного проекта)
«Тайный покупатель» (пример реализованного проекта) История физики 3
История физики 3 Крошка Енот и тот кто сидит в пруду - презентация для начальной школы
Крошка Енот и тот кто сидит в пруду - презентация для начальной школы Природа света
Природа света Солнечные опреснительные установки
Солнечные опреснительные установки  Системы диспетчерского управления движением поездов
Системы диспетчерского управления движением поездов Презентация "Что мы узнали о деньгах" - скачать презентации по Экономике
Презентация "Что мы узнали о деньгах" - скачать презентации по Экономике ПРОЛОЛ
ПРОЛОЛ Монголия
Монголия  Технология создания учебно-методического пособия
Технология создания учебно-методического пособия Участие прокурора в рассмотрении дел судами. Лекция № 6:
Участие прокурора в рассмотрении дел судами. Лекция № 6: Стандартизация
Стандартизация  ЛАБОРАТОРНАЯ РАБОТА ОБУЧЕНИЕ ПЕРСОНАЛА
ЛАБОРАТОРНАЯ РАБОТА ОБУЧЕНИЕ ПЕРСОНАЛА Презентация на тему "Современные модели организации обучения" - скачать презентации по Педагогике
Презентация на тему "Современные модели организации обучения" - скачать презентации по Педагогике буддизм
буддизм Fun And Interesting Sports Facts
Fun And Interesting Sports Facts