Содержание
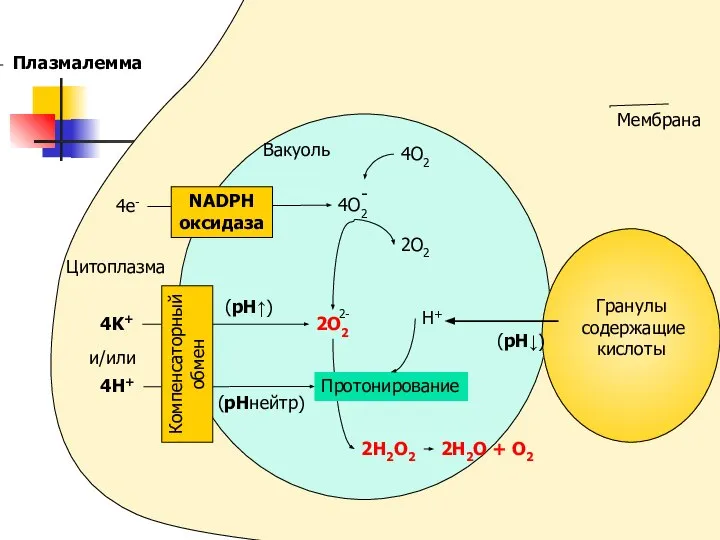
- 2. 4O2 2O2 H+ 2H2O2 2H2O + O2 (pH↓) Цитоплазма 4e- Вакуоль 4K+ и/или 4H+ (pHнейтр) (pH↑)
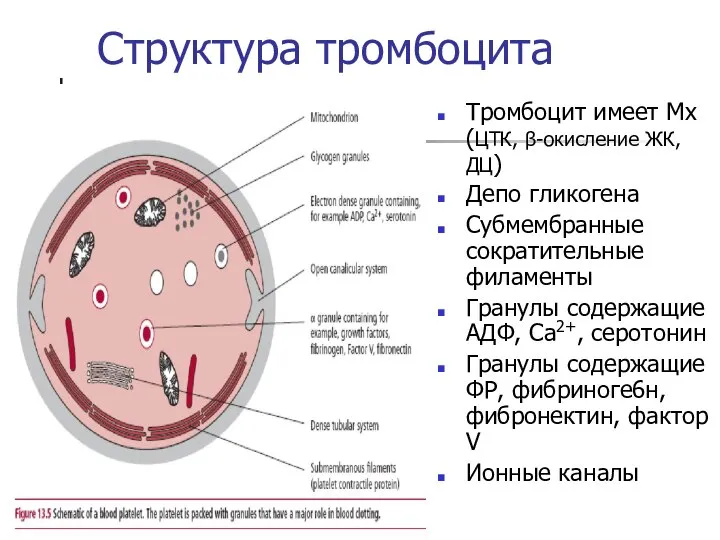
- 3. Структура тромбоцита Тромбоцит имеет Мх (ЦТК, β-окисление ЖК, ДЦ) Депо гликогена Субмембранные сократительные филаменты Гранулы содержащие
- 4. Новые научные данные о метаболизме железа Лойко О. В., Котова И. А. Студентки гр. Л-205 Гомельский
- 5. * Введение Fe играет важную роль в метаболизме, т.к. оно может легко отдавать е- (Hb, Mb,
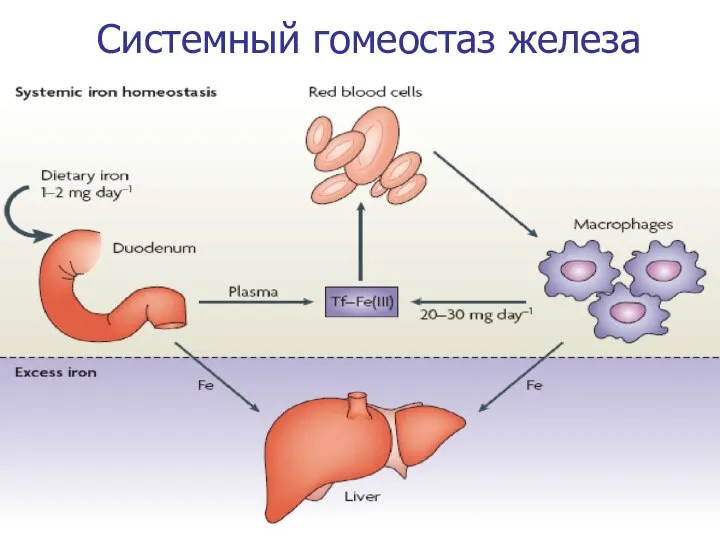
- 6. * Системный гомеостаз железа
- 7. * Всасывание Fe в в 12-п и в верхней части тощей кишки 1.Транспорт Fe через апикальную
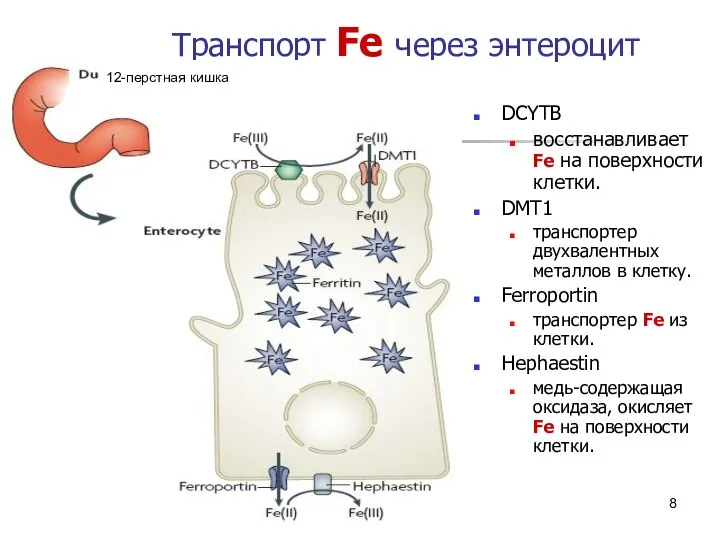
- 8. * Транспорт Fe через энтероцит DCYTB восстанавливает Fe на поверхности клетки. DMT1 транспортер двухвалентных металлов в
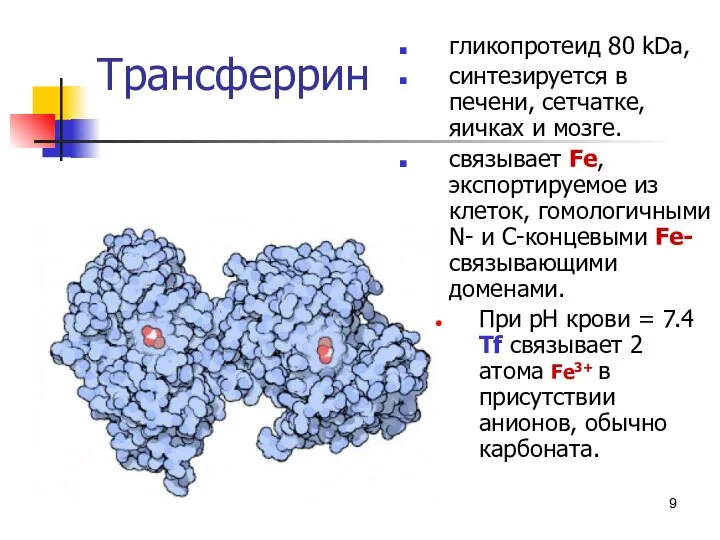
- 9. * Трансферрин гликопротеид 80 kDa, синтезируется в печени, сетчатке, яичках и мозге. связывает Fe, экспортируемое из
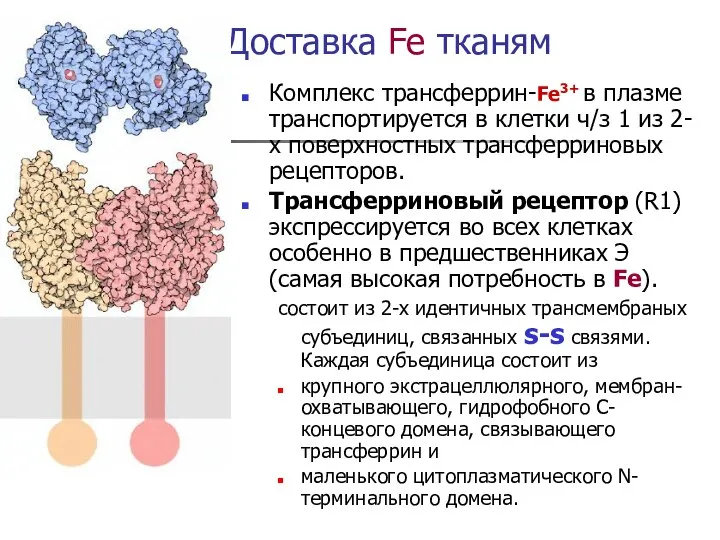
- 10. Доставка Fe тканям Комплекс трансферрин-Fe3+ в плазме транспортируется в клетки ч/з 1 из 2-х поверхностных трансферриновых
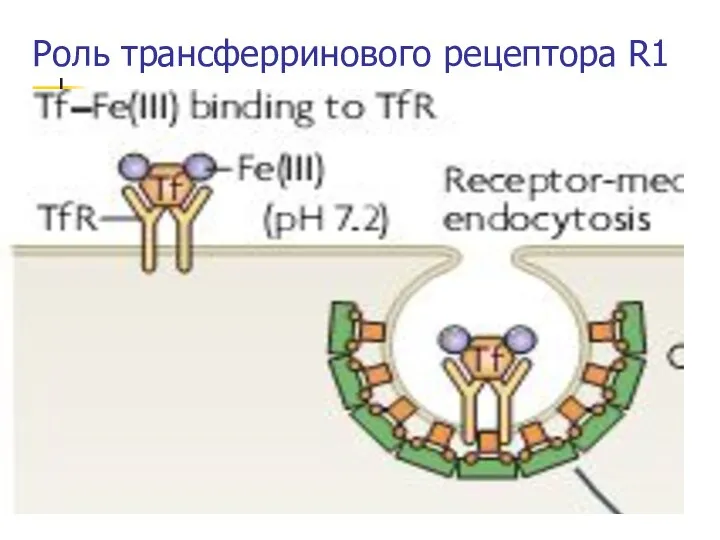
- 11. * Роль трансферринового рецептора R1
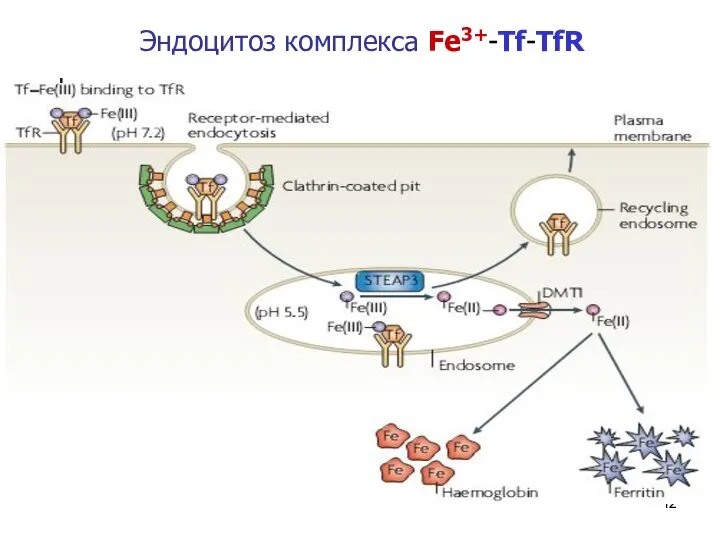
- 12. * Эндоцитоз комплекса Fe3+-Tf-TfR
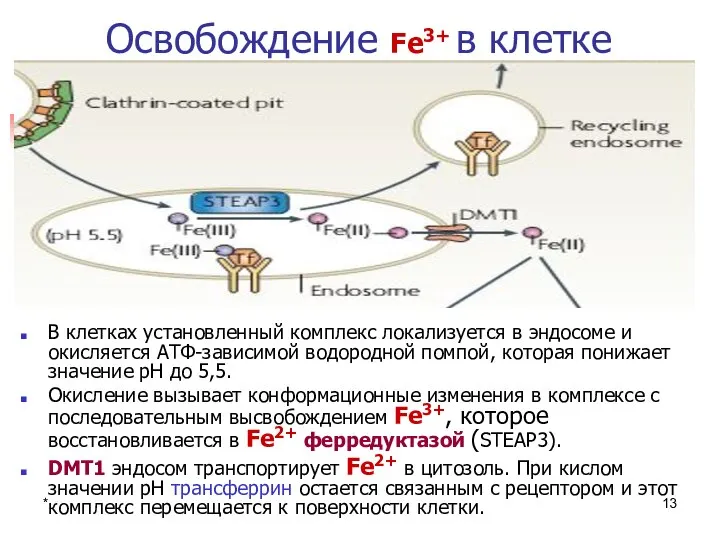
- 13. * Освобождение Fe3+ в клетке В клетках установленный комплекс локализуется в эндосоме и окисляется АТФ-зависимой водородной
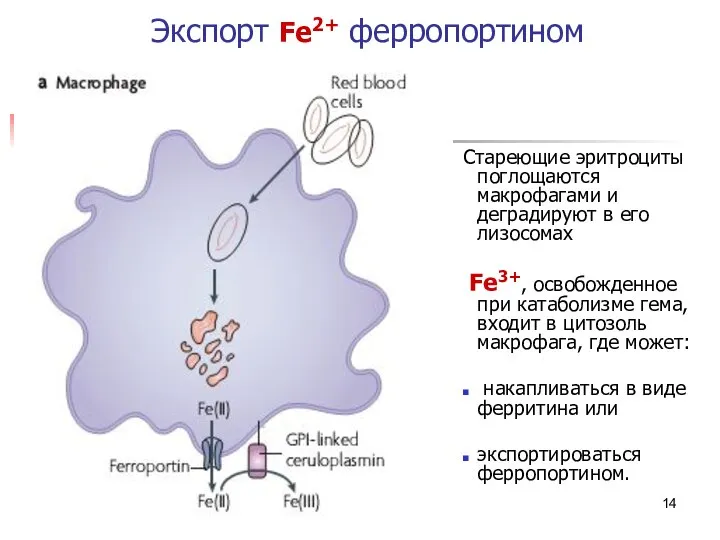
- 14. * Экспорт Fe2+ ферропортином Стареющие эритроциты поглощаются макрофагами и деградируют в его лизосомах Fe3+, освобожденное при
- 15. Накопление Fe3+ Клеточное накапливается Fe3+ в виде ферритина. Ферритин – полимер, состоящий из 24 субъединиц, включает
- 16. * Регуляция клеточного гомеостаза Fe Существует 2 механизма регуляции поступления и накопления Fe : Транскрипционый –
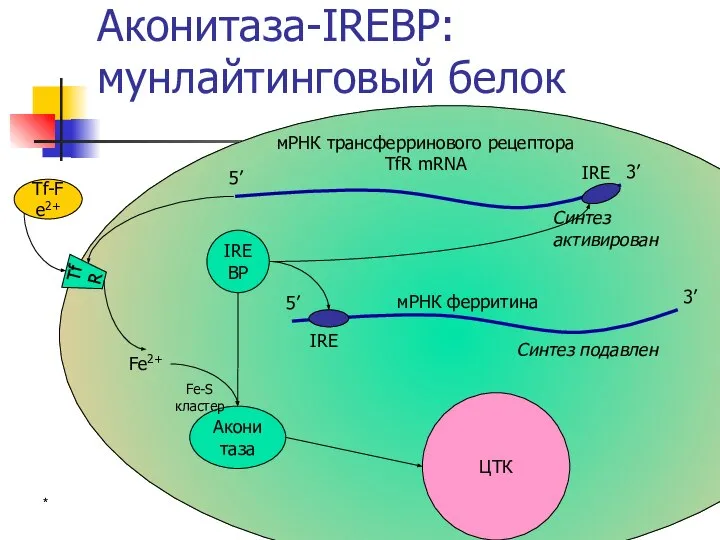
- 17. * Аконитаза-IREBP: мунлайтинговый белок IREBP Аконитаза 5’ 3’ мРНК трансферринового рецептора TfR mRNA IRE TfR Tf-Fe2+
- 18. * Молекулярная регуляция системного метаболизма Fe Поступление железа регулируется в зависимости от потребности в нем организма.
- 19. * Гепцидин - негативный регулятор транспорта Fe Гепцидин - пептидный гормон, член семейства дефензинов, регулирует поступление
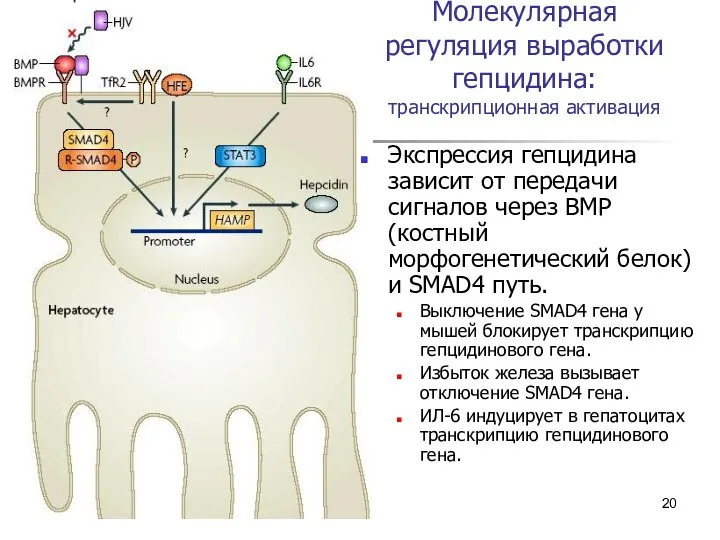
- 20. * Молекулярная регуляция выработки гепцидина: транскрипционная активация Экспрессия гепцидина зависит от передачи сигналов через ВМР (костный
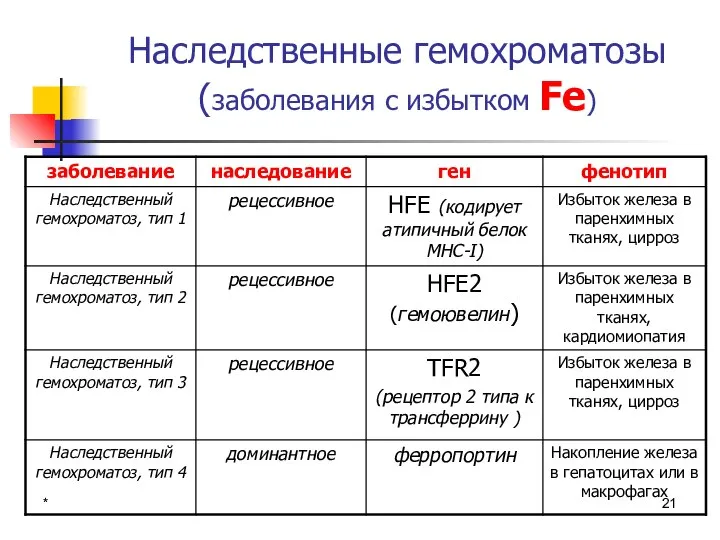
- 21. * Наследственные гемохроматозы (заболевания с избытком Fe)
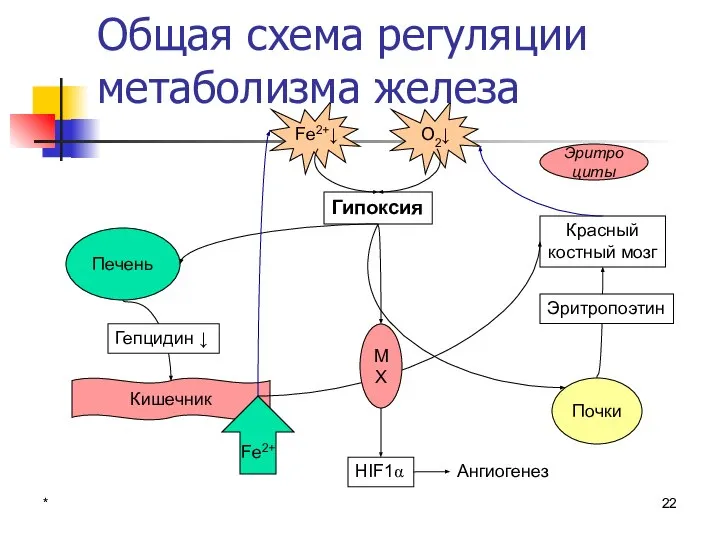
- 22. * Общая схема регуляции метаболизма железа Гипоксия Почки Печень Красный костный мозг Кишечник O2↓ Fe2+↓ Fe2+
- 23. * Заключение Поступление железа – строго регулируемый процесс. Связано с его важными функциями: Входит в состав
- 25. Скачать презентацию








 Презентация Понятие и признаки найма жилого помещения
Презентация Понятие и признаки найма жилого помещения Игровой ПК. Сборка до 90000 рублей. Магазин OLDI.RU
Игровой ПК. Сборка до 90000 рублей. Магазин OLDI.RU Жизнь, неподвластная смерти
Жизнь, неподвластная смерти Қасым Аманжолов — (1911-1955)
Қасым Аманжолов — (1911-1955) Оплата труда. Охрана труда
Оплата труда. Охрана труда Ортомиксовирусы
Ортомиксовирусы Крепежные изделия
Крепежные изделия Международный терроризм
Международный терроризм Разрез здания
Разрез здания Мәдениет және өркениет
Мәдениет және өркениет Картинный ДИКТАНТ.
Картинный ДИКТАНТ.  ПРИРОДА ПОЛИТИЧЕСКОГО ЛИДЕРСТВА. КЛАССИФИКАЦИЯ ЛИДЕРСТВА НА ОСНОВЕ ТИПОЛОГИИ М.ВЕБЕРА. Подготовила: Приходько Ю. Т082
ПРИРОДА ПОЛИТИЧЕСКОГО ЛИДЕРСТВА. КЛАССИФИКАЦИЯ ЛИДЕРСТВА НА ОСНОВЕ ТИПОЛОГИИ М.ВЕБЕРА. Подготовила: Приходько Ю. Т082 Олімпійський тиждень
Олімпійський тиждень Цифровая схемотехника. КМОП логика
Цифровая схемотехника. КМОП логика Сопровождение онлайн: как удержать новичка и поддерживать его активность. Система, инструменты, фишки
Сопровождение онлайн: как удержать новичка и поддерживать его активность. Система, инструменты, фишки Стратегия и стратегическое планирование в НКО
Стратегия и стратегическое планирование в НКО Автомобиль йўлларини эксплуатация қилишда ҳаракат хавфсизлигини таъминлаш
Автомобиль йўлларини эксплуатация қилишда ҳаракат хавфсизлигини таъминлаш Культы и религии
Культы и религии Наплавляемая кровля
Наплавляемая кровля Внутренняя и внешняя память компьютера
Внутренняя и внешняя память компьютера Презентация на тему "Туберкулез -Чума ХХІ века" - скачать презентации по Медицине
Презентация на тему "Туберкулез -Чума ХХІ века" - скачать презентации по Медицине Арка Главного штаба. Александровская колонна.
Арка Главного штаба. Александровская колонна.  Практические вопросы построения МП систем
Практические вопросы построения МП систем Синтаксис оператора
Синтаксис оператора Всеукраїнська партiя духовностi i патрiотизму
Всеукраїнська партiя духовностi i патрiотизму Кустодиев Борис Михайлович (1878-1927) Советский живописец, график, театральный художник
Кустодиев Борис Михайлович (1878-1927) Советский живописец, график, театральный художник Инкапсуляция в C++
Инкапсуляция в C++ Костюм Древней Греции
Костюм Древней Греции