Содержание
- 2. Лекция 1
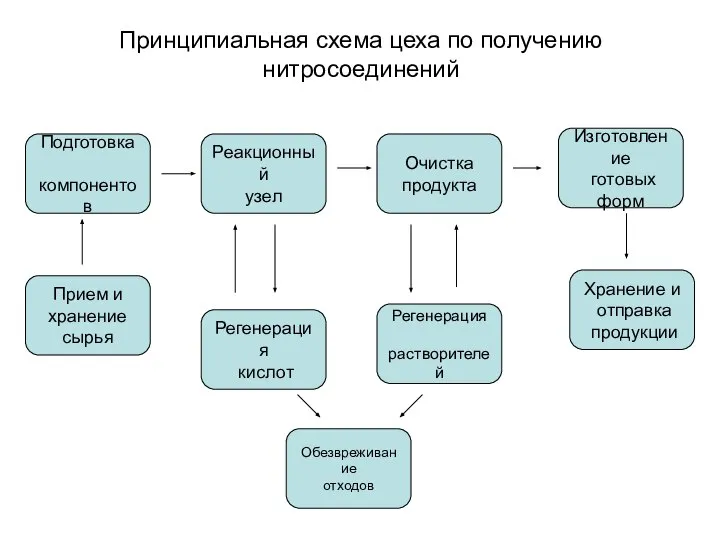
- 3. Принципиальная схема цеха по получению нитросоединений Прием и хранение сырья Подготовка компонентов Реакционный узел Очистка продукта
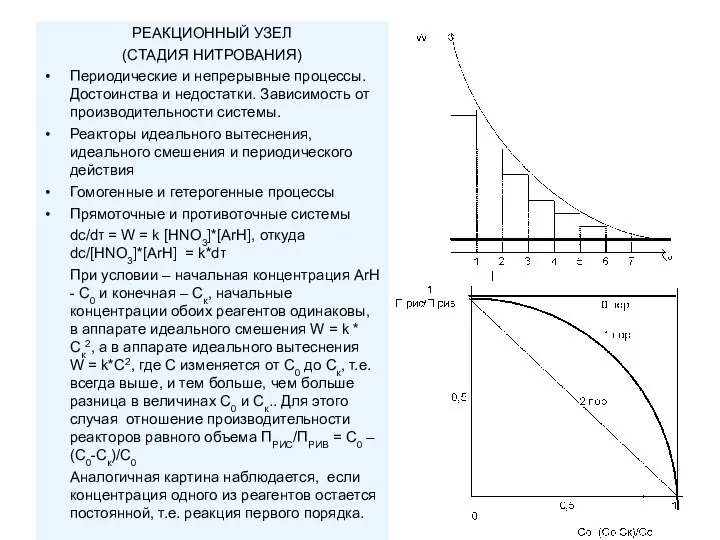
- 4. РЕАКЦИОННЫЙ УЗЕЛ (СТАДИЯ НИТРОВАНИЯ) Периодические и непрерывные процессы. Достоинства и недостатки. Зависимость от производительности системы. Реакторы
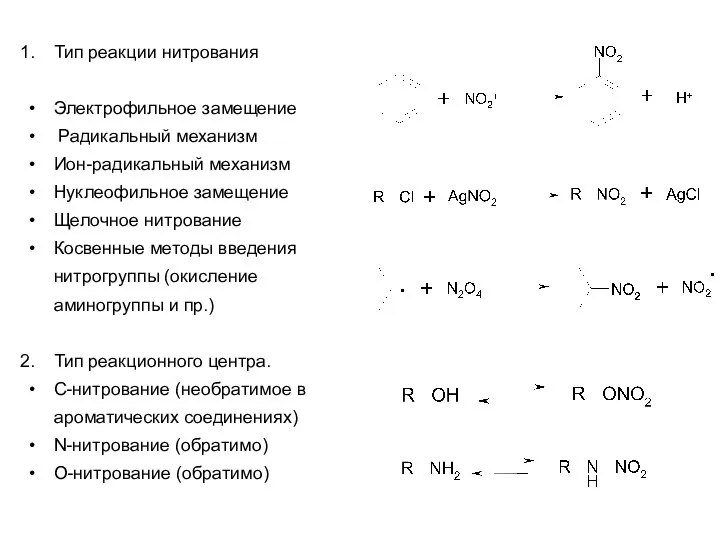
- 5. Тип реакции нитрования Электрофильное замещение Радикальный механизм Ион-радикальный механизм Нуклеофильное замещение Щелочное нитрование Косвенные методы введения
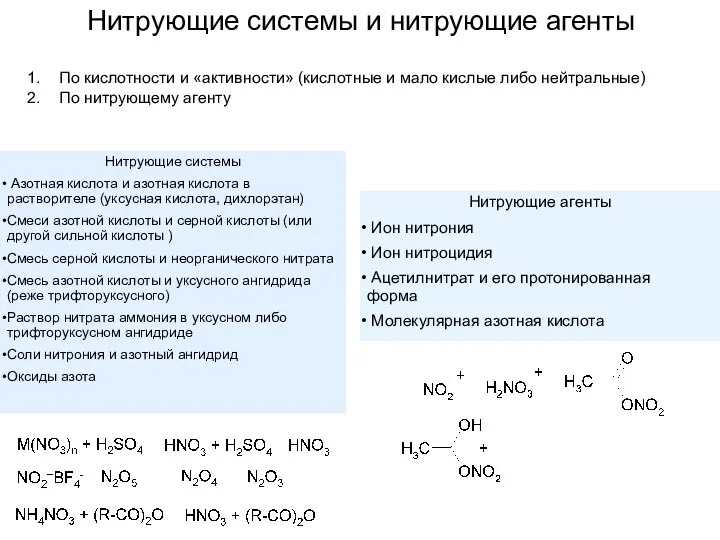
- 6. Нитрующие системы и нитрующие агенты По кислотности и «активности» (кислотные и мало кислые либо нейтральные) По
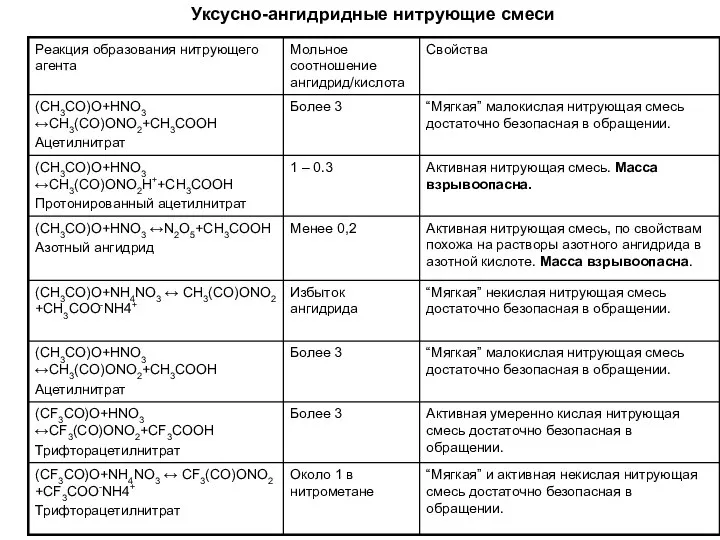
- 7. Уксусно-ангидридные нитрующие смеси
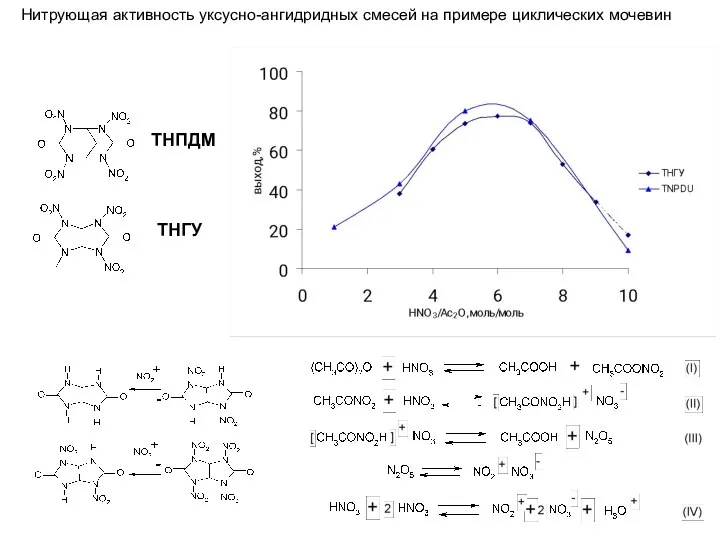
- 8. ТНПДМ ТНГУ Нитрующая активность уксусно-ангидридных смесей на примере циклических мочевин
- 9. Нитрующие смеси на кислотной основе
- 10. Механизм нитрования Механизм реакции – совокупность элементарных процессов Методы изучения: изучение кинетики процессов, физико-химическине (спектральные) и
- 11. В настоящее время общепринятым является механизм электофильного нитрования с участием иона нитрония NO2+ (А.И. Титов, К.
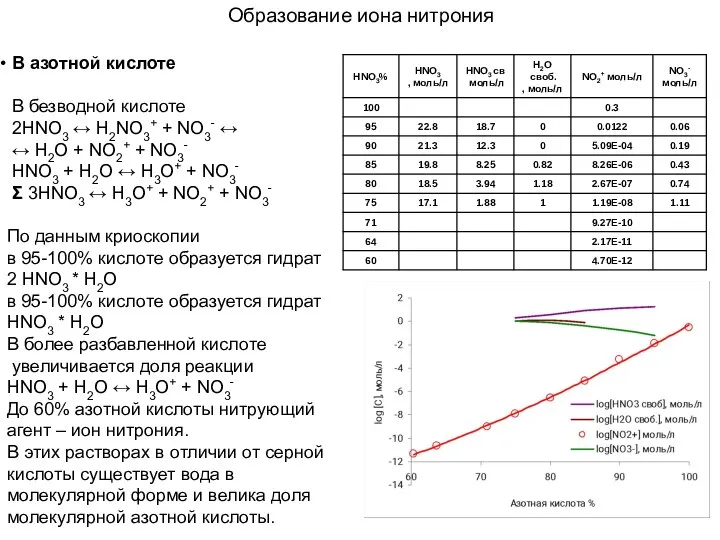
- 12. Образование иона нитрония В азотной кислоте В безводной кислоте 2HNO3 ↔ H2NO3+ + NO3- ↔ ↔
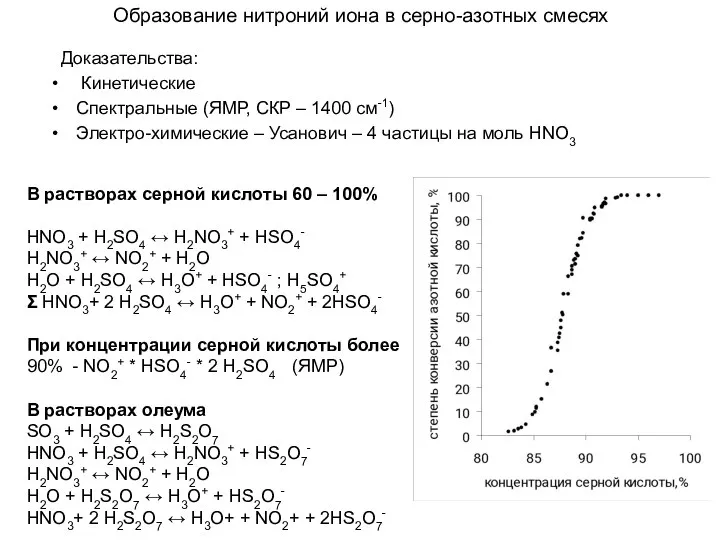
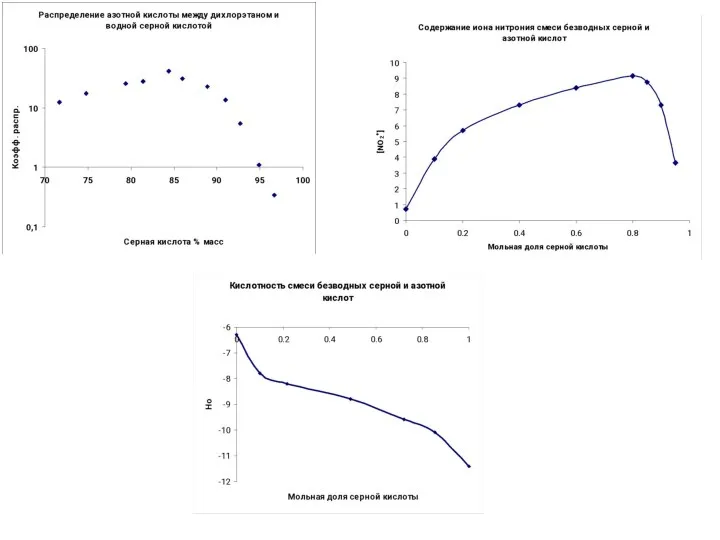
- 13. Образование нитроний иона в серно-азотных смесях Доказательства: Кинетические Спектральные (ЯМР, СКР – 1400 см-1) Электро-химические –
- 14. Лекция 2
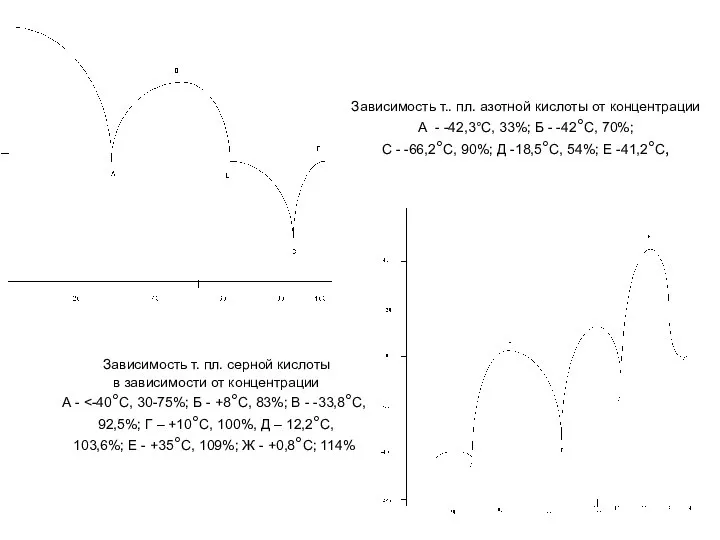
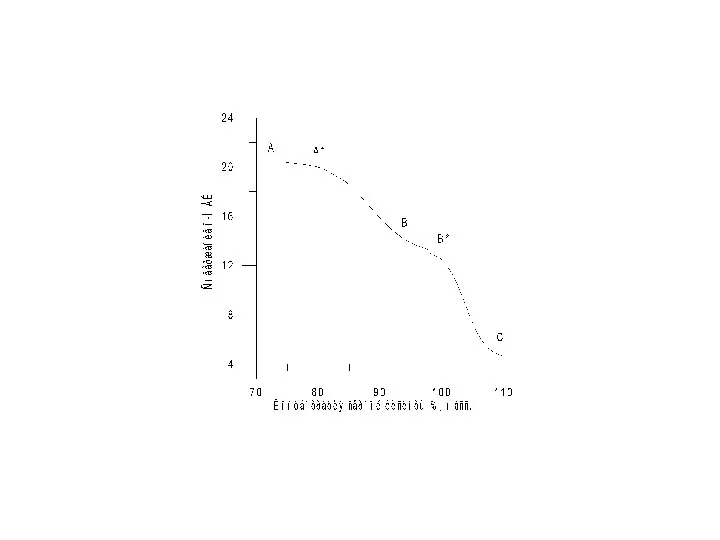
- 15. Зависимость т.. пл. азотной кислоты от концентрации А - -42,3°С, 33%; Б - -42°С, 70%; С
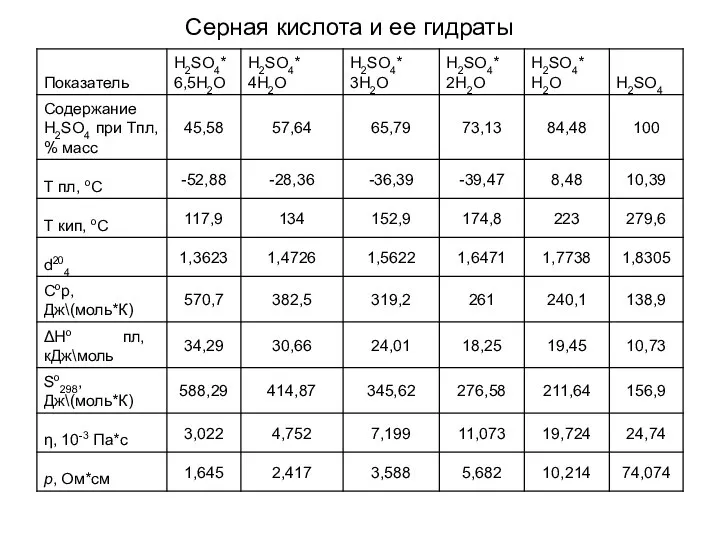
- 16. Серная кислота и ее гидраты
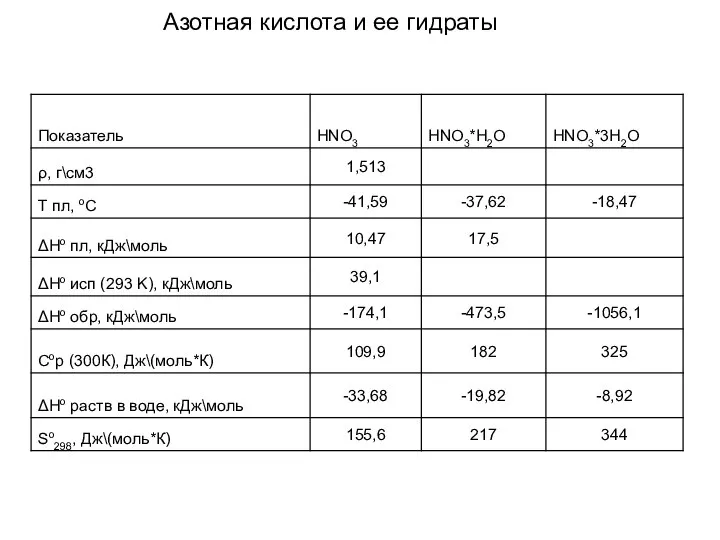
- 17. Азотная кислота и ее гидраты
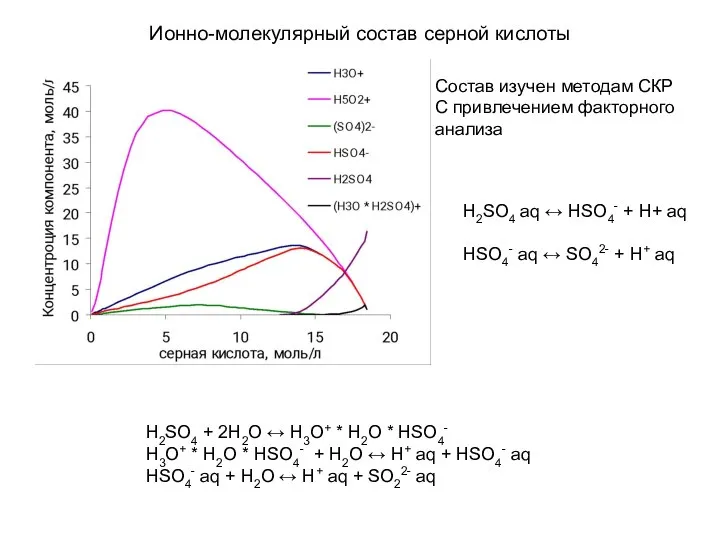
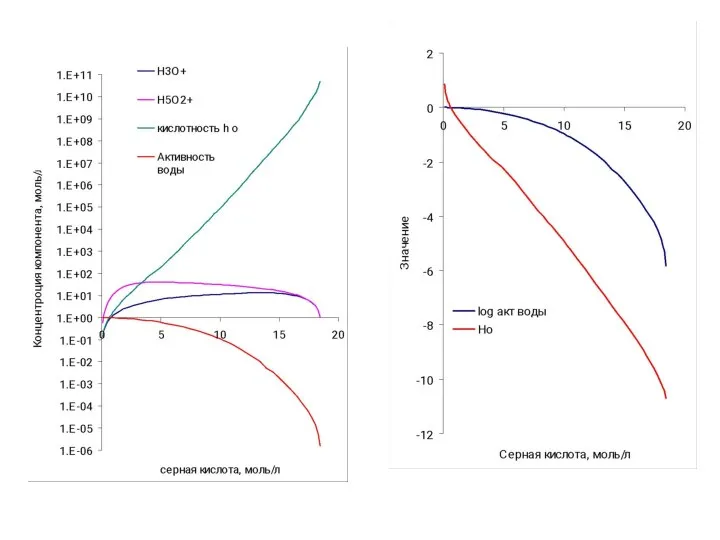
- 18. Ионно-молекулярный состав серной кислоты H2SO4 + 2H2O ↔ H3O+ * H2O * HSO4- H3O+ * H2O
- 19. Функции кислотности Теория Бренстеда – Лоури. Согласно теории Бренстеда – Лоури кислота рассматривается как вещество, поставляющее
- 20. Физический смысл и меры основности в газовой фазе Основностью в газовой фазе называют свободную энергию (
- 21. Протонирование слабых органических оснований в водных растворах кислот. Протонирование многих слабых органических оснований происходит в достаточно
- 22. В зависимости от концентрации минеральной кислоты, характер специфической сольватации непрерывно меняется. Избыточные протоны, имеющиеся в водных
- 23. Гаммет и Дейруп: серия органических соединений, обладающие максимально сходной молекулярной структурой, так называемых кислотно-основных индикаторов. Протонирование
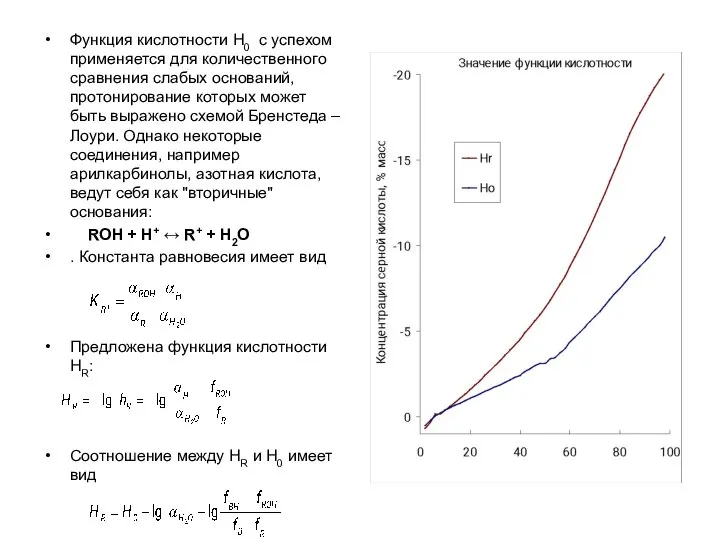
- 25. Функция кислотности Н0 с успехом применяется для количественного сравнения слабых оснований, протонирование которых может быть выражено
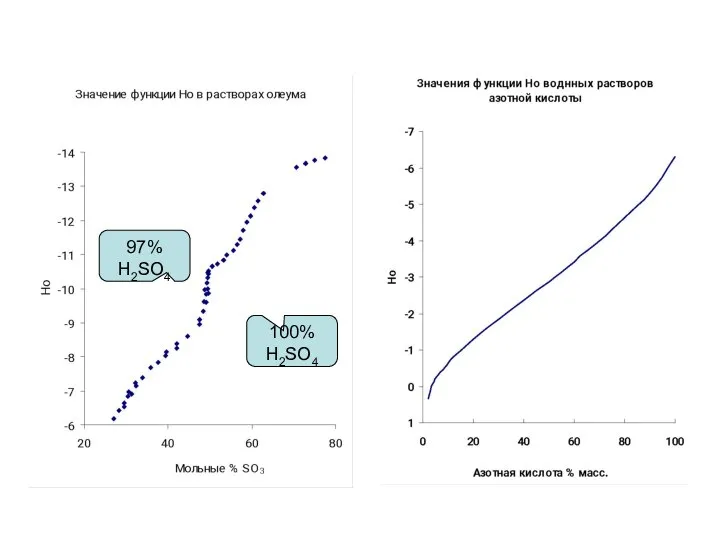
- 26. 100% H2SO4 97% H2SO4
- 27. Кроме функций Нo и Hr существуют функции построенные на других рядах индикаторов: амидах (Ha), индолах и
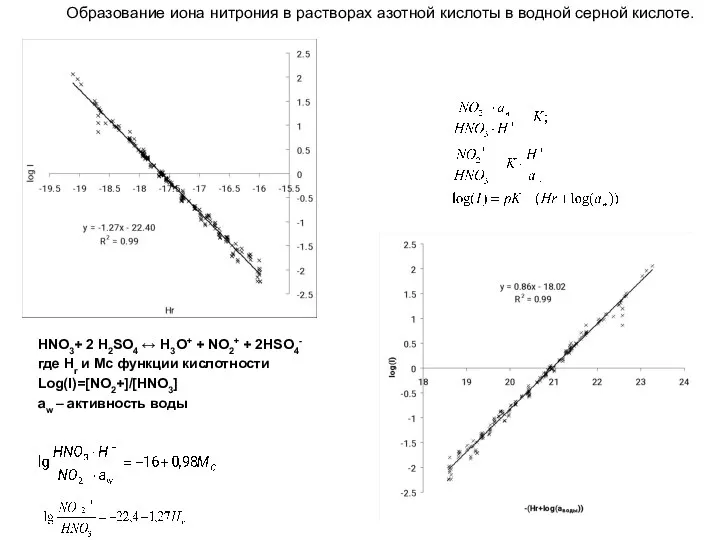
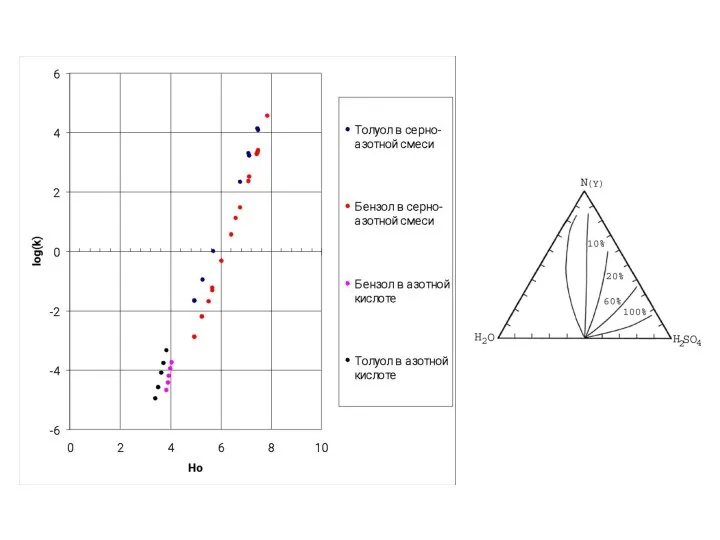
- 28. HNO3+ 2 Н2SO4 ↔ H3O+ + NO2+ + 2HSO4- где Hr и Mc функции кислотности Log(I)=[NO2+]/[HNO3]
- 30. Лекция 3
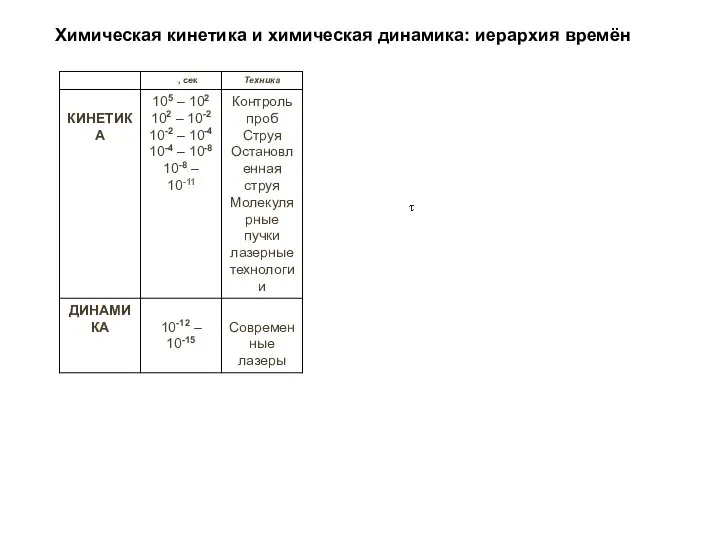
- 32. Химическая кинетика и химическая динамика: иерархия времён
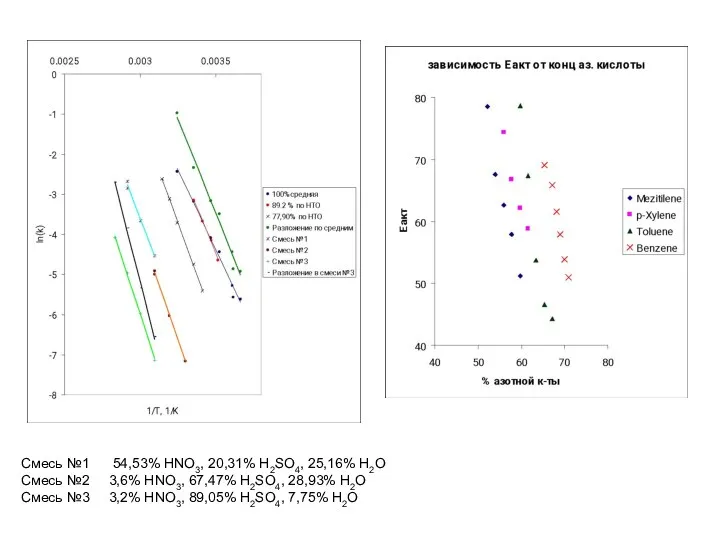
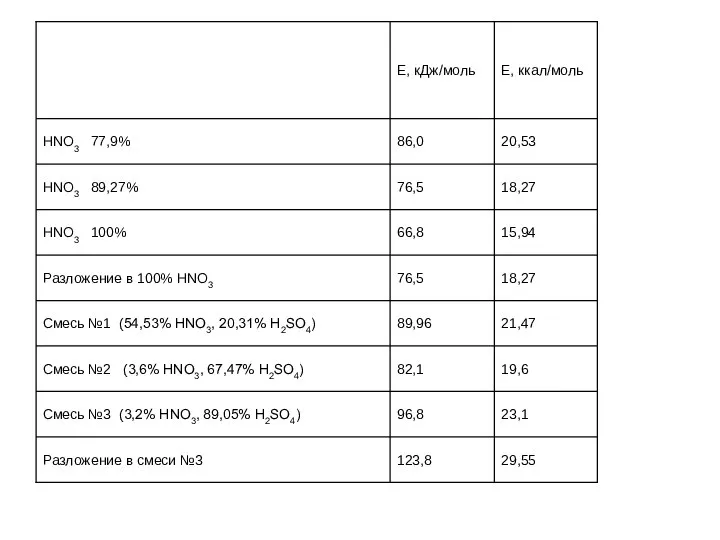
- 33. Смесь №1 54,53% HNO3, 20,31% H2SO4, 25,16% H2O Смесь №2 3,6% HNO3, 67,47% H2SO4, 28,93% H2O
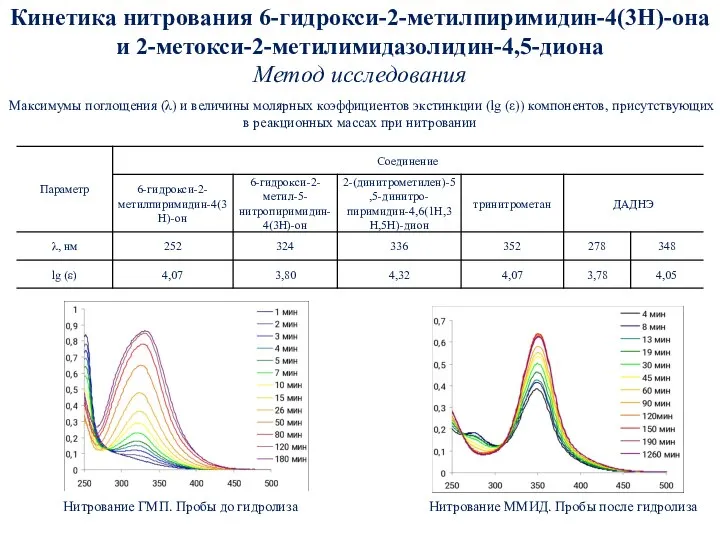
- 35. Кинетика нитрования 6-гидрокси-2-метилпиримидин-4(3Н)-она и 2-метокси-2-метилимидазолидин-4,5-диона Метод исследования Нитрование ГМП. Пробы до гидролиза Нитрование ММИД. Пробы после
- 36. Пример кинетической кривой нитрования в серно-азотной нитрующей смеси, содержащей 73,5% серную кислоту, при 60оС.
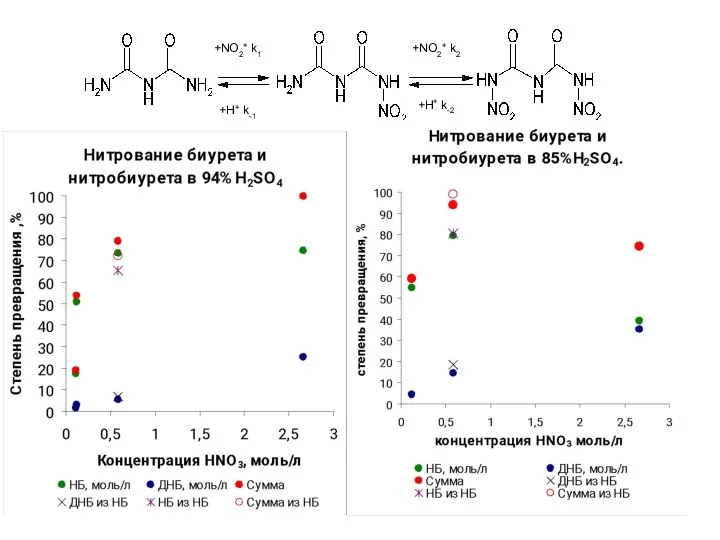
- 37. +NO2+ k1 +H+ k-1 +NO2+ k2 +H+ k-2
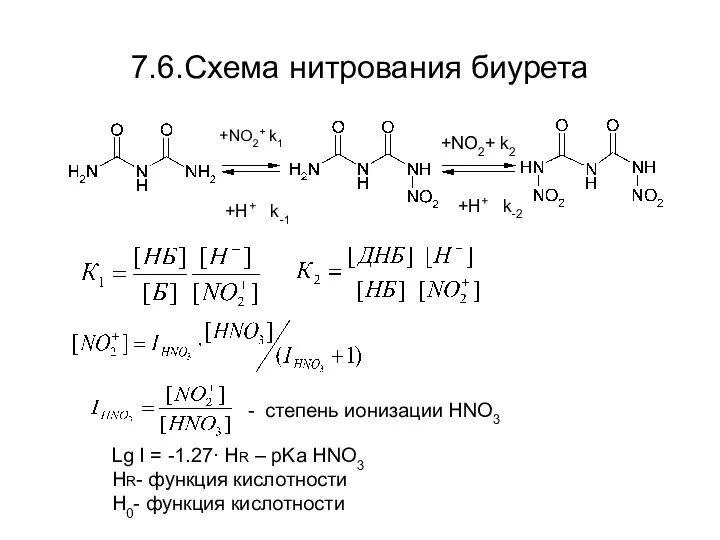
- 38. 7.6.Схема нитрования биурета +NO2+ k1 +H+ k-1 +NO2+ k2 +H+ k-2 - степень ионизации HNO3 Lg
- 39. Примеры обработки кинетических данных по уравнению для последовательных реакций 80 % 85 % 93 % 20
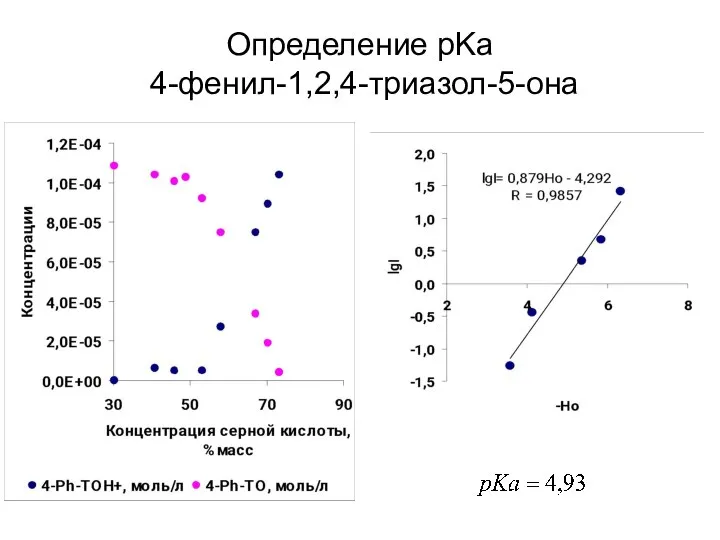
- 42. Определение pKa 4-фенил-1,2,4-триазол-5-она
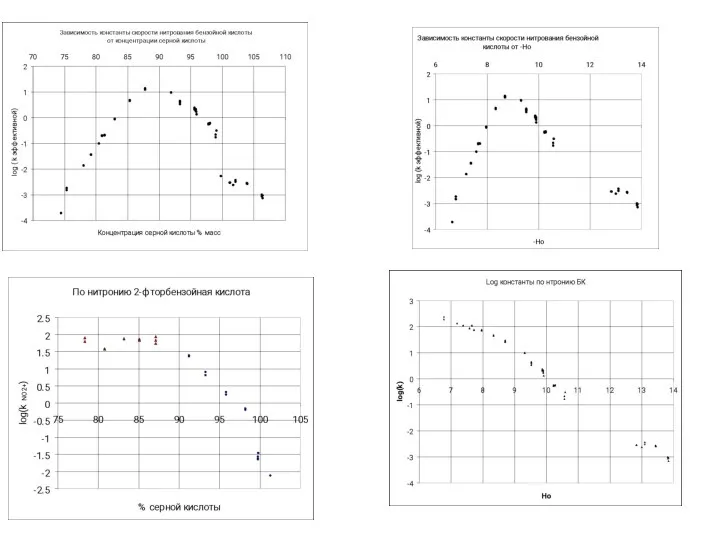
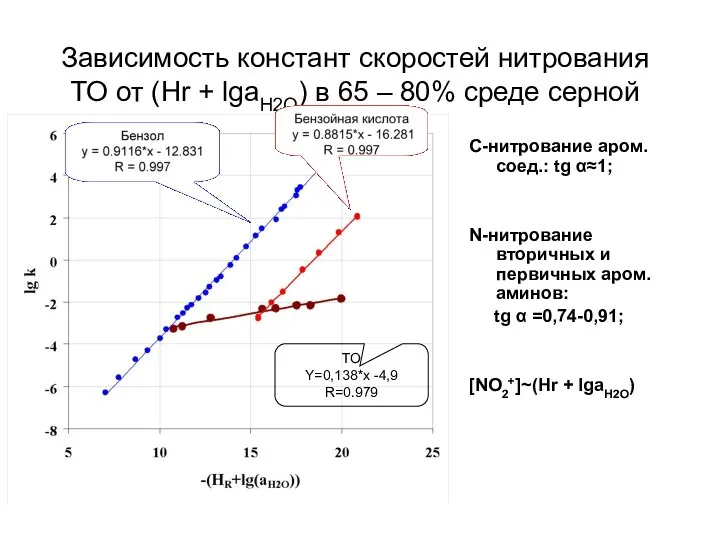
- 43. Зависимость констант скоростей нитрования ТО от (Hr + lgaH2O) в 65 – 80% среде серной кислоты.
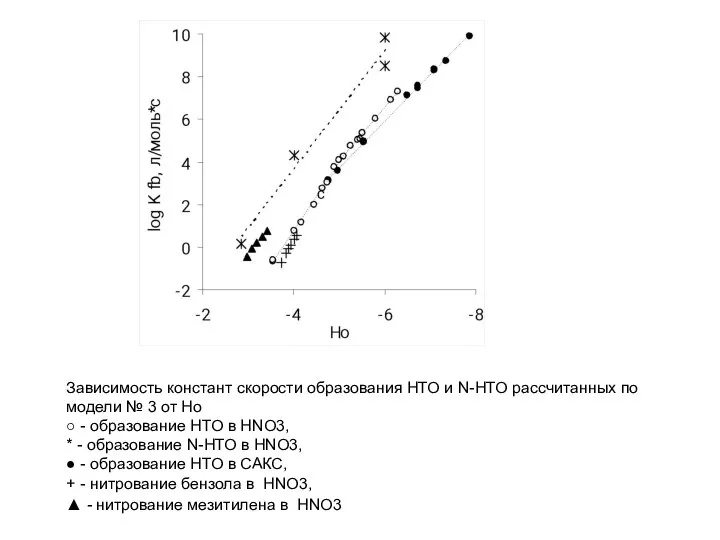
- 44. Зависимость констант скорости образования НТО и N-НТО рассчитанных по модели № 3 от Но ○ -
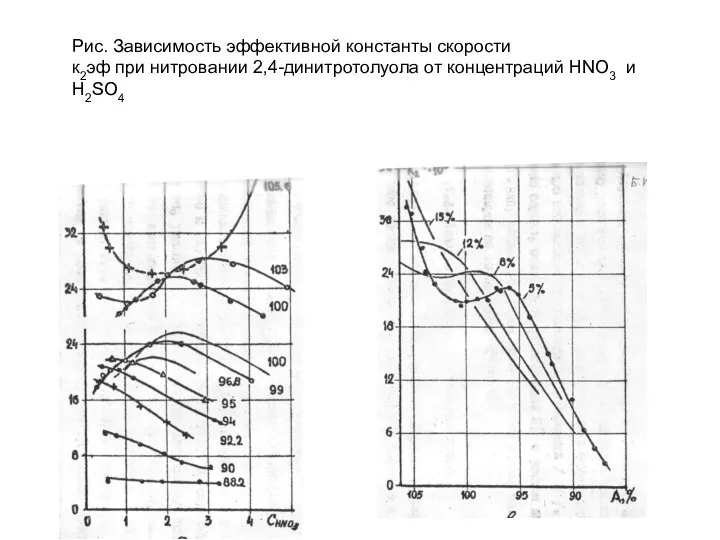
- 46. Рис. Зависимость эффективной константы скорости к2эф при нитровании 2,4-динитротолуола от концентраций HNO3 и H2SO4
- 48. ТЕПЛОВЫЕ ЭФФЕКТЫ ПРИ НИТРОВАНИИ Тепловой баланс. Q приход = Q1 + Q2 + Q3 Приход Q1
- 49. Суммарный тепловой эффект нитрования при получении мононитротолуола ~ 123 кДж/мол (29 ккал/моль) динитротолуола ~ 139 кДж/моль
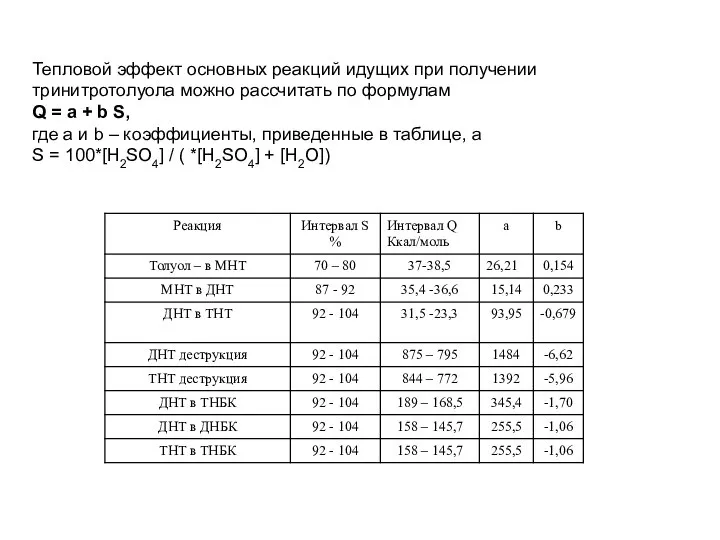
- 50. Тепловой эффект основных реакций идущих при получении тринитротолуола можно рассчитать по формулам Q = a +
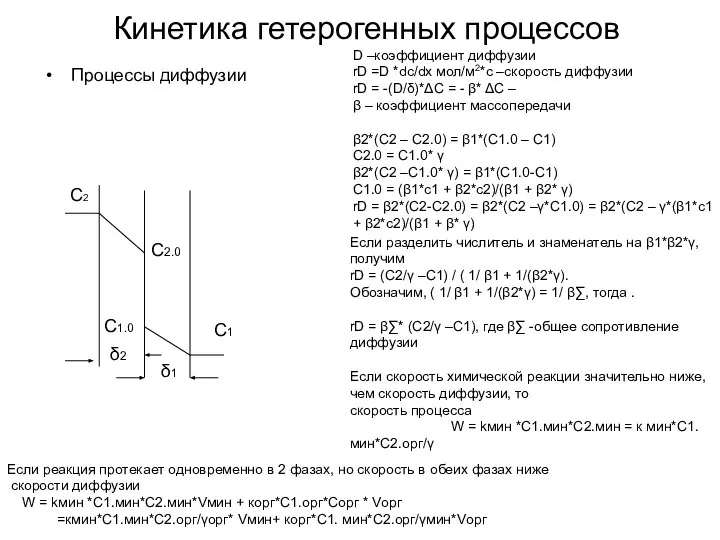
- 51. rD = β∑* (C2/γ –C1), где β∑ -общее сопротивление диффузии Если скорость химической реакции значительно ниже,
- 52. Кинетика гетерогенных процессов Процессы диффузии С2 С2.0 С1.0 С1 D –коэффициент диффузии rD =D *dc/dx мол/м2*с
- 53. Влияние азотистой кислоты В водных растворах H2SO4 и HClO4 (с концентрацией менее 50%) HNO2 присутствует преимущественно
- 54. Изучение кинетики каталитического процесса строго доказало первоначальное нитрозирование с последующим быстрым окислением С-нитрозосоединения и регенерацией HNO2.
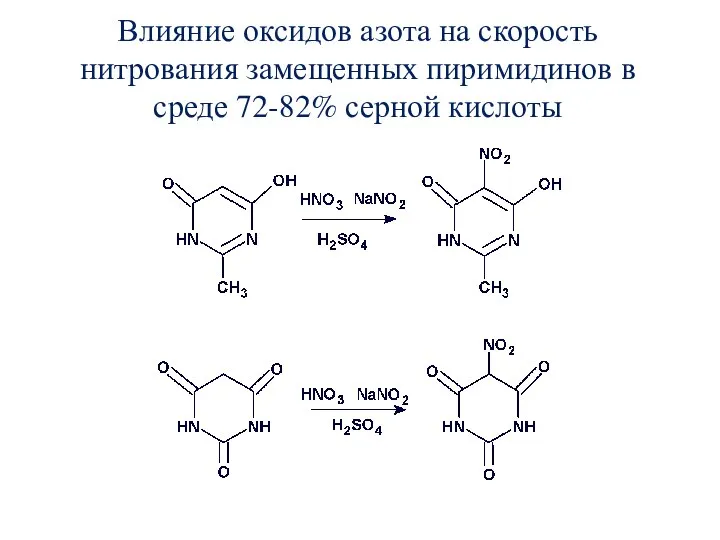
- 55. Влияние оксидов азота на скорость нитрования замещенных пиримидинов в среде 72-82% серной кислоты
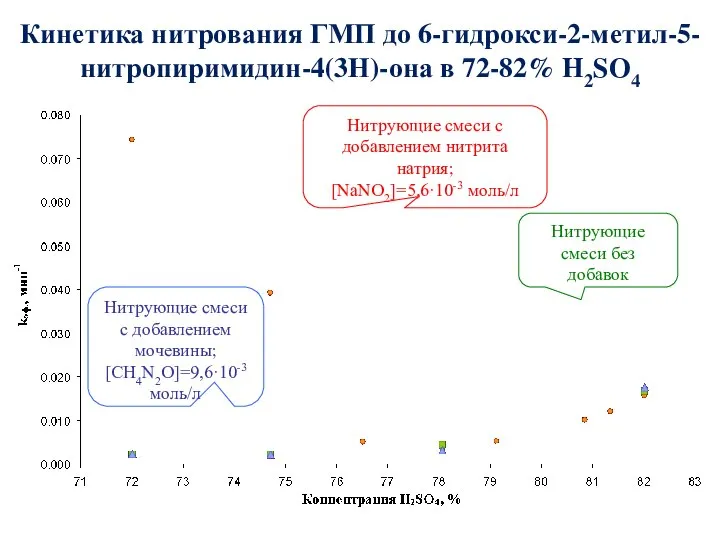
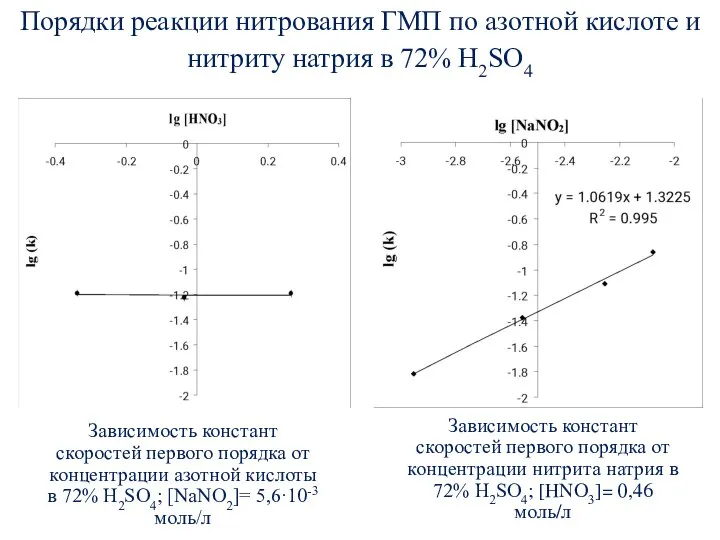
- 56. Кинетика нитрования ГМП до 6-гидрокси-2-метил-5-нитропиримидин-4(3Н)-она в 72-82% H2SO4 Нитрующие смеси с добавлением нитрита натрия; [NaNO2]=5,6·10-3 моль/л
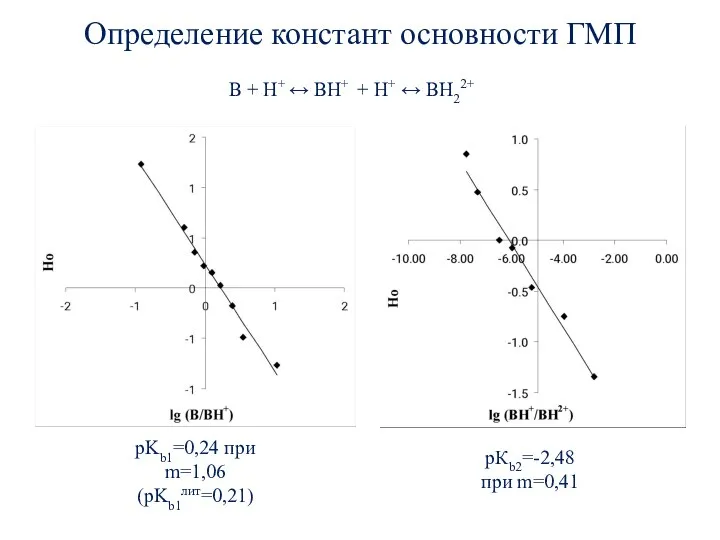
- 57. Определение констант основности ГМП B + H+ ↔ BH+ + H+ ↔ BH22+ pKb1=0,24 при m=1,06
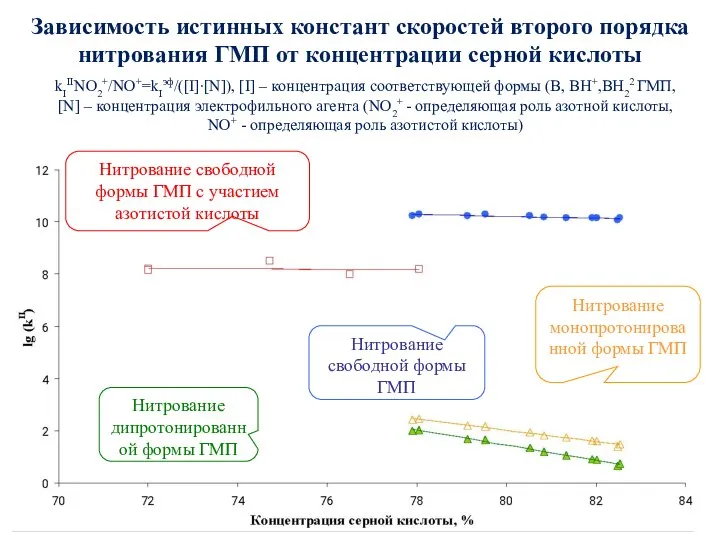
- 58. Зависимость истинных констант скоростей второго порядка нитрования ГМП от концентрации серной кислоты Нитрование монопротонированной формы ГМП
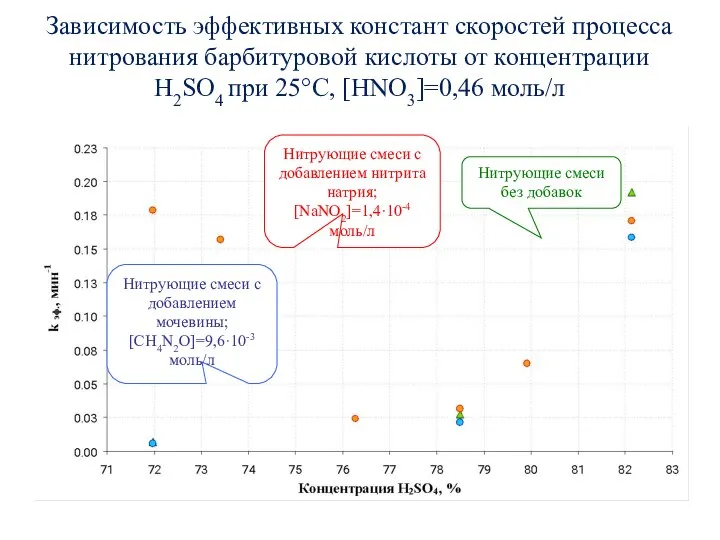
- 59. Зависимость эффективных констант скоростей процесса нитрования барбитуровой кислоты от концентрации H2SO4 при 25°С, [HNO3]=0,46 моль/л Нитрующие
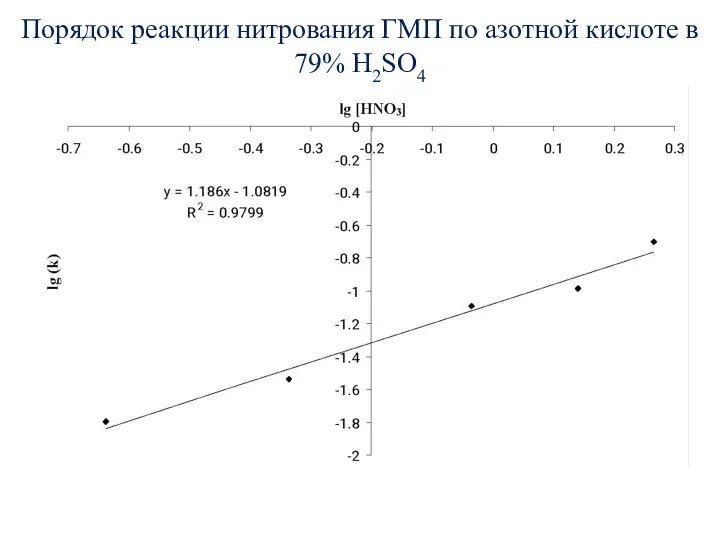
- 60. Порядок реакции нитрования ГМП по азотной кислоте в 79% H2SO4
- 61. Порядки реакции нитрования ГМП по азотной кислоте и нитриту натрия в 72% H2SO4 Зависимость констант скоростей
- 62. Последующие исследования показали, что при каталитическом действии низших оксидов азота не всегда происходит нитрозирование. Этот явление
- 63. В 70-80-е годы образование относительно стабильных катион-радикалов (КР) спектральными методами или в форме солей было обнаружено
- 65. Скачать презентацию





















 Архитектура и искусство Великобритании XVIІІ в
Архитектура и искусство Великобритании XVIІІ в техника философиясы
техника философиясы Тәуелсіз Қазақстан Республикасының құрылуы мен қалыптасуындағы Тұнғыш Президент Н.Ә. Назарбаевтың рөлі мен қызметі
Тәуелсіз Қазақстан Республикасының құрылуы мен қалыптасуындағы Тұнғыш Президент Н.Ә. Назарбаевтың рөлі мен қызметі Центральный банк Российской Федерации (Банк России)
Центральный банк Российской Федерации (Банк России) Презентация "Искусство витража" - скачать презентации по МХК
Презентация "Искусство витража" - скачать презентации по МХК Ядовитые технические жидкости
Ядовитые технические жидкости Необходимость, возможности и пределы государственного управления
Необходимость, возможности и пределы государственного управления ТМ для Горизонта. Как всё и везде успеть
ТМ для Горизонта. Как всё и везде успеть Презентация "Святая великомученица Варвара" - скачать презентации по МХК
Презентация "Святая великомученица Варвара" - скачать презентации по МХК бизнес
бизнес Премии качества
Премии качества c2-ccf75d66
c2-ccf75d66 Расчет многоэтажных зданий
Расчет многоэтажных зданий Игра - Welcome to Scotland
Игра - Welcome to Scotland Как построить новый дом? (окружающий мир, 2 класс)
Как построить новый дом? (окружающий мир, 2 класс) Презентация на тему "моя малая родина Кубань" - скачать презентации по Педагогике
Презентация на тему "моя малая родина Кубань" - скачать презентации по Педагогике Автор: Шарова Валентина Степановна Учитель математики МОУ «СОШ №4» город Новочебоксарск Чувашской Республики Повторяем математику… Справочник Презентация к уроку математики «Путешествие в страну дробных чисел»
Автор: Шарова Валентина Степановна Учитель математики МОУ «СОШ №4» город Новочебоксарск Чувашской Республики Повторяем математику… Справочник Презентация к уроку математики «Путешествие в страну дробных чисел» Управление функциями организма
Управление функциями организма Аппаратные средства визуализации
Аппаратные средства визуализации Презентация Понятия форм собственности на природные объекты
Презентация Понятия форм собственности на природные объекты  Android Broadcast receivers
Android Broadcast receivers Организация стока поверхностных вод (Тема 3)
Организация стока поверхностных вод (Тема 3) Альбрехт Дюрер - один из величайших мастеров западноевропейского Ренессанса
Альбрехт Дюрер - один из величайших мастеров западноевропейского Ренессанса Педагогический контроль в подготовке спортсмена
Педагогический контроль в подготовке спортсмена Ранние формы религии. Часть I
Ранние формы религии. Часть I Камеральная налоговая проверка
Камеральная налоговая проверка Виды наследования
Виды наследования Космическая тема в музыке, живописи и кино
Космическая тема в музыке, живописи и кино