Содержание
- 2. ПЛАН ЛЕКЦИИ Клиническая иммунология: определение, предмет и задачи Трансплантационная иммунология. Механизмы трансплантационного иммунитета. Иммунные реакции на
- 3. КЛИНИЧЕСКАЯ ИММУНОЛОГИЯ Раздел медицины, использующий знания об иммунной системе для обеспечения адекватной жизнедеятельности организма
- 4. ОБОСНОВАНИЕ ВЫДЕЛЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ В ОТДЕЛЬНЫЙ РАЗДЕЛ МЕДИЦИНЫ Наработка большого количества иммунных тестов и методов иммунологического
- 5. ОБОСНОВАНИЕ ВЫДЕЛЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ В ОТДЕЛЬНЫЙ РАЗДЕЛ МЕДИЦИНЫ 3. Быстрое увеличение уровня выявления больных с иммунной
- 6. ПРЕДМЕТ ИЗУЧЕНИЯ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ заболевания, связанные с дисфункциями иммунной системы и заболевания, в которых иммунным реакциям
- 7. ЗАДАЧИ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ Обследование, диагностика и лечение больных с заболеваниями или патологическими процессами, развивающимися в результате
- 8. РАЗДЕЛЫ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ ПРОФИЛАКТИЧЕСКАЯ ИММУНОЛОГИЯ ЛЕЧЕБНАЯ ИММУНОЛОГИЯ ТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯ ИММУНОЛОГИЯ РЕПРОДУКЦИИ
- 9. ПРОФИЛАКТИЧЕСКАЯ ИММУНОЛОГИЯ СПЕЦИФИЧЕСКАЯ ИММУНОПРОФИЛАКТИКА (ВАКЦИНАЦИЯ) – ПРОФИЛАКТИКА ОТНОСИТЕЛЬНО НЕБОЛЬШОГО КОЛИЧЕСТВА ЭТИОЛОГИЧЕСКИ КОНКРЕТНЫХ ЗАБОЛЕВАНИЙ НЕСПЕЦИФИЧЕСКАЯ ИММУНОПРОФИЛАКТИКА (ПРОФИЛАКТИЧЕСКАЯ
- 10. ЛЕЧЕБНАЯ ИММУНОЛОГИЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ ИММУНОПАТОЛОГИЯ СОЧЕТАННЫЙ ПРОЦЕСС
- 11. ИММУННАЯ НЕДОСТАТОЧНОСТЬ а) экзоантигенная – связанная с повреждающей инициативой экзоантигенов (острые или хронические воспалительные процессы) б)
- 12. ИММУНОПАТОЛОГИЯ ИЗВРАЩЕНИЕ ФУНКЦИЙ КОМПОНЕНТОВ ИЛИ ИММУННОЙ СИСТЕМЫ В ЦЕЛОМ АЛЛЕРГИЧЕСКИЕ ЗАБОЛЕВАНИЯ АУТОИММУННЫЕ ЗАБОЛЕВАНИЯ
- 13. СОЧЕТАННЫЙ ПРОЦЕСС ЛИМФОПРОЛИФЕРАТИВНЫЙ СИНДРОМ ИММУНОПРОЛИФЕРАТИВНЫЕ ЗАБОЛЕВАНИЯ ГРАНУЛЕМАТОЗНЫЕ ПРОЦЕССЫ
- 14. ТРАНСПЛАНТАЦИОННАЯ ИММУНОЛОГИЯ РАЗДЕЛ КЛИНИЧЕСКОЙ ИММУНОЛОГИИ, ИЗУЧАЮЩИЙ МЕХАНИЗМЫ ТРАНСПЛАНТАЦИИ ТКАНЕЙ И ОРГАНОВ
- 15. ТРАНСПЛАНТАЦИОННЫЙ ИММУНИТЕТ ЭТО ИММУННЫЕ РЕАКЦИИ, РАЗВИВАЕМЫЕ ОРГАНИЗМОМ – РЕЦИПИЕНТОМ ПРОТИВ АНТИГЕНОВ ПЕРЕСАЖЕННОЙ ТКАНИ ИЛИ ОРГАНА В
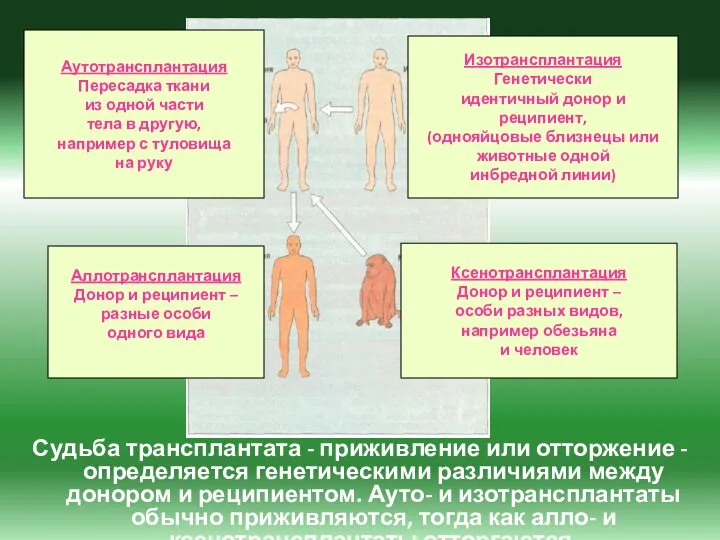
- 16. Судьба трансплантата - приживление или отторжение - определяется генетическими различиями между донором и реципиентом. Ауто- и
- 17. Пересадка органов и тканей в историческом аспекте Иммунологическая природа отторжения чужеродных трансплантатов была доказана в 40-е
- 18. Пересадка органов и тканей в историческом аспекте 3. С использованием генетически чистых линий мышей были связаны
- 19. ГЕНЕТИЧЕСКИЕ ЗАКОНЫ ТРАНСПЛАНТАЦИИ При пересадки тканей внутри линии ткани приживаются, а при пересадках между линиями –
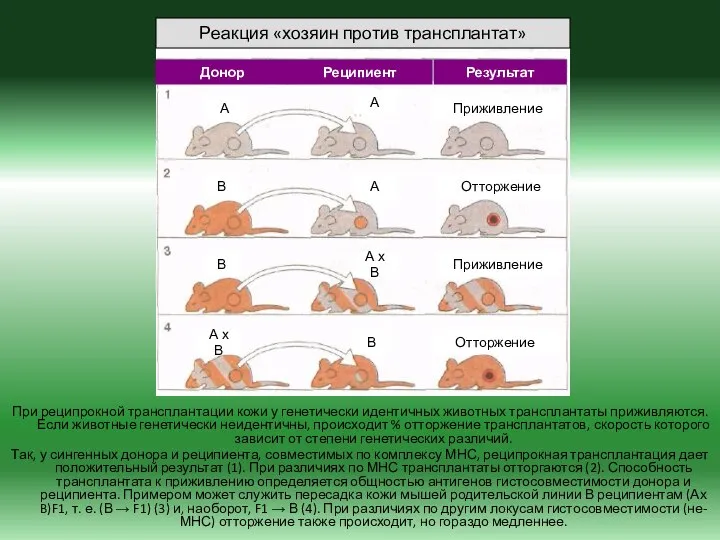
- 20. При реципрокной трансплантации кожи у генетически идентичных животных трансплантаты приживляются. Если животные генетически неидентичны, происходит %
- 21. Механизмы трансплантационного иммунитета существует много генетических локусов, обусловливающих гистосовместимость, но только с одним локусом МНС (II
- 22. Механизмы трансплантационного иммунитета Иммунный ответ на трансплантат обусловлен распознаванием антигенов HLA донора лимфоцитами реципиента. Это вызывает
- 23. ОТТОРЖЕНИЕ ТРАНСПЛАНТАТА СВЕРХОСТРОЕ (в первые часы после пересадки) ОСТРОЕ (в течение первых 2 – 3 недель)
- 24. ПАТОГЕНЕЗ СВЕРХОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА Развивается при наличии в организме донора ПРЕДСУЩЕСТВУЮЩИХ АНТИТЕЛ – иммуноглобулинов против некоторых
- 25. ПАТОГЕНЕЗ СВЕРХОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА Комплексы, состоящие из антигенов трансплантата и антител реципиента, активируют свертывание крови и
- 26. ПРЕДСУЩЕСТВУЮЩИЕ АНТИТЕЛА при пересадке тканей обязательно исследуют наличие предсуществующих антител в организме реципиента к основыми разновидностям
- 27. ПАТОГЕНЕЗ ОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА Первичным механизмом распознавания является антигенная презентация иммуногенных пептидов трансплантата дендритными клетками пересаженного
- 28. ПАТОГЕНЕЗ ОСТРОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА 6. Цитокины Тh1 (ФНОα и ФНОβ) оказывают прямое повреждающее действие на трансплантат.
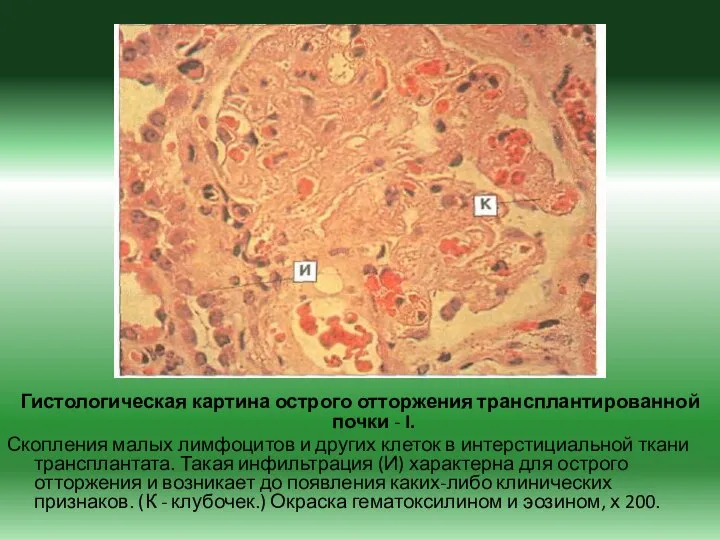
- 29. Гистологическая картина острого отторжения трансплантированной почки - I. Скопления малых лимфоцитов и других клеток в интерстициальной
- 30. ПАТОГЕНЕЗ ХРОНИЧЕСКОГО ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА Развивается в случае, когда проводимая иммуносупрессивная терапия предотвращает реализацию клеточных механизмов острого
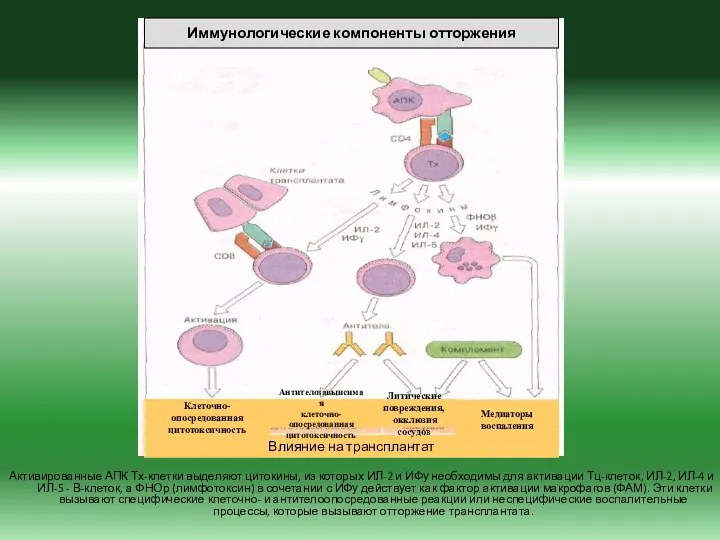
- 31. Активированные АПК Тх-клетки выделяют цитокины, из которых ИЛ-2 и ИФу необходимы для активации Тц-клеток, ИЛ-2, ИЛ-4
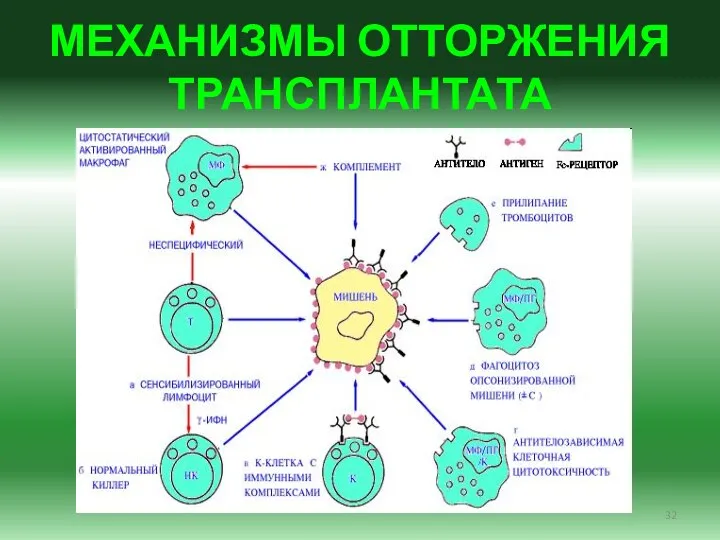
- 32. МЕХАНИЗМЫ ОТТОРЖЕНИЯ ТРАНСПЛАНТАТА
- 33. ВТОРИЧНАЯ РЕАКЦИЯ ОТТОРЖЕНИЯ Реакцию на повторную подсадку ткани от того же донора называют second-set («второй заход»)
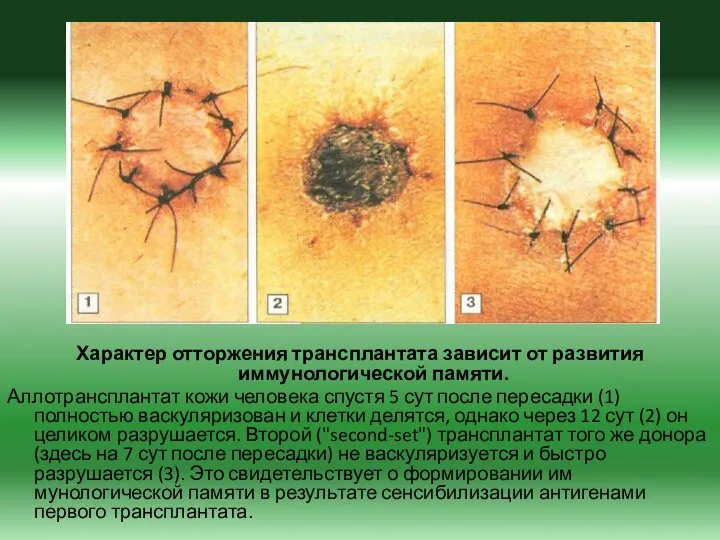
- 34. Характер отторжения трансплантата зависит от развития иммунологической памяти. Аллотрансплантат кожи человека спустя 5 сут после пересадки
- 35. ТРАНСПЛАНТАЦИЯ КОСТНОГО МОЗГА Занимает обособленное место в практике трансплантации Осуществляется в форме инфузии суспензированной ткани, а
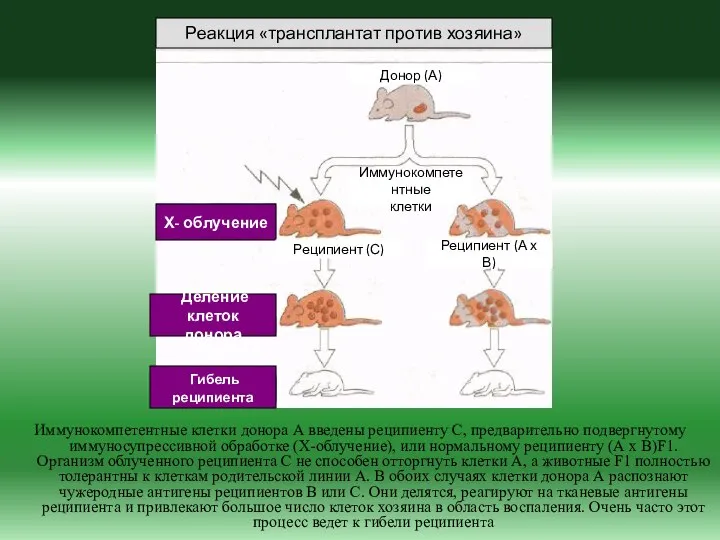
- 36. «ТРАНСПЛАНТАТ ПРОТИВ ХОЗЯИНА» Ткани трансплантатов содержат иммунокомпетентные и антигенпредставляющие клетки («клетки-пассажиры»), которые могут опосредовать иммунную агрессию
- 37. Иммунокомпетентные клетки донора А введены реципиенту С, предварительно подвергнутому иммуносупрессивной обработке (Х-облучение), или нормальному реципиенту (А
- 38. КЛИНИЧЕСКАЯ КАРТИНА РТПХ Проявляется у мышей через 7 – 10 дней , у человека на второй
- 39. ПОДХОДЫ К ПРЕОДОЛЕНИЮ ТРАНСПЛАНТАЦИОННОЙ РЕАКЦИИ ПОДБОР ДОНОРОВ ТРАНСПЛАНТАТОВ ПО ПРИНЦИПУ МАКСИМАЛЬНОГО СООТВЕТСТВИЯ ПО НАБОРУ МОЛЕКУЛ ГИСТОСОВМЕСТИМОСТИ
- 40. Индекс гистосовместимости 25% - если донор и реципиент содержат одинаковые молекулы HLA одного локуса 50% -
- 41. РЕЗЮМЕ Не существует каких-либо специфических механизмов трансплантационного иммунитета, так как пересадка органов и тканей в естественных
- 43. Скачать презентацию

































 Где живут слоны? Почему слоны не живут в Воронежской области?
Где живут слоны? Почему слоны не живут в Воронежской области? Теоретические основы электротехники. Нелинейные электрические цепи
Теоретические основы электротехники. Нелинейные электрические цепи Кейс на тему «ОСАГО без страхования жизни»
Кейс на тему «ОСАГО без страхования жизни» Структура нормы права
Структура нормы права Информация как основа принятия решений в экономических задачах
Информация как основа принятия решений в экономических задачах Типы, переменные, управляющие инструкции. Ссылочные типы и переменные. (Тема 2.3)
Типы, переменные, управляющие инструкции. Ссылочные типы и переменные. (Тема 2.3) Эзофагопластика
Эзофагопластика Основные принципы торговой политики РФ
Основные принципы торговой политики РФ Использование ИКТ на уроках географии. Пирогова Наталья Анатольевна Учитель географии МБОУ СОШ №120
Использование ИКТ на уроках географии. Пирогова Наталья Анатольевна Учитель географии МБОУ СОШ №120 Религия как одна из форм культуры
Религия как одна из форм культуры БОРИС МИХАЙЛОВИЧ КУСТОДИЕВ (1878-1927)
БОРИС МИХАЙЛОВИЧ КУСТОДИЕВ (1878-1927)  Алгоритмы с ветвящейся структурой
Алгоритмы с ветвящейся структурой Электрокардиография Основные нормативы ЭКГ
Электрокардиография Основные нормативы ЭКГ Анализ причин терроризма как основной угрозы XXI века
Анализ причин терроризма как основной угрозы XXI века Я знаю свої права
Я знаю свої права Презентация на тему Закономерности изменчивости: модификационная и мутационная изменчивость
Презентация на тему Закономерности изменчивости: модификационная и мутационная изменчивость  Регуляция соматических функций
Регуляция соматических функций РУССКОЕ ИЗОБРАЗИТЕЛЬНОЕ ИСКУССТВО
РУССКОЕ ИЗОБРАЗИТЕЛЬНОЕ ИСКУССТВО Мошенничество в сфере кредитования
Мошенничество в сфере кредитования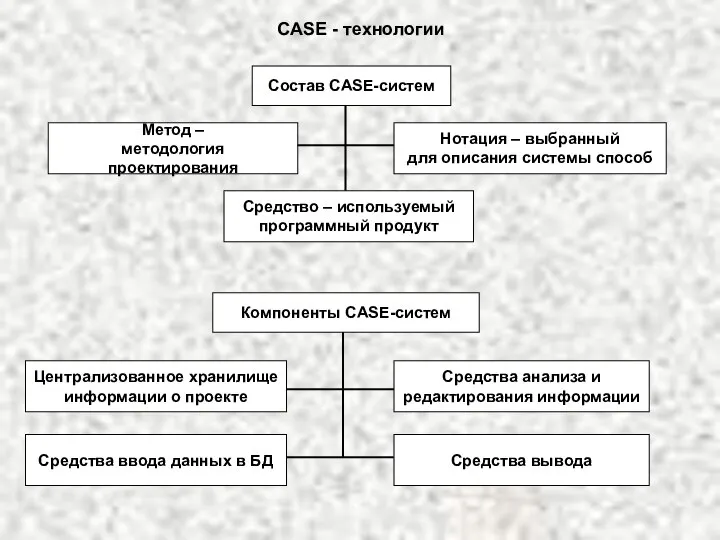 Case технология
Case технология  Т Е М А «ПРОДАЖА НЕДВИЖИМОСТИ. ПРОДАЖА ПРЕДПРИЯТИЯ»
Т Е М А «ПРОДАЖА НЕДВИЖИМОСТИ. ПРОДАЖА ПРЕДПРИЯТИЯ» Основы языка структурированных запросов SQL
Основы языка структурированных запросов SQL Понятие интерфейса пользователя
Понятие интерфейса пользователя Қазақ фонологиясының өзекті мәселелері
Қазақ фонологиясының өзекті мәселелері Презентация Правовая характеристика и особенности дисциплинарной ответственности должностных лиц таможенных органов
Презентация Правовая характеристика и особенности дисциплинарной ответственности должностных лиц таможенных органов  Новейшая геополитика России
Новейшая геополитика России Парные звонкие и глухие согласные в корне слова. 2 класс
Парные звонкие и глухие согласные в корне слова. 2 класс Основы конституционного права РФ. Тема 5
Основы конституционного права РФ. Тема 5