Содержание
- 2. Химическая связь и межмолекулярное взаимодействие Деформационная электронная плотность При сближении атомов проявляются след. взаимодействия: - Каждый
- 3. Деформационная электронная плотность δρ(r) позволяет представить, как изменилось электронное распределение при образовании молекулы из атомов. δρ(r)=ρмол(r)
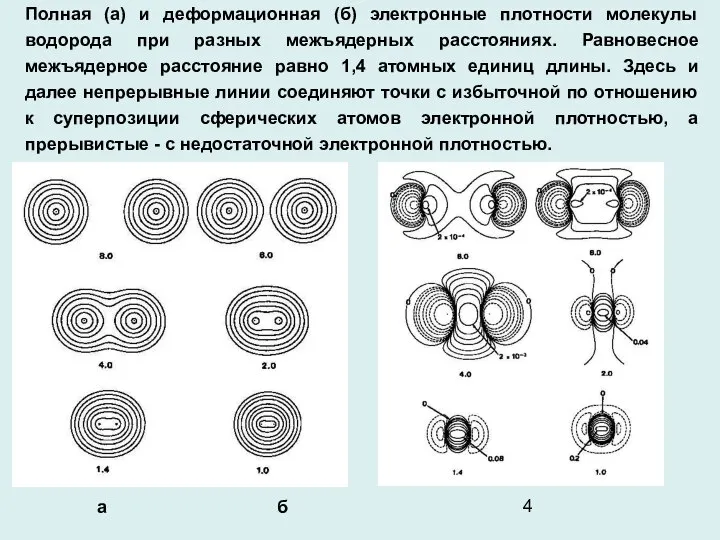
- 4. Полная (а) и деформационная (б) электронные плотности молекулы водорода при разных межъядерных расстояниях. Равновесное межъядерное расстояние
- 5. Атомы входят в промолекулу как свободные и, в принципе, каждый из них должен находиться в низшем
- 6. Пример. Свободный атом С имеет три электронные конфигурации с одинаковой энергией: (ls)2(2s)2(2рx)1(2рy)1(2рz)0, (ls)2(2s)2(2рx)0(2рy)1(2рz)1 и (ls)2(2s)2(2рx)1(2рy)0(2рz)1. Усредненная
- 7. Величины положительных максимумов и отрицательных минимумов в областях σ- и π-связей на стандартных картах деформационной ЭП
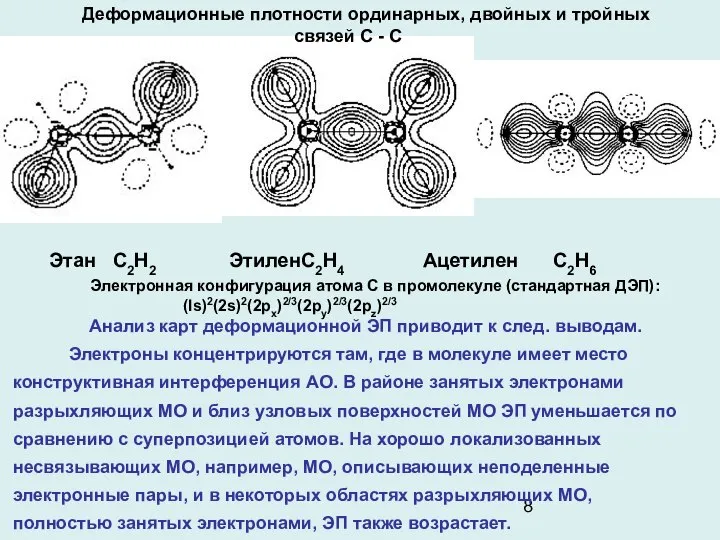
- 8. Деформационные плотности ординарных, двойных и тройных связей C - C Этан С2Н2 Этилен С2Н4 Ацетилен С2Н6
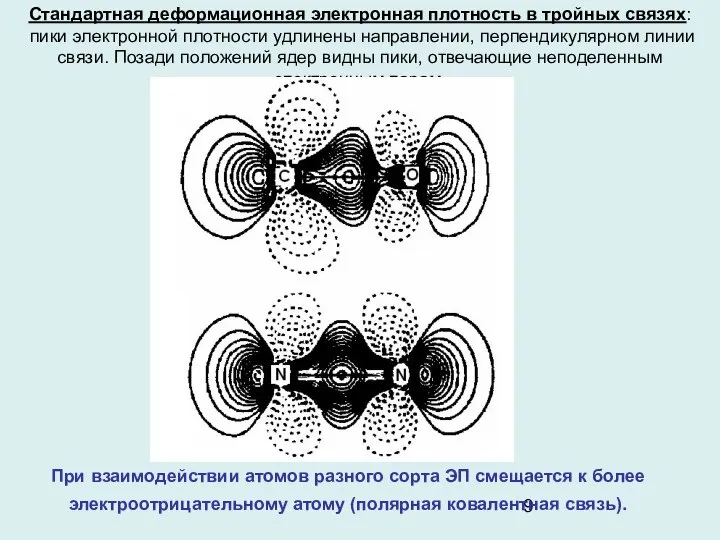
- 9. При взаимодействии атомов разного сорта ЭП смещается к более электроотрицательному атому (полярная ковалентная связь). Стандартная деформационная
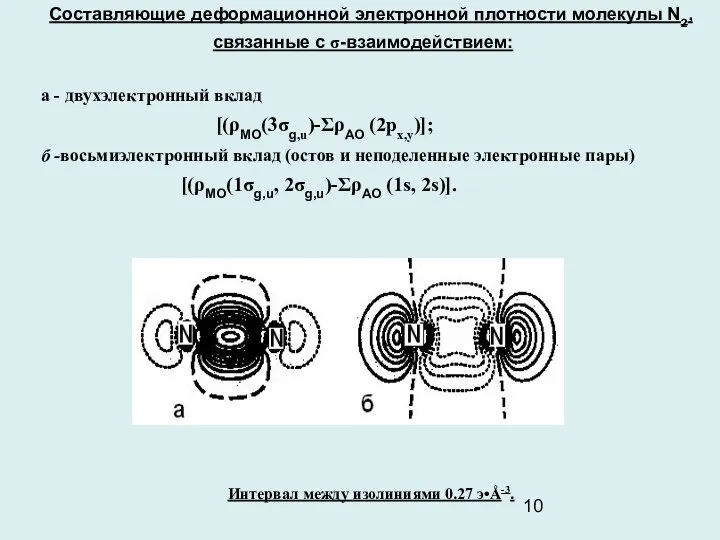
- 10. Составляющие деформационной электронной плотности молекулы N2, связанные с σ-взаимодействием: а - двухэлектронный вклад [(ρМО(3σg,u)-ΣρАО (2px,y)]; б
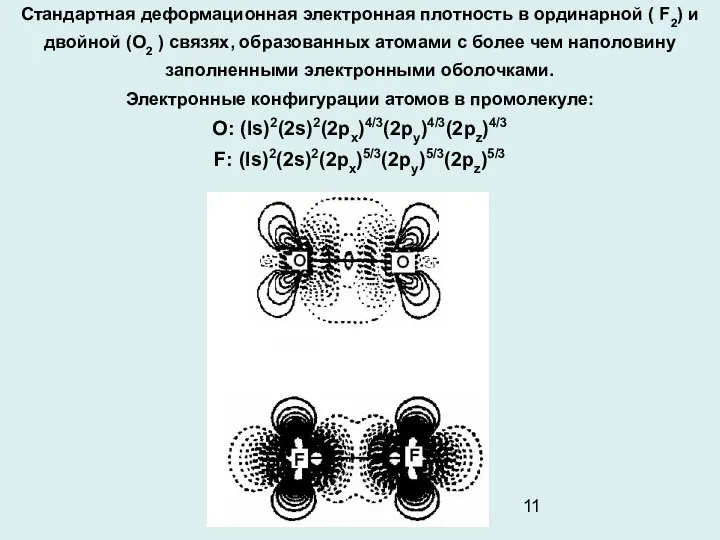
- 11. Стандартная деформационная электронная плотность в ординарной ( F2) и двойной (O2 ) связях, образованных атомами с
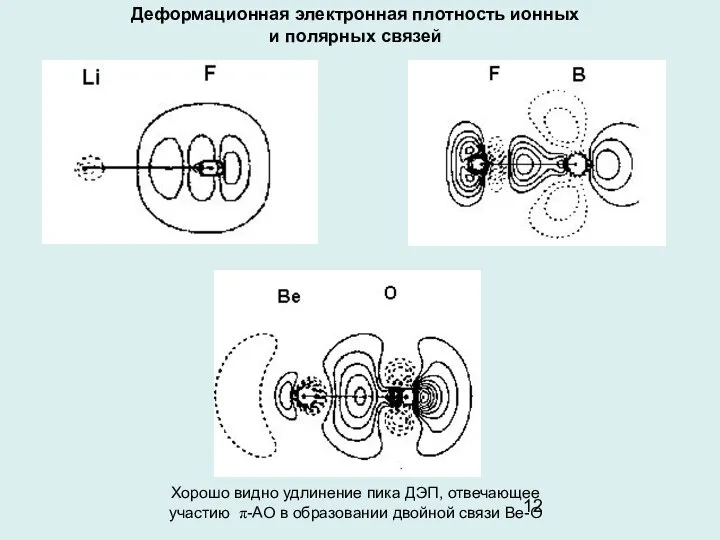
- 12. Деформационная электронная плотность ионных и полярных связей Хорошо видно удлинение пика ДЭП, отвечающее участию π-АО в
- 13. Силовой и энергетический аспекты описания химической связи Гамильтониан молекулы Н состоит из членов, описывающих кинетические Т
- 14. Если λ=Rа - ядерные координаты [V=V(Rа)], то для ядра а молекулы имеем: ∂Е/∂Ra = - ∂V/∂Ra
- 15. Силу F(R) можно записать через ЭП: В равновесии F(Re)=0. Примем, что ρ(г)>0 (знак электронного заряда игнорируем):
- 16. Для стабильности молекулы необходимо, чтобы ЭП в связывающей области при R=Re создавала силы, компенсирующие отталкивание ядер
- 17. 2)Теорема вириала устанавливает соотношение между энергией молекулы и ее кинетической и потенциальной компонентами. Плотности кинетической g(r)
- 18. Эти выражения отражают содержание теоремы вириала и характеризуют систему в равновесии. Они справедливы как для молекулы,
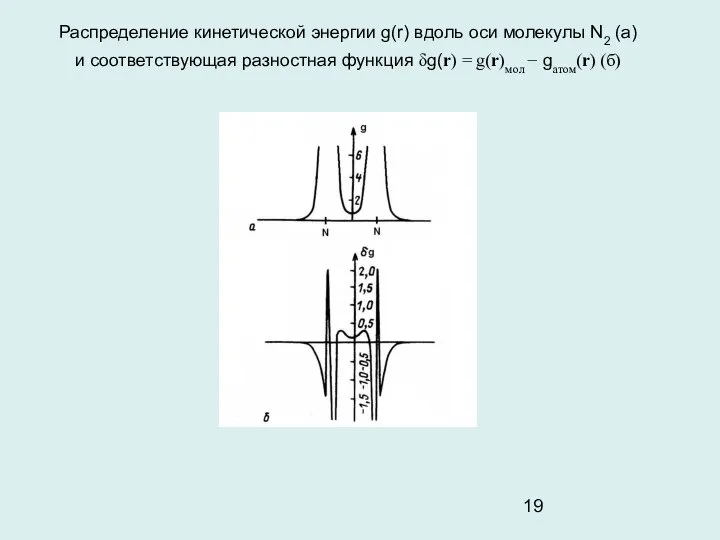
- 19. Распределение кинетической энергии g(r) вдоль оси молекулы N2 (а) и соответствующая разностная функция δg(r) = g(r)мол
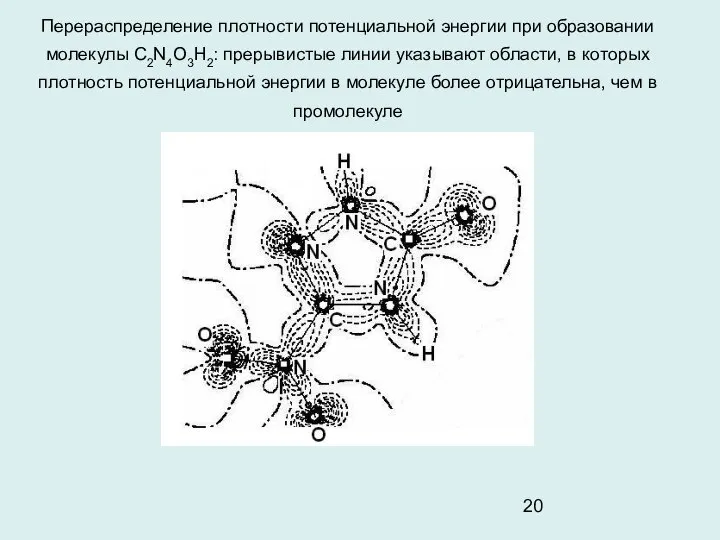
- 20. Перераспределение плотности потенциальной энергии при образовании молекулы С2N4O3H2: прерывистые линии указывают области, в которых плотность потенциальной
- 22. Скачать презентацию






![Если λ=Rа - ядерные координаты [V=V(Rа)], то для ядра а молекулы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1297928/slide-13.jpg)




 Комплект легких балластировочных машин непрерывного действия, состав, назначение, условия применения, принцип работы
Комплект легких балластировочных машин непрерывного действия, состав, назначение, условия применения, принцип работы Презентация на тему "Дидактические игры как одна из активных форм обучения" - скачать презентации по Педагогике
Презентация на тему "Дидактические игры как одна из активных форм обучения" - скачать презентации по Педагогике what_39_s_this
what_39_s_this Взаимоотношения заказчик-исполнитель при разработке ПО
Взаимоотношения заказчик-исполнитель при разработке ПО Linguistic Anthropology. Week 2
Linguistic Anthropology. Week 2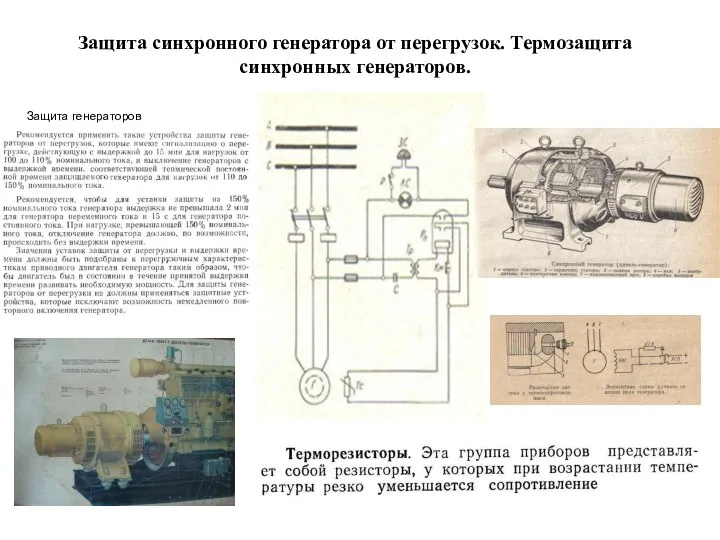 Защита синхронного генератора от перегрузок. Техническое обслуживание судовых электроприводов. (Билет 10)
Защита синхронного генератора от перегрузок. Техническое обслуживание судовых электроприводов. (Билет 10) Временный ввоз товаров для личного пользования. Временный вывоз физическими лицами товаров для личного пользования. Подготовили
Временный ввоз товаров для личного пользования. Временный вывоз физическими лицами товаров для личного пользования. Подготовили Системный анализ экономических структур
Системный анализ экономических структур  Government of the Russian Federation
Government of the Russian Federation Культурное пространство Европы и культура Руси
Культурное пространство Европы и культура Руси Конфликты: взрослые и дети
Конфликты: взрослые и дети Теория управления портфелем
Теория управления портфелем  Фармтерапия сердечной недостаточности
Фармтерапия сердечной недостаточности Физиология соматосенсорного анализатора
Физиология соматосенсорного анализатора Способы проектирования земельных участков
Способы проектирования земельных участков Работа с семьей ГОУ школа 512
Работа с семьей ГОУ школа 512 Презентация Динамика цен на автомобильном рынке
Презентация Динамика цен на автомобильном рынке  Сущность и структура политического процесса. (Лекция 4)
Сущность и структура политического процесса. (Лекция 4) Портрет Виды и типы портрета
Портрет Виды и типы портрета Иркутская летопись Презентацию подготовила: учитель литературы Ложникова Е. Ф. МОУ «Седановская СОШ»
Иркутская летопись Презентацию подготовила: учитель литературы Ложникова Е. Ф. МОУ «Седановская СОШ» Персонализованная медицина
Персонализованная медицина Гражданин России
Гражданин России Комбинаторика Размещение и сочитание
Комбинаторика Размещение и сочитание Влияние вредных примесей на свойства стали
Влияние вредных примесей на свойства стали Будова атомів і молекул
Будова атомів і молекул труд - презентация для начальной школы
труд - презентация для начальной школы Славянский ход Мурман – Черногория 2018
Славянский ход Мурман – Черногория 2018 Процедуры и функции в Pascal’е
Процедуры и функции в Pascal’е