Содержание
- 2. 1.Общие понятия и определения
- 3. Термодинамика изучает законы превращения энергии в различных процессах, происходящих в макроскопических системах и сопровождающихся тепловыми эффектами.
- 4. Термодинамическая система Термодинамическая система представляет собой совокупность материальных тел, находящихся в механическом и тепловом взаимодействиях друг
- 5. Термодинамическая система Термодинамическую систему, которая не может обмениваться теплотой с окружающей средой, называют теплоизолированной или адиабатной.
- 6. 2. Основные параметры состояния газа Давление обусловлено взаимодействием молекул рабочего тела с поверхностью и численно равно
- 7. Температура Температурой называется физическая величина, характеризующая степень нагретости тела. Понятие о температуре вытекает из следующего утверждения:
- 8. Температура В системе СИ единицей температуры является кельвин (К); на практике широко применяется градус Цельсия (°С).
- 9. Удельный объем Удельный объем v — это объем единицы массы вещества. Если однородное тело массой М
- 10. Уравнение состояния идеального газа Для равновесной термодинамической системы существует функциональная связь между параметрами состояния, которая называется
- 11. Уравнение состояния идеального газа Для идеального газа выполняется уравнение Менделеева-Клапейрона: R = 8,31 Дж/( )– универсальная
- 12. Модель идеального газа: газ называется идеальным, если можно пренебречь: размерами молекул по сравнению с расстояниями между
- 13. Объединённый газовый закон Для двух состояний газа при постоянной массе газа:
- 14. Изопроцессы На практике трудно одновременно наблюдать за изменением всех параметров, поэтому один из параметров поддерживают постоянным.
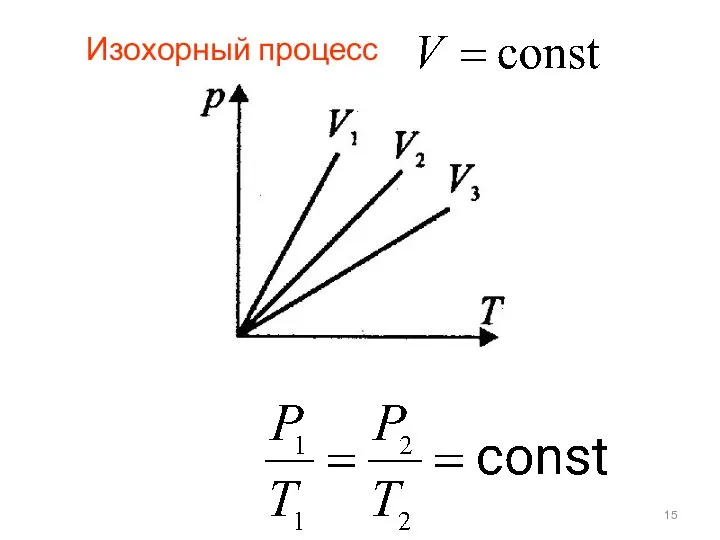
- 15. Изохорный процесс
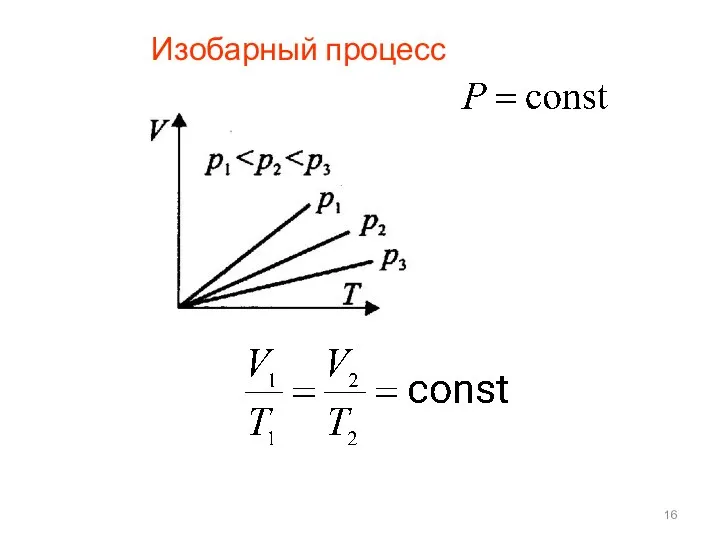
- 16. Изобарный процесс
- 17. Изотермический процесс
- 18. Основное уравнение молекулярно-кинетической теории устанавливает связь между макроскопическими и микроскопическими параметрами. Микроскопические параметры: масса, импульс, кинетическая
- 19. Давление газа на стенки сосуда обу- словлено передачей молекулами свое- го импульса стенкам сосуда. Учитывая, что
- 20. Уравнение Менделеева-Клапейрона можно переписать так: Здесь – потоянная Больцмана. – концентрация молекул.
- 21. Сравнивая и Получим для средней кинетической энергии поступательного движения молекулы
- 22. 4. Газовые смеси
- 23. Закон Дальтона Рассмотрим смесь газов, состоящую из N типов молекул. В единице объема содержится n молекул:
- 24. Парциальные (partial), т.е. частичные давления: Эта формула выражает закон Дальтона: давление смеси идеальных газов равно сумме
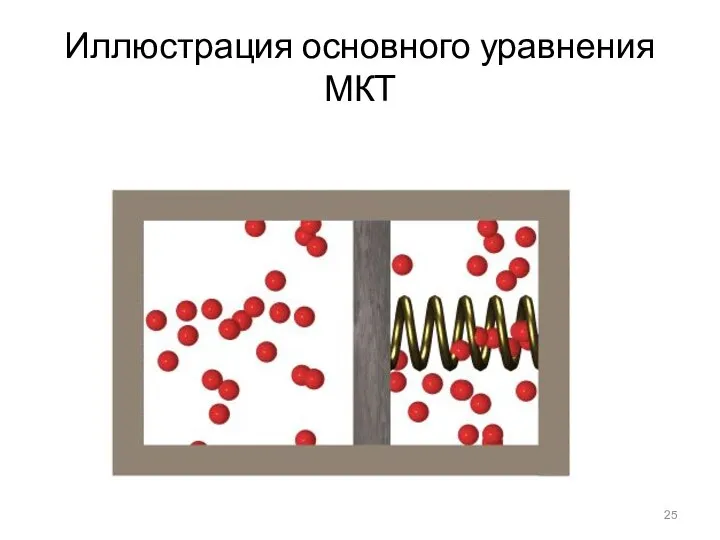
- 25. Иллюстрация основного уравнения МКТ
- 26. В общем случае средняя кинетическая энергия молекулы равна: число степеней свободы молекулы. Энергия молекулы равномерно распределяется
- 27. Число независимых друг от друга движений тела (или независимых координат, определяющих его положение в пространстве) называется
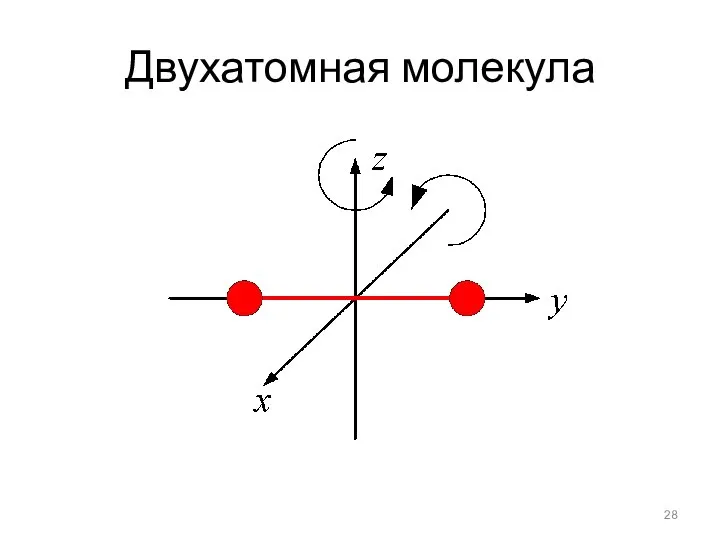
- 28. Двухатомная молекула
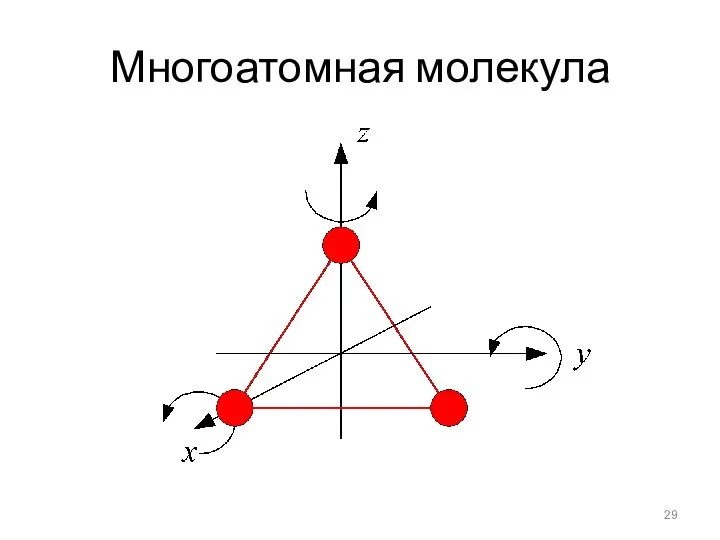
- 29. Многоатомная молекула
- 30. Одноатомная молекула Модель молекулы одноатомного газа – материальная точка, для описания ее положения в пространстве задаются
- 31. Одноатомная молекула: i = 3. Д Двухатомная молекула с жесткой связью: i = 5 - три
- 32. 5. Количество теплоты. Теплоемкость
- 33. Приращение внутренней энергии в процессе чистого теплообмена называется количеством теплоты или просто – теплотой (Q). Теплота
- 34. Количество теплоты, необходимое для нагревания тела на один кельвин, называется теплоемкостью тела Удельная теплоёмкость Молярная теплоёмкость
- 36. Скачать презентацию




























 Равноускоренное прямолинейное движение
Равноускоренное прямолинейное движение Энтропия в техносфере
Энтропия в техносфере Презентация по физике "Физический калейдоскоп" - скачать
Презентация по физике "Физический калейдоскоп" - скачать  Уравнения теории упругости. Напряженное состояние в точке. Гипотеза Сен-Венана. (Лекции 1-2)
Уравнения теории упругости. Напряженное состояние в точке. Гипотеза Сен-Венана. (Лекции 1-2) Термодинамические свойства воды и водяного пара
Термодинамические свойства воды и водяного пара Теплолічильник. (Задача 2)
Теплолічильник. (Задача 2) Методы анализа, основанные на испускании излучения. Особенности валидации физико-химических методов
Методы анализа, основанные на испускании излучения. Особенности валидации физико-химических методов Линза. Виды линз
Линза. Виды линз Основні положення молекулярно-кінетичної теорії будови речовини та її дослідне обґрунтування. Маса та розміри атомів і молекул
Основні положення молекулярно-кінетичної теорії будови речовини та її дослідне обґрунтування. Маса та розміри атомів і молекул Физика – (греч . ta physika, от physis - природа), наука о природе. (Лекция 1)
Физика – (греч . ta physika, от physis - природа), наука о природе. (Лекция 1) Электростатическое поле в вакууме. Тема 1
Электростатическое поле в вакууме. Тема 1 Методы зондирования окружающей среды. Радиофизические характеристики атмосферы Земли
Методы зондирования окружающей среды. Радиофизические характеристики атмосферы Земли Двигатель внутреннего сгорания
Двигатель внутреннего сгорания Тонкостенные железобетонные оболочки
Тонкостенные железобетонные оболочки Нагрузки, действующие на элементы наземной космической инфраструктуры
Нагрузки, действующие на элементы наземной космической инфраструктуры Атмосферное давление на разных высотах. Манометры
Атмосферное давление на разных высотах. Манометры Рентгеновское излучение
Рентгеновское излучение Бұлшықет жиырылу биофизикасы
Бұлшықет жиырылу биофизикасы Измерение атмосферного давления. Барометр - анероид (урок 39)
Измерение атмосферного давления. Барометр - анероид (урок 39) Электромагнитные колебания. (Лекция 28)
Электромагнитные колебания. (Лекция 28) Электродвижущие силы при несинусоидальном поле
Электродвижущие силы при несинусоидальном поле Кручение стержней некруглого сечения
Кручение стержней некруглого сечения Магнитные наносистемы и наноматериалы
Магнитные наносистемы и наноматериалы система конструирования отопительных устройств
система конструирования отопительных устройств Презентация по физике "Електричний струм в рідинах" - скачать бесплатно
Презентация по физике "Електричний струм в рідинах" - скачать бесплатно Пути прохождения электрического тока через тело человека
Пути прохождения электрического тока через тело человека Три состояния вещества
Три состояния вещества Презентация по физике "Кинематика материальной точки." - скачать _
Презентация по физике "Кинематика материальной точки." - скачать _