Опорный конспект по изопроцессам. Автор презентации: Малышев Сергей Васильевич МКОУ Тойдинская СОШ Воронежская область Пан
Содержание
- 2. Цели: 1. Образовательные: познакомить учащихся с газовыми законами; обобщить и систематизировать знания учащихся о свойствах газов.
- 3. Что является объектом изучения МКТ? Идеальный газ. Что в МКТ называется идеальным газом? Идеальный газ –
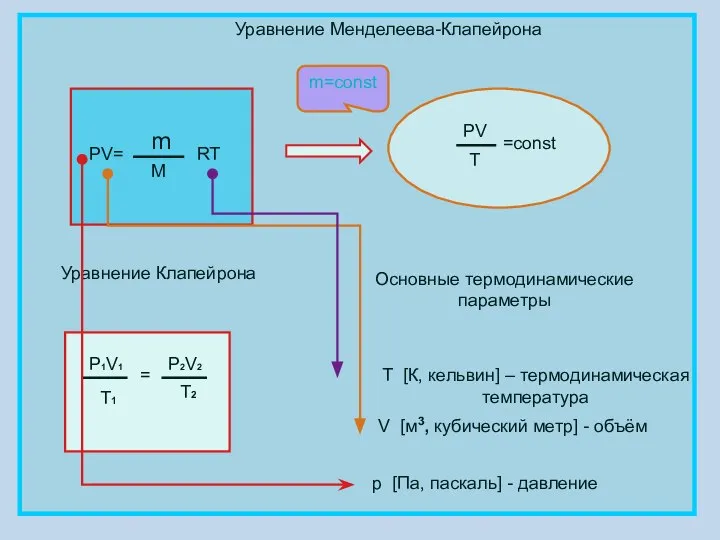
- 4. Уравнение Менделеева-Клапейрона PV= m M RT PV T =const Уравнение Клапейрона P1V1 T1 = P2V2 T2
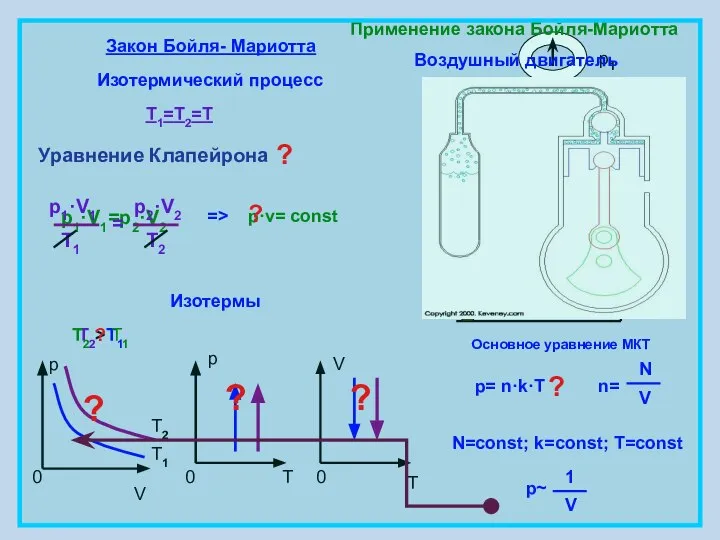
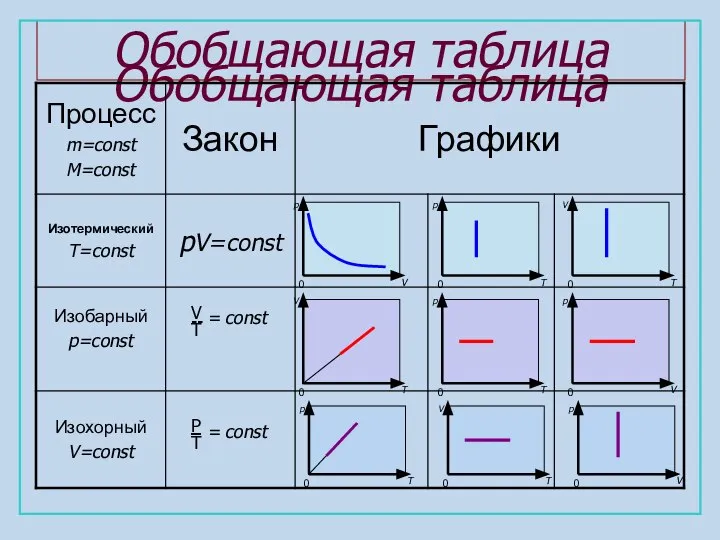
- 5. Закон Бойля- Мариотта Изотермический процесс T1=T2=T p·v= const p1·V1=p2·V2 p V 0 p 0 T V
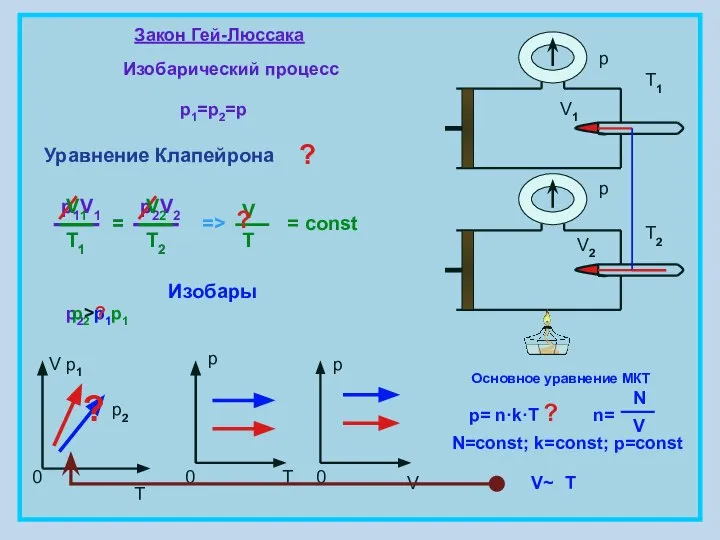
- 6. Закон Гей-Люссака Изобарический процесс p1=p2=p = const V T 0 p 0 T p 0 V
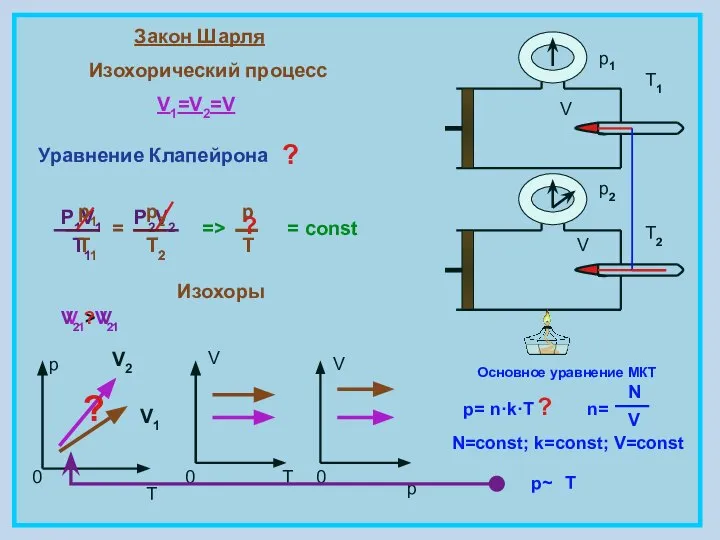
- 7. Закон Шарля Изохорический процесс V1=V2=V = const p T 0 V 0 T V 0 p
- 8. Обобщающая таблица Обобщающая таблица V T -- = const P T const =
- 9. Прошу Вас оценить урок, насколько он был успешен. Мне все понравилось Мне ничего не понравилось Мне
- 11. Скачать презентацию



 ТЕПЛОМАССОПЕРЕНОС В ЯДЕРНО-ЭНЕРГЕТИЧЕСКИХ УСТАНОВКАХ
ТЕПЛОМАССОПЕРЕНОС В ЯДЕРНО-ЭНЕРГЕТИЧЕСКИХ УСТАНОВКАХ  Электромагнетизм
Электромагнетизм Развитие представлений о свете
Развитие представлений о свете Пара сил. (Лекция 3)
Пара сил. (Лекция 3) Принцип действия ламп накаливания это преобразование электрической энергии в световую энергию. Вольфрамовая нить разогревае
Принцип действия ламп накаливания это преобразование электрической энергии в световую энергию. Вольфрамовая нить разогревае Термодинамическая картина мира
Термодинамическая картина мира Выполнила: Пузырёва Э.Э. ученица 11 класса. Руководитель: Бекетова Т.Г. учитель физики
Выполнила: Пузырёва Э.Э. ученица 11 класса. Руководитель: Бекетова Т.Г. учитель физики  Геометрическая оптика. (Лекция 4)
Геометрическая оптика. (Лекция 4) Вязкость нефти и нефтепродуктов
Вязкость нефти и нефтепродуктов Коливальні рухи. Гармонічні коливання
Коливальні рухи. Гармонічні коливання Давление. Сила давления. Билет 18
Давление. Сила давления. Билет 18 Спектральдік және басқа да оптикалық әдістер
Спектральдік және басқа да оптикалық әдістер ravnoperemennoe_dvizhenie
ravnoperemennoe_dvizhenie Общая характеристика электротехнических сталей
Общая характеристика электротехнических сталей Основы специальной теории относительности © В.Е.Фрадкин, 2004
Основы специальной теории относительности © В.Е.Фрадкин, 2004 Магнітне поле. Магнітний потік
Магнітне поле. Магнітний потік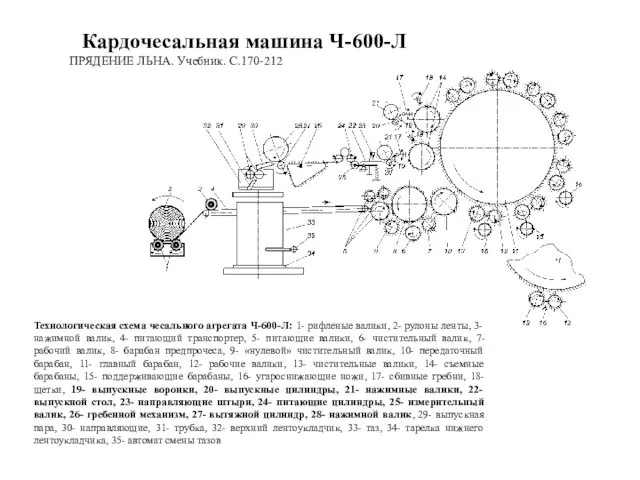 Кардочесальная машина Ч-600-Л
Кардочесальная машина Ч-600-Л Распределение напряжений в швах и сопротивление усталости сварных соединений
Распределение напряжений в швах и сопротивление усталости сварных соединений Температура
Температура Применение тепловых насосов в теплоэнергетике ООО «ПСП Энергия» ООО «Климатек» 2008 г.
Применение тепловых насосов в теплоэнергетике ООО «ПСП Энергия» ООО «Климатек» 2008 г. Стоячая волна
Стоячая волна  Heat transfer
Heat transfer Работа и мощность электрического тока
Работа и мощность электрического тока Виды сборки. Виды соединений и технология их сборки
Виды сборки. Виды соединений и технология их сборки Открытие фотоэффекта. 1886 – 1889 года,
Открытие фотоэффекта. 1886 – 1889 года, ААМЖЗ жағдайында металл сымдарды үздіксіз орауға арналған электржетегін жасау
ААМЖЗ жағдайында металл сымдарды үздіксіз орауға арналған электржетегін жасау Презентация по физике "Физические явления в литературных произведениях" - скачать
Презентация по физике "Физические явления в литературных произведениях" - скачать 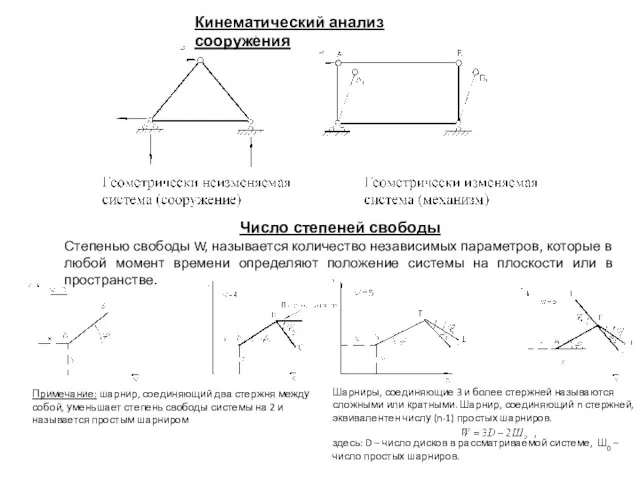 Кинематический анализ сооружения
Кинематический анализ сооружения