Содержание
- 2. Аліциклічні вуглеводні ще називаються циклопарафінами, циклоалканами або, якщо вони містять в циклі 5-6 атомів вуглецю –
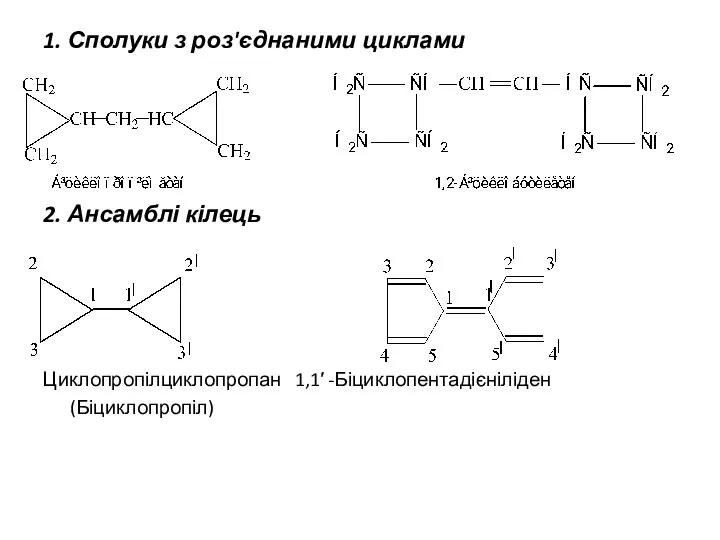
- 3. 2. Ансамблі кілець Циклопропілциклопропан 1,1′ -Біциклопентадієніліден (Біциклопропіл) 1. Сполуки з роз'єднаними циклами
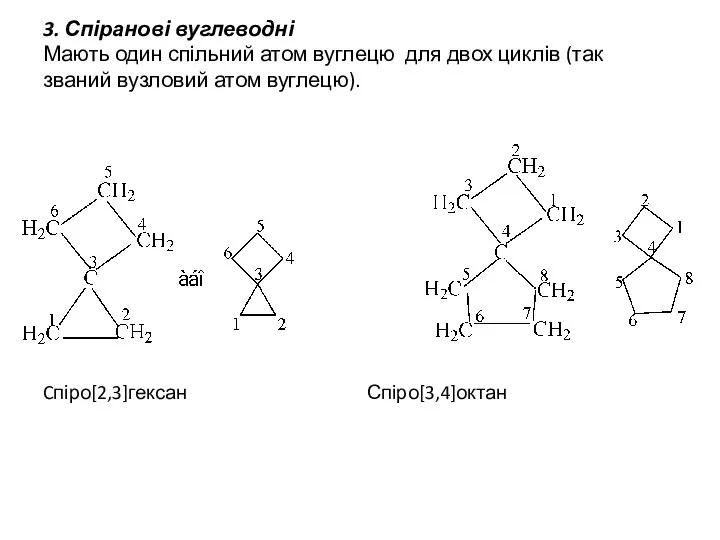
- 4. 3. Спіранові вуглеводні Мають один спільний атом вуглецю для двох циклів (так званий вузловий атом вуглецю).
- 5. 4. Місткові вуглеводні Це сполуки, які мають два або більше спільних (вузлових) атомів вуглецю Біцикло[3,2,1]октан 2-Метилбіцикло[3,3,0]октан
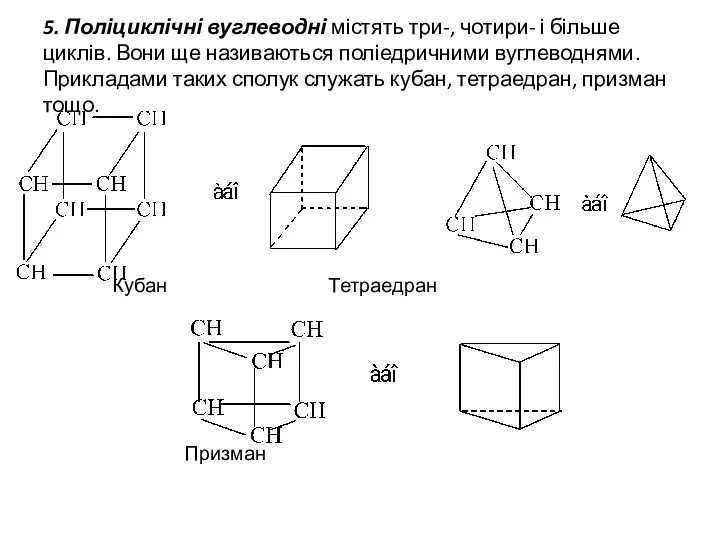
- 6. 5. Поліциклічні вуглеводні містять три-, чотири- і більше циклів. Вони ще називаються поліедричними вуглеводнями. Прикладами таких
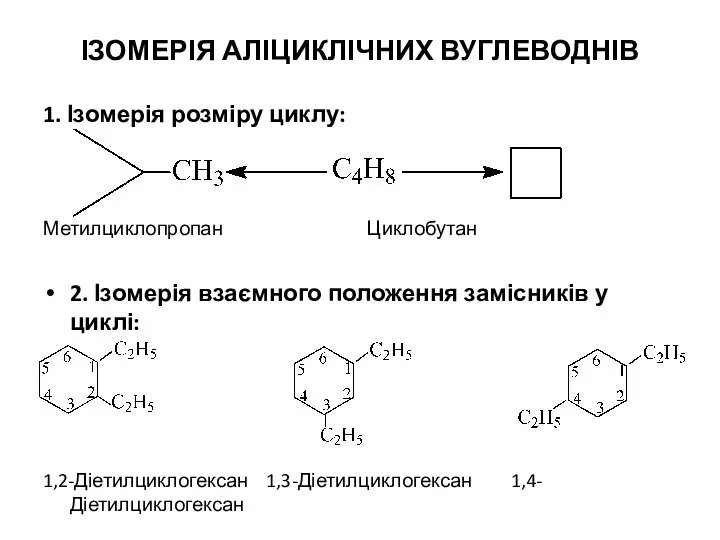
- 7. ІЗОМЕРІЯ АЛІЦИКЛІЧНИХ ВУГЛЕВОДНІВ 1. Ізомерія розміру циклу: Метилциклопропан Циклобутан 2. Ізомерія взаємного положення замісників у циклі:
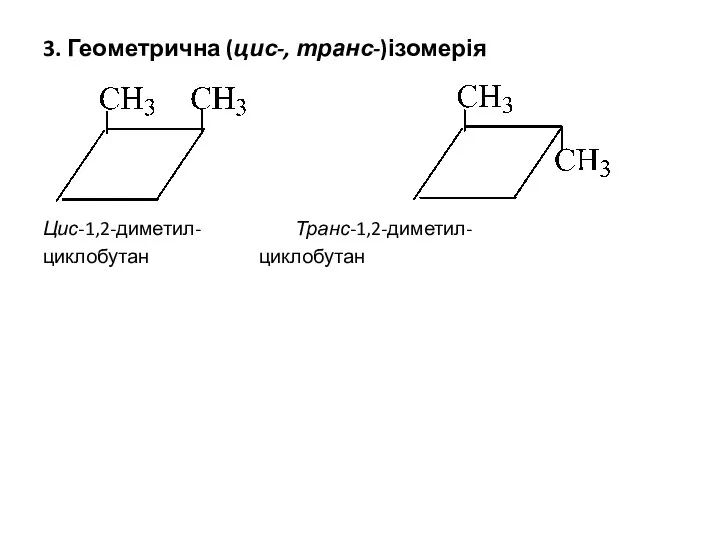
- 8. 3. Геометрична (цис-, транс-)ізомерія Цис-1,2-диметил- Транс-1,2-диметил- циклобутан циклобутан
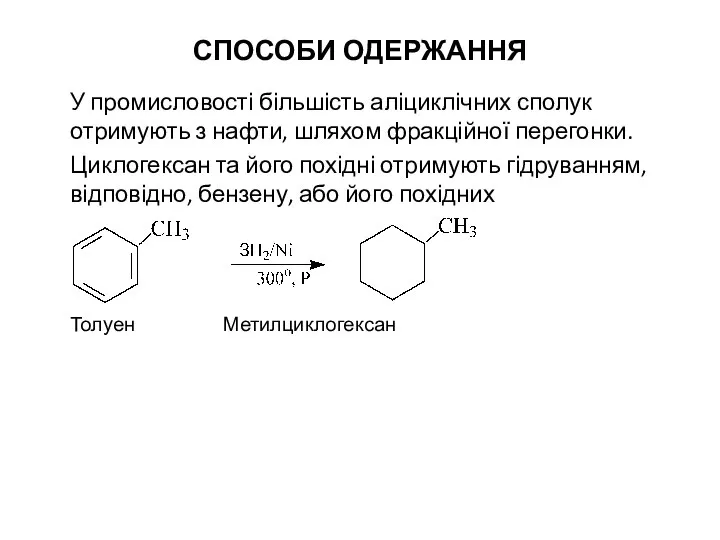
- 9. СПОСОБИ ОДЕРЖАННЯ У промисловості більшість аліциклічних сполук отримують з нафти, шляхом фракційної перегонки. Циклогексан та його
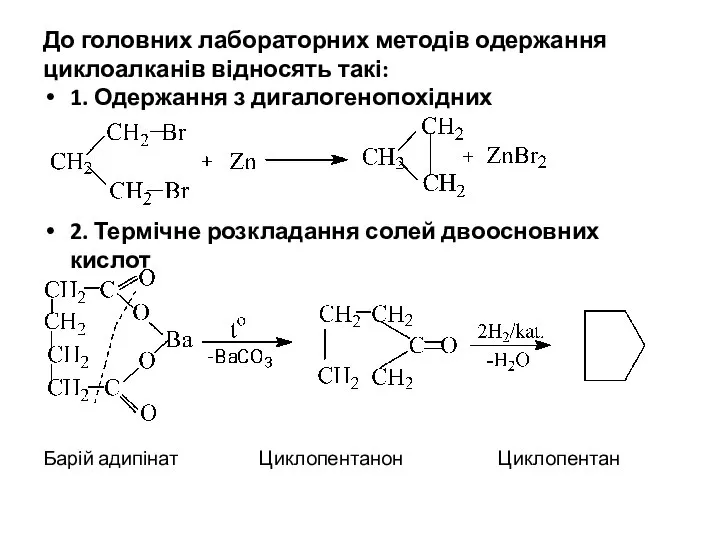
- 10. До головних лабораторних методів одержання циклоалканів відносять такі: 1. Одержання з дигалогенопохідних 2. Термічне розкладання солей
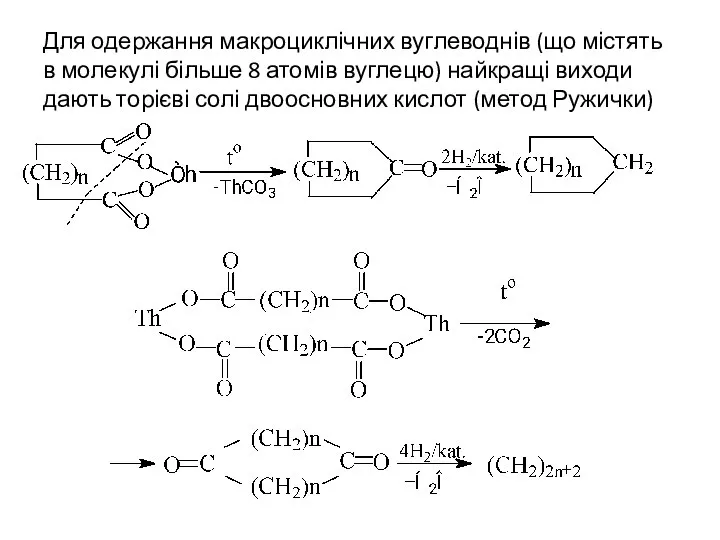
- 11. Для одержання макроциклічних вуглеводнів (що містять в молекулі більше 8 атомів вуглецю) найкращі виходи дають торієві
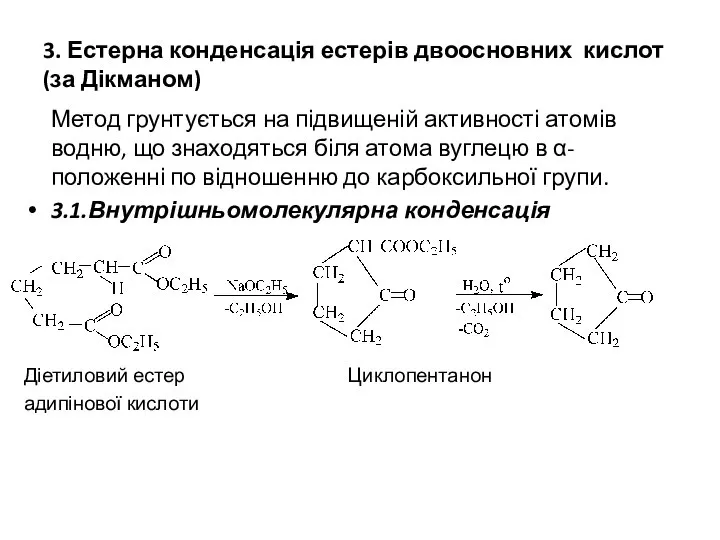
- 12. 3. Естерна конденсація естерів двоосновних кислот (за Дікманом) Метод грунтується на підвищеній активності атомів водню, що
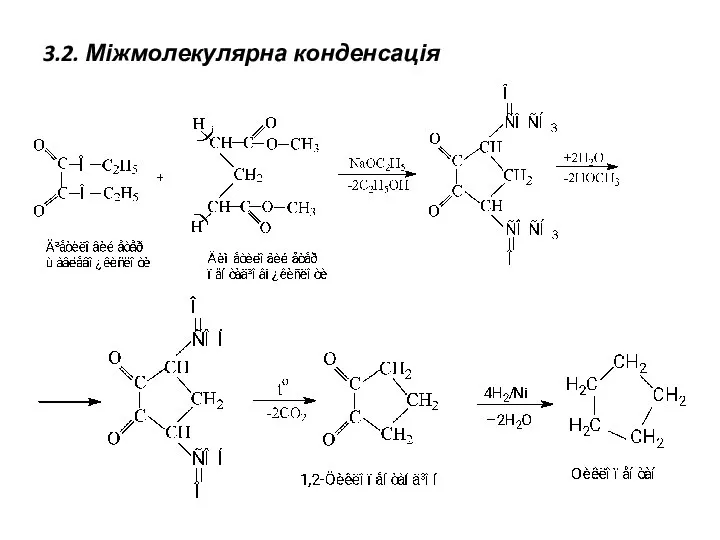
- 13. 3.2. Міжмолекулярна конденсація
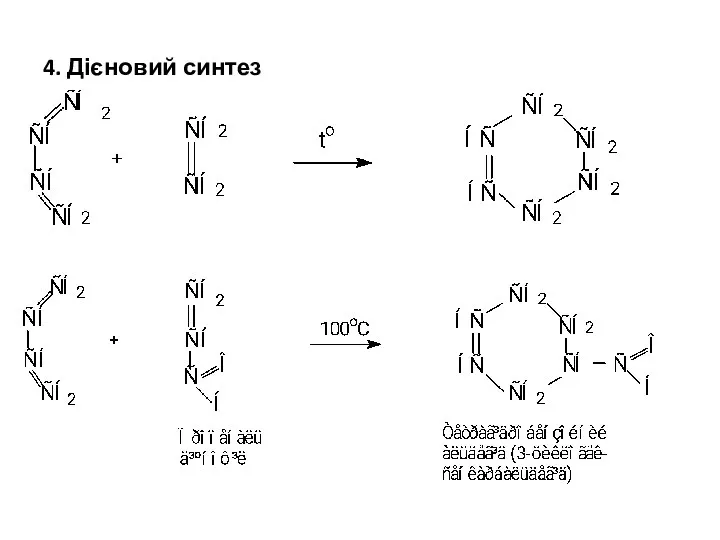
- 14. 4. Дієновий синтез
- 15. ФІЗИЧНІ ТА ХІМІЧНІ ВЛАСТИВОСТІ Циклоалкани (С3-С4) - це гази, (С5-С10) - безбарвні рідини, котрі не розчиняються
- 16. Відносну стійкість циклоалканів Байєр пояснював напругою, що виникає в циклі при його утворенні (теорія напружень Байера).
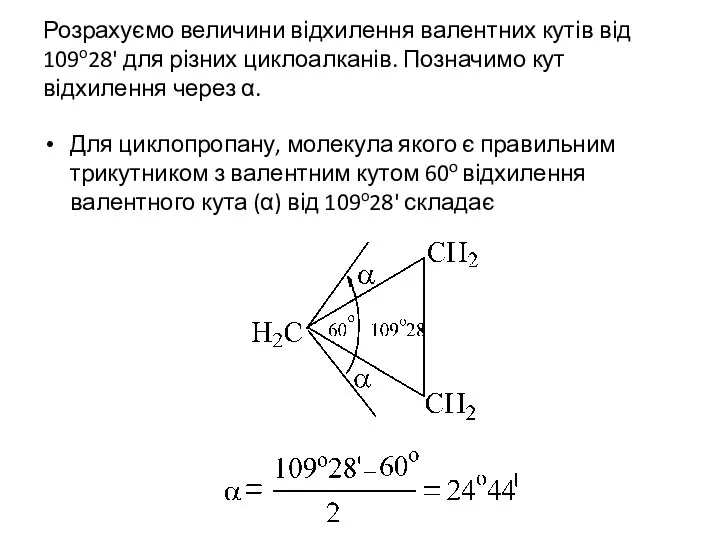
- 17. Розрахуємо величини відхилення валентних кутів від 109o28' для різних циклоалканів. Позначимо кут відхилення через α. Для
- 18. Для циклобутану Для циклопентану α = 0o4', для циклогексану (α = -5o16') і по мірі збільшення
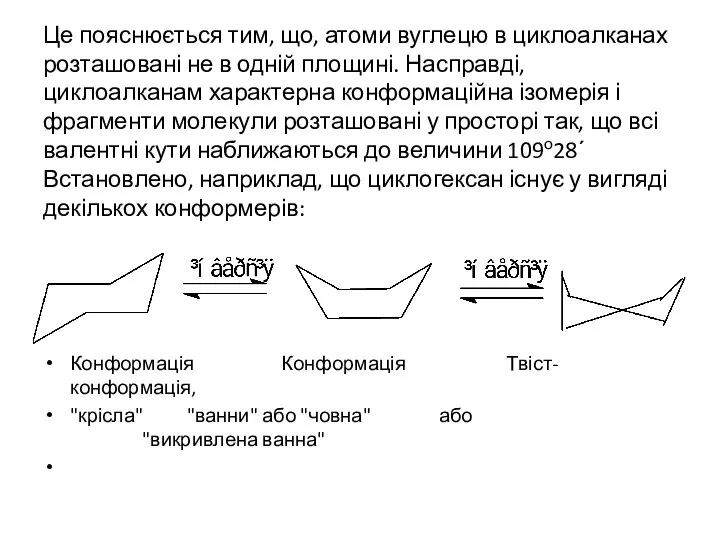
- 19. Це пояснюється тим, що, атоми вуглецю в циклоалканах розташовані не в одній площині. Насправді, циклоалканам характерна
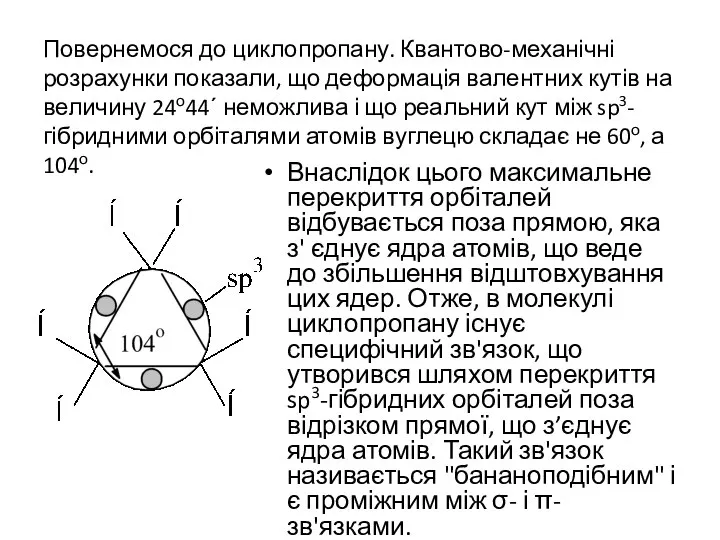
- 20. Повернемося до циклопропану. Квантово-механічні розрахунки показали, що деформація валентних кутів на величину 24о44΄ неможлива і що
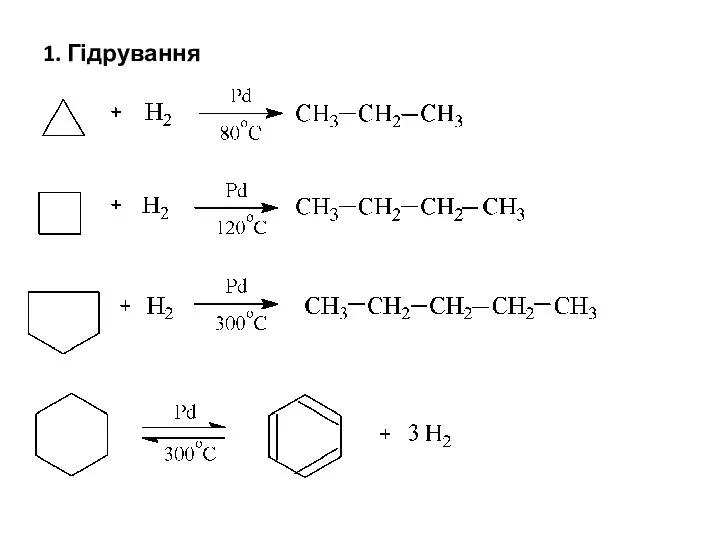
- 21. 1. Гідрування
- 22. Як видно зі схеми, циклопропан гідрується доволі легко, гідрування циклобутану вимагає жорсткіших умов, циклопентан розщеплюється воднем
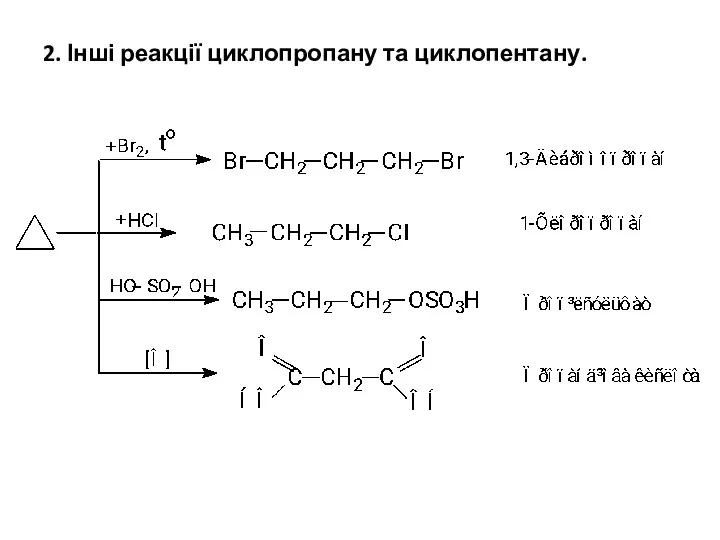
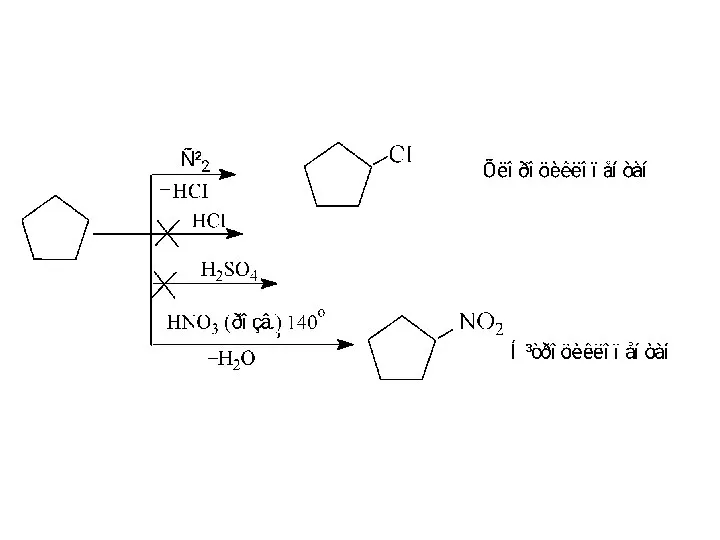
- 23. 2. Інші реакції циклопропану та циклопентану.
- 25. Порівняння цих двох схем показує, що циклопропан легко вступає в реакції приєднання з розривом напруженого трьохчленного
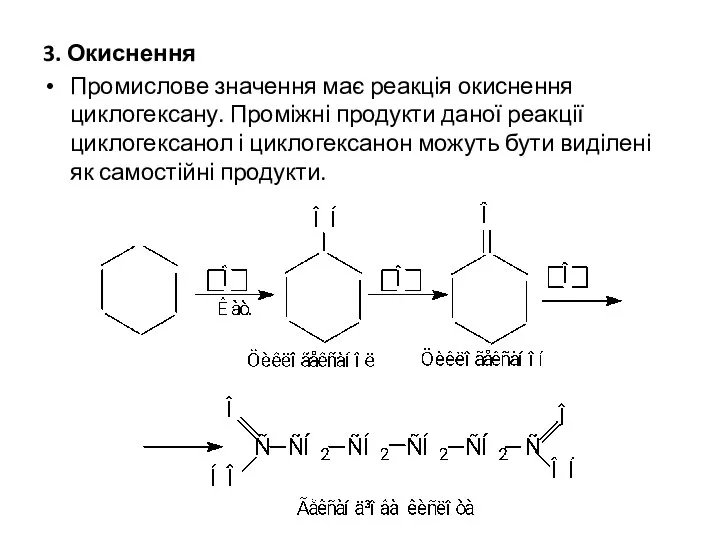
- 26. 3. Окиснення Промислове значення має реакція окиснення циклогексану. Проміжні продукти даної реакції циклогексанол і циклогексанон можуть
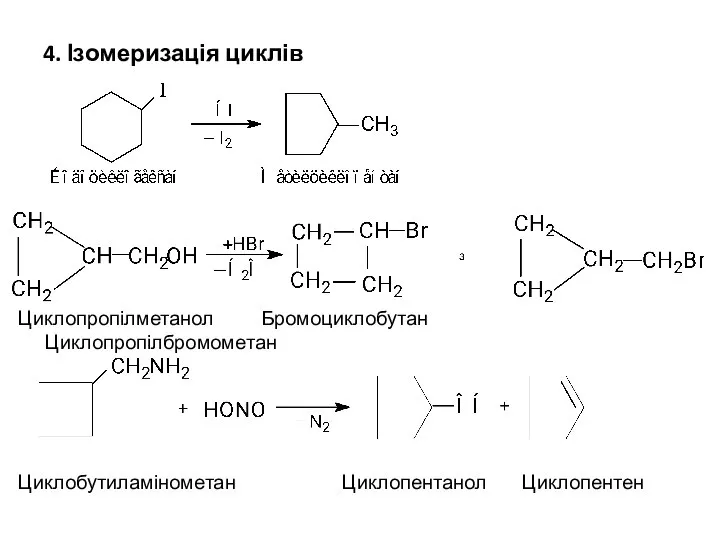
- 27. 4. Ізомеризація циклів Циклопропілметанол Бромоциклобутан Циклопропілбромометан Циклобутиламінометан Циклопентанол Циклопентен
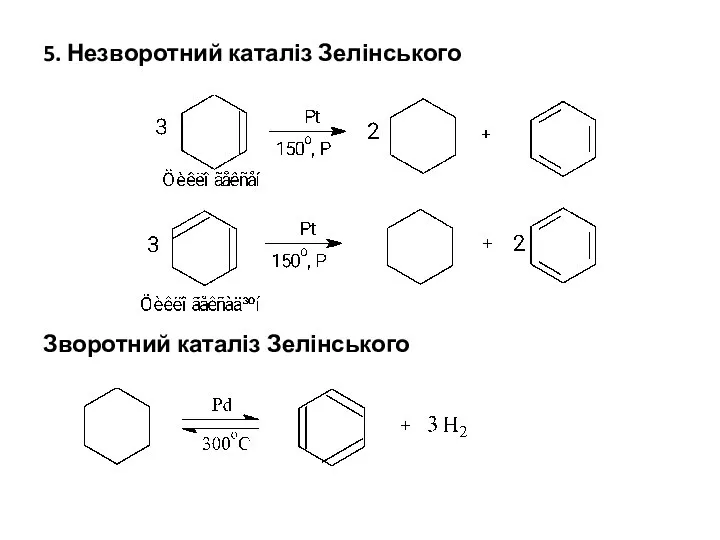
- 28. 5. Незворотний каталіз Зелінського Зворотний каталіз Зелінського
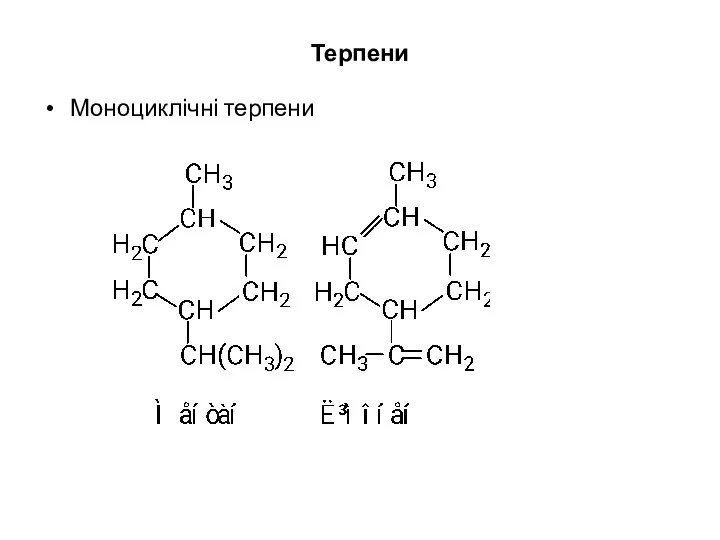
- 29. Терпени Моноциклічні терпени
- 31. Скачать презентацию

![4. Місткові вуглеводні Це сполуки, які мають два або більше спільних (вузлових) атомів вуглецю Біцикло[3,2,1]октан 2-Метилбіцикло[3,3,0]октан](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396278/slide-4.jpg)





 Обзор свойств неметаллов.. Окислительно-восстановительные свойства типичных неметаллов
Обзор свойств неметаллов.. Окислительно-восстановительные свойства типичных неметаллов Яковлева Татьяна Алексеевна Ярославль, 2009 г.
Яковлева Татьяна Алексеевна Ярославль, 2009 г.  Природный газ
Природный газ Роль йода в организме
Роль йода в организме Спиртовое, масляное и кисломолочное брожение
Спиртовое, масляное и кисломолочное брожение Вермикулит. Технические характеристики
Вермикулит. Технические характеристики Правила безпечного використання засобів побутової хімії.
Правила безпечного використання засобів побутової хімії.  Кислород
Кислород Фосфорорганические соединения
Фосфорорганические соединения Алкадиены. Состав и строение
Алкадиены. Состав и строение Активна реакція водних розчинів
Активна реакція водних розчинів Система приготовления и подачи реагентов KPJ
Система приготовления и подачи реагентов KPJ Презентация по химии Количественный анализ Химические методы анализа
Презентация по химии Количественный анализ Химические методы анализа  Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Кислотность и основность органических соединений. Реакционная способность спиртов, фенолов, тиолов и аминов
Кислотность и основность органических соединений. Реакционная способность спиртов, фенолов, тиолов и аминов Бор и его соединения
Бор и его соединения Сероводород. Сернистый водород, сульфид водорода, дигидросульфид
Сероводород. Сернистый водород, сульфид водорода, дигидросульфид Презентация по Химии "Дисперсные системы" - скачать смотреть
Презентация по Химии "Дисперсные системы" - скачать смотреть  Atomic structure. Introduction
Atomic structure. Introduction Нафта та її переробка
Нафта та її переробка  Особенности сжигания твердого, жидкого и газообразного топлива
Особенности сжигания твердого, жидкого и газообразного топлива Аттестационная работа. Развитие творческих возможностей учащихся через организацию исследовательской работы по химии
Аттестационная работа. Развитие творческих возможностей учащихся через организацию исследовательской работы по химии Презентация Типы изомерий 10 класс
Презентация Типы изомерий 10 класс Кремний
Кремний Хроматографія. Мікрогетерогенні дисперсні системи
Хроматографія. Мікрогетерогенні дисперсні системи Третья группа ПС
Третья группа ПС Презентацию подготовила: Учитель химии высшей категории Отрошко Елена Александровна МОУ СОШ № 6 Ст. Старотитаровской Темрюкс
Презентацию подготовила: Учитель химии высшей категории Отрошко Елена Александровна МОУ СОШ № 6 Ст. Старотитаровской Темрюкс Липиды молока и молочных продуктов. Группы липидов
Липиды молока и молочных продуктов. Группы липидов