Содержание
- 2. Алкадиены - ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи между атомами углерода
- 3. Алкадиены с кумулированным расположением двойных связей (аллены) Углеводороды содержащие две двойные связи ,находящиеся возле соседних атомов
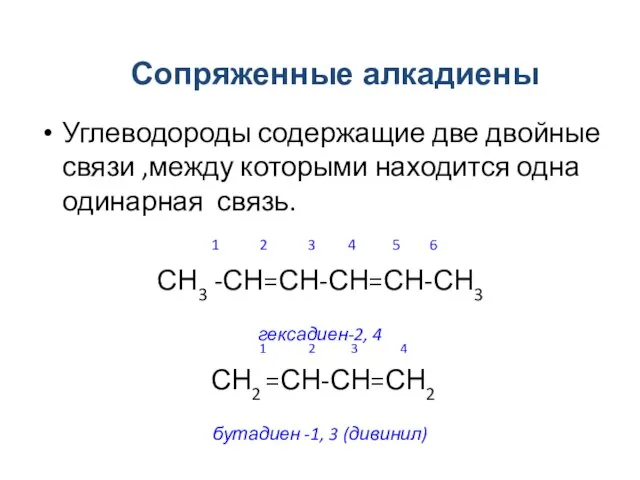
- 4. Углеводороды содержащие две двойные связи ,между которыми находится одна одинарная связь. 1 2 3 4 5
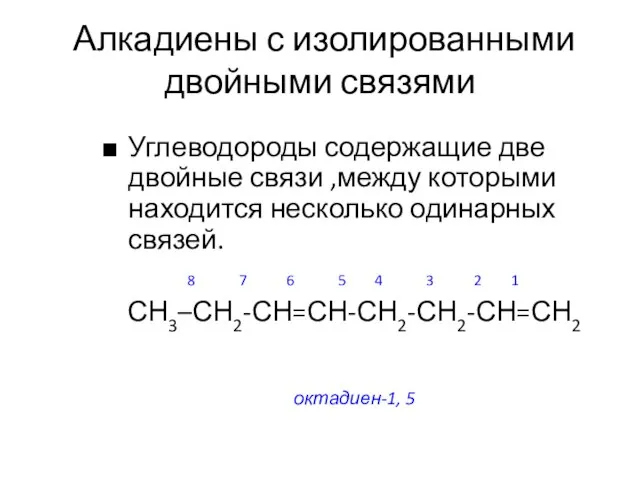
- 5. Алкадиены с изолированными двойными связями Углеводороды содержащие две двойные связи ,между которыми находится несколько одинарных связей.
- 6. Номенклатура алкадиенов Правила: 1. Главная цепь должна содержать обе двойные связи. 2. Нумерацию ведут с того
- 7. ИЗОМЕРИЯ АЛКАДИЕНОВ 1. Структурная: а) изомерия углеродного скелета б) изомерия положения двойных связей. 2. Пространственная: а)цис-транс
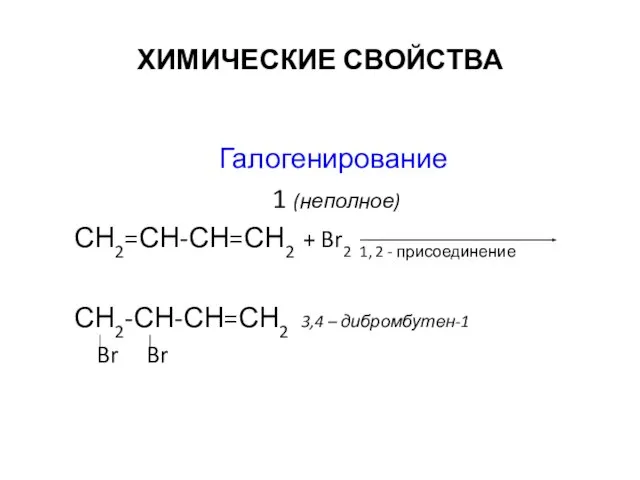
- 8. ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 1 (неполное) СН2=СН-СН=СН2 + Br2 1, 2 - присоединение СН2-СН-СН=СН2 3,4 – дибромбутен-1
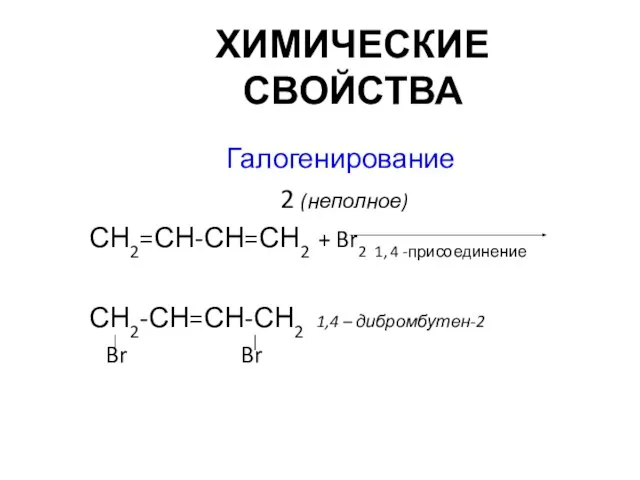
- 9. ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 2 (неполное) СН2=СН-СН=СН2 + Br2 1, 4 -присоединение СН2-СН=СН-СН2 1,4 – дибромбутен-2 Br
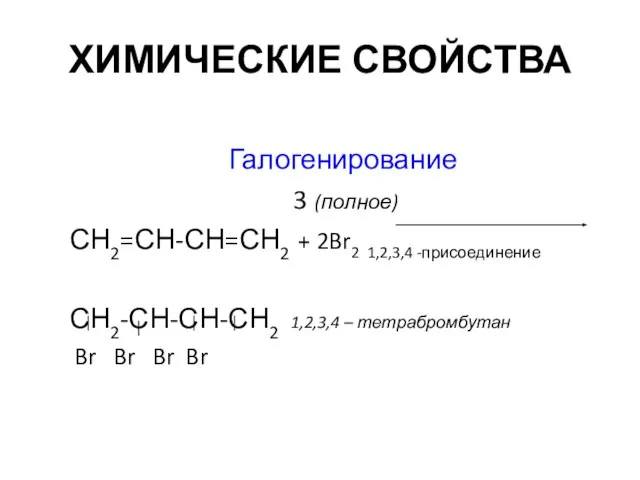
- 10. ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 3 (полное) СН2=СН-СН=СН2 + 2Br2 1,2,3,4 -присоединение СН2-СН-СН-СН2 1,2,3,4 – тетрабромбутан Br Br
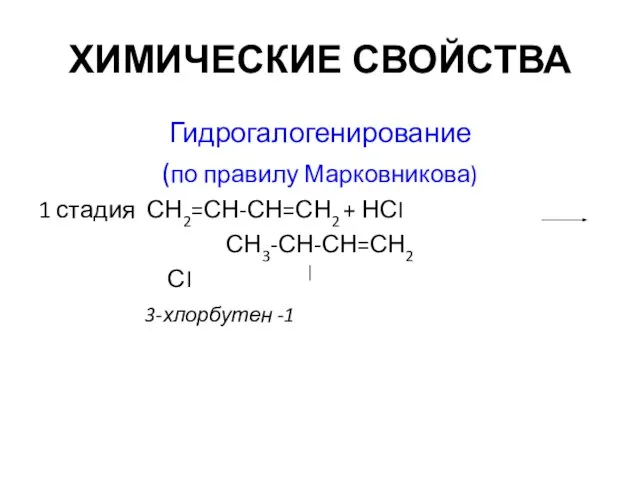
- 11. ХИМИЧЕСКИЕ СВОЙСТВА Гидрогалогенирование (по правилу Марковникова) 1 стадия СН2=СН-СН=СН2 + НСI СН3-СН-СН=СН2 СI 3-хлорбутен -1
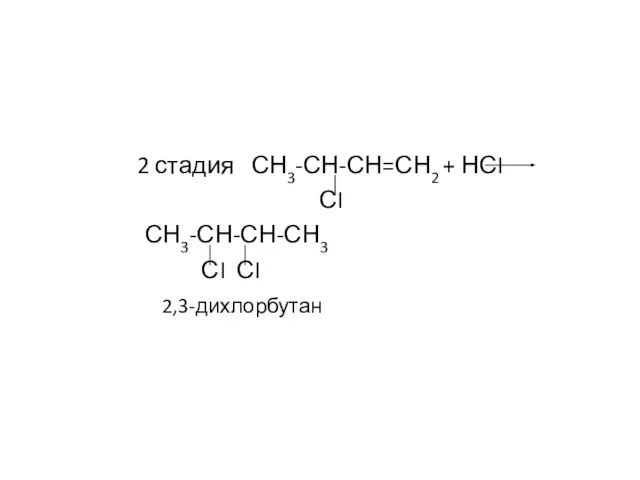
- 12. 2 стадия СН3-СН-СН=СН2 + НСI СI СН3-СН-СН-СН3 СI СI 2,3-дихлорбутан
- 13. ХИМИЧЕСКИЕ СВОЙСТВА Горение 2СН2=СН-СН=СН2 + 11О2 8СО2 + 6Н2О или 2С4Н6 + 11О2 8СО2 + 6Н2О
- 14. ХИМИЧЕСКИЕ СВОЙСТВА Полимеризация Полимеризация диеновых УВ приводит к образованию каучуков – полимеров, обладающих высокой эластичностью. бутадиен
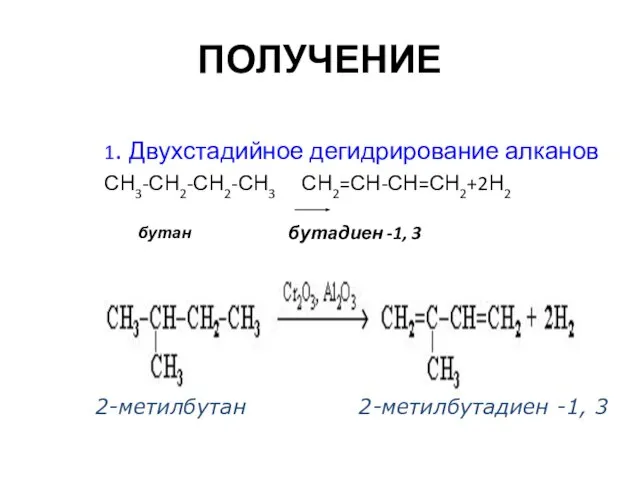
- 15. ПОЛУЧЕНИЕ 1. Двухстадийное дегидрирование алканов СН3-СН2-СН2-СН3 СН2=СН-СН=СН2+2Н2 бутан бутадиен -1, 3 2-метилбутан 2-метилбутадиен -1, 3
- 16. ПОЛУЧЕНИЕ 2. Синтез дивинила по методу С. В. Лебедева
- 17. Каучуки Каучуки — натуральные или синтетические материалы, характеризующиеся эластичностью, водонепроницаемостью и электроизоляционными свойствами, из которых путём
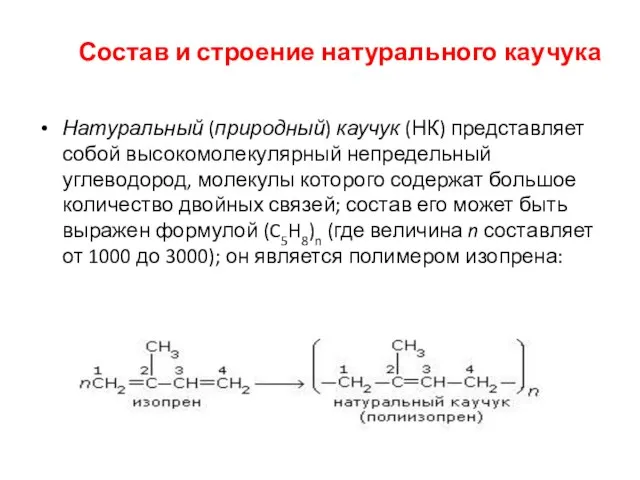
- 18. Состав и строение натурального каучука Натуральный (природный) каучук (НК) представляет собой высокомолекулярный непредельный углеводород, молекулы которого
- 20. Скачать презентацию








 Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ»
Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ» Анализ качества лекарственных средств, производных алифатических и ароматических аминов
Анализ качества лекарственных средств, производных алифатических и ароматических аминов Щелочные металлы
Щелочные металлы Презентация по Химии "Природные источники углеводородов" - скачать смотреть
Презентация по Химии "Природные источники углеводородов" - скачать смотреть  Кислотность и основность органических соединений. Реакционная способность спиртов, фенолов, тиолов и аминов
Кислотность и основность органических соединений. Реакционная способность спиртов, фенолов, тиолов и аминов Презентация по Химии "Классификация веществ" - скачать смотреть
Презентация по Химии "Классификация веществ" - скачать смотреть  Тотығутотықсыздану титрлеу әдістері. Дәріс № 7
Тотығутотықсыздану титрлеу әдістері. Дәріс № 7 Хімія в житті суспільства
Хімія в житті суспільства  Химическое сопротивление эластомеров. Резины. Дерево
Химическое сопротивление эластомеров. Резины. Дерево Федосовой Таисии 8 «в»
Федосовой Таисии 8 «в» Коррозия металлов
Коррозия металлов Химиялық қару
Химиялық қару Твердотільний ямр
Твердотільний ямр Жири (тригліцериди)
Жири (тригліцериди) Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ
Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ Фазовые равновесия в растворах
Фазовые равновесия в растворах Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Индикаторы
Индикаторы Проектная работа «Кристаллизация»
Проектная работа «Кристаллизация» Углеводороды. Алкены, этилен
Углеводороды. Алкены, этилен Презентация по Химии "аавв" - скачать смотреть
Презентация по Химии "аавв" - скачать смотреть  Защита металлоконструкций от коррозии
Защита металлоконструкций от коррозии Общие свойства металлов. Сплавы
Общие свойства металлов. Сплавы Презентация по Химии "Термическая и химико-термическая обработка металлов" - скачать смотреть
Презентация по Химии "Термическая и химико-термическая обработка металлов" - скачать смотреть  Рибофлавин - «витамин красоты»
Рибофлавин - «витамин красоты» Биохимия человека
Биохимия человека Цветные реакции белков Качественные реакции на остатки аминокислот
Цветные реакции белков Качественные реакции на остатки аминокислот Адам ағзасында кездесетін химиялық элементтер
Адам ағзасында кездесетін химиялық элементтер