Содержание
- 2. (иначе насыщенные углеводороды, парафины, алифатические соединения) — ациклические углеводороды линейного или разветвленного строения, содержащие только простые
- 3. Углеводороды. Предельные (насыщенные, алканы) Алканы - углеводороды, состав которых выражается общей формулой CnH2n+2, где n –
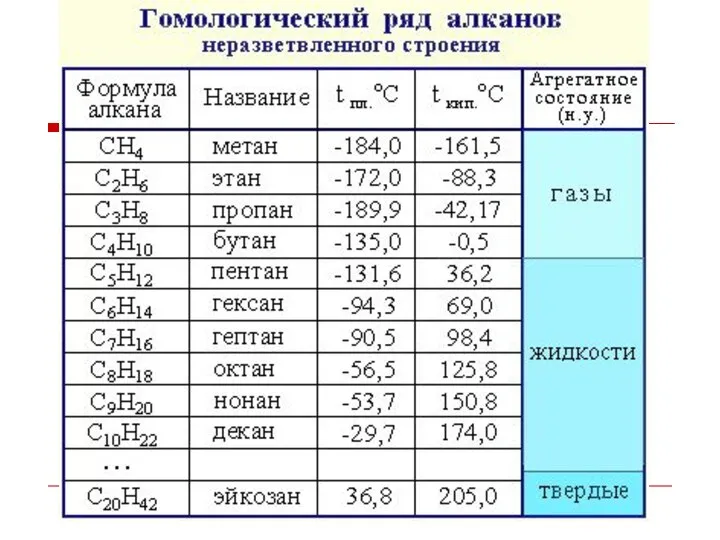
- 5. Физические свойства Температуры плавления и кипения увеличиваются с молекулярной массой и длиной главной углеродной цепи При
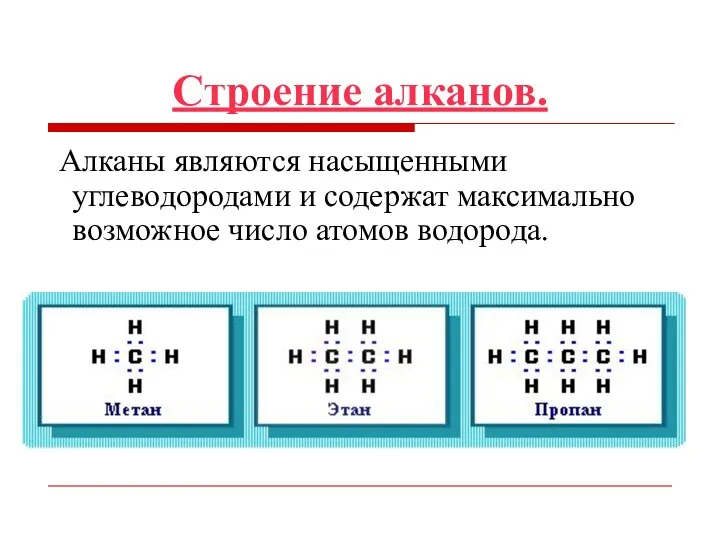
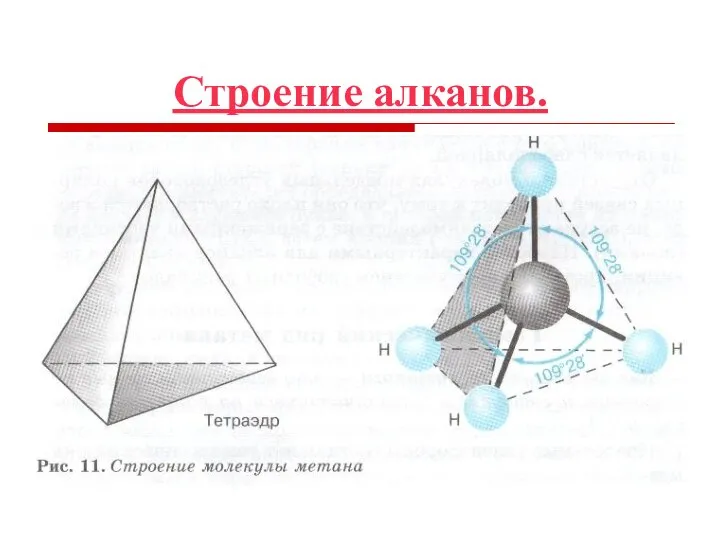
- 6. Строение алканов. Алканы являются насыщенными углеводородами и содержат максимально возможное число атомов водорода.
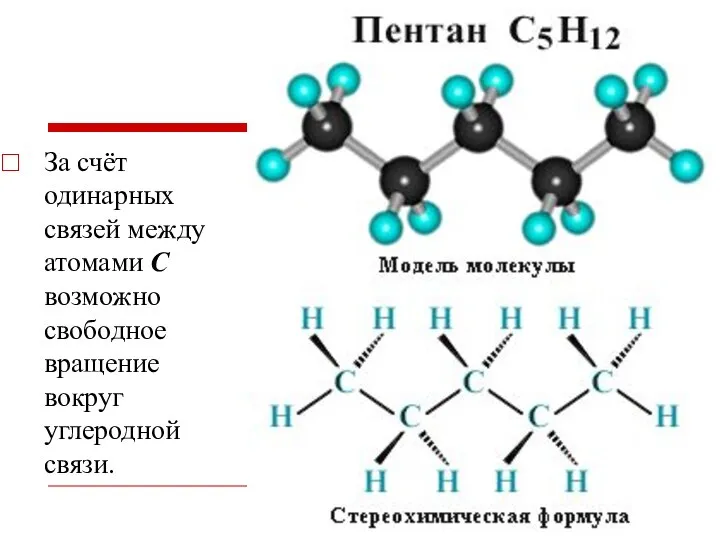
- 7. За счёт одинарных связей между атомами С возможно свободное вращение вокруг углеродной связи.
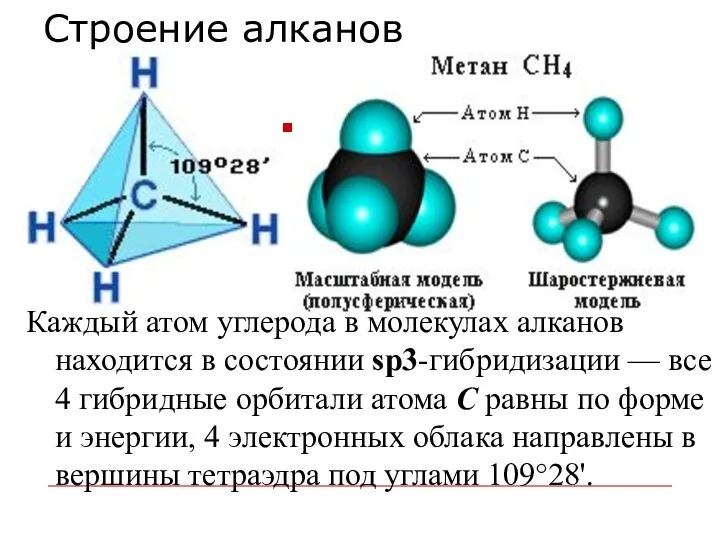
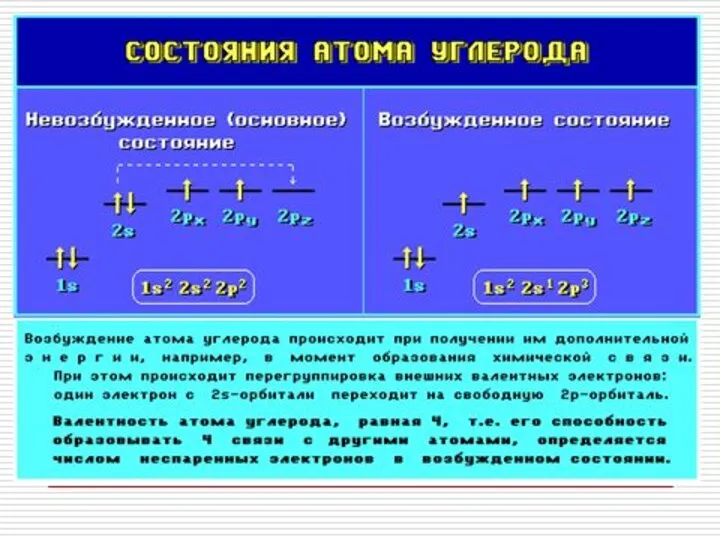
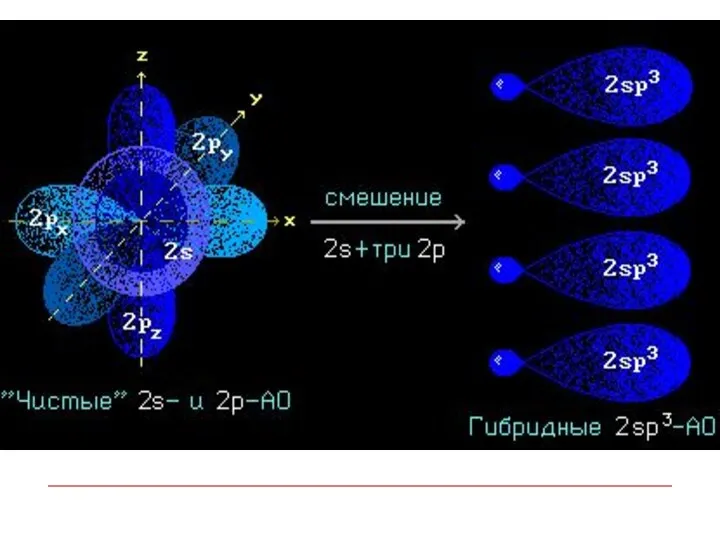
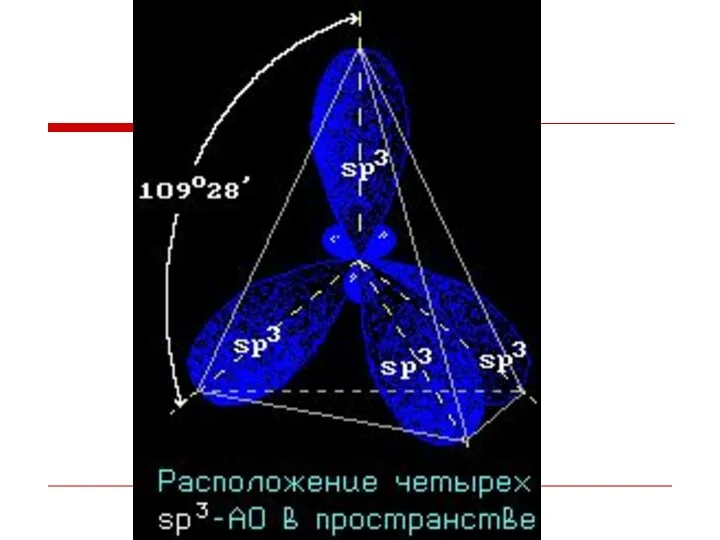
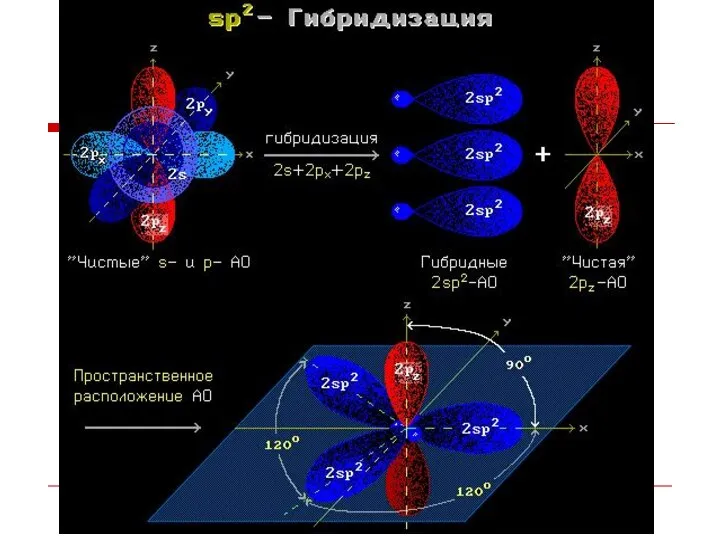
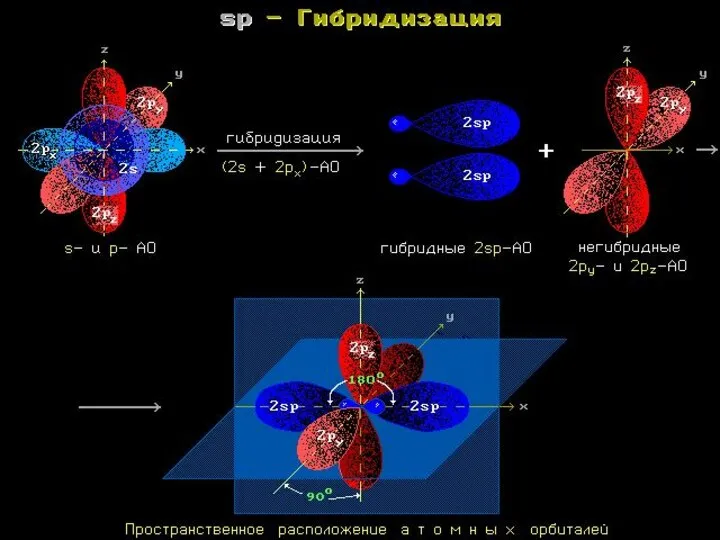
- 8. Строение алканов Каждый атом углерода в молекулах алканов находится в состоянии sp3-гибридизации — все 4 гибридные
- 9. Строение алканов.
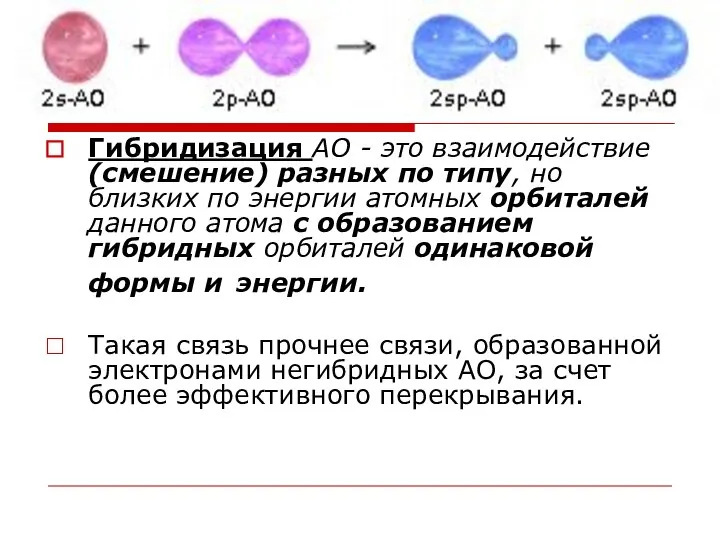
- 11. Гибридизация АО - это взаимодействие (смешение) разных по типу, но близких по энергии атомных орбиталей данного
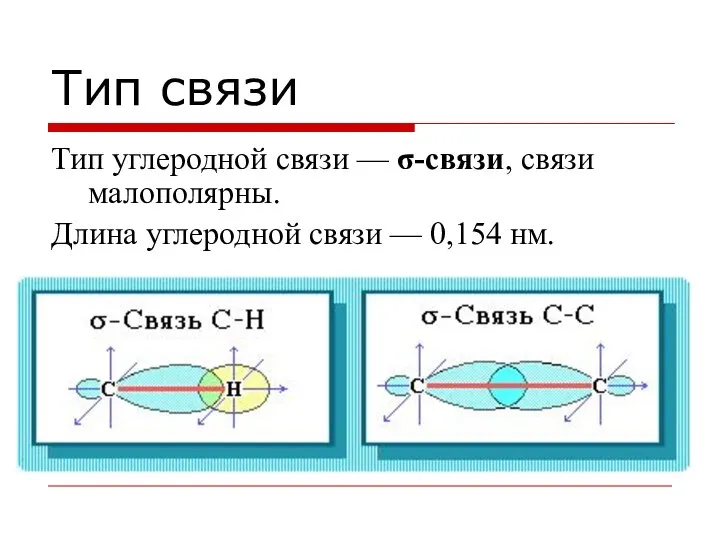
- 14. Тип связи Тип углеродной связи — σ-связи, связи малополярны. Длина углеродной связи — 0,154 нм.
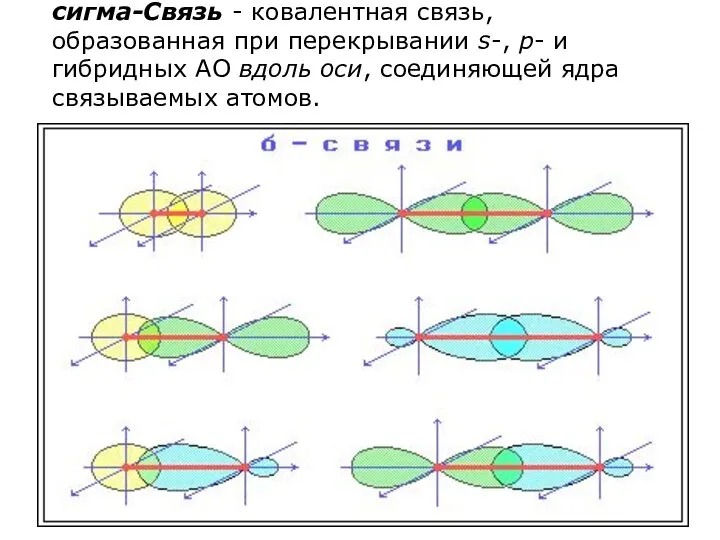
- 15. сигма-Связь - ковалентная связь, образованная при перекрывании s-, p- и гибридных АО вдоль оси, соединяющей ядра
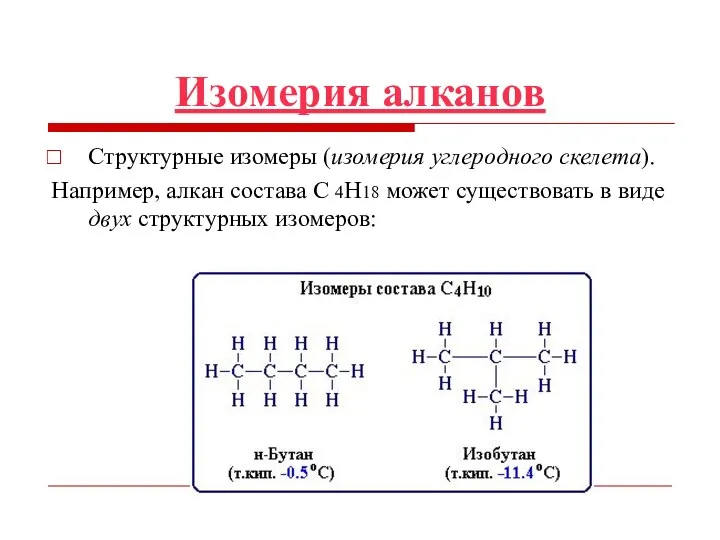
- 16. Изомерия алканов Структурные изомеры (изомерия углеродного скелета). Например, алкан состава C 4H18 может существовать в виде
- 17. Получение алканов В промышленности: извлекают из природного газа, нефти; синтез из простых веществ (проходит при повышенной
- 18. Получение алканов 2. Гидрирование непредельных углеводородов Из алкенов CnH2n + H2→ CnH2n+2 Из алкинов CnH2n-2 +
- 19. Получение алканов В лаборатории: 1) Метан получают гидролизом карбида алюминия: Al₄C₃ +12H₂O→ 4Al(OH)₃↓+3CH₄↑
- 20. Получение алканов В лаборатории: 2) реакция Вюрца: t CH₃Cl + 2Na + ClCH₃ →C₂H₆ + +
- 21. Химические свойства алканов Так как все связи насыщены до предела, для алканов характерны реакции Разложение (крекинг)
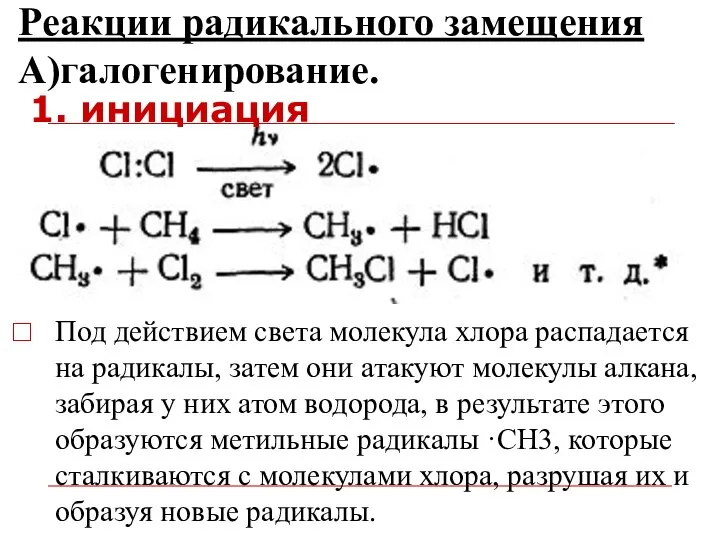
- 22. Под действием света молекула хлора распадается на радикалы, затем они атакуют молекулы алкана, забирая у них
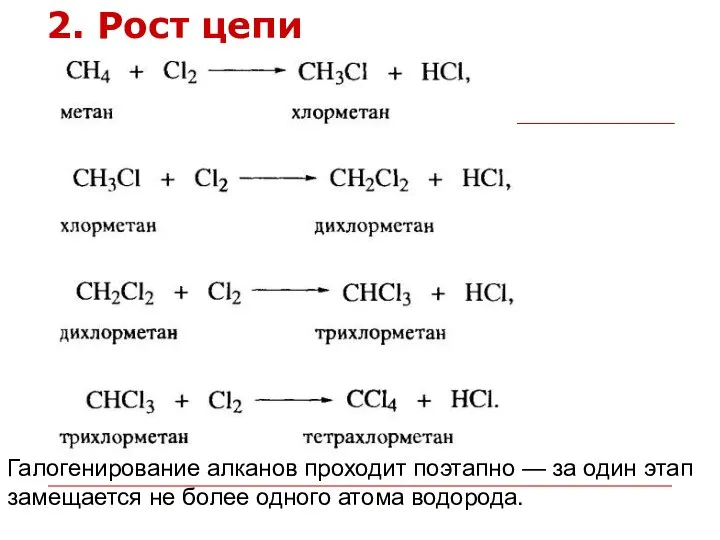
- 23. Галогенирование алканов проходит поэтапно — за один этап замещается не более одного атома водорода. 2. Рост
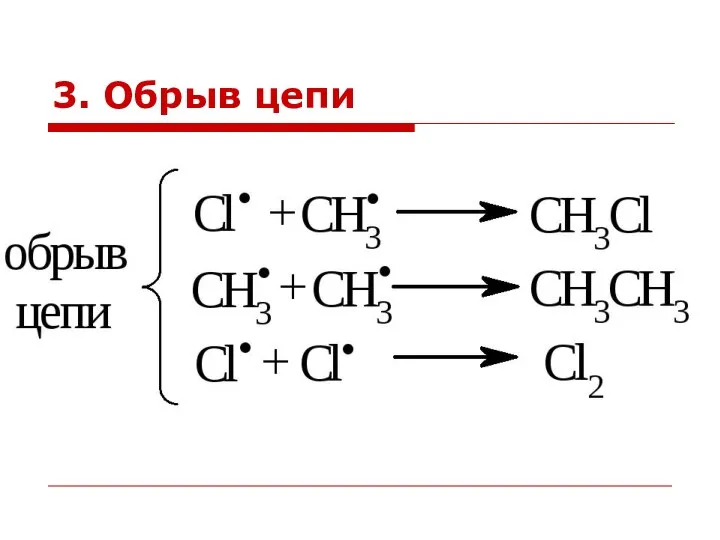
- 24. 3. Обрыв цепи
- 25. Общая схема радикального замещения
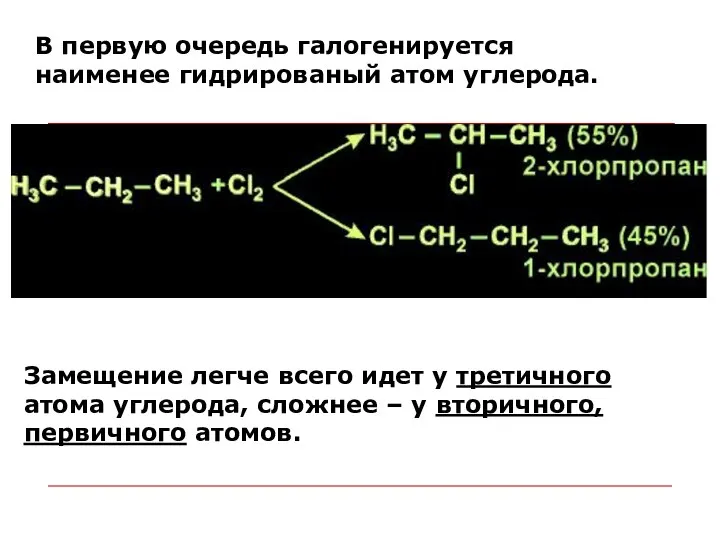
- 26. Замещение легче всего идет у третичного атома углерода, сложнее – у вторичного, первичного атомов. В первую
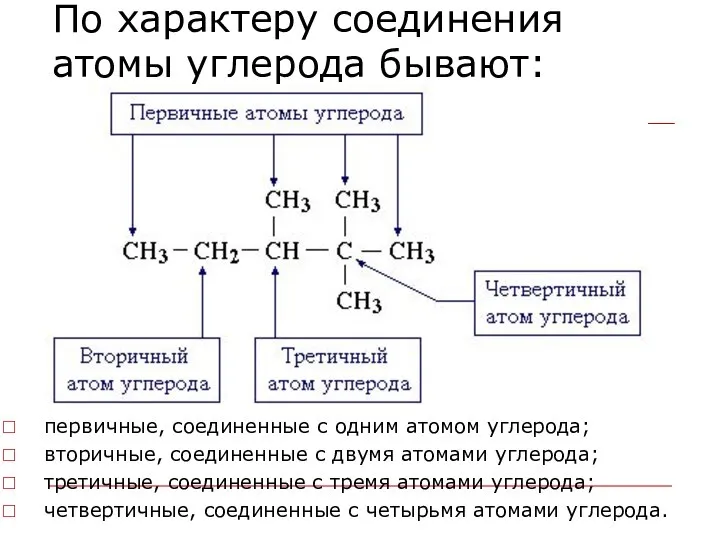
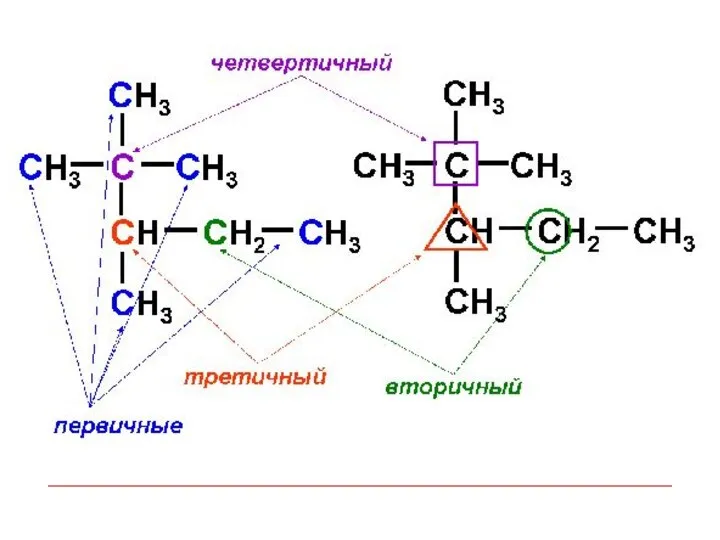
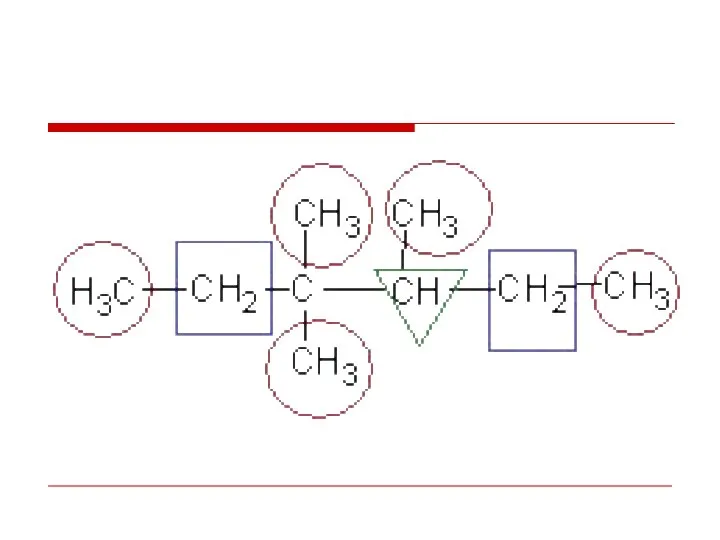
- 27. По характеру соединения атомы углерода бывают: первичные, соединенные с одним атомом углерода; вторичные, соединенные с двумя
- 30. б) Нитрование (реакция Коновалова). Алканы реагируют с 10 % раствором HNO₃ или оксидом азота NO₂ в
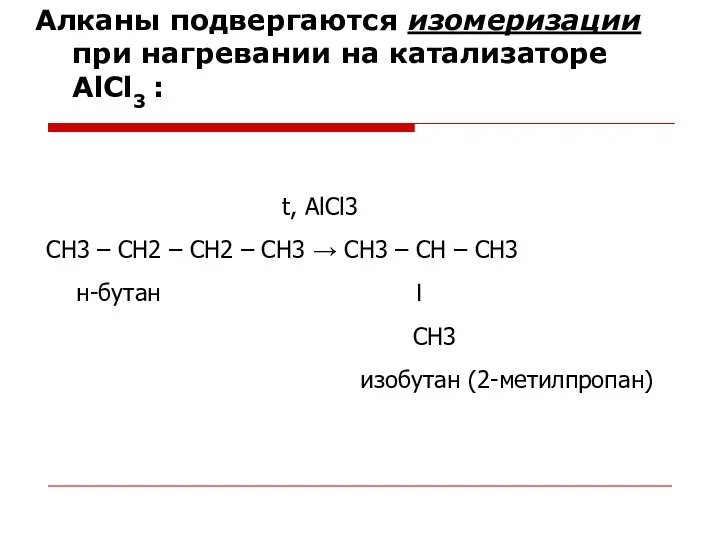
- 31. Алканы подвергаются изомеризации при нагревании на катализаторе AlCl3 : t, AlCl3 CH3 – CH2 – CH2
- 32. Задание. Построить и назвать изомеры для гексана.
- 33. Алгоритм построения изомеров для алканов По корню слова строят углеродный скелет (гекса – 6 атомов углерода)
- 34. Пускают разветвление с другой стороны С – С – С – С С С это третий
- 35. Доставить атомы водорода с учётом, что углерод 4-хвалентен СН3 – СН2 – СН2 – СН2 –
- 36. Порядок построения названия 1.Выбрать в молекуле главную углеродную цепь. Во-первых, она должна быть самой длинной. Во-вторых,
- 37. Порядок построения названия 2. Пронумеровать атомы углерода в главной цепи с той стороны, к которой ближе
- 38. Порядок построения названия 3. Указать в префиксе (приставке) положение (номер атома углерода) и название радикала (функциональной
- 39. Порядок построения названия 4. Записать корень, соответствующий числу атомов углерода в главной цепи. 5. Если есть
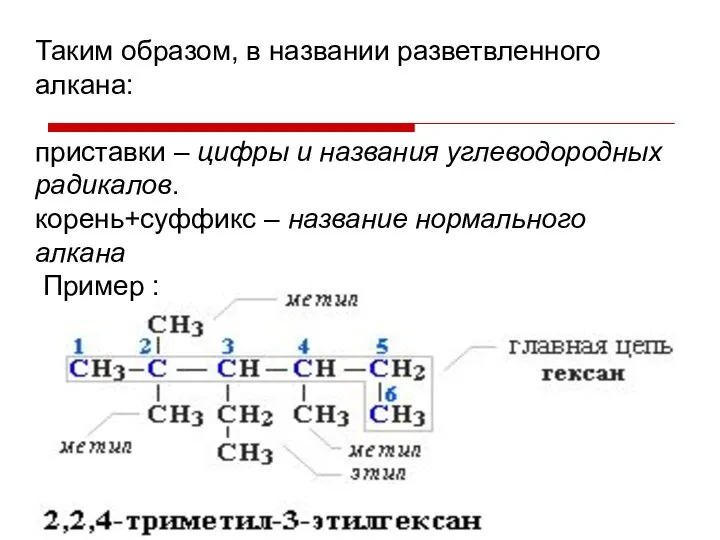
- 40. Таким образом, в названии разветвленного алкана: приставки – цифры и названия углеводородных радикалов. корень+суффикс – название
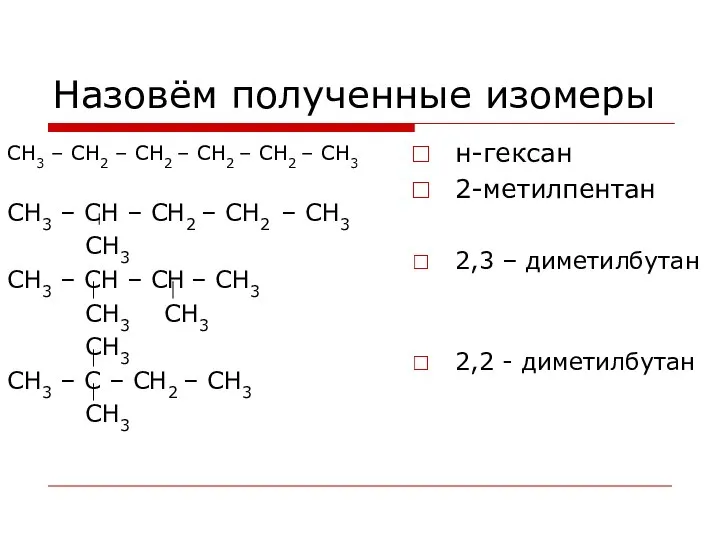
- 41. Назовём полученные изомеры СН3 – СН2 – СН2 – СН2 – СН2 – СН3 СН3 –
- 42. СПАСИБО ЗА ВНИМАНИЕ!!!
- 43. Алкены
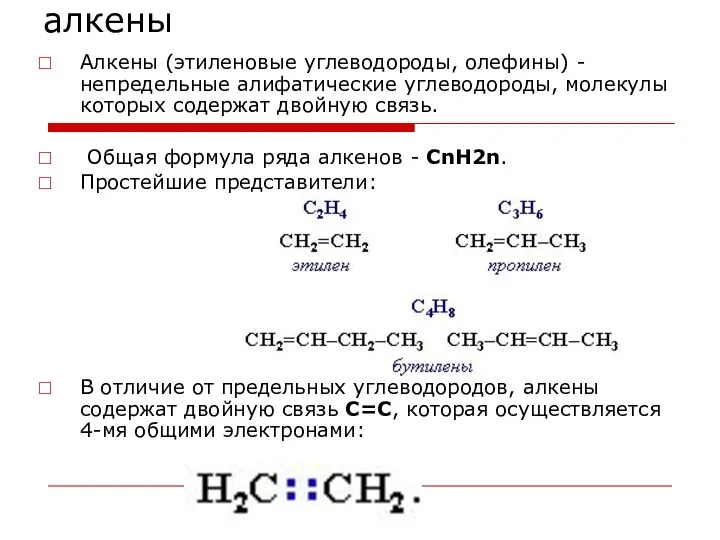
- 44. алкены Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула
- 45. Гомологический ряд алкенов Этен Пропен Бутен Пентен Гексен Гептен C2H4 C3H6 C4H8 C5H10 C6H12 C7H14 Общая
- 46. Для простейших алкенов применяются также исторически сложившиеся названия:этилен (этен), пропилен (пропен), бутилен (бутен-1), изобутилен (2-метилпропен) и
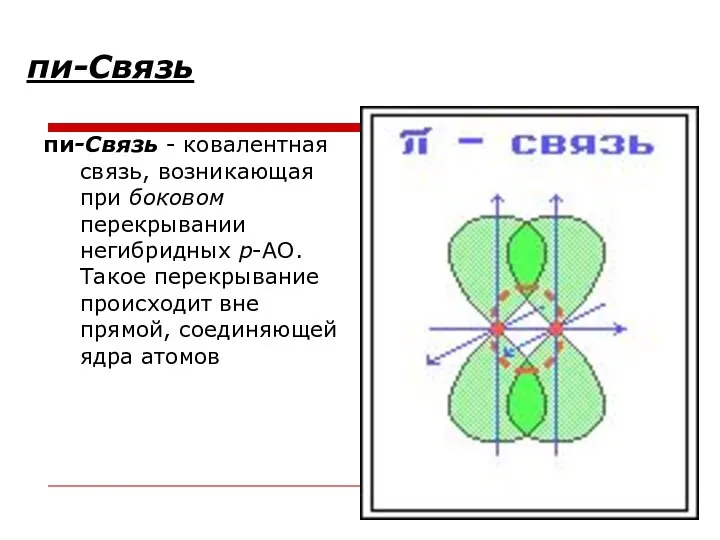
- 48. пи-Связь пи-Связь - ковалентная связь, возникающая при боковом перекрывании негибридных р-АО. Такое перекрывание происходит вне прямой,
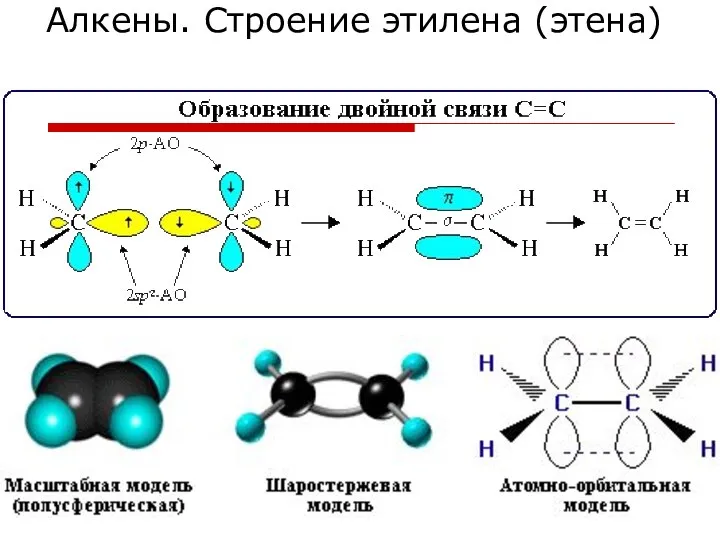
- 49. Алкены. Строение этилена (этена)
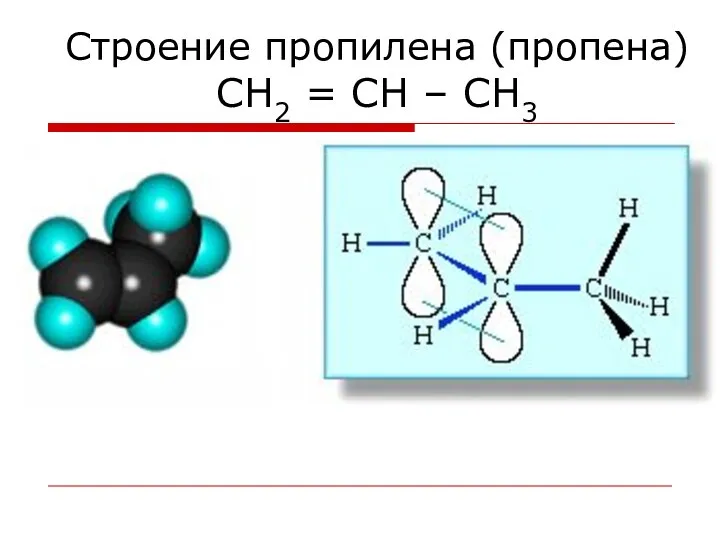
- 50. Строение пропилена (пропена) СН2 = СН – СН3
- 51. Номенклатура алкенов Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение
- 52. Изомерия алкенов Для алкенов возможны два типа изомерии: 1-ый тип – структурная изомерия: углеродного скелета положения
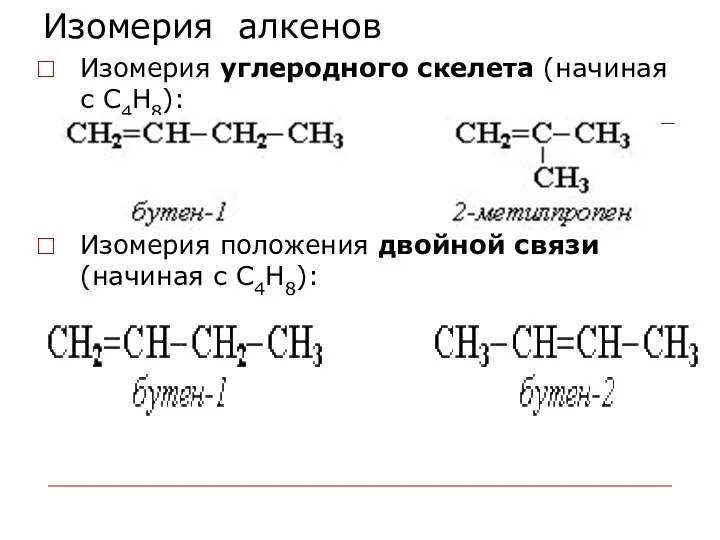
- 53. Изомерия алкенов Изомерия углеродного скелета (начиная с С4Н8): Изомерия положения двойной связи (начиная с С4Н8):
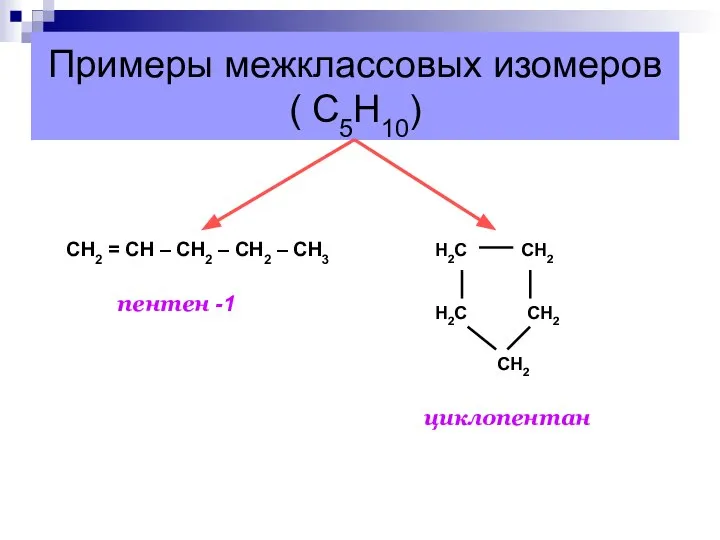
- 54. Примеры межклассовых изомеров ( С5Н10) СН2 = СН – СН2 – СН2 – СН3 пентен -1
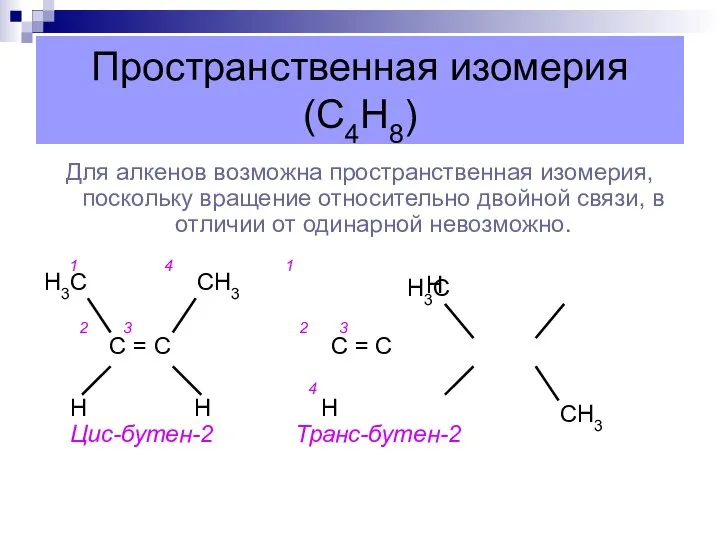
- 55. Пространственная изомерия (С4Н8) Для алкенов возможна пространственная изомерия, поскольку вращение относительно двойной связи, в отличии от
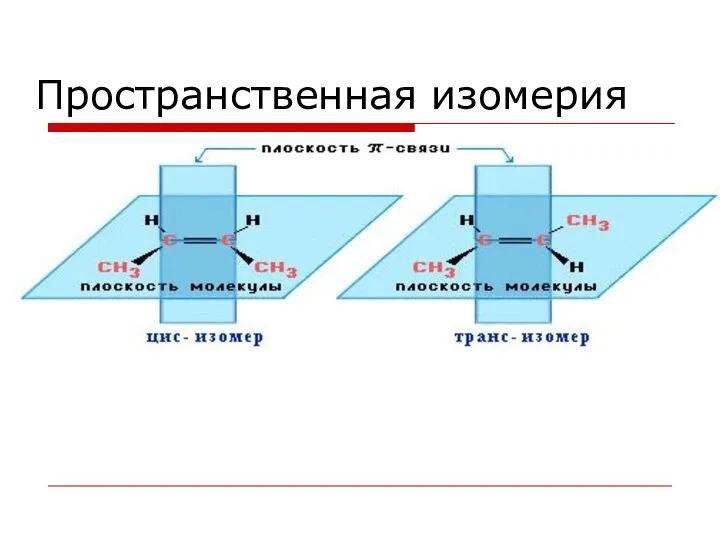
- 56. Пространственная изомерия
- 57. Геометрические изомеры бутена Цис-изомер Транс-изомер
- 58. Физические свойства алкенов Алкены плохо растворимы в воде, но хорошо растворяются в органических растворителях. С2– С4
- 59. Химические свойства алкенов Алкены более химически активные вещества, в отличие от алканов, что обусловлено наличием двойной
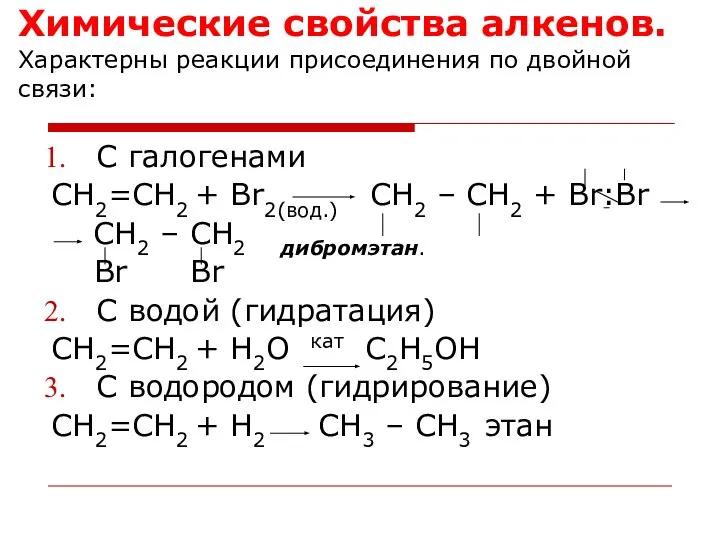
- 60. Химические свойства алкенов. Характерны реакции присоединения по двойной связи: С галогенами CH2=CH2 + Br2(вод.) СH2 –
- 61. Гидрогалогенирование гомологов этилена Правило В.В. Марковникова Атом водорода присоединяется к наиболее гидрированному атому углерода при двойной
- 62. Реакция полимеризации CH2=CH2 + CH2=CH2 + CH2=CH2 + … -СH2 – CH2- + -СH2 – CH2-
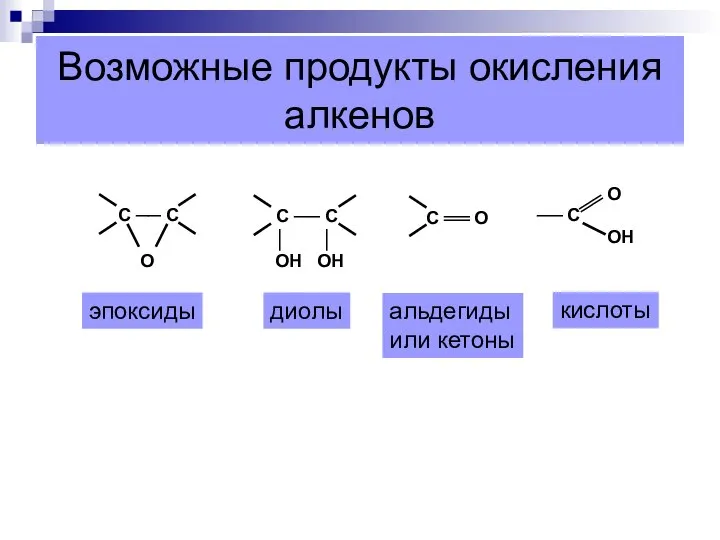
- 63. Возможные продукты окисления алкенов эпоксиды диолы альдегиды или кетоны кислоты
- 64. Реакции окисления Реакция Вагнера. (Мягкое окисление раствором перманганата калия). 3СН2 = СН2 + 2КМnО4 + 4Н2О
- 65. Горение алкенов Алкены горят красноватым светящимся пламенем, в то время как пламя предельных углеводородов голубое. Горение
- 66. Лабораторные способы получения алкенов При получении алкенов необходимо учитывать правило А.М. Зайцева: при отщеплении галогеноводорода или
- 67. Лабораторные способы получения алкенов Дегидратация спиртов. Н3С ─ СН2 ─ ОН → Н2С ═ СН2 +
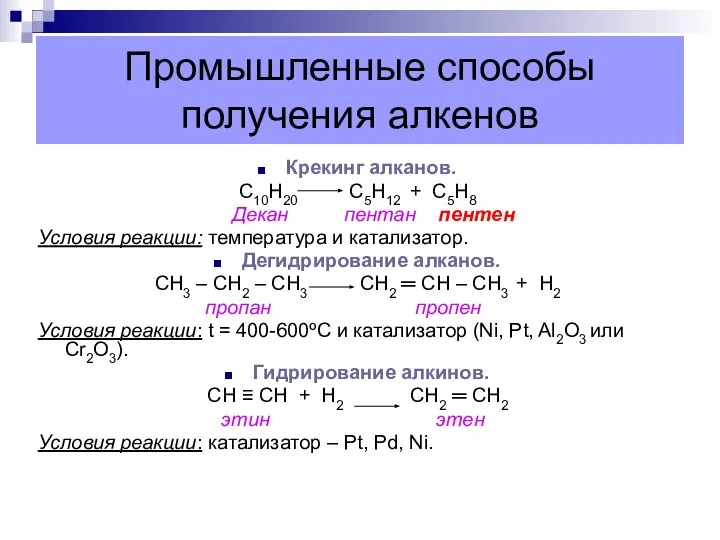
- 68. Промышленные способы получения алкенов Крекинг алканов. С10Н20 С5Н12 + С5Н8 Декан пентан пентен Условия реакции: температура
- 69. Алкины
- 70. Алкины Алкины (Производные ацетилена) – непредельные углеводороды, молекулы которых содержат одну тройную связь. Общая формула алкинов
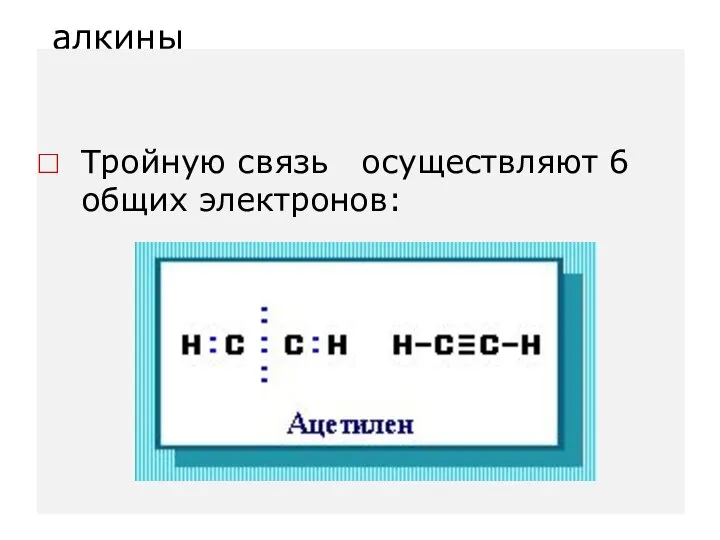
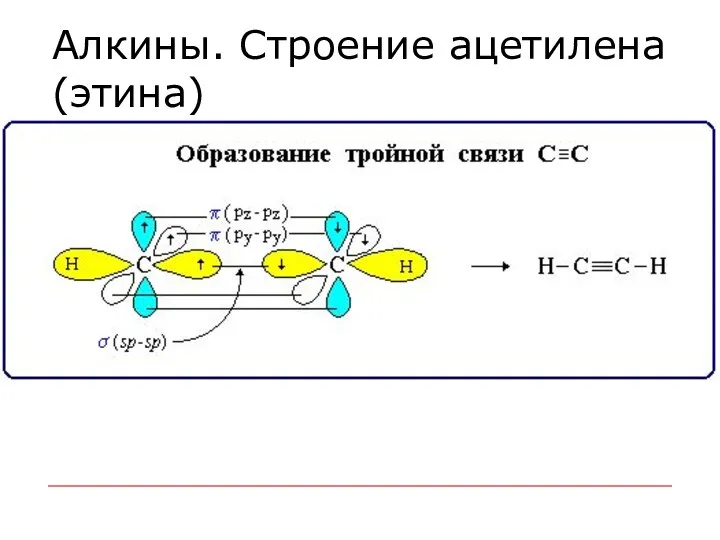
- 71. алкины Тройную связь осуществляют 6 общих электронов:
- 73. Алкины. Строение ацетилена (этина)
- 74. Номенклатура алкинов названия ацетиленовых углеводородов соответствуют названиям алканов суффикс –ан меняют на –ин: Главная цепь должна
- 75. Для простейших алкенов применяются также исторически сложившиеся названия: ацетилен (этин), аллилен (пропин), кротонилен (бутин-1), валерилен (пентин-1).
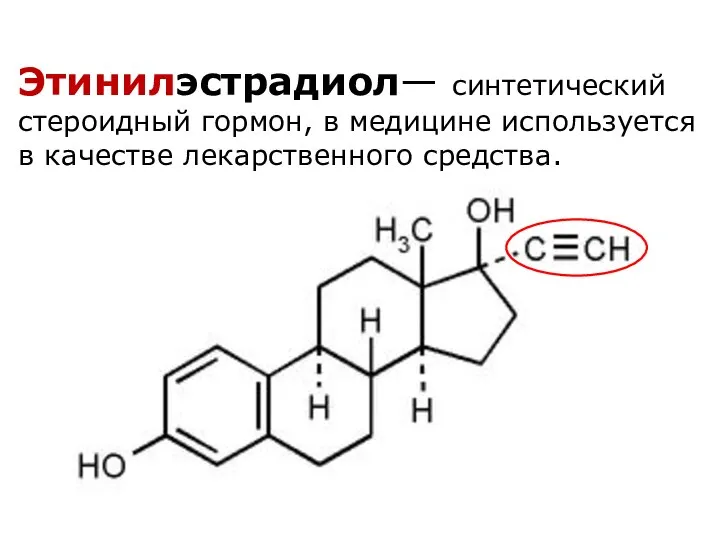
- 76. Этинилэстрадиол— синтетический стероидный гормон, в медицине используется в качестве лекарственного средства.
- 77. Способы получения Крекинг
- 78. Из карбида кальция Способы получения
- 79. Дегидрогалогенирование Способы получения
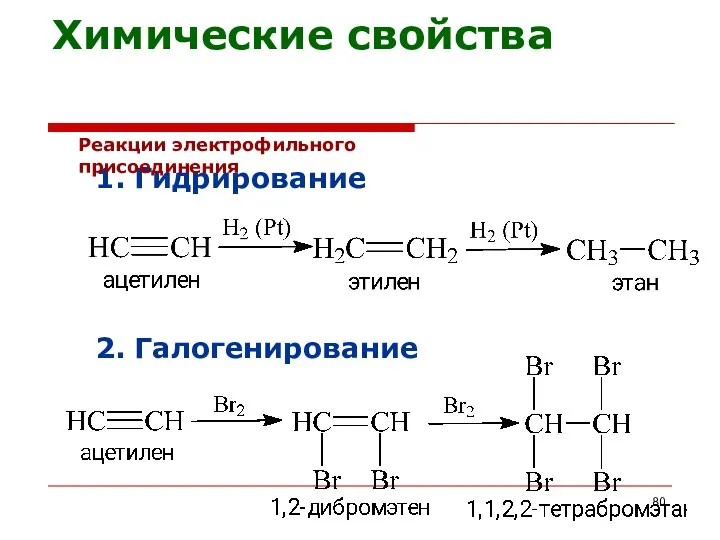
- 80. 1. Гидрирование Реакции электрофильного присоединения 2. Галогенирование Химические свойства
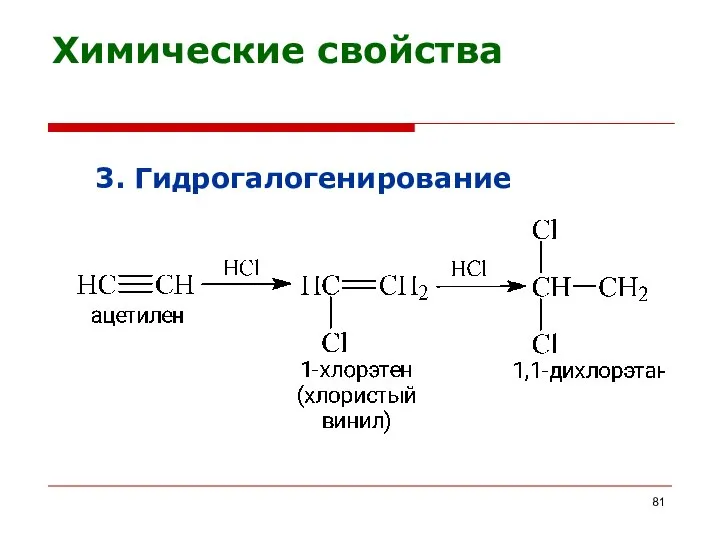
- 81. 3. Гидрогалогенирование Химические свойства
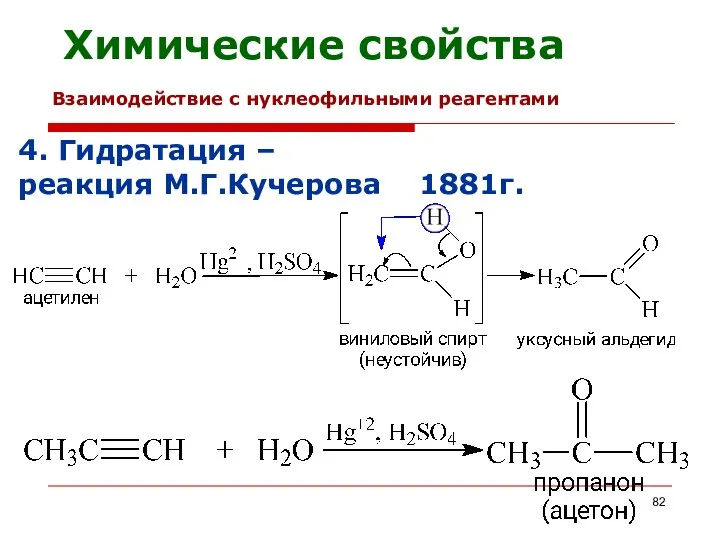
- 82. Химические свойства 4. Гидратация – реакция М.Г.Кучерова 1881г. Взаимодействие с нуклеофильными реагентами
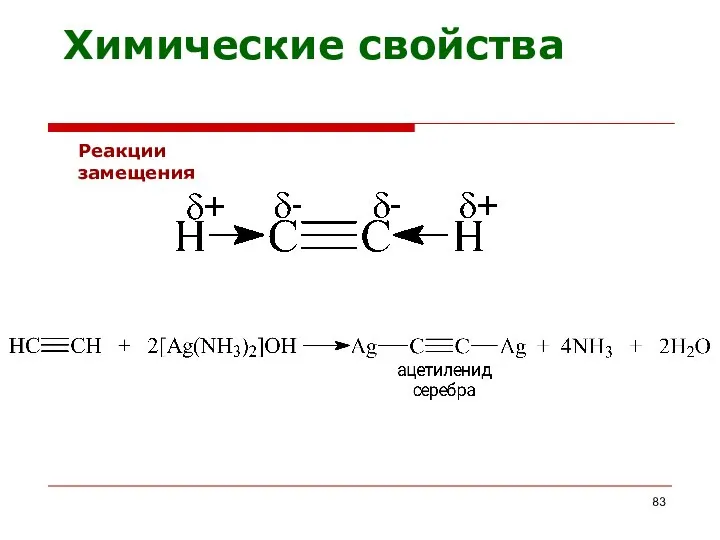
- 83. Реакции замещения Химические свойства
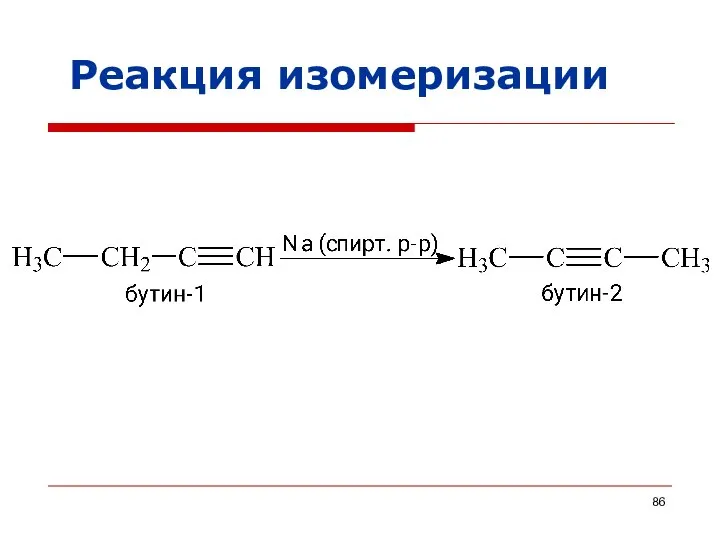
- 86. Реакция изомеризации
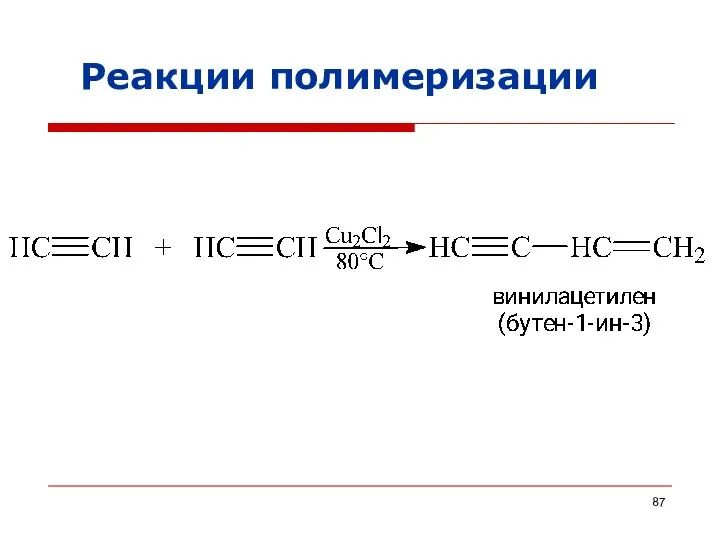
- 87. Реакции полимеризации
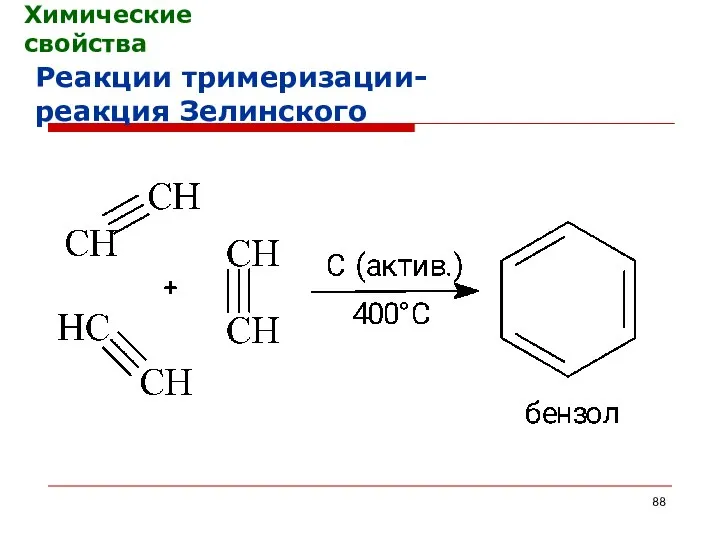
- 88. Химические свойства Реакции тримеризации- реакция Зелинского
- 90. СПАСИБО ЗА ВНИМАНИЕ!!!
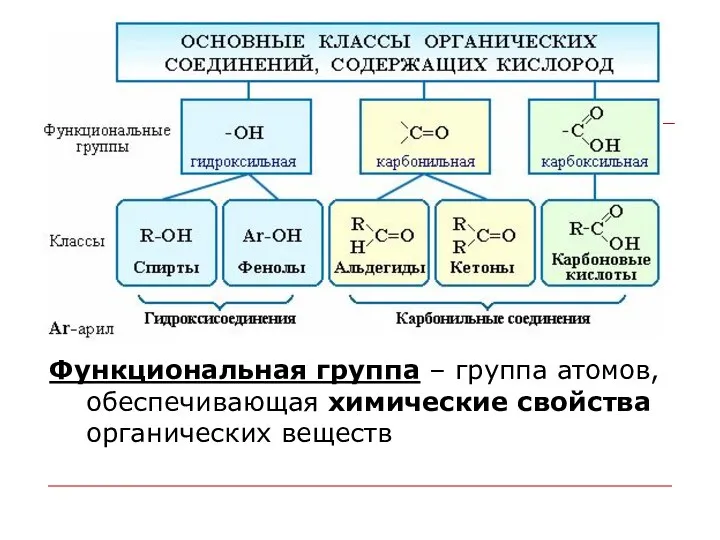
- 91. Функциональная группа – группа атомов, обеспечивающая химические свойства органических веществ
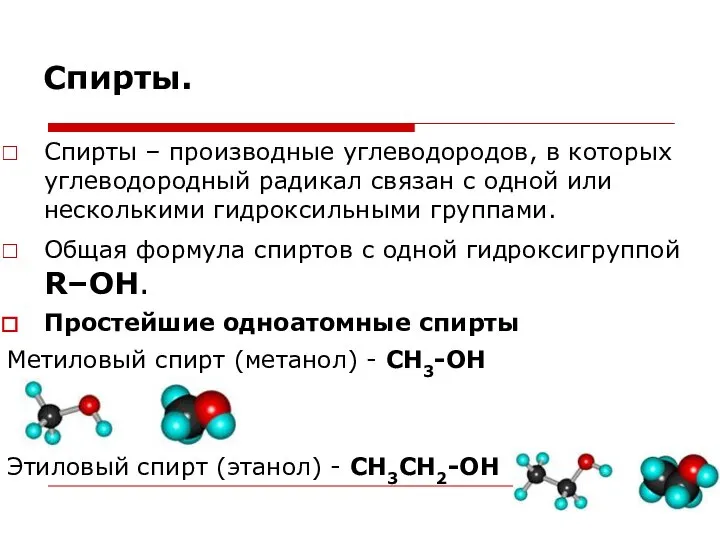
- 92. Спирты. Спирты – производные углеводородов, в которых углеводородный радикал связан с одной или несколькими гидроксильными группами.
- 93. Многоатомные спирты Этиленгликоль – двухатомный спирт СН2 – СН2 ОН ОН Как его можно получить? Бесцветная
- 94. Многоатомные спирты Глицерин – трёхатомный спирт СН2 – СН – СН2 ОН ОН ОН Густая сиропообразная
- 95. Химические свойства спиртов обусловлены наличием функциональной группы - ОН Взаимодействует: С кислотами С активными металлами Горит
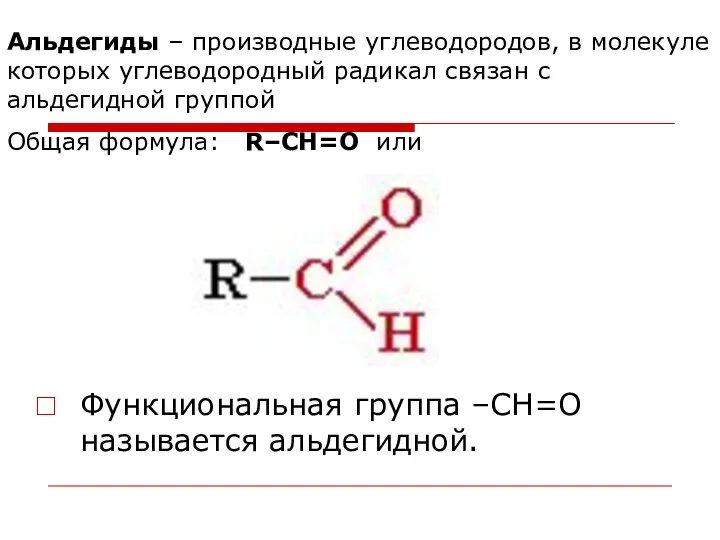
- 96. Альдегиды – производные углеводородов, в молекуле которых углеводородный радикал связан с альдегидной группой Общая формула: R–CН=O
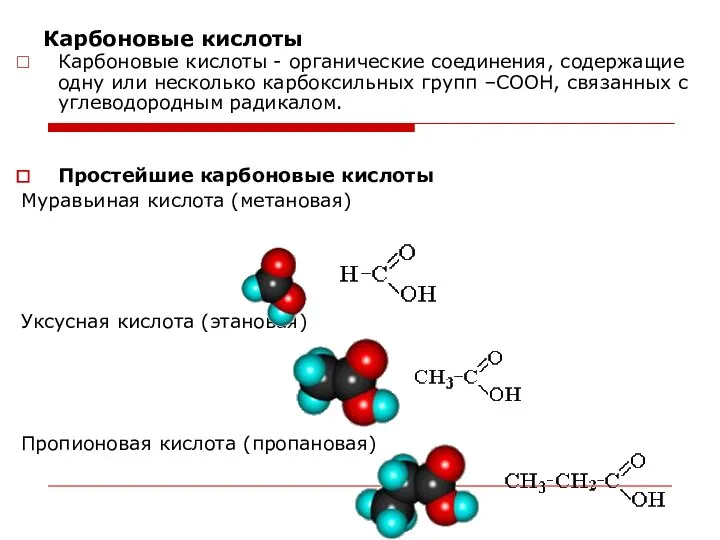
- 97. Карбоновые кислоты Карбоновые кислоты - органические соединения, содержащие одну или несколько карбоксильных групп –СООН, связанных с
- 98. Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота. HCOOH
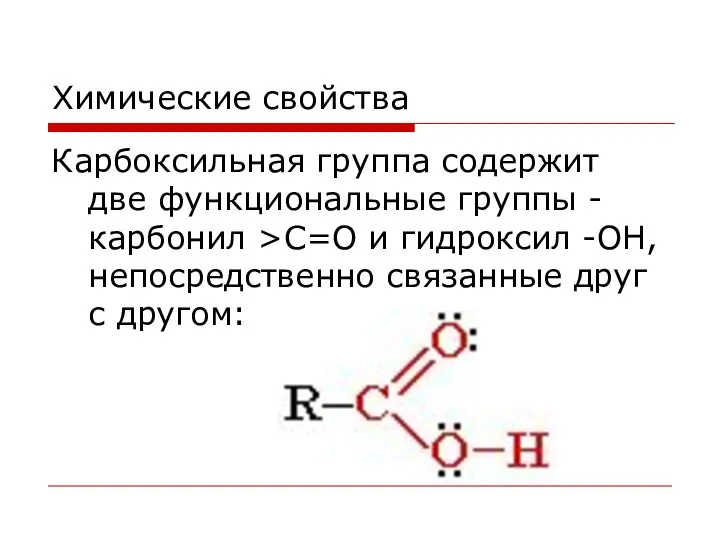
- 99. Химические свойства Карбоксильная группа содержит две функциональные группы - карбонил >С=О и гидроксил -OH, непосредственно связанные
- 100. Характерны реакции с: Со спиртами (реакция этерификации) Продуктом является сложный эфир Составьте уравнение реакции взаимодействия уксусной
- 101. С солями более слабых карбоновых кислот Составьте уравнение реакции взаимодействия уксусной кислоты и карбоната натрия, назовите
- 102. Жиры. Жиры - сложные эфиры глицерина и высших одноатомных карбоновых кислот. В состав природных триглицеридов входят
- 103. Жидкие жиры превращают в твердые путем реакции гидрирования. При этом водород присоединяется по двойной связи, содержащейся
- 104. Углеводы (сахара) - органические вещества, состав которых выражается формулой Cx(H2O)y, где x и y > 3.
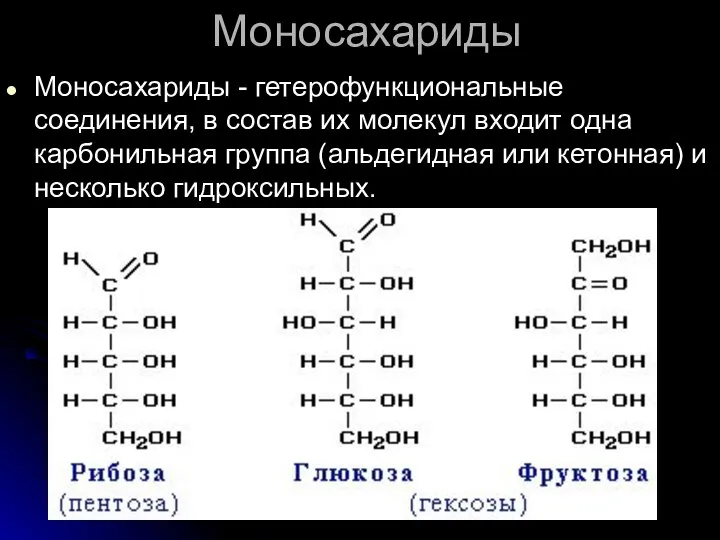
- 105. Моносахариды Моносахариды - гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (альдегидная или кетонная)
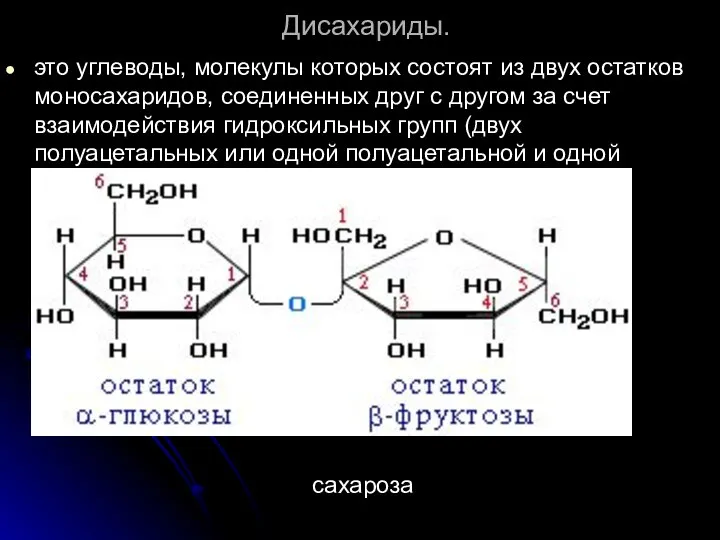
- 106. Дисахариды. это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет
- 107. Крахмал В его состав входят: амилоза (внутренняя часть крахмального зерна) - 10-20% амилопектин (оболочка крахмального зерна)
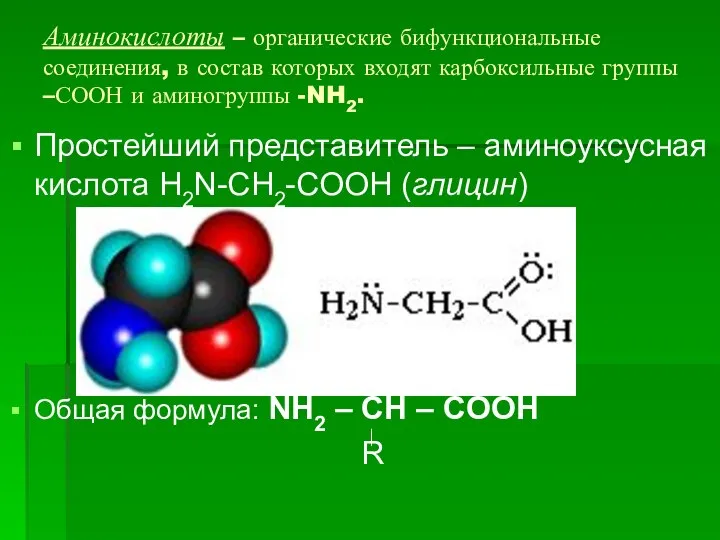
- 108. Аминокислоты – органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы -NH2. Простейший
- 109. Физические свойства Аминокислоты – твердые кристаллические вещества с высокой т.пл., при плавлении разлагаются. Хорошо растворимы в
- 110. Химические свойства Аминокислоты проявляют свойства оснований за счет аминогруппы и свойства кислот за счет карбоксильной группы,
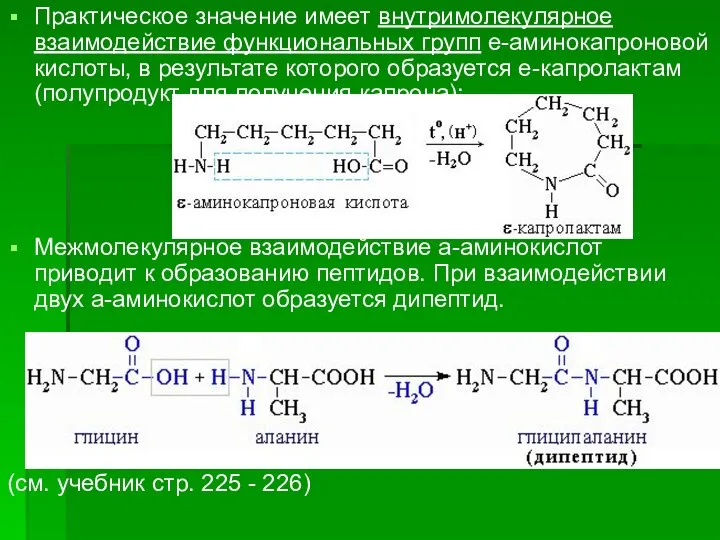
- 111. Практическое значение имеет внутримолекулярное взаимодействие функциональных групп e-аминокапроновой кислоты, в результате которого образуется e-капролактам (полупродукт для
- 112. Белки
- 113. Белки (полипептиды) - биополимеры, построенные из остатков a-аминокислот, соединённых пептидными (амидными) связями. Функции белков в природе
- 114. Уровни структурной организации белков.
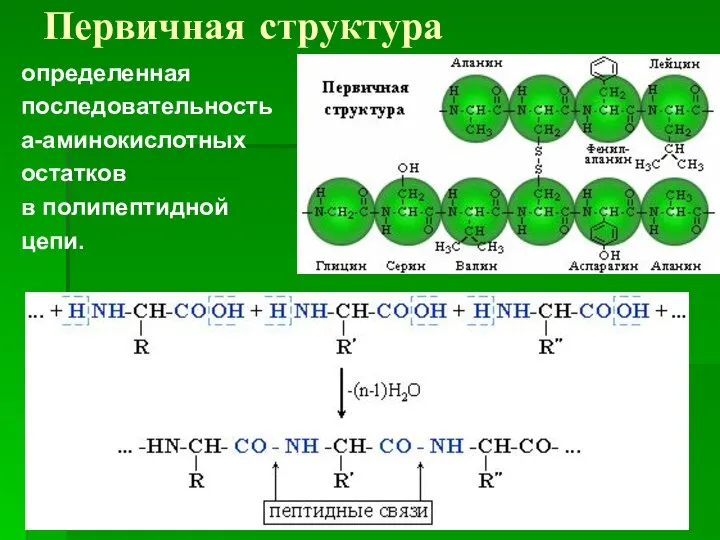
- 115. Первичная структура определенная последовательность a-аминокислотных остатков в полипептидной цепи.
- 116. Вторичная структура конформация полипептидной цепи, закрепленная множеством водородных связей между группами N-H и С=О. Одна из
- 117. Третичная структура - форма закрученной спирали в пространстве, образованная главным образом за счет дисульфидных мостиков -S-S-,
- 118. Четвертичная структура - агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей.
- 120. Скачать презентацию





























































 Альбітит-грейзенові родовища
Альбітит-грейзенові родовища Применение металлов в быту
Применение металлов в быту Презентация по Химии "Спирт" - скачать смотреть бесплатно
Презентация по Химии "Спирт" - скачать смотреть бесплатно Решение задач по уравнениям химических реакций
Решение задач по уравнениям химических реакций 1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки
1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки  Математический аппарат квантовой механики
Математический аппарат квантовой механики Кремний
Кремний Алканы и циклоалканы
Алканы и циклоалканы Презентация по Химии "Введение в современную неорганическую химию" - скачать смотреть
Презентация по Химии "Введение в современную неорганическую химию" - скачать смотреть  Презентация по Химии "Польза жиров" - скачать смотреть
Презентация по Химии "Польза жиров" - скачать смотреть  Безпечна для довкілля хімія green chemistry. Основні напрямки та перспективи розвитку
Безпечна для довкілля хімія green chemistry. Основні напрямки та перспективи розвитку Презентация по Химии "Мінеральні добрива" - скачать смотреть бесплатно
Презентация по Химии "Мінеральні добрива" - скачать смотреть бесплатно Азот
Азот Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ
Правила техники безопасности при работе в химическом кабинете. Ознакомление с лабораторным оборудованием. Инструктаж по ТБ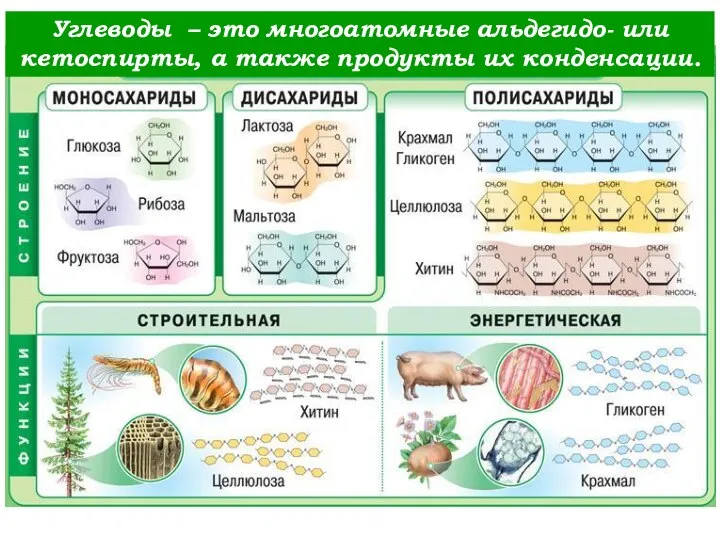 Углеводы. Классификация углеводов. Явление мутаротации. (Лекция 4)
Углеводы. Классификация углеводов. Явление мутаротации. (Лекция 4) Сера. Аллотропия серы. Физические и химические свойства серы. Применение
Сера. Аллотропия серы. Физические и химические свойства серы. Применение Анализ красителей и консервантов, входящих в состав безалкогольных газированных и негазированных напитков
Анализ красителей и консервантов, входящих в состав безалкогольных газированных и негазированных напитков Презентация по Химии "Алотропія карбону" - скачать смотреть
Презентация по Химии "Алотропія карбону" - скачать смотреть  Презентация Качество продукции
Презентация Качество продукции  Химический практикум для олимпиадной команды. Количественный анализ
Химический практикум для олимпиадной команды. Количественный анализ Выращивание кристаллов медного купороса в домашних условиях
Выращивание кристаллов медного купороса в домашних условиях Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13)
Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13) № 12.
№ 12.  Геохимия изотопов стабильных элементов
Геохимия изотопов стабильных элементов Химическая кинетика. Лекция 4
Химическая кинетика. Лекция 4 Нефть и способы ее переработки
Нефть и способы ее переработки Роль химических элементов в жизнедеятельности организма
Роль химических элементов в жизнедеятельности организма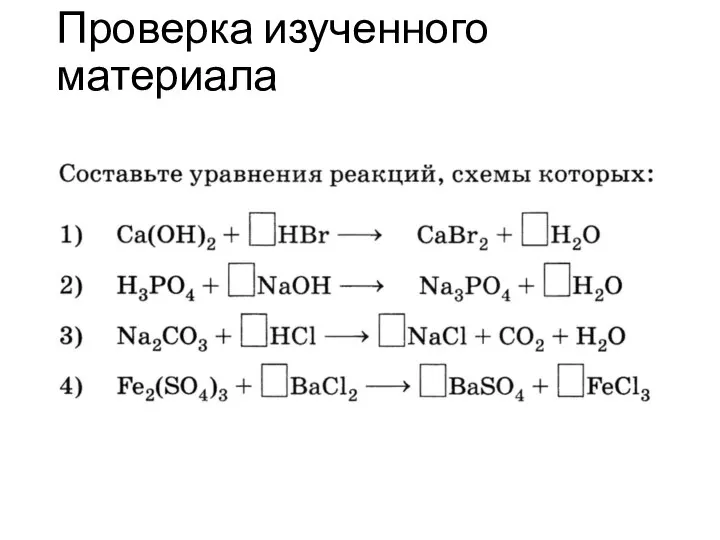 Реакции замещения
Реакции замещения