Содержание
- 2. Ответьте на вопросы Какое строение имеет кислород? Степень окисления в соединениях? Когда и кем открыт был
- 3. Немало сера знаменита, И в древности ее Гомер воспел, С ней много тысяч лет прожито, И
- 4. ТЕМА УРОКА: Сера. Аллотропия серы. Физические и химические свойства серы. Применение
- 5. Цели урока: Рассмотреть аллотропные модификации серы и ее физические и химические свойства. Охарактеризовать нахождение серы в
- 6. План урока: Положение серы в ПСХЭ Строение атома, возможные степени окисления Физические свойства серы Нахождение в
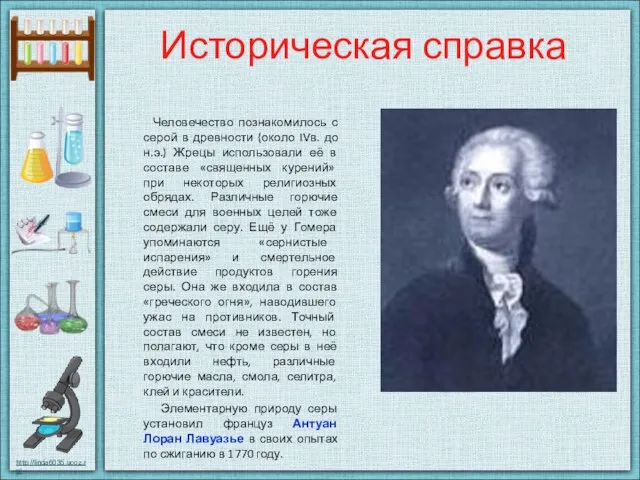
- 7. Историческая справка Человечество познакомилось с серой в древности (около IVв. до н.э.) Жрецы использовали её в
- 8. Латинское название серы «сульфур» происходит от санскритского “спать” или англосаксонского «убивать», что очевидно объясняется ядовитостью сернистого
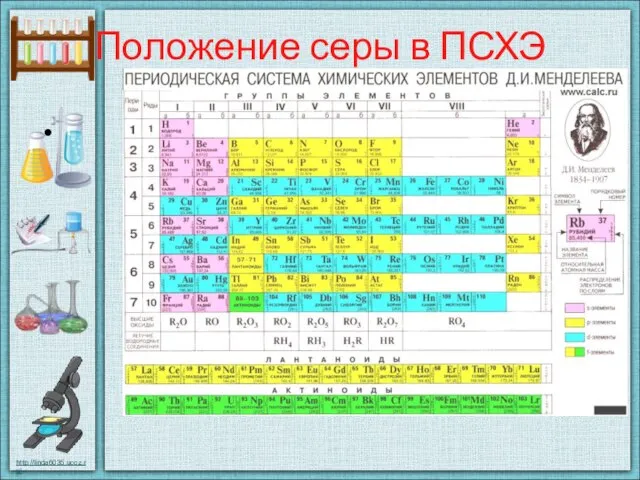
- 9. Положение серы в ПСХЭ
- 10. Строение атома серы 3 период VI группа главная подгруппа Заряд ядра +16 Электронная формула 1s22s22p63s23p4
- 11. Физические свойства серы — твердое агрегатное состояние — желтого цвета — не растворима в воде —
- 12. Нахождение серы в природе Сера находится на 16 месте по распространенности в земной коре, Встречается в
- 13. СЕРА САМОРОДНАЯ
- 14. СЕРА САМОРОДНАЯ
- 15. СЕРА САМОРОДНАЯ
- 16. СЕРА САМОРОДНАЯ
- 17. Пирит – «огненный камень» (соединение серы в природе)
- 18. Сера также встречается в виде сульфатов - солей серной кислоты - мирабилит
- 19. Сера в природе Сера входит в состав белков. Особенно много серы в белках волос, рогов, шерсти.
- 20. Серой богаты бобовые растения (горох, чечевица), овсяные хлопья, яйца
- 21. Аллотропные модификации серы РОМБИЧЕСКАЯ МОНОКЛИННАЯ ПЛАСТИЧЕСКАЯ У жёлтой серы есть корона, Но нет ни подданных, ни
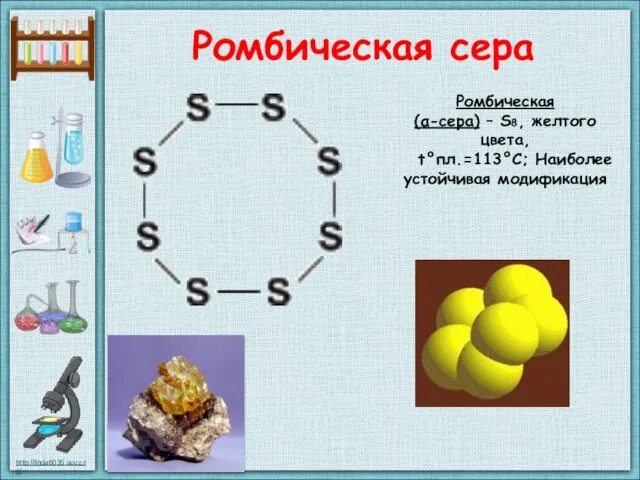
- 22. Ромбическая сера Ромбическая (α-сера) – S8, желтого цвета, t°пл.=113°C; Наиболее устойчивая модификация
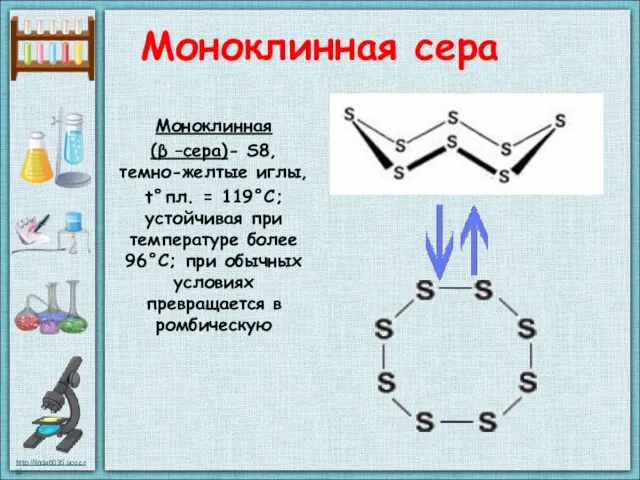
- 23. Моноклинная сера Моноклинная (β –сера)- S8, темно-желтые иглы, t°пл. = 119°C; устойчивая при температуре более 96°С;
- 24. Пластическая сера Пластическая сера- коричневая резиноподобная (аморфная) масса. Она неустойчива и через некоторое время становится хрупкой,
- 25. Получение пластической серы
- 26. ФИЗМИНУТКА Глубоко вздохнули: вот, мы набрали кислород. Выдохнув из легких чистых газ уходит углекислый. Руки вверх,
- 27. Химические свойства серы
- 31. Химические свойства серы (закончите уравнения реакций)
- 32. Химические свойства серы
- 33. Применение серы S
- 34. Биологическое значение серы: участвует в биохимических реакциях обмена веществ, окислительно-восстановительных и ферментативных процессах. Однако, при постоянном
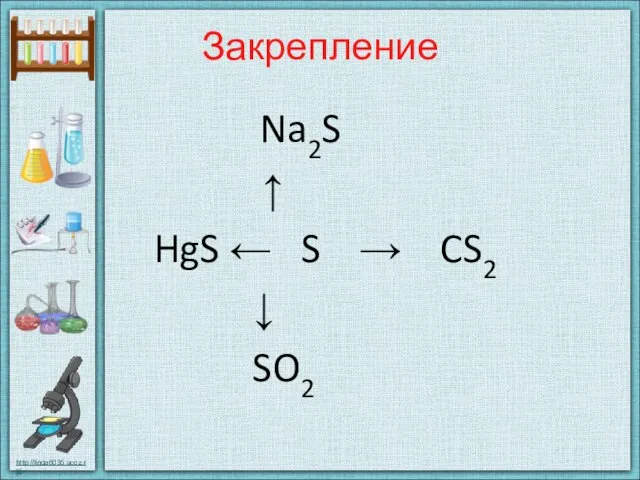
- 35. Закрепление Na2S ↑ HgS ← S → CS2 ↓ SO2
- 36. S + Hg = HgS S + 2Na = Na2S 2S + C = CS2 S
- 38. Поставить +, если согласны с утверждением (не подписывать) Я узнал много нового. Мне это пригодится в
- 40. Скачать презентацию



























 Электрохимический ряд напряжений металлов
Электрохимический ряд напряжений металлов  Предмет химии. Вещества. 8 клвсс
Предмет химии. Вещества. 8 клвсс Реологические свойства полимерных материалов
Реологические свойства полимерных материалов Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Химический элемент медь
Химический элемент медь Цемент. (9 класс)
Цемент. (9 класс) «Конструкции из дерева и пластмасс» ЛЕКЦИЯ 2 2. Свойства древесины и пластмасс как конструкционных материалов
«Конструкции из дерева и пластмасс» ЛЕКЦИЯ 2 2. Свойства древесины и пластмасс как конструкционных материалов  Презентация по Химии "Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам курса неорганической химии&qu
Презентация по Химии "Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам курса неорганической химии&qu Вещество. Атом. Молекула. Простые и сложные вещества
Вещество. Атом. Молекула. Простые и сложные вещества Презентация по Химии "Тепловой эффект химических реакций" - скачать смотреть
Презентация по Химии "Тепловой эффект химических реакций" - скачать смотреть  Циклоалканы (полиметиленовые, циклопарафины, ациклические)
Циклоалканы (полиметиленовые, циклопарафины, ациклические) Fiber. Iron. Calcium
Fiber. Iron. Calcium Коррозия углеродистых и низколегированных сталей в различных средах
Коррозия углеродистых и низколегированных сталей в различных средах Предмет химии. Вещества. Изучаемые понятия: Вещество и тело. Атом и молекула. Свойства вещ
Предмет химии. Вещества. Изучаемые понятия: Вещество и тело. Атом и молекула. Свойства вещ Фосфор и его свойства
Фосфор и его свойства Воспламенение (зажигание) газовых смесей
Воспламенение (зажигание) газовых смесей Природа и классификация химических связей
Природа и классификация химических связей Структура и содержание КИМ-22
Структура и содержание КИМ-22 МОУ «Вышинская СОШ» Природные источники углеводородов _____________________________ Урок по химии в 10 классе Учитель: Лазарева Наталья Его
МОУ «Вышинская СОШ» Природные источники углеводородов _____________________________ Урок по химии в 10 классе Учитель: Лазарева Наталья Его Аллотропные модификации
Аллотропные модификации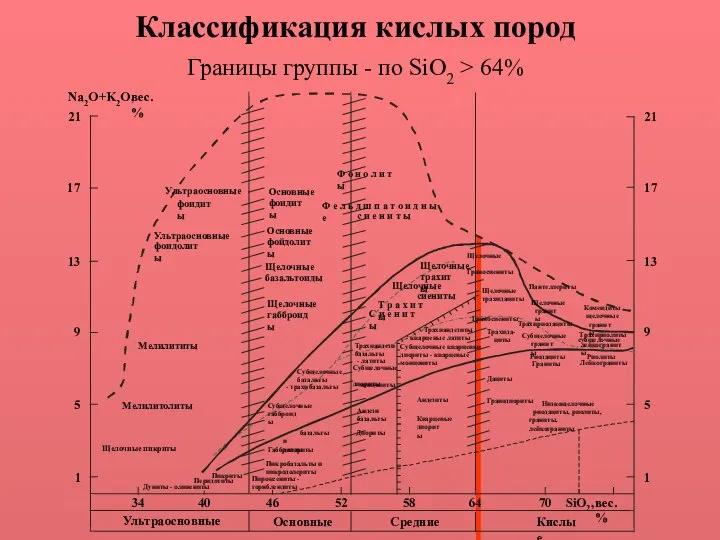 Классификация кислых пород
Классификация кислых пород Полимер. Использование и вред
Полимер. Использование и вред Минералы
Минералы Хлор
Хлор Амилаза. Строение амилазы
Амилаза. Строение амилазы Основные классы неорганических соединений
Основные классы неорганических соединений Electrolysis
Electrolysis Тепловой эффект химических реакций
Тепловой эффект химических реакций