Содержание
- 2. Цель урока: Продолжить формирование представлений учащихся об изомерии и номенклатуре органических веществ, умений составлять структурные формулы
- 3. Задачи: Обучающие:- обобщение и систематизация знаний по теме «Алкины»;- выявление уровня усвоения основных понятий, правил; проверка
- 4. Сегодня на уроке вы узнаете: Понятие о непредельных углеводородах. Характеристика тройной связи. Изомерия и номенклатура алкинов.
- 5. Понятие об алкинах Алкины – углеводороды, содержащие в молекуле одну тройную связь между атомами углерода, а
- 6. Характеристика тройной связи Вид гибридизации – sp Валентный угол – 180 Длина связи С = С
- 7. Схема образования sp -гибридных орбиталей
- 8. Схема образования sp -гибридных орбиталей
- 9. Номенклатура алкинов. (Согласно международной номенклатуре названия ацетиленовых углеводородов производят от соответствующего алкана с заменой суффикса –ан
- 10. Гомологический ряд алкинов C2H2 C3H4 C4H6 C5H8 C6H10 C7H12 Этин Пропин Бутин Пентин Гексин Гептин
- 11. Изомерия алкинов Структурная изомерия 1. Изомерия положения тройной связи (начиная с С4Н6): СН ≡С−СН2−СН3 СН3−С≡С−СН3 бутин-1
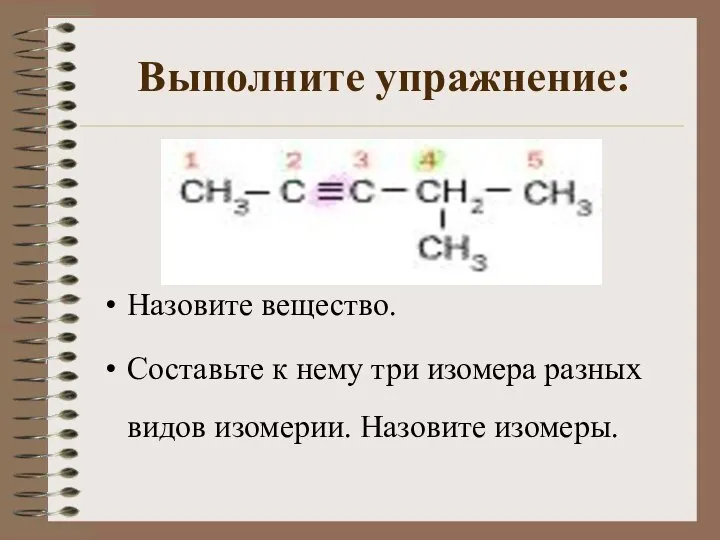
- 12. Выполните упражнение: Назовите вещество. Составьте к нему три изомера разных видов изомерии. Назовите изомеры.
- 13. Физические свойства Температуры кипения и плавления алкинов, так же как и алкенов, закономерно повышаются при увеличении
- 14. Ацетилен получают в промышленности двумя способами: 1. Термический крекинг метана: 1500°С 2СН4 ⎯⎯→ С2Н2 + 3Н2
- 15. Химические свойства алкинов Химические свойства ацетилена и его гомологов в основном определяются наличием в их молекулах
- 16. Реакции присоединения 1. Галогенирование Обесцвечивание бромной воды является качественной реакцией на все непредельные углеводороды
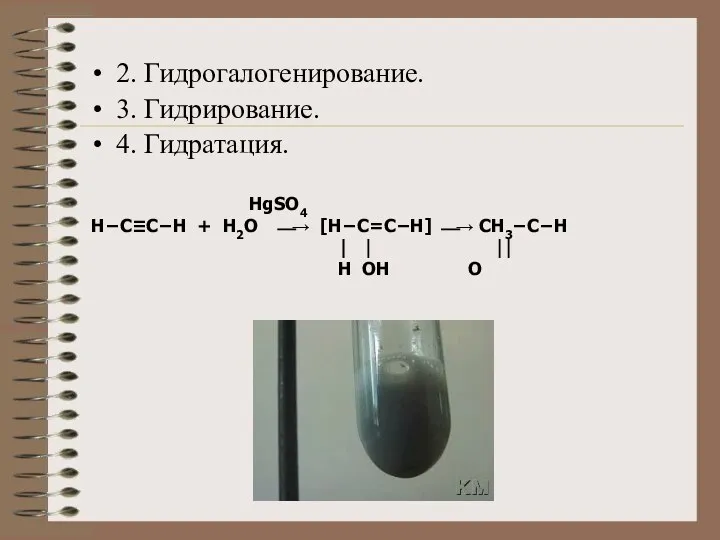
- 17. 2. Гидрогалогенирование. 3. Гидрирование. 4. Гидратация. HgSO4 Н−C≡C−H + H2O ⎯→ [H−C=C−H] ⎯→ CH3−C−H ⏐ ⏐
- 18. Окисление Ацетилен и его гомологи окисляются перманганатом калия с расщеплением тройной связи и образованием карбоновых кислот:
- 19. Горение ацетилена При сгорании (полном окислении) ацетилена выделяется большое количества тепла: HC≡CH + 2О2 ⎯→ 2СО2
- 20. Реакции замещения При взаимодействии ацетилена (или R−C≡C−H) с аммиачными растворами оксида серебра выпадают осадки нерастворимых ацетиленидов:
- 21. Реакция полимеризации 1. Димеризация под действием водного раствора CuCl и NH4Cl: НC≡CH + НC≡CH ⎯→ Н2C=CH−C≡CH
- 22. Применение алкинов
- 23. Домашнее задание
- 25. Скачать презентацию




















 Классификация топлива. Показатели качества топлива (Лекция 1)
Классификация топлива. Показатели качества топлива (Лекция 1) Значение периодического закона и периодической системы химических элементов Д.И. Менделеева
Значение периодического закона и периодической системы химических элементов Д.И. Менделеева Яды и химикаты
Яды и химикаты История развития химии
История развития химии Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері
Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері Свойства ковалентной связи Гибридизация Поляризация Направленность Насыщаемость
Свойства ковалентной связи Гибридизация Поляризация Направленность Насыщаемость Строение и свойства белков
Строение и свойства белков Алкалоиды
Алкалоиды Анализ качества лекарственных средств, производных алифатических и ароматических аминов
Анализ качества лекарственных средств, производных алифатических и ароматических аминов Химия и производство
Химия и производство Курс лекций по химии
Курс лекций по химии Химическая техника. Экстракция
Химическая техника. Экстракция Бытовая химия. Правила обращения с бытовыми химикатами
Бытовая химия. Правила обращения с бытовыми химикатами Детонаційна стійкість бензину
Детонаційна стійкість бензину Определение качества нефтепродуктов (на примере бензинов и дизельного топлива)
Определение качества нефтепродуктов (на примере бензинов и дизельного топлива) Тема урока Атомы химических элементов Задачи урока: повторить, обобщить и закрепить знания о строении атомов химических элемент
Тема урока Атомы химических элементов Задачи урока: повторить, обобщить и закрепить знания о строении атомов химических элемент Периодический закон химических элементов Д. И. Менделеева и периодическая система
Периодический закон химических элементов Д. И. Менделеева и периодическая система Изотермический процесс в реакционном объеме. (Тема 6.2)
Изотермический процесс в реакционном объеме. (Тема 6.2) Диффузия
Диффузия Физические и химические свойства кислот
Физические и химические свойства кислот Многоатомные спирты
Многоатомные спирты Особенности связей и строение фосфазенов
Особенности связей и строение фосфазенов Предмет органической химии
Предмет органической химии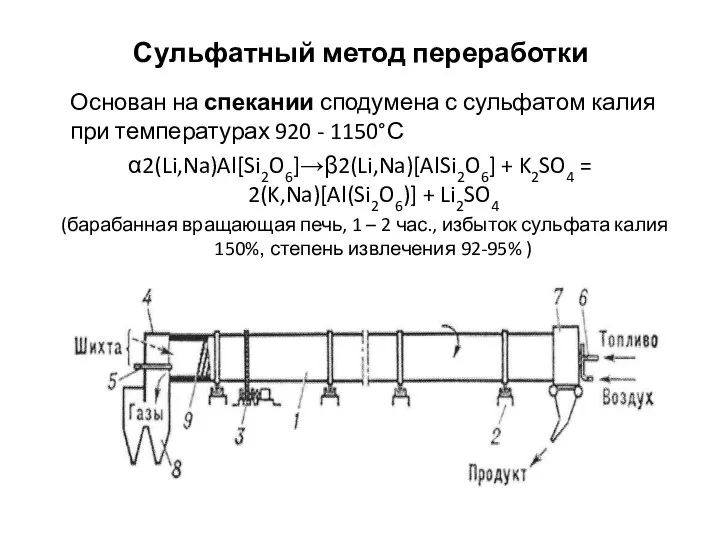 Сульфатный метод переработки
Сульфатный метод переработки Арены и ароматичность
Арены и ароматичность Соли в свете теории электролитической диссоциации
Соли в свете теории электролитической диссоциации Именные реакции в органической химии. Органический синтез. Механизмы химических процессов
Именные реакции в органической химии. Органический синтез. Механизмы химических процессов Использование химии в медицине
Использование химии в медицине