Содержание
- 2. Кроме того, к аминам относятся азотсодержащие циклы, в которых атом азота связан с углеродными атомами. Например
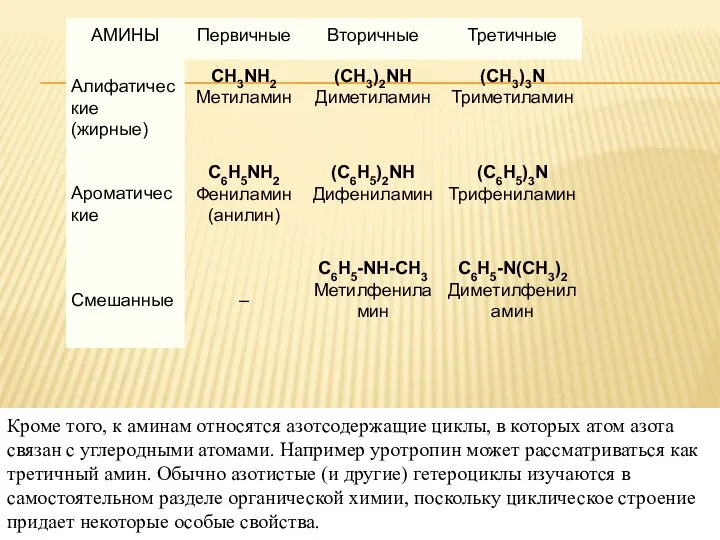
- 3. 2.1. Номенклатура аминов В большинстве случаев названия аминов образуют из названий углеводородных радикалов и суффикса амин.
- 4. Первичные амины часто называют как производные углеводородов, в молекулах которых один или несколько атомов водорода замещены
- 5. Для смешанных аминов, содержащих алкильные и ароматические радикалы, за основу названия обычно берется название первого представителя
- 6. 2.2. Изомерия аминов Структурная изомерия - углеродного скелета, начиная с С4H9NH2: - положения аминогруппы, начиная с
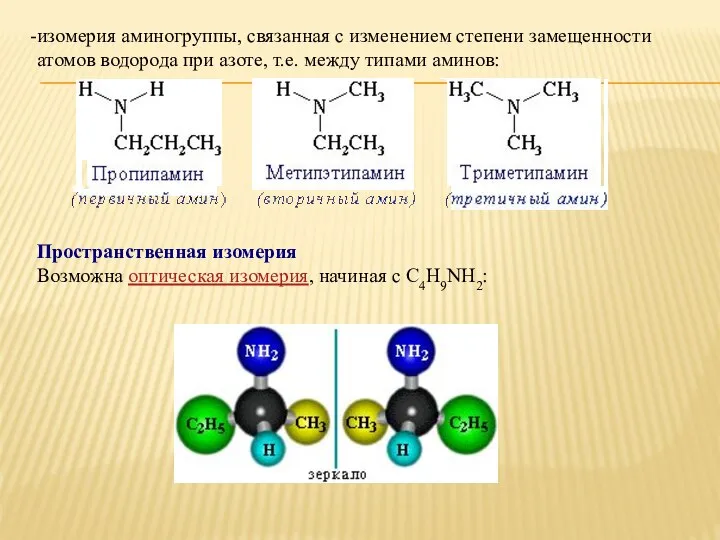
- 7. изомерия аминогруппы, связанная с изменением степени замещенности атомов водорода при азоте, т.е. между типами аминов: Пространственная
- 8. 2.3. Свойства аминов Изучая новый класс соединений – амины, попробуем предсказать их основные физические и химические
- 9. Нуклеофильность - способность частицы предоставить электронную пару на образование связи с углеродом или с другим положительно
- 10. 2.3.1. Физические свойства аминов Связь N–H является полярной, поэтому первичные и вторичные амины образуют межмолекулярные водородные
- 11. При обычной температуре только низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака),
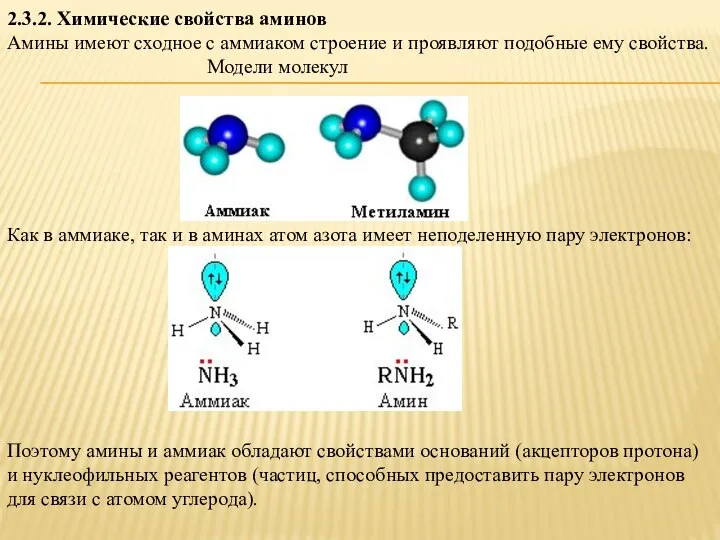
- 12. 2.3.2. Химические свойства аминов Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. Модели
- 13. 2.3.2.1. Основность аминов Для аминов характерны ярко выраженные основные свойства (за что их часто называют органическими
- 14. Связь протона с амином, как и с аммиаком, образуется по донорно-акцепторному механизму за счет неподеленной электронной
- 15. Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Поэтому
- 16. На основность аминов влияют различные факторы: электронные эффекты углеводородных радикалов, пространственное экранирование радикалами атома азота, а
- 17. 2.3.2.2. Окисление аминов Алифатические амины окисляются под действием сильных окислителей. В отличие от аммиака, низшие газообразные
- 18. Краситель бензидиновый синий образуется при окислении дифениламина азотной (или азотистой) кислотой: Эта реакция применяется в экологии
- 19. 2.3.2.3. Взаимодействие с азотистой кислотой Азотистая кислота HNO2 - неустойчивое соединение. Поэтому она используется только в
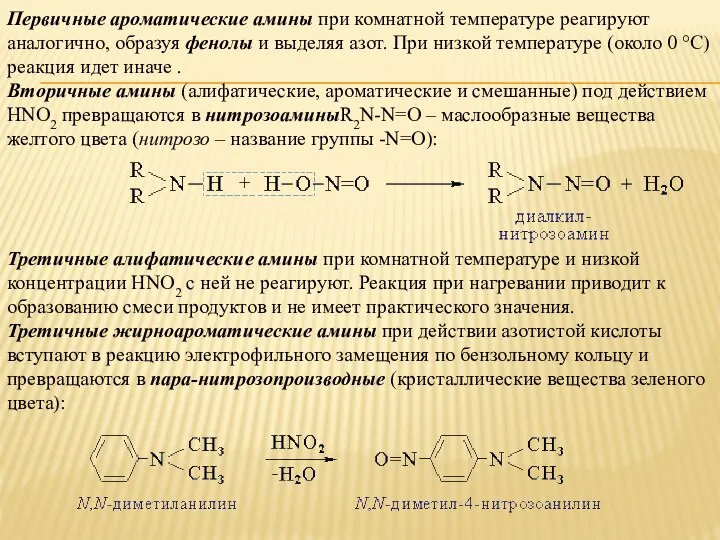
- 20. Первичные ароматические амины при комнатной температуре реагируют аналогично, образуя фенолы и выделяя азот. При низкой температуре
- 21. 2.4. Анилин Анилин (фениламин) С6H5NH2 – важнейший из ароматических аминов: Он находит широкое применение в качестве
- 22. С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол.
- 23. Практическое значение имеет реакция анилина с азотистой кислотой при пониженной температуре (около 0 °С). В результате
- 24. 2.5. Получение аминов В аминах атом азота находится в низшей степени окисления, поэтому многие способы их
- 25. 2.Восстановление амидов (восстановитель - алюмогидрид лития LiAH4): Восстановление нитрилов с образованием первичных аминов: R-C N +
- 27. Скачать презентацию




















 Химические и физические явления
Химические и физические явления Количественное определение лекарственных веществ
Количественное определение лекарственных веществ Сплавы со специальными свойствами
Сплавы со специальными свойствами Поли- и гетерофункциональные соединения
Поли- и гетерофункциональные соединения Липиды. Омыляемые липиды. Рубежный контроль №2
Липиды. Омыляемые липиды. Рубежный контроль №2 Кремний и его соединения
Кремний и его соединения Всі відомості Автор презентації – Розмаїтий Дмитро 7-Б клас
Всі відомості Автор презентації – Розмаїтий Дмитро 7-Б клас  Рентгеноструктуралық анализ. Лауе тәжірибесі, Брегг-Вульф теңдеуі, оны шығару жолдары
Рентгеноструктуралық анализ. Лауе тәжірибесі, Брегг-Вульф теңдеуі, оны шығару жолдары The Sulphur cycle. The Sulphur dioxide problems
The Sulphur cycle. The Sulphur dioxide problems Композиционные материалы
Композиционные материалы Арены. Бензол. Среди 22 миллионов органических соединений немного найдется таких , которые оказали на развитие органической химии
Арены. Бензол. Среди 22 миллионов органических соединений немного найдется таких , которые оказали на развитие органической химии  Растворы. Часть 2
Растворы. Часть 2 Органическая химия. Установочная лекция
Органическая химия. Установочная лекция Биохимические изменения компонентов молока в процессе переработки
Биохимические изменения компонентов молока в процессе переработки CaSO4:Tb3+ кристалында радиациялық ақаулардың пайда болуының нәтижелерін теориялық мәләметтерге сәйкестігін зерттеу
CaSO4:Tb3+ кристалында радиациялық ақаулардың пайда болуының нәтижелерін теориялық мәләметтерге сәйкестігін зерттеу Кислотно-основні рівноваги в біологічних системах. (Лекція 2)
Кислотно-основні рівноваги в біологічних системах. (Лекція 2) Исследование явления адсорбции на поверхности твердых тел (метод бумажной хроматографии). Асоян Пайлак Зарифи Джамшед 9 “a” класс ГБОУ лицей № 389 “ЦЭО” Руководитель: Скрижеева Е.В.
Исследование явления адсорбции на поверхности твердых тел (метод бумажной хроматографии). Асоян Пайлак Зарифи Джамшед 9 “a” класс ГБОУ лицей № 389 “ЦЭО” Руководитель: Скрижеева Е.В. Производство серной кислоты
Производство серной кислоты Органическая химия. История развития
Органическая химия. История развития Химическая связь
Химическая связь Водород. Растворы. 8 класс
Водород. Растворы. 8 класс Псевдогалогены и их соединения
Псевдогалогены и их соединения Розчини електролітів
Розчини електролітів Гетерогенные и лигандообменные равновесия и процессы
Гетерогенные и лигандообменные равновесия и процессы Презентация Предельные углеводороды
Презентация Предельные углеводороды  Біоорганічна хімія. Реакційна здатність біоорганічних сполук
Біоорганічна хімія. Реакційна здатність біоорганічних сполук Функціональні матеріали для високоенергетичної електроніки. (Лекція 1)
Функціональні матеріали для високоенергетичної електроніки. (Лекція 1) Железо и его соединения
Железо и его соединения