Содержание
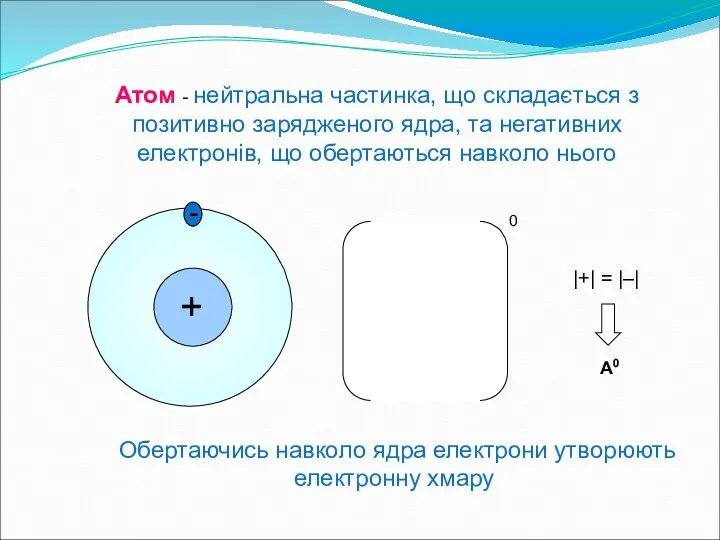
- 2. Атом - нейтральна частинка, що складається з позитивно зарядженого ядра, та негативних електронів, що обертаються навколо
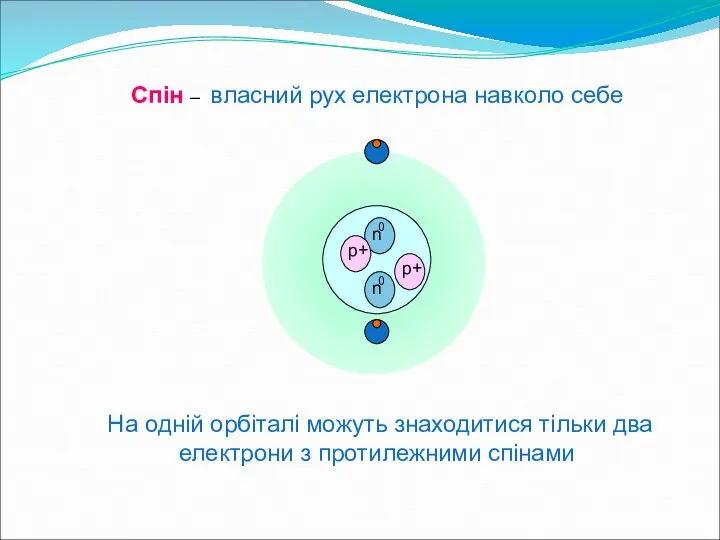
- 3. 0 n 0 n Спін – власний рух електрона навколо себе На одній орбіталі можуть знаходитися
- 4. Прості та складні речовини Закон збереження маси Матеріали до теми:
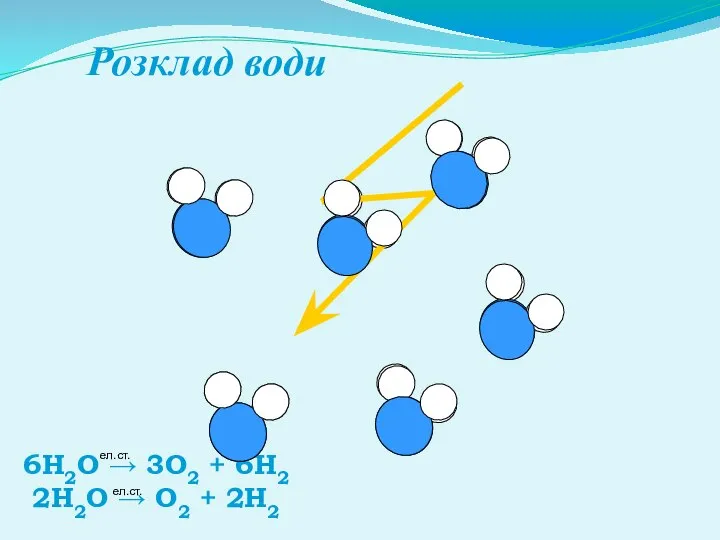
- 5. Розклад води 6Н2О → 3О2 + 6Н2 2Н2О → О2 + 2Н2 ел.ст. ел.ст.
- 6. Валентність атомів Матеріали до теми:
- 7. Давайте замислимося: Чому в природі так мало окремих атомів, більшість існує тільки у поєднанні з іншими
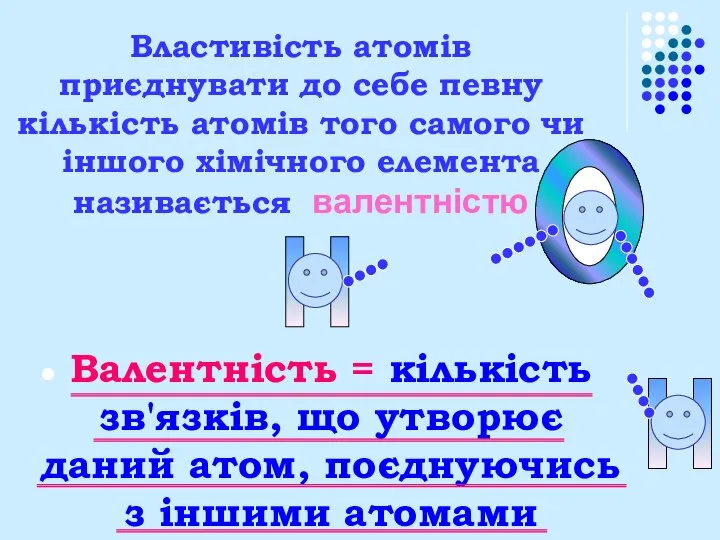
- 8. Властивість атомів приєднувати до себе певну кількість атомів того самого чи іншого хімічного елемента називається валентністю
- 9. Валентність залежіть від будови атома
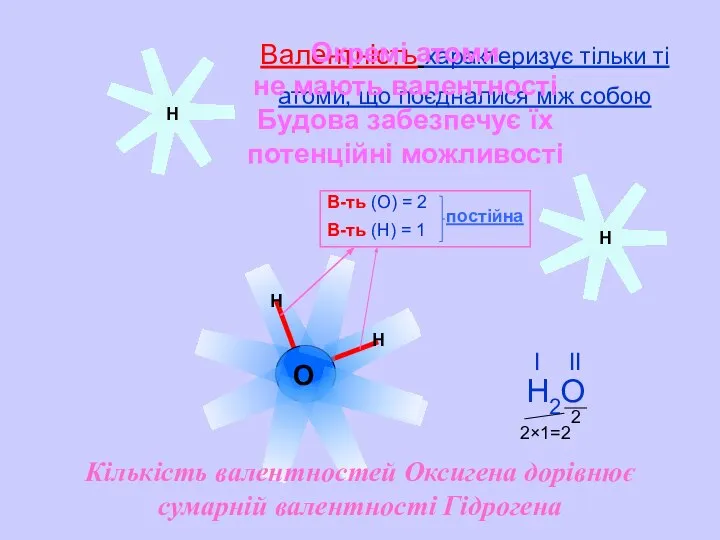
- 10. Н Н Н Н О Валентність характеризує тільки ті атоми, що поєдналися між собою Окремі атоми
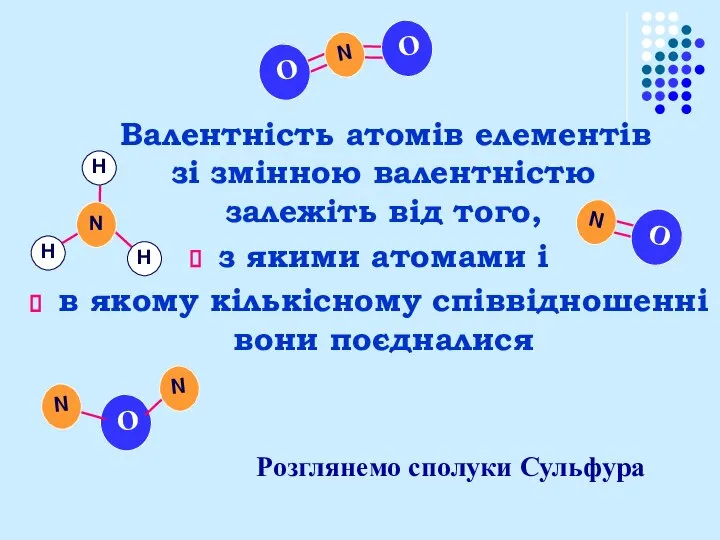
- 11. Валентність атомів елементів зі змінною валентністю залежіть від того, з якими атомами і в якому кількісному
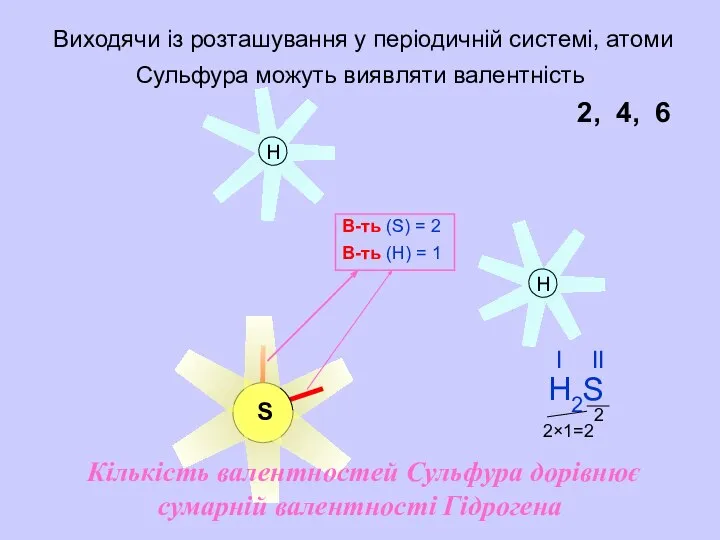
- 12. S Виходячи із розташування у періодичній системі, атоми Сульфура можуть виявляти валентність 2, 4, 6 В-ть
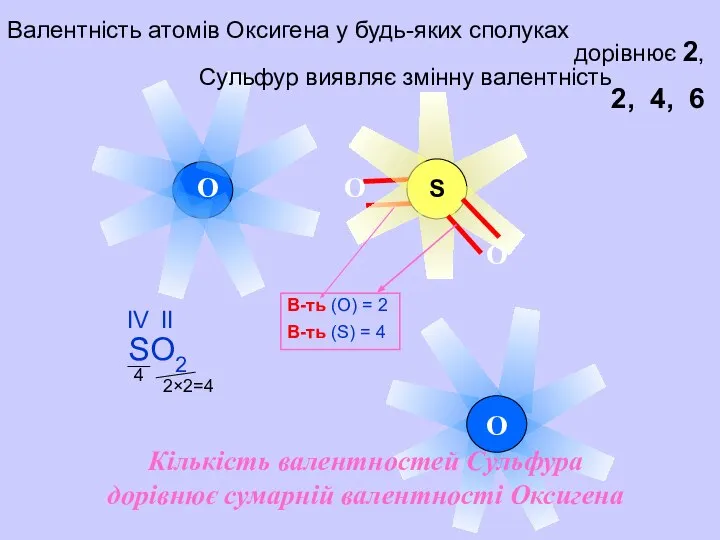
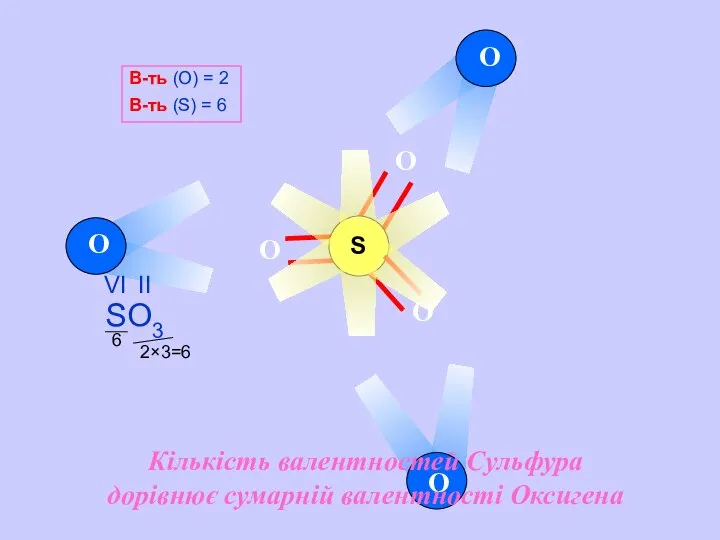
- 13. S O O O O Валентність атомів Оксигена у будь-яких сполуках дорівнює 2, Сульфур виявляє змінну
- 14. 2×3=6 6 O O O S O O O В-ть (О) = 2 В-ть (S) =
- 15. Загальні властивості металів Матеріали до теми:
- 16. Жодна речовина не має комплексу властивостей, який притаманний металам
- 17. Чому?
- 18. легко віддають електрони зовнішнього рівня Атоми металів при цьому перетворюючись на йони
- 20. Скачать презентацию








 Электронная формула атома магния
Электронная формула атома магния Стабилизация растворов для инъекций
Стабилизация растворов для инъекций Модифицированные природные полимеры
Модифицированные природные полимеры Презентация по Химии "Дидактические игровые задания для уроков закрепления и повторения или для обобщающего повторения в 8 клас
Презентация по Химии "Дидактические игровые задания для уроков закрепления и повторения или для обобщающего повторения в 8 клас Химия и экология
Химия и экология Тотығып фосфорлану
Тотығып фосфорлану Презентация по Химии "Вода как жизнь" - скачать смотреть бесплатно
Презентация по Химии "Вода как жизнь" - скачать смотреть бесплатно Аттестационная работа. Образовательная программа, элективный курс Химия в задачах и упражнениях
Аттестационная работа. Образовательная программа, элективный курс Химия в задачах и упражнениях Презентация по химии ученика 10 класса “Б” гимназии №1567 Ляпина Руслана.
Презентация по химии ученика 10 класса “Б” гимназии №1567 Ляпина Руслана. Внеклеточный матрикс – основа минерализованных тканей Автор – доцент кафедры биохимии Е.А. Рыскина
Внеклеточный матрикс – основа минерализованных тканей Автор – доцент кафедры биохимии Е.А. Рыскина  Геохимия агроландшафтов
Геохимия агроландшафтов Общая характеристика биогенных элементов
Общая характеристика биогенных элементов Поведение солей в водных растворах
Поведение солей в водных растворах Резина Искусственные и синтетические
Резина Искусственные и синтетические  Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..  Выполнила: Здановская Карина 9 А класс
Выполнила: Здановская Карина 9 А класс  Презентация для заочников
Презентация для заочников Решение задач на массовую долю вещества
Решение задач на массовую долю вещества Азот. Кислородные соединения
Азот. Кислородные соединения Диаграммы Пурбе
Диаграммы Пурбе Органикалық қосылыстар құрылысының теориялық негіздері және олардың реакцияға қабілеттілігін анықтаушы факторлар
Органикалық қосылыстар құрылысының теориялық негіздері және олардың реакцияға қабілеттілігін анықтаушы факторлар Сурьма, Sb
Сурьма, Sb Nucleic acids
Nucleic acids Перемешивание в жидких средах
Перемешивание в жидких средах Биосенсорные системы
Биосенсорные системы Budowa pasmowa ciał stałych
Budowa pasmowa ciał stałych Їх згубна дія на організм людини СПИРТИ
Їх згубна дія на організм людини СПИРТИ  Атомно-емісійна спектрометрія з індуктивно-зв’язаною плазмою та рентгенофлуоресцентний аналіз 2
Атомно-емісійна спектрометрія з індуктивно-зв’язаною плазмою та рентгенофлуоресцентний аналіз 2