Содержание
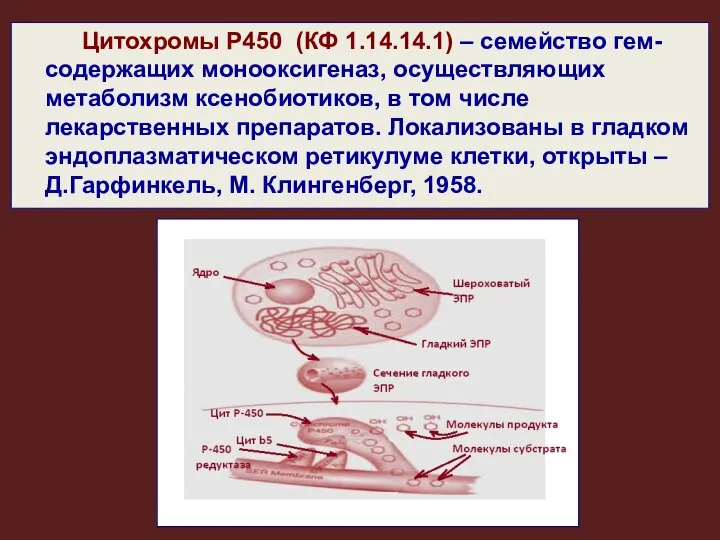
- 2. Цитохромы Р450 (КФ 1.14.14.1) – семейство гем-содержащих монооксигеназ, осуществляющих метаболизм ксенобиотиков, в том числе лекарственных препаратов.
- 3. Цитохром Р450 (англ.Cytochrome P450, CYP) Название указывает на то, что он окрашен (Р – от английского
- 4. Использование термина «цитохром» применительно к гемопротеинам класса Р450 нельзя считать удачным, так как функцией цитохромов является
- 5. Молекулярная масса различных цит. Р450 колеблется 44 - 60 кДа. Мономеры гемопротеина состоят из одной полипептидной
- 6. Цит. Р450 из P. putida содержит 4 антипараллельных спиральных участка, смесь спиралей и неупорядоченных структур, перемежающихся
- 7. Все мембранные цитохромы Р450 на N-концевом фрагменте пептидной цепи имеют короткий гидрофобный участок, содержащий от 12
- 8. Цитохромы P450 отсутствуют только у облигатно анаэробных организмов. Описано не менее 11 500 ? белков системы
- 9. Система цит. P450 участвует в окислении многочисленных соединений, как эндогенных, так и экзогенных. Цит. Р450-зависимые монооксигеназы
- 10. Ферменты семейства цитохрома P450 разнообразны и различаются: по функциям, типами ферментативной активности, регуляторами активности (ингибитораи, индукторами).
- 11. Цитохром Р450, наряду с монооксигеназной активностью, может проявлять оксидазную (А.И. Арчаков с сотр.), т.е. катализировать удаление
- 12. Цит. P-450 кодируются суперсемейством генов. У человека в системе цит. Р-450 выявлено 57 генов и более
- 13. В настоящее время известны тысячи изоформ (изоферментов) цит. Р-450. Изоформы, имеющие более 40 % общего аминокислотного
- 14. Цит. P450 катализируют ω-окисление насыщенных жирных кислот (ж.к.), перекисное окисление ненасыщеных ж.к., гидроксилирование стероидных гормонов, желчных
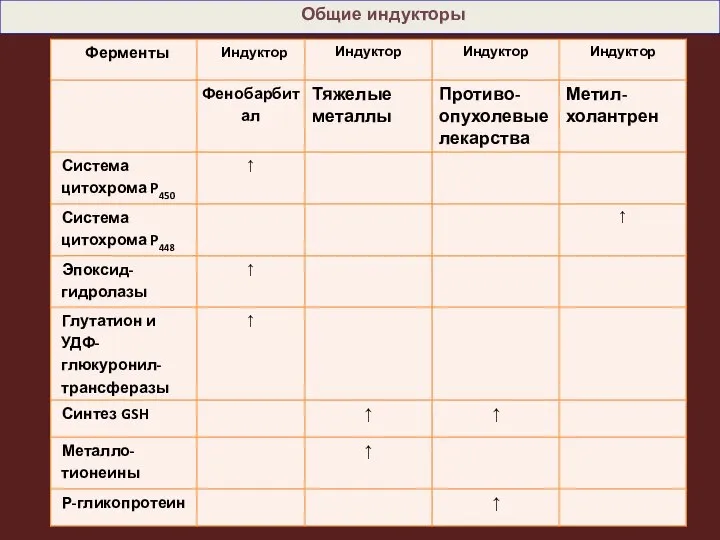
- 15. Общие индукторы
- 16. Фенобарбитал активирует синтез цит. Р450, УДФ-глюкуронилтрансферазы и эпоксид гидролазы. Например, у животных, которым вводили индуктор фенобарбитал,
- 17. В настоящее время описано более 250 химических соединений, вызывающих индукцию микросомальных ферментов. Индукторы монооксигеназных систем разделяются
- 18. Имеются химические вещества, способные ингибировать как ферменты 1-й фазы биотрансформации (изоферменты цитохрома Р-450) и 2-й фазы
- 19. Элетронтранспортные цепи ЭПР 1 цепь включает: 1) цитохром P450, имеет центры связывания для O2 и гидрофобного
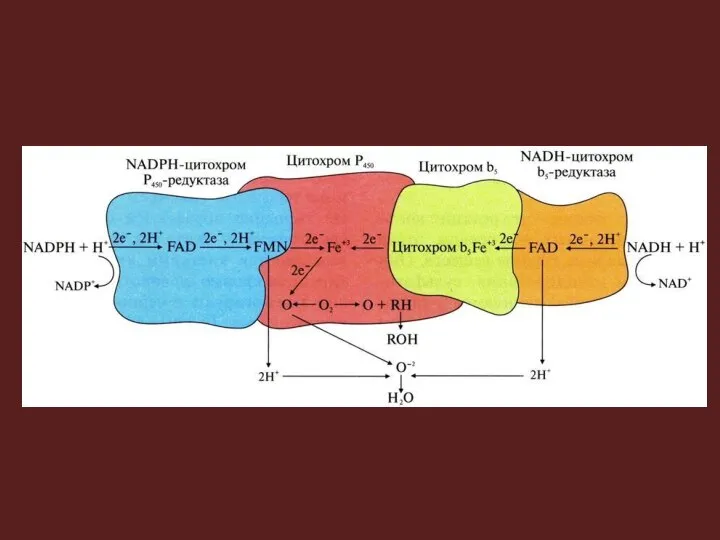
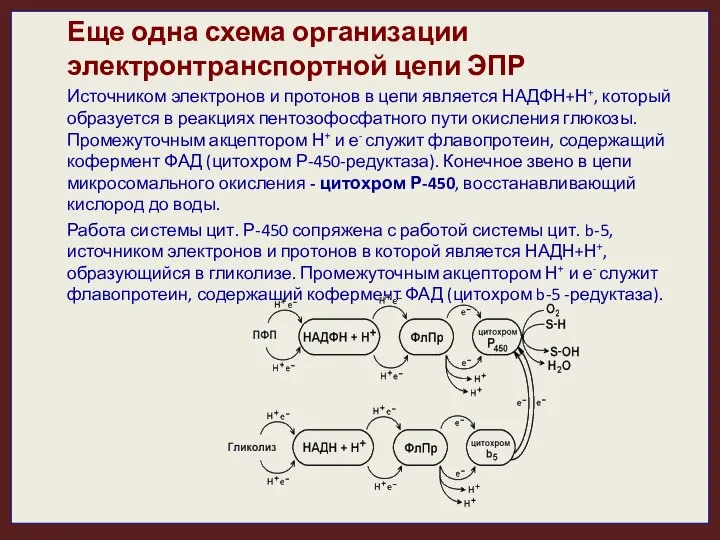
- 21. Еще одна схема организации электронтранспортной цепи ЭПР Источником электронов и протонов в цепи является НАДФН+Н+, который
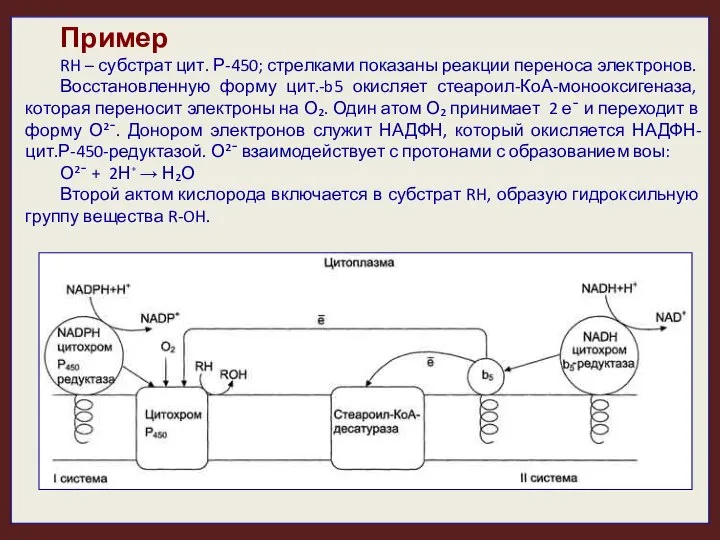
- 22. Пример RH – субстрат цит. Р-450; стрелками показаны реакции переноса электронов. Восстановленную форму цит.-b5 окисляет стеароил-КоА-монооксигеназа,
- 23. НАДФ-Н-цитохром Р-450-редуктаза – флавопротеин. Один моль фермента содержит по одному молю флавинмононуклеотида (ФМН) и флавинадениндинуклеотида (ФАД).
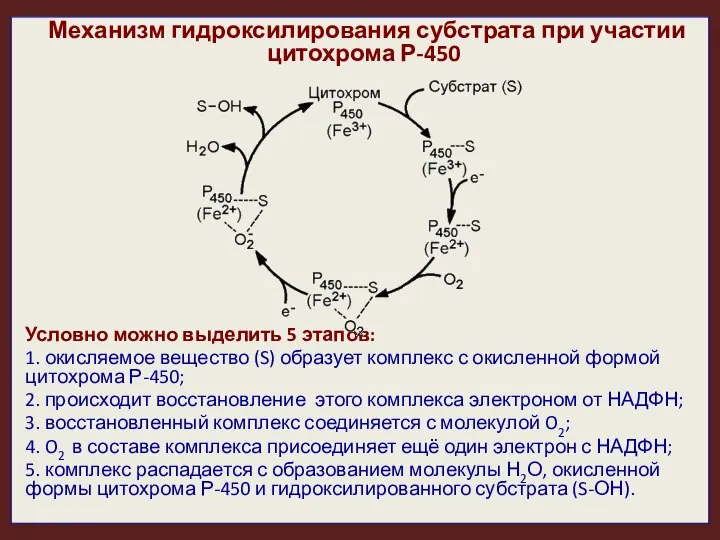
- 24. Механизм гидроксилирования субстрата при участии цитохрома Р-450 Условно можно выделить 5 этапов: 1. окисляемое вещество (S)
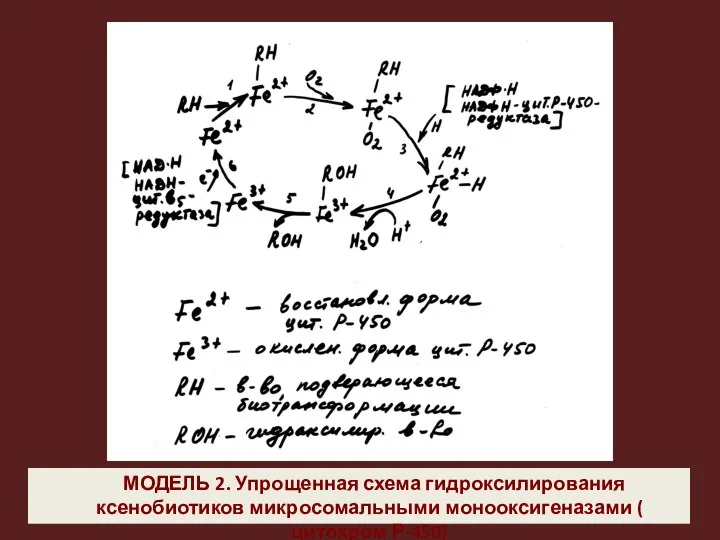
- 25. МОДЕЛЬ 2. Упрощенная схема гидроксилирования ксенобиотиков микросомальными монооксигеназами ( цитохром Р-450)
- 26. В отличие от митохондриальной дыхательной цепи, в монооксигеназной цепи при переносе электронов не происходит аккумулирования энергии
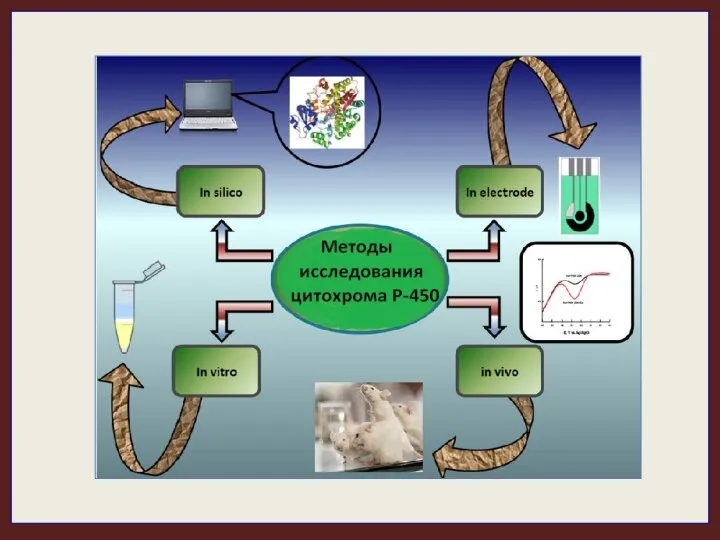
- 28. Цитохромы Р-450 являются мембранными белками и при исследовании их каталитической активности требуется сложное реконструирование монооксигеназной системы
- 29. В настоящее время разработаны электрохимические биосенсорные системы на основе иммобилизованных на электроде цитохромов Р-450. Электрокаталитическая реакция
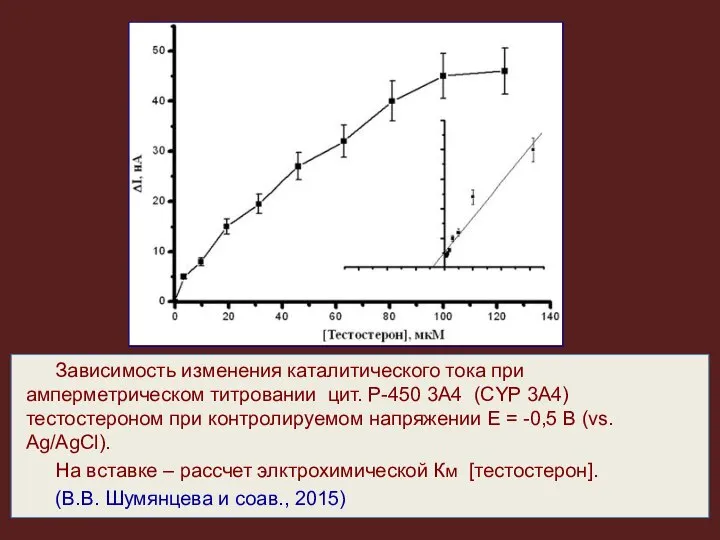
- 30. Зависимость изменения каталитического тока при амперметрическом титровании цит. Р-450 3А4 (CYP 3А4) тестостероном при контролируемом напряжении
- 31. Разработка биосенсоров на основе электрохимических цитохром Р450-содержащих систем позволяет выявлять субстраты (ксенобиотики), исследовать эффекты лекарственных препаратов
- 32. Преимущества электрохимического метода исследования цитохром Р450-монооксигеназной системы 1) электрохимическая система не требует использования дорогостоящих и неустойчивых
- 33. Методы оценки состояния системы биотранс- формации ксенобиотиков: Высокоэффективная жидкостная хроматография (ВЭЖХ). Дает возможность исследовать аналиты в
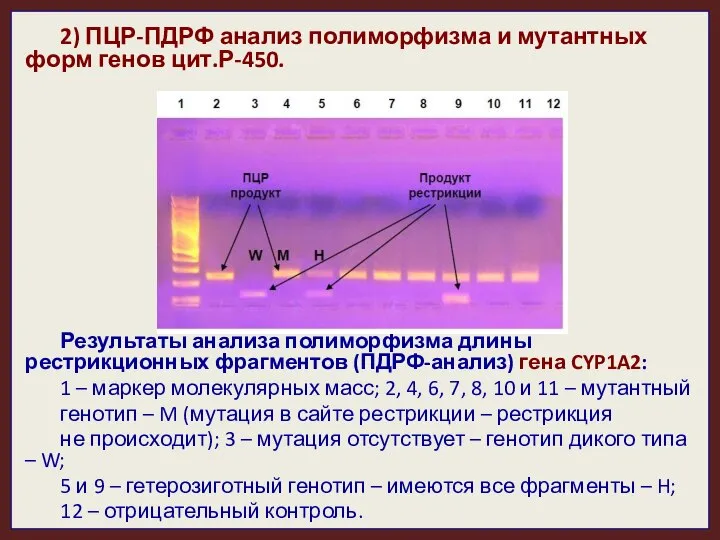
- 34. 2) ПЦР-ПДРФ анализ полиморфизма и мутантных форм генов цит.Р-450. Результаты анализа полиморфизма длины рестрикционных фрагментов (ПДРФ-анализ)
- 35. 3) ДНК-чипы Позволяют одновременно определять очень большое количество полиморфизмов в одной пробе. На твердом чипе очень
- 36. 4) Компьютерные программы для моделирования взаимодействия лигандов с цитохромами Р450 Для изучения взаимодействия субстрата и фермента
- 37. При описании взаимодействия цит.Р-450 и лигандов оценивается роль пространственных и энергетических факторов, т.к. вклад этих факторов
- 38. Р-ция наз. региоспецифичной, если в качестве единств. продукта (в пределах ошибки) образуется один из двух или
- 39. QSAR модели. Количественные взаимоотношения структура-активность (QSAR - англ. сокр. от Quantitative Structure-Activity Relationships) позволяют по описанию
- 40. Суперсемейство цит. Р-450 катализирует большое количество реакций, проходящих по разным механизмам, поэтому классические QSAR методы не
- 41. Основные цитохромы Р450, ответственные за метаболизм лекарств в организме человека исследуемые in silico – это подсемейство
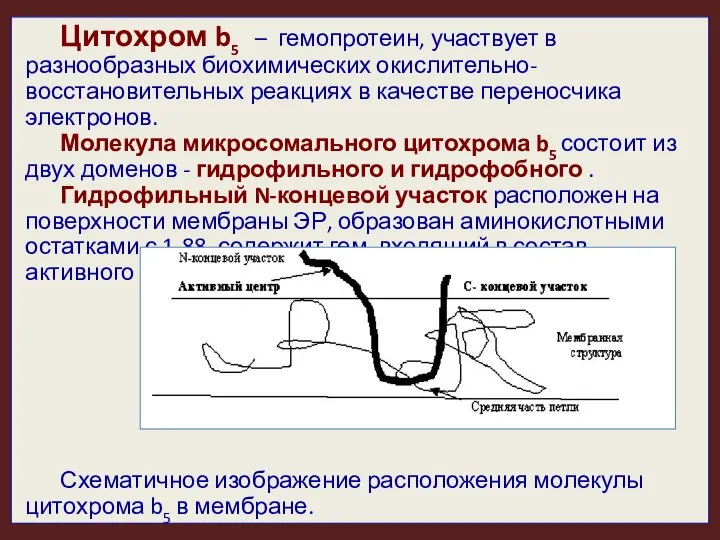
- 42. Цитохром b5 – гемопротеин, участвует в разнообразных биохимических окислительно-восстановительных реакциях в качестве переносчика электронов. Молекула микросомального
- 43. Гидрофобный домен цитохрома b5 заякорен в липидном бислое (ЭПР или митохондриальной), спирализован, образован остатками аминокислот C-
- 44. Цитохром b5 наружной мембраны митохондриий, по сравнению с микросомальным обладает более низким редокс-потенциалом, молекула более устойчива
- 45. Роль цитохрома b5 в реакциях, катализируемых изоформами системы цитохрома Р-450. Возможные механизмы стимулирующего влияния цит. b5
- 46. цит. b5 взаимодействует с цит. Р-450 с образованием комплекса двух гемопротеинов и последующей передачей двух электронов
- 47. Влияние цит. b5 на изменение скорости реакции, спектра метаболитов и образование активных форм кислорода в реакциях
- 48. цит. b5 у разных видов (человек и хомячок) может не изменять скорости окисления соединения (нитрозамин) или
- 49. Влияние цитохрома b5 на изменение скорости реакции, спектра метаболитов и образование активных форм кислорода в реакциях
- 51. Скачать презентацию




































 Физико-химические и электро-физические свойства А3В5. Сравнительный анализ
Физико-химические и электро-физические свойства А3В5. Сравнительный анализ Алкадиены
Алкадиены Основные классы неорганических веществ
Основные классы неорганических веществ Уравнение материального баланса для элементарного объема проточного химического реактора
Уравнение материального баланса для элементарного объема проточного химического реактора Липиды. Химические свойства
Липиды. Химические свойства Лекция 8. Стационарная кинетика (продолжение). Сложные ферментативные реакции
Лекция 8. Стационарная кинетика (продолжение). Сложные ферментативные реакции Витамины в нашей еде
Витамины в нашей еде Стиральные порошки и средства для стирки 2016
Стиральные порошки и средства для стирки 2016 Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Норми радіаційної безпеки (НРБУ-97)
Норми радіаційної безпеки (НРБУ-97) Альбітит-грейзенові родовища
Альбітит-грейзенові родовища Водород
Водород Микробиологическая лаборатория и ее задачи. Микроскоп и работа с ним. Морфология шаровидных бактерий
Микробиологическая лаборатория и ее задачи. Микроскоп и работа с ним. Морфология шаровидных бактерий Кислоты
Кислоты Вредное воздействие нитратов на организм человека Выполнила: ученица 10 класса «А» Средней школы №1120
Вредное воздействие нитратов на организм человека Выполнила: ученица 10 класса «А» Средней школы №1120  Морфология палочковидных и извитых бактерий. Краски используемые в микробиологии. Приготовление бакпрепаратов. Методы окраски
Морфология палочковидных и извитых бактерий. Краски используемые в микробиологии. Приготовление бакпрепаратов. Методы окраски Механизмы нейропротекторного действия уабаина при эксайтотоксическом стрессе в нейронах коры крыс
Механизмы нейропротекторного действия уабаина при эксайтотоксическом стрессе в нейронах коры крыс Аммиак. Физические и химические свойства. Получение и применение
Аммиак. Физические и химические свойства. Получение и применение Мило. Мийні засоби
Мило. Мийні засоби  Презентация по Химии "Оксиген. Кисень" - скачать смотреть бесплатно
Презентация по Химии "Оксиген. Кисень" - скачать смотреть бесплатно Получение витаминов
Получение витаминов Изомерия алкенов
Изомерия алкенов Мыла: прошлое, настоящее, будущее
Мыла: прошлое, настоящее, будущее Кислородные соединения азота
Кислородные соединения азота Клиническая биохимия азотистого обмена. (Лекция 7)
Клиническая биохимия азотистого обмена. (Лекция 7) Основные свойства адсорбентов. Определение их параметров
Основные свойства адсорбентов. Определение их параметров Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой
Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой Единые смеси
Единые смеси