Содержание
- 2. Тема урока «Основания органические и неорганические»
- 3. Цель урока: Обобщить и систематизировать знания об основаниях
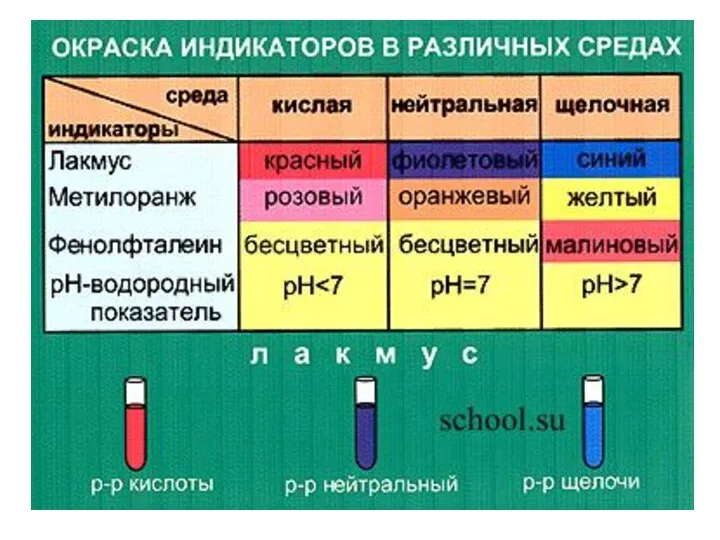
- 4. Исследовательская работа Определите с помощью индикатора (лакмуса, фенолфталеина или метилового оранжевого) в какой пробирке находится основание.
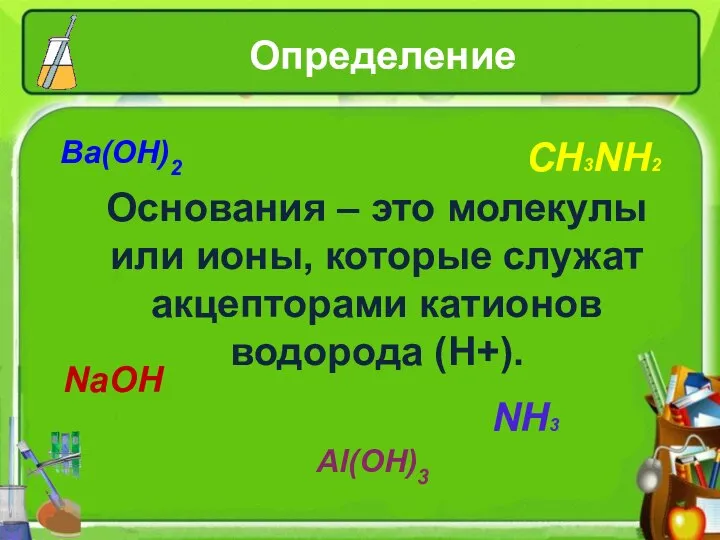
- 6. Определение Ba(OH)2 CH3NH2 NaOH Al(OH)3 NH3 Основания – это молекулы или ионы, которые служат акцепторами катионов
- 7. Признаки классификации оснований Растворимость Наличие кислорода Кислотность Степень ЭД Летучесть Стабильность
- 8. Свойства оснований Физические: Растворимые основания – бесцветный раствор Нерастворимые основания – цветные осадки Химические: Изменение окраски
- 11. Свойства оснований Физические: Растворимые основания – бесцветный раствор Нерастворимые основания – цветные осадки Химические: Изменение окраски
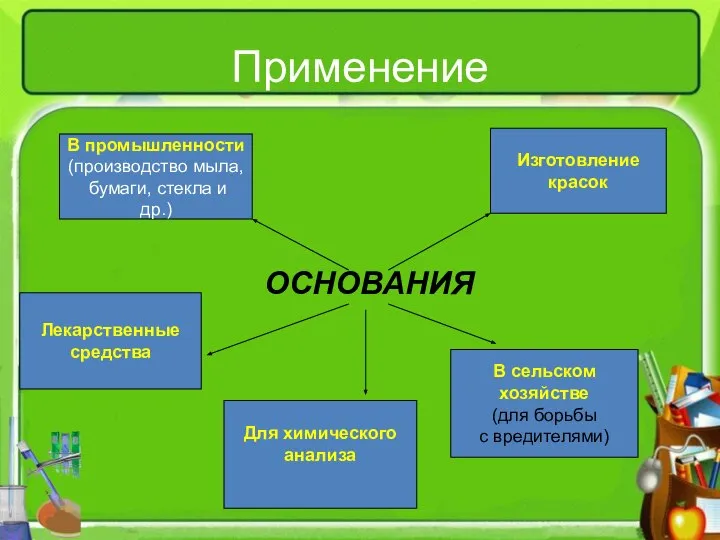
- 12. Применение ОСНОВАНИЯ В промышленности (производство мыла, бумаги, стекла и др.) Изготовление красок Лекарственные средства В сельском
- 13. Закрепление Задание №1. Дайте классификационную характеристику Ba(OH)2. Задание №2. Запишите уравнения реакций, подтверждающих его основные свойства.
- 14. Домашнее задание стр.251-257 (п.21) Дайте классификационную характеристику и запишите уравнения реакций, подтверждающих основные свойства Со(ОН)2. *
- 16. Скачать презентацию










 Тема урока: Силикатная промышленность
Тема урока: Силикатная промышленность Використання хімічних явищ у художній творчості й народних ремеслах
Використання хімічних явищ у художній творчості й народних ремеслах Электронная формула атома магния
Электронная формула атома магния Қатты денеерітінді шекарасындағы адсорбция. Адсорбенттер
Қатты денеерітінді шекарасындағы адсорбция. Адсорбенттер Металлы II А группы
Металлы II А группы Хлор 11 класс - Презентация
Хлор 11 класс - Презентация Алкены (этен)
Алкены (этен) Деконтаминация в ЛПО. Подбор дезинфицирующих средств. Практикум 7
Деконтаминация в ЛПО. Подбор дезинфицирующих средств. Практикум 7 Решение задач. Алкины
Решение задач. Алкины Гидролиз
Гидролиз Лужні метали Підготувала: Анна Сідорова
Лужні метали Підготувала: Анна Сідорова  Металлическая связь
Металлическая связь Циклоалканы. Физические свойства циклоалканов
Циклоалканы. Физические свойства циклоалканов Увеличение эффективности печи установки АТ
Увеличение эффективности печи установки АТ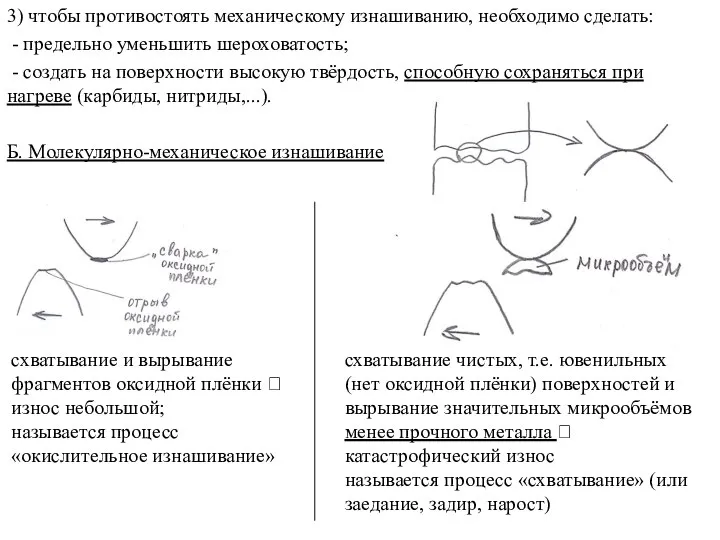 Молекулярно-механическое изнашивание
Молекулярно-механическое изнашивание Производство аммиака и азотной кислоты
Производство аммиака и азотной кислоты Коллоидно-химический синтез квантовых точек на основе сульфидов свинца и кадмия
Коллоидно-химический синтез квантовых точек на основе сульфидов свинца и кадмия Солеобразующие оксиды
Солеобразующие оксиды Растворы. рН среды. Вспомогательные вещества. Химические вещества и материалы в индустрии красоты. Лекция 7
Растворы. рН среды. Вспомогательные вещества. Химические вещества и материалы в индустрии красоты. Лекция 7 Высшие жирные кислоты. Липиды
Высшие жирные кислоты. Липиды Предмет химии. Вещества и их физические свойства. (8 класс)
Предмет химии. Вещества и их физические свойства. (8 класс)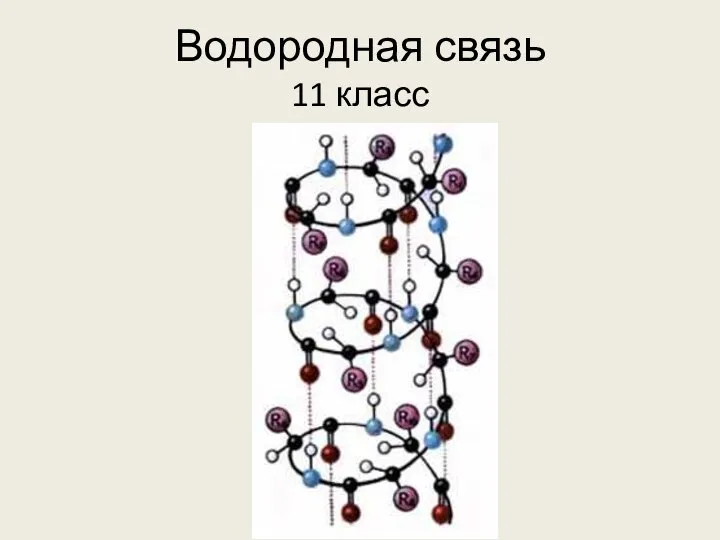 Водородная связь
Водородная связь Железо в сплавах и природе. Состав железа
Железо в сплавах и природе. Состав железа рН среды и здоровье человека
рН среды и здоровье человека Б Е Л К И
Б Е Л К И Сера и ее свойства
Сера и ее свойства Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов
Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов Микроэлементы
Микроэлементы