Содержание
- 2. Атомы металлов легко отдают электроны т. к. у них большой атомный радиус и мало электронов на
- 3. МЕТАЛЛИЧЕСКАЯ СВЯЗЬ - связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов
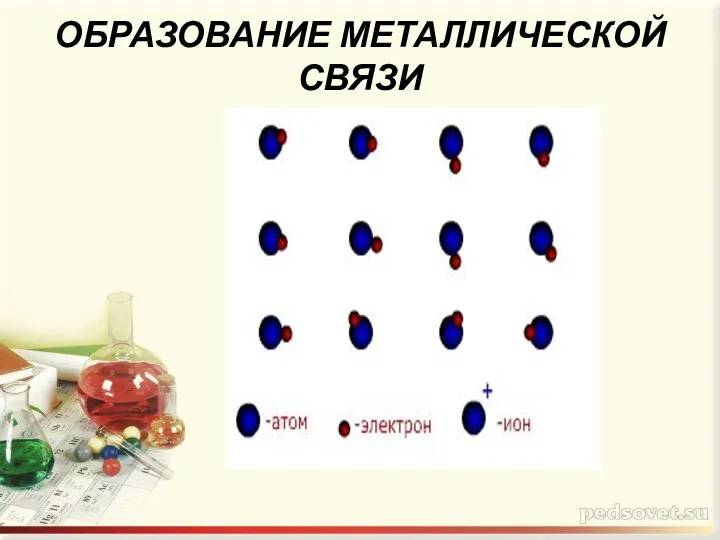
- 4. ОБРАЗОВАНИЕ МЕТАЛЛИЧЕСКОЙ СВЯЗИ
- 5. Оторвавшиеся электроны перемещаются от одного иона к другому , связывая их в единое целое Небольшое количество
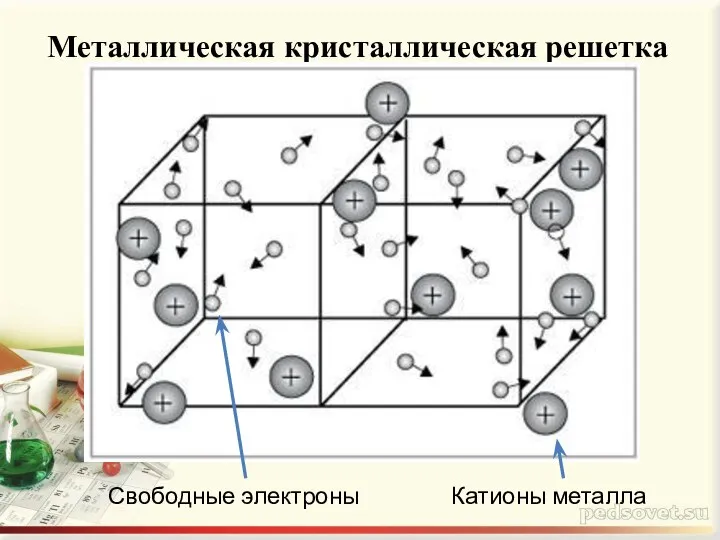
- 6. Металлическая кристаллическая решетка Свободные электроны Катионы металла
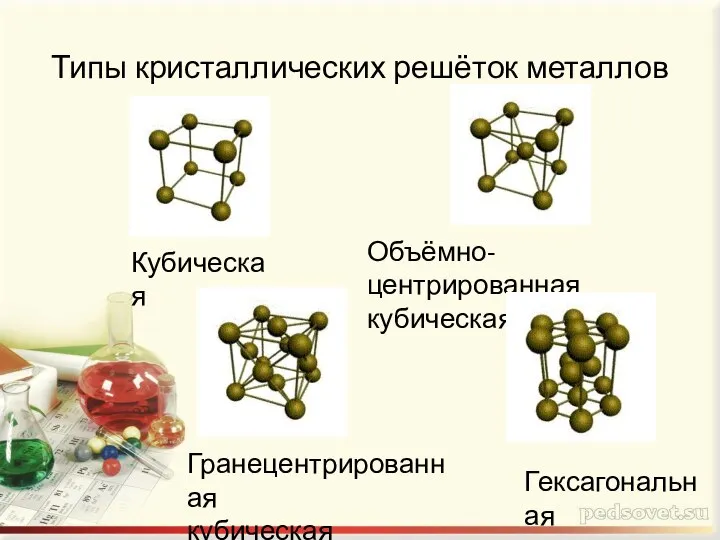
- 7. Типы кристаллических решёток металлов Кубическая Объёмно-центрированная кубическая Гранецентрированная кубическая Гексагональная
- 8. Металлическая связь характерна для металлов и их сплавов в твёрдом и жидком состоянии
- 9. Металлическая связь характеризуется: Небольшим числом валентных электронов Она слабее ковалентной и ионной связи Она определяет все
- 10. Металлический блеск Теплопроводность Электропроводность Ковкость (пластичность) Наличием свободных электронов объясняются физические свойства металлов
- 11. Металлическая связь похожа на Ионную связь (происходит образование катионов, ē связывают ионы Ме за счет электростатического
- 12. Металлическая химическая связь характерна для металлов и их сплавов Металлическая связь как и ковалентная образуется за
- 13. В металлической связи как и в ионной образуются ионы. Основа химической связи одна - электростатическое взаимодействие
- 16. Скачать презентацию










 Оксиди
Оксиди Задача №2 «Спящий Амур». Команда гимназии №1 «Берлинская лазурь»
Задача №2 «Спящий Амур». Команда гимназии №1 «Берлинская лазурь» Алканы. Предельные углеводороды. Парафины. Насыщенные углеводороды
Алканы. Предельные углеводороды. Парафины. Насыщенные углеводороды Симметрия кристаллов, текстур и элементы кристаллофизики
Симметрия кристаллов, текстур и элементы кристаллофизики Кинетика сложных реакций
Кинетика сложных реакций Механизмы органических реакций
Механизмы органических реакций Простые вещества неметаллы
Простые вещества неметаллы Химия вокруг нас
Химия вокруг нас Фармацевтические эмульсии
Фармацевтические эмульсии Қазіргі кезде қолданылатын дезинсектицидтер
Қазіргі кезде қолданылатын дезинсектицидтер Полимеры
Полимеры Материаловедение и технология обработки материалов
Материаловедение и технология обработки материалов Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на.
Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на.  Цветные реакции белков Качественные реакции на остатки аминокислот
Цветные реакции белков Качественные реакции на остатки аминокислот  Сера. Свойства серы
Сера. Свойства серы Синтез реакционноспособных олигомеров и полимеров на их основе. Лекция 1
Синтез реакционноспособных олигомеров и полимеров на их основе. Лекция 1 Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей
Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей Презентация по Химии "кпк" - скачать смотреть бесплатно
Презентация по Химии "кпк" - скачать смотреть бесплатно Открытия в области химии во время Великой Отечественной войны
Открытия в области химии во время Великой Отечественной войны Необходимые навыки для составления уравнений ОВР
Необходимые навыки для составления уравнений ОВР Периодический закон, периодическая система. Формулировка периодического закона Д.И. Менделеева
Периодический закон, периодическая система. Формулировка периодического закона Д.И. Менделеева Пестициды (ядохимикаты)
Пестициды (ядохимикаты) Химическое оборудование в быту. Урок №3
Химическое оборудование в быту. Урок №3 6-членные гетероциклы с одним гетероатомом
6-членные гетероциклы с одним гетероатомом Карбоновые кислоты
Карбоновые кислоты Арены. Природные источники углеводородов
Арены. Природные источники углеводородов Синтез сополимеров с заданным порядком присоединения звеньев в цепи методом интербиполиконденсации
Синтез сополимеров с заданным порядком присоединения звеньев в цепи методом интербиполиконденсации