Содержание
- 2. * Дисперсной называют систему (ДС), состоящую из дисперсной фазы – совокупности раздробленных частиц и непрерывной дисперсионной
- 3. * Количественная характеристика дисперсности – степень раздробленности D = 1/l, где l – размер дисперсных частиц.
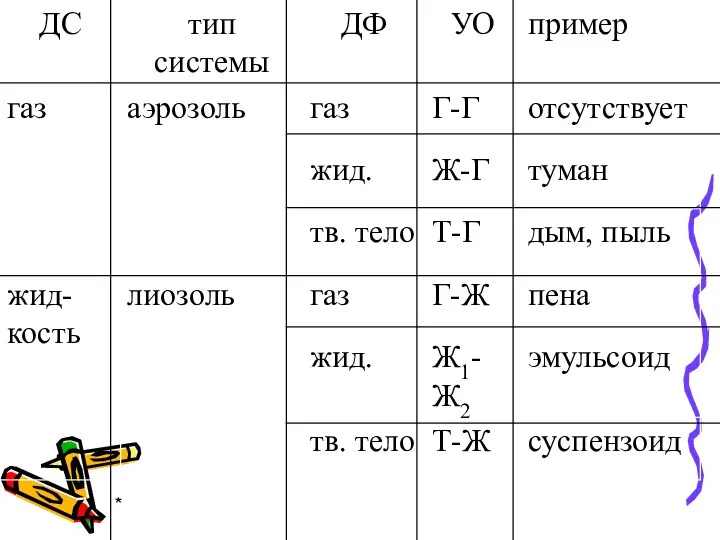
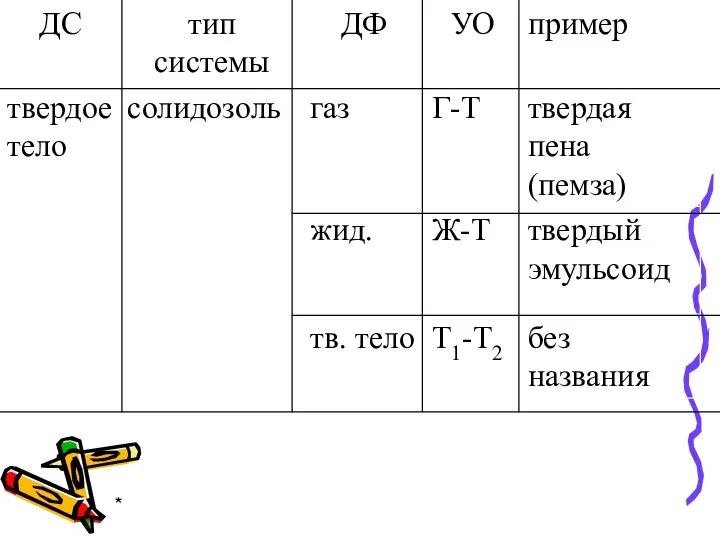
- 4. * Классификация по агрегатному состоянию
- 5. *
- 6. *
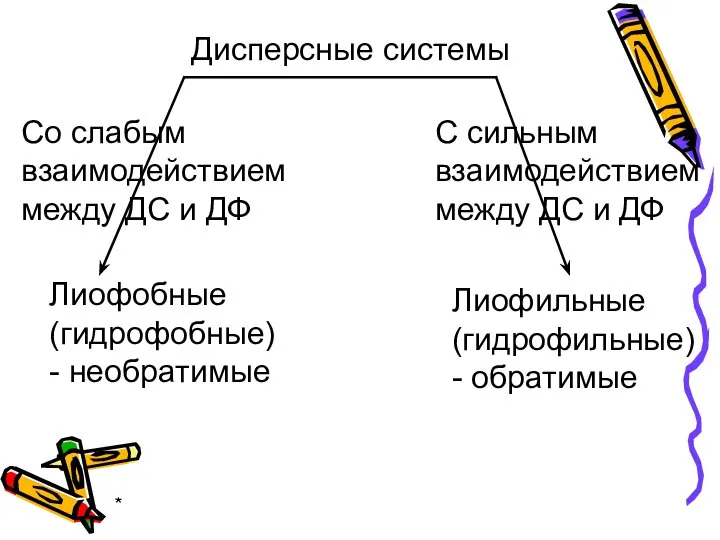
- 7. * Дисперсные системы Со слабым взаимодействием между ДС и ДФ С сильным взаимодействием между ДС и
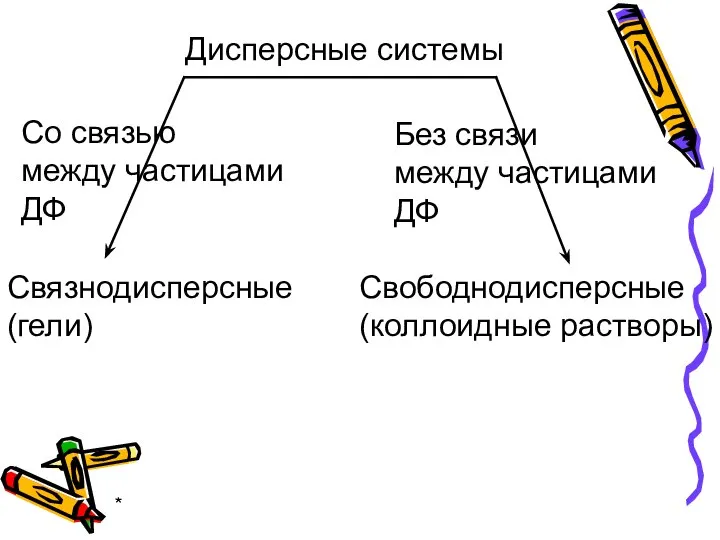
- 8. * Дисперсные системы Со связью между частицами ДФ Без связи между частицами ДФ Связнодисперсные (гели) Свободнодисперсные
- 9. * Методы получения лиофобных коллоидов: 1. диспергационные механическое дробление измельчение с помощью ультразвука электрическое диспергирование химическое
- 10. * 2. конденсационные физическая конденсация (замена растворителя) химическая конденсация (реакции гидролиза, окисления, восстановления, конденсации)
- 11. * Метод получения лиофильных коллоидов: Увеличение концентрации ПАВ до критической концентрации мицелообразования.
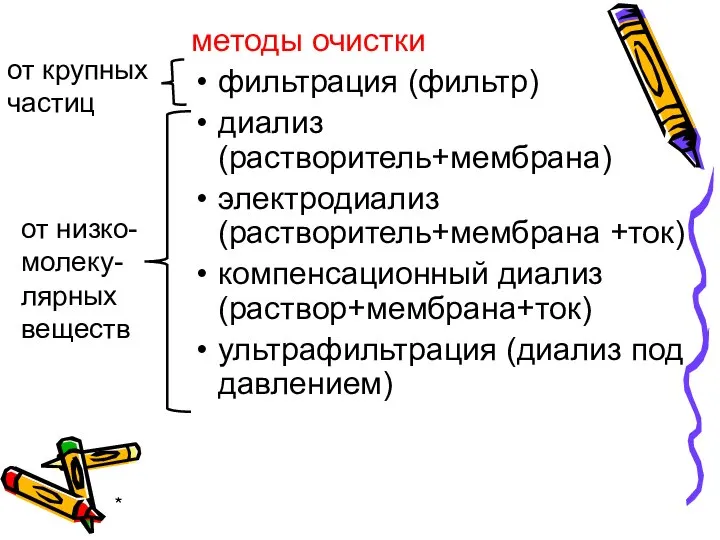
- 12. * методы очистки фильтрация (фильтр) диализ (растворитель+мембрана) электродиализ (растворитель+мембрана +ток) компенсационный диализ (раствор+мембрана+ток) ультрафильтрация (диализ под
- 13. * Строение мицелл в лиофобных коллоидных растворах. Мицеллой лиофобной системы называется гетерогенная микросистема, которая состоит из
- 14. * Pb(NO3)2 + 2KI = PbI2 + 2KNO3 избыток mPbI2 nPb2+ 2(n-x)NO3- 2x NO3- 2x+ агрегат
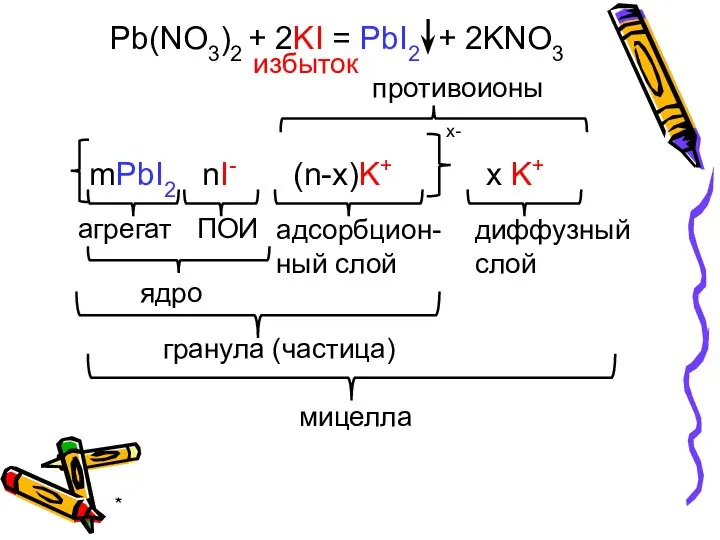
- 15. * Pb(NO3)2 + 2KI = PbI2 + 2KNO3 избыток mPbI2 nI- (n-x)K+ x K+ x- агрегат
- 16. * Строение мицелл в лиофильных коллоидных растворах. Мицеллами лиофильных коллоидных растворов называются ассоциаты из молекул ПАВ
- 17. * Коллоидные ПАВ – вещества, которые с одним и тем же растворителем в зависимости от условий
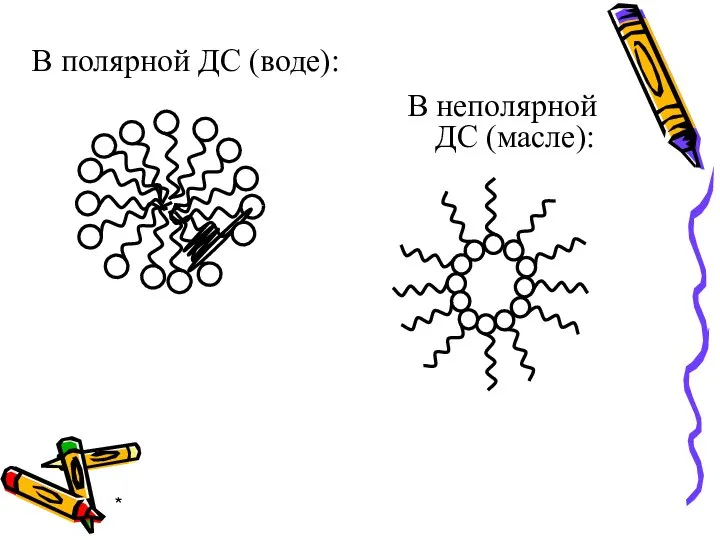
- 18. * В полярной ДС (воде): В неполярной ДС (масле):
- 19. * Способностью к мицеллообразованию обладают не все ПАВ. В водных растворах к мицеллообразующим соединениям относятся соли
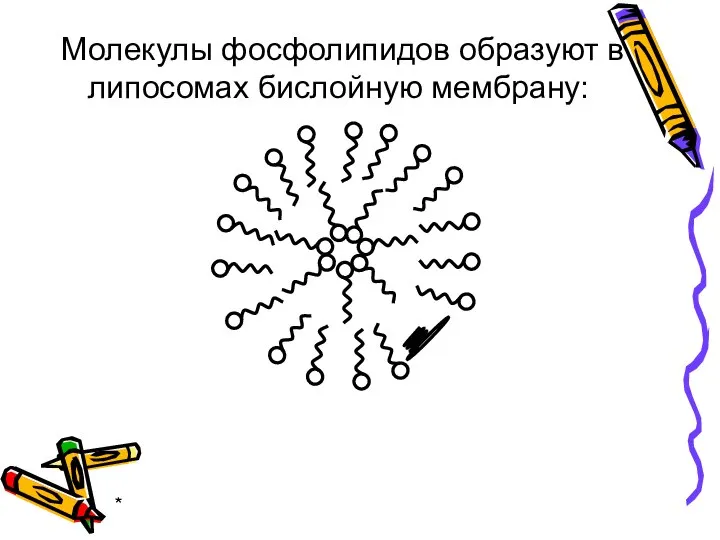
- 20. * Молекулы фосфолипидов образуют в липосомах бислойную мембрану:
- 21. * Липосомы используют для направленной доставки лекарственных веществ (противоопухолевых препаратов, инсулина) к определенным органам или зонам
- 22. * Важнейшее свойство растворов коллоидных ПАВ – солюбилизация. Солюбилизация – самопроизвольный переход нерастворимых или малорастворимых низкомолекулярных
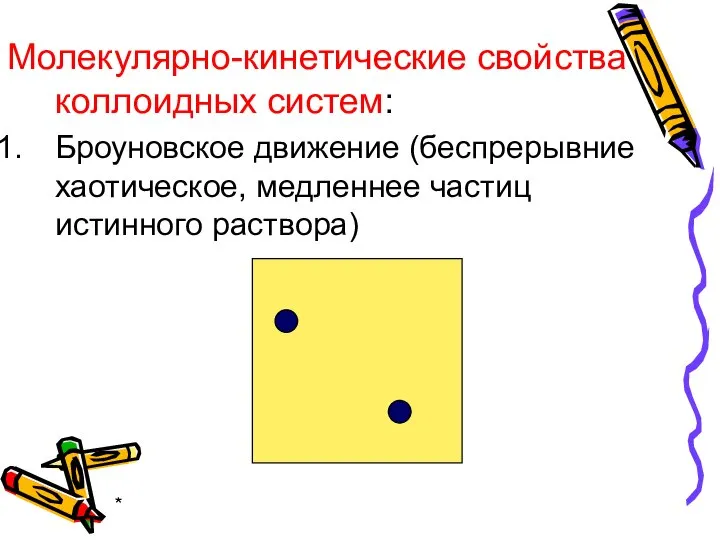
- 23. * Молекулярно-кинетические свойства коллоидных систем: Броуновское движение (беспрерывние хаотическое, медленнее частиц истинного раствора)
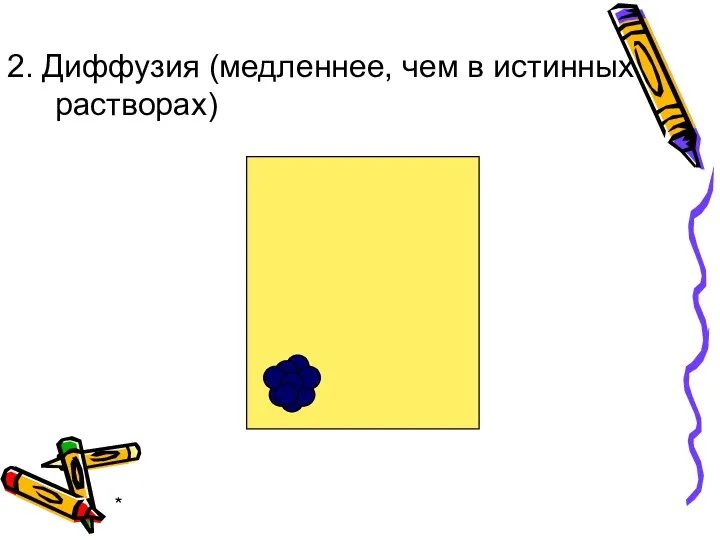
- 24. * 2. Диффузия (медленнее, чем в истинных растворах)
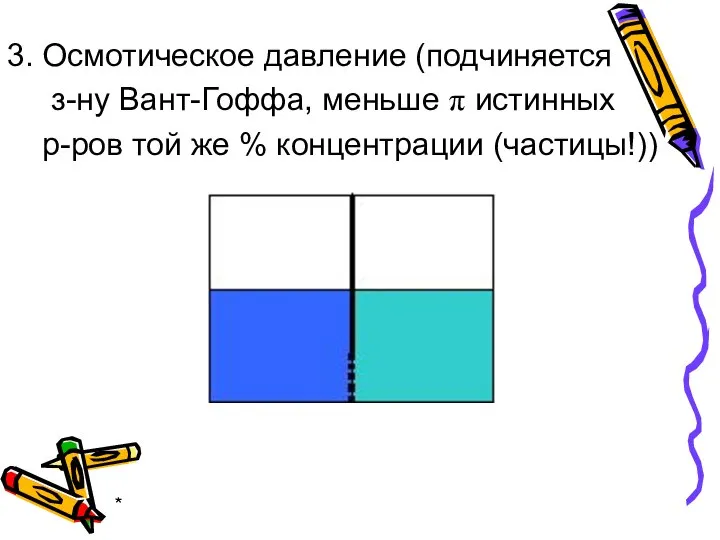
- 25. * 3. Осмотическое давление (подчиняется з-ну Вант-Гоффа, меньше π истинных р-ров той же % концентрации (частицы!))
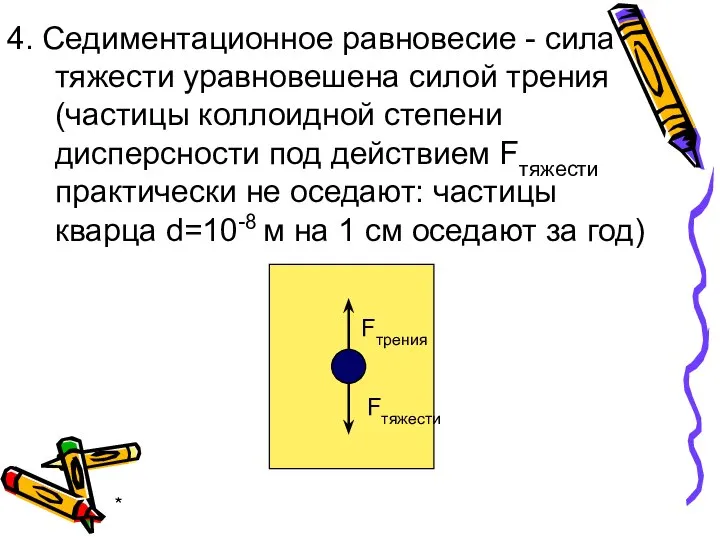
- 26. * 4. Седиментационное равновесие - сила тяжести уравновешена силой трения (частицы коллоидной степени дисперсности под действием
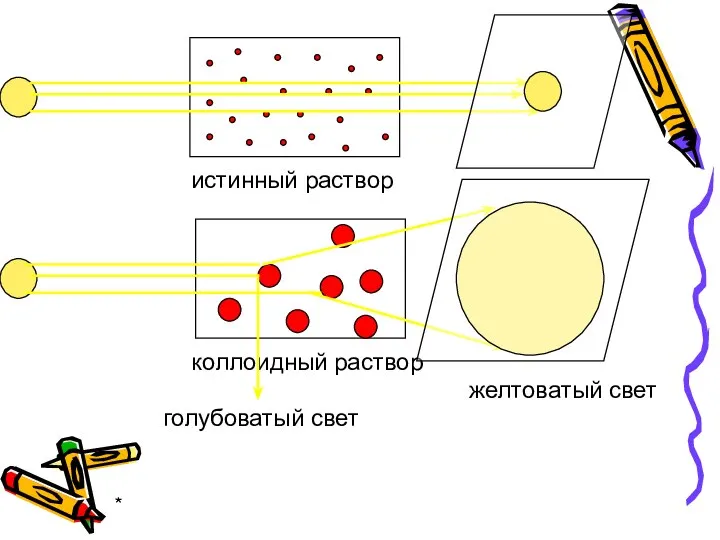
- 27. * Оптические свойства коллоидных систем: рассеяние света опалесценция (окраска в рассеянном и проходящем свете разная, наиболее
- 28. *
- 29. * истинный раствор коллоидный раствор свет свет желтоватый свет голубоватый свет
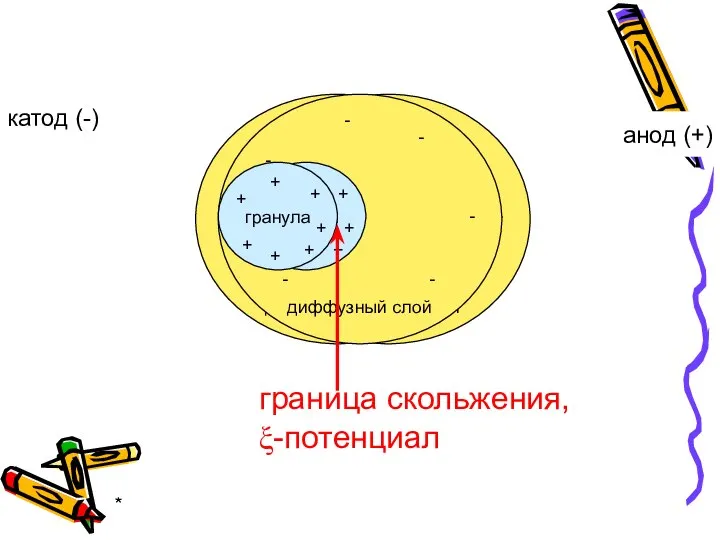
- 30. * Электрические свойства коллоидных систем: перемещение частиц одной фазы относительно частиц другой фазы под действием электрического
- 31. * катод (-) анод (+) граница скольжения, ξ-потенциал
- 32. * Биологические жидкости организма (кровь, плазма, моча и т. п.) - коллоидные системы. О состоянии организма
- 33. * Седиментационная (кинетическая) устойчивость способность частиц ДФ находится во взвешенном состоянии и не оседать под действием
- 34. * Конденсационная устойчивость -способность дисперсных систем сохранять неизменной с течением времени удельную поверхность.
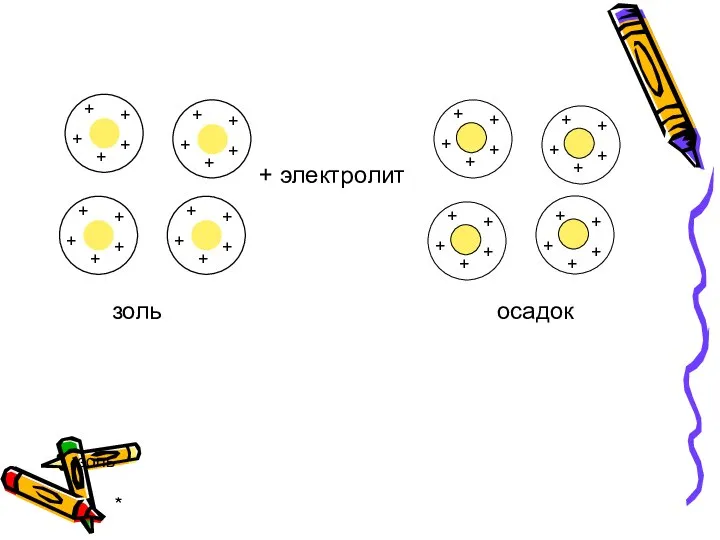
- 35. * Коагуляция процесс слипания коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной
- 36. * золь + электролит осадок золь
- 37. * Правило Шульце-Гарди: коагулирующая способность электролита возрастает с увеличением заряда коагулирующего иона, а коагулирующим действием обладает
- 38. * Для биологических систем наибольшее значение имеет коагуляция при добавлении электролита (коллоидные растворы биологических жидкостей находятся
- 39. * Пептизация – процесс перехода свежеполученного при коагуляции осадка в золь под действием веществ-пептизаторов (процесс обратный
- 40. * Значение коллоидной защиты: недостаток защитного действия – образование в организме почечных и желчных камней, отложение
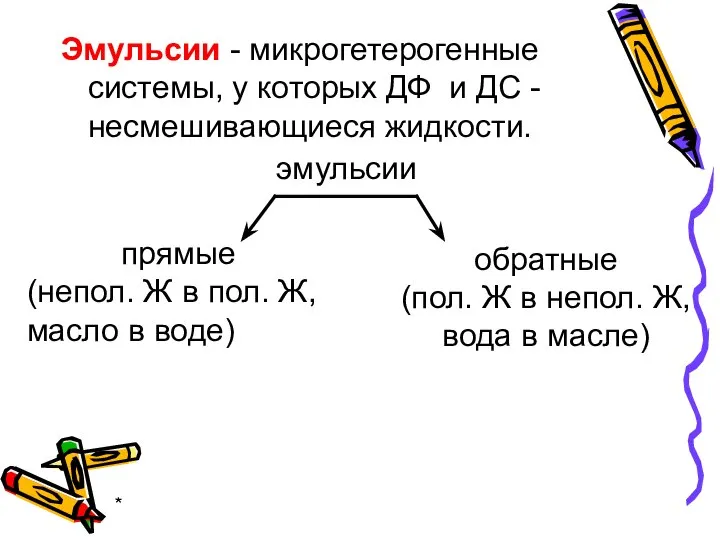
- 41. * Эмульсии - микрогетерогенные системы, у которых ДФ и ДС - несмешивающиеся жидкости. эмульсии прямые (непол.
- 42. * Суспензии – микрогетергенные системы с жидкой ДС и твердыми частицами ДФ. Аэрозоли – дисперсные системы
- 43. * Значение для медицины: положительное Эмульсии лекарственных веществ прямые – для внутреннего применения, обратные – для
- 45. Скачать презентацию


























 Обзор и анализ современных порошковых материалов в аддитивных технологиях
Обзор и анализ современных порошковых материалов в аддитивных технологиях Динамическая вулканизация термоэластопластов
Динамическая вулканизация термоэластопластов Сода: мифы и реальность
Сода: мифы и реальность Органические вещества. Углеводы. Липиды
Органические вещества. Углеводы. Липиды Нуклеиновые кислоты
Нуклеиновые кислоты Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства Стероиды. Дицетин-холестерин-ацилтрансферазная реакция
Стероиды. Дицетин-холестерин-ацилтрансферазная реакция Ионные уравнения
Ионные уравнения Титан (лат. Titanium; обозначается символом Ti)
Титан (лат. Titanium; обозначается символом Ti) Волшебный мир кристаллов
Волшебный мир кристаллов Поліетелен. Застосування поліетилену
Поліетелен. Застосування поліетилену Химический элемент платина
Химический элемент платина Жидкие кристаллы
Жидкие кристаллы Масс-спектрометрические методы определения газового состава
Масс-спектрометрические методы определения газового состава Розчинник
Розчинник Устойчивость и коагуляция золей
Устойчивость и коагуляция золей Изомерия органических соединений. 10 класс
Изомерия органических соединений. 10 класс Свойства и классификация нефти
Свойства и классификация нефти Аминокилоты. Получение и применение
Аминокилоты. Получение и применение Строение атома
Строение атома Важнейшие кислоты и кислотные остатки. (Леция 1)
Важнейшие кислоты и кислотные остатки. (Леция 1) Презентация по Химии "Химия в жизни человека" - скачать смотреть
Презентация по Химии "Химия в жизни человека" - скачать смотреть  Сложные эфиры в природе и их применение
Сложные эфиры в природе и их применение Биологически важные гетероциклы
Биологически важные гетероциклы Теория растворов (лекция 1)
Теория растворов (лекция 1) Коррозия металлов Учитель химии: Ильязова Р. Т.
Коррозия металлов Учитель химии: Ильязова Р. Т.  Нитрофенилалкиламины
Нитрофенилалкиламины Твердое состояние вещества. Плавление
Твердое состояние вещества. Плавление