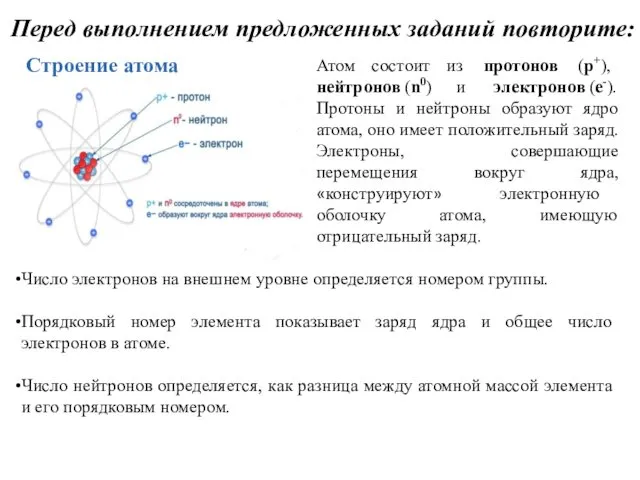
Энергетические уровни
Количество энергетических уровней равно номеру периода в периодической таблице, в
котором находится элемент.
К примеру, фосфор (Р) находится в третьем периоде, значит, атом фосфора имеет три энергетических уровня.
Внешний электронный слой заполняется у элементов главных подгрупп, причем число внешних электронов соответствует номеру группы. У элементов побочных подгрупп (d – элементы) заполняется предвнешний слой, а во внешнем слое остаются один или (чаще всего) два электрона.
Первый энергетический уровень включает s-подуровень, второй s- и p- подуровни, третий s-, p- и d-подуровни, а четвертый уровень s-, p-, d- и f-подуровни.
На s-подуровне могут находиться только 2 электрона, на p-подуровне- максимум 6 электронов, на d-подуровне - 10 электронов, а на f-подуровне до 14 электронов.











 Условная оптимизация методом классического математического анализа с применением множителей
Условная оптимизация методом классического математического анализа с применением множителей Metode electrochimice. Generalităţi
Metode electrochimice. Generalităţi Методика выделения чистых культур (3 день исследования)
Методика выделения чистых культур (3 день исследования) Сплавы, растворы и смеси. Задачи на концентрвцию
Сплавы, растворы и смеси. Задачи на концентрвцию КОВАЛЕНТНАЯ СВЯЗЬ ПОЛЯРНАЯ И НЕПОЛЯРНАЯ
КОВАЛЕНТНАЯ СВЯЗЬ ПОЛЯРНАЯ И НЕПОЛЯРНАЯ Д.И. Менделеевтің өмірі мен қызметі. Периодтық заңның маңызы
Д.И. Менделеевтің өмірі мен қызметі. Периодтық заңның маңызы Органическая химия. Этапы развития органической химии
Органическая химия. Этапы развития органической химии Функціональні матеріали для високоенергетичної електроніки. (Лекція 1)
Функціональні матеріали для високоенергетичної електроніки. (Лекція 1) Монокристаллы InSb. Свойства, выращивание, применение
Монокристаллы InSb. Свойства, выращивание, применение Периодический закон и периодическая система элементов Д.И. Менделеева
Периодический закон и периодическая система элементов Д.И. Менделеева Процессы формирования водородной плазмы в зоне резания
Процессы формирования водородной плазмы в зоне резания Вода. Растворимость, растворы
Вода. Растворимость, растворы Медьсодержащие соединения
Медьсодержащие соединения Наблюдения в сходящемся свете. Коноскопия
Наблюдения в сходящемся свете. Коноскопия Коллоидные растворы. Методы получения и очистки коллоидных растворов. Строение мицеллы гидрофобных систем. (Часть 1)
Коллоидные растворы. Методы получения и очистки коллоидных растворов. Строение мицеллы гидрофобных систем. (Часть 1) Общая химическая технология
Общая химическая технология Нафтены
Нафтены Соединения галогенов
Соединения галогенов Спирты. Строение. Физические и химические свойства. Спиртами (или алканолами ) называются органические вещества , молекулы которых
Спирты. Строение. Физические и химические свойства. Спиртами (или алканолами ) называются органические вещества , молекулы которых История мыловарения. Мыло своими руками
История мыловарения. Мыло своими руками Расчёт равновесного состава
Расчёт равновесного состава Коррозия металла
Коррозия металла Биополимерлер және олардың құрылымдық құрам бөліктері
Биополимерлер және олардың құрылымдық құрам бөліктері Физические и химические свойства воды
Физические и химические свойства воды Химические свойства алканов
Химические свойства алканов Реакции ионного обмена
Реакции ионного обмена Галлий
Галлий Группа рассеянных химических элементов
Группа рассеянных химических элементов