Содержание
- 2. Все вещества по электрической проводимости подразделяются на электролиты и неэлектролиты. Электролитами называют вещества, растворы или расплавы
- 3. ещё раз повторим:
- 4. Процесс распада электролитов на заряженные частицы ─ ионы называют электролитической диссоциацией («dissociation» ─ разобщение). Основные положения
- 5. Диссоциация протекает или в водных растворах, или при расплавлении электролита. В первом случае причиной диссоциации является
- 6. Уравнение, отражающее обратимый процесс (↔) диссоциации данного вещества, называется уравнением диссоциации. В растворе или расплаве преимущественно
- 7. Диссоциация кислот Кислотами называют электролиты, которые при диссоциации образуют катионы только Н+, например: HNO3 ⬄ H+
- 8. Основаниями называют электролиты, которые при диссоциации образуют анионы только OH─ : NaOH ⬄ Na+ + OH
- 9. Солями называют электролиты, которые при диссоциации образуют катионы металла (или аммония NH4+) и анионы кислотного остатка:
- 10. Сила электролитов определяется их степенью диссоциации ─ α (альфа). Степень диссоциации это отношение числа диссоциированных молекул
- 11. Итак, не все электролиты в одинаковой степени распадаются на ионы. Растворимые соли в водных растворах диссоциируют
- 12. Реакции обмена между растворами или расплавами электролитов называют ионообменными или ионными реакциями. Протекание таких реакций обнаруживается
- 13. С образованием осадка ( при написании уравнений используем «Таблицу растворимости» ): 1) NaCl + AgNO3 →
- 14. С выделением газа: 1) K2CO3 + 2HCl → 2KCl + H2CO3 2K+ + CO32─ + 2H+
- 15. С образованием воды (нейтрализация): 1) NaOH + HNO3 → NaNO3 + H2O Na+ + OH─ +
- 16. Ионные реакции между некоторыми солями и водой, протекающие с образованием новых ионов, называются гидролизом солей («водным
- 17. 2) Вода и соль сильного основания, но слабой кислоты образуют недиссоциирующие ионы слабой кислоты, а в
- 18. 3) Вода и соль слабого основания, но сильной кислоты образуют недиссоциирующие ионы слабого основания, а в
- 19. 4) Соли, образованные слабыми основаниями и слабыми кислотами необратимо разрушаются водой, иными словами происходит их полный
- 20. Электролиты ─ это вещества, которые при растворении в воде или расплавлении распадаются на ионы, их растворы
- 21. Кислотами называют электролиты, которые при диссоциации образуют катионы только Н+. Основаниями называют электролиты, которые при диссоциации
- 23. Скачать презентацию




















 Изопроцессы в идеальном газе
Изопроцессы в идеальном газе Технологія жирів і жирозамінників
Технологія жирів і жирозамінників Смеси и растворы
Смеси и растворы Термодинамика поверхностных явлений. (Часть 2)
Термодинамика поверхностных явлений. (Часть 2) Ароматические соединения. Галогенпроизводные
Ароматические соединения. Галогенпроизводные Химическое образование в современной средней (полной) общеобразовательной школе
Химическое образование в современной средней (полной) общеобразовательной школе معطر الجو(الهواء) يستعمل معطر الجو لتلطيف الرائحة االستعمال للحمامات او الغرف
معطر الجو(الهواء) يستعمل معطر الجو لتلطيف الرائحة االستعمال للحمامات او الغرف Промышленный биокатализ
Промышленный биокатализ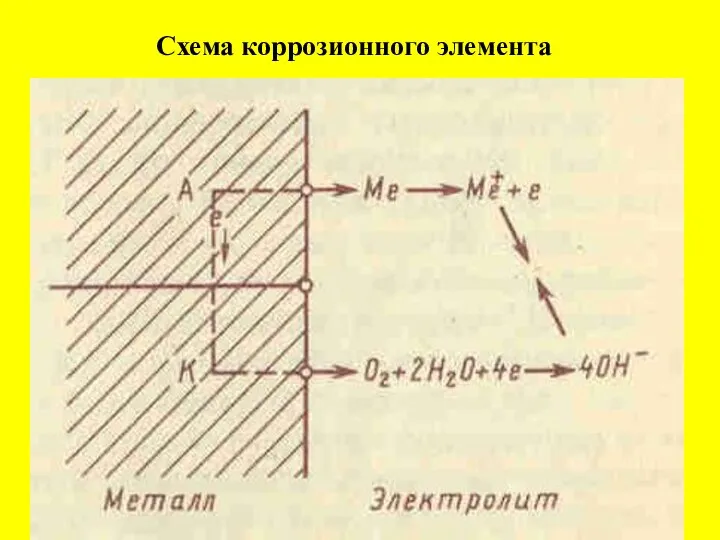 Схема коррозионного элемента
Схема коррозионного элемента Строение атома фосфора. Строение оксида фосфора (V) и его физические свойства
Строение атома фосфора. Строение оксида фосфора (V) и его физические свойства Физические основы методов анализа вещества
Физические основы методов анализа вещества Ванадатты фосфаттар. Орынбасар фосфаттар. Төменгі оксоқышқылдар
Ванадатты фосфаттар. Орынбасар фосфаттар. Төменгі оксоқышқылдар Мұнай
Мұнай Всем известно, всем понятно, что здоровым быть приятно!
Всем известно, всем понятно, что здоровым быть приятно! Алкины. Ацетилен
Алкины. Ацетилен Периодический закон Менделеева и периодическая система химических элементов
Периодический закон Менделеева и периодическая система химических элементов  Предмет и задачи фармацевтической химии. Общие методы анализа лекарственных средств неорганической природы согласно ГФУ
Предмет и задачи фармацевтической химии. Общие методы анализа лекарственных средств неорганической природы согласно ГФУ Поливинилацетат
Поливинилацетат Анализ физико-химических свойств синтетических моющих средств (СМС) и их значение в жизни человека
Анализ физико-химических свойств синтетических моющих средств (СМС) и их значение в жизни человека Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым Изменения, происходящие с белками в процессах технологической переработки сырья
Изменения, происходящие с белками в процессах технологической переработки сырья Карбоновые кислоты. Гидрокси-, оксокислоты. Лекция 2
Карбоновые кислоты. Гидрокси-, оксокислоты. Лекция 2 Интегрированный урок История+Химия
Интегрированный урок История+Химия Золото. Что о нём мы можем рассказать?
Золото. Что о нём мы можем рассказать? Термодинамика. 2 закон термодинамики. Энтропия
Термодинамика. 2 закон термодинамики. Энтропия Элективный курс по химии «Лаборатория юных химиков» Для учащихся 8 класса Разработала учитель химии МОУ СОШ №3 Звёздочкина С.А.
Элективный курс по химии «Лаборатория юных химиков» Для учащихся 8 класса Разработала учитель химии МОУ СОШ №3 Звёздочкина С.А. Электрохимические методы. (Лекция 3)
Электрохимические методы. (Лекция 3) «Соединения химических элементов»
«Соединения химических элементов»