Содержание
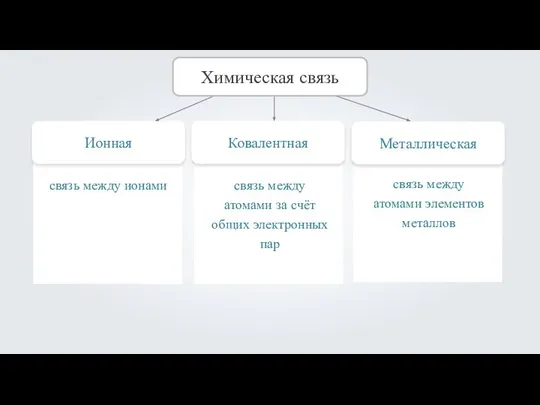
- 2. Ионная Химическая связь Ковалентная Металлическая
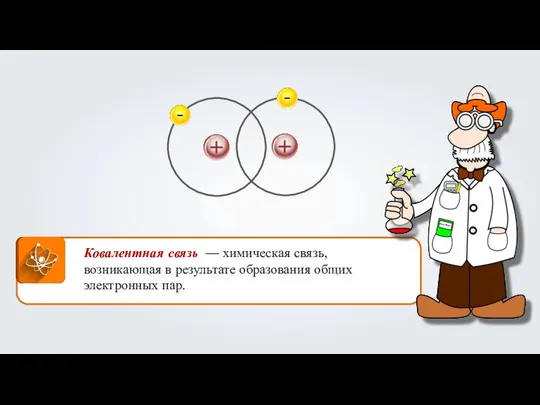
- 3. Ковалентная связь — химическая связь, возникающая в результате образования общих электронных пар.
- 4. Полярная Ковалентная связь Неполярная
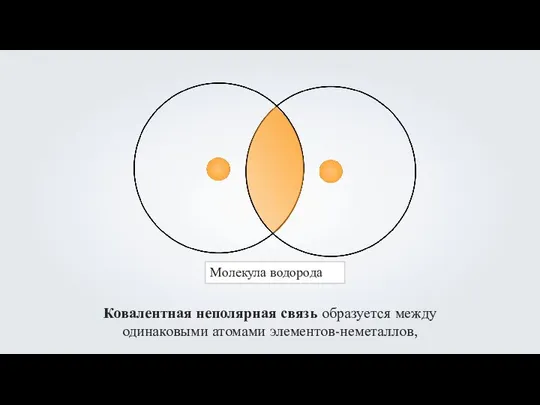
- 5. Молекула водорода Ковалентная неполярная связь образуется между одинаковыми атомами элементов-неметаллов,
- 6. Полярная ковалентная связь может образовываться только между атомами разных элементов-неметаллов. фтороводород НF
- 7. Молекула фторводорода H1 1S1 F9 1S2 / 2S2 2p5 H F Неспаренный электрон Неспаренный электрон
- 8. H F + → H F
- 9. Электроотрицательность — это способность атомов химического элемента смещать к себе общие электронные пары, участвующие в образовании
- 10. F→ O→ N → CI → Br → I → S → C → Si →P
- 11. H F + → H F F→ O→ N → CI → Br → I →
- 12. H F + → H F + - Частичный заряд, приобретаемый атомами, обозначается латинской буквой «дельта»
- 13. Смещение электроотрицательности в молекулах воды Н2О и оксида азота NO Н2О NO 2H + O →
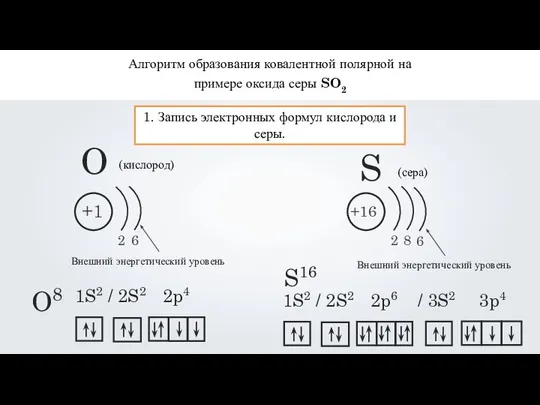
- 14. Алгоритм образования ковалентной полярной на примере оксида серы SO2 1. Запись электронных формул кислорода и серы.
- 15. Алгоритм образования ковалентной полярной на примере оксида серы SO2 2. Изображение расположения внешних электронов у знаков
- 16. Алгоритм образования ковалентной полярной на примере оксида серы SO2 3. Запись электронно-структурной формулы образовавшейся молекулы оксида
- 17. Алгоритм образования ковалентной полярной на примере оксида серы SO2 3. Определение по рассмотренному нами ранее химическому
- 18. Валентность — это число ковалентных связей, которыми атом одного химического элемента связан с атомами этого же
- 19. Аммиак NH3 NIIIHI Вода H2O HIOII Оксид фосфора P2O5 PVOII Запись валентности
- 20. Если валентность обоих элементов кратна какому-нибудь числу, то индексы записываются, уменьшенными на это число. SO3 S2O6
- 21. Al III S II S VI S IV
- 22. По формуле также можно определить валентность одного элемента, если валентность другого известна. SO2 II ? 4
- 24. Скачать презентацию



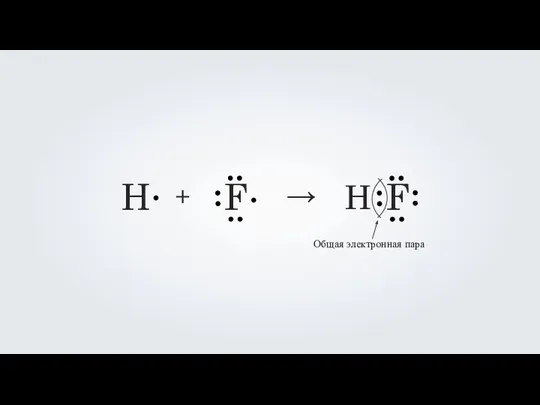


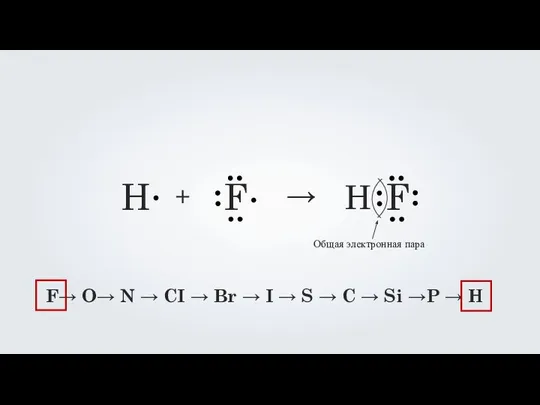










 каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами
каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами Правила оформления лабораторных работ
Правила оформления лабораторных работ Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Презентация по Химии "Синтез сложных эфиров" - скачать смотреть
Презентация по Химии "Синтез сложных эфиров" - скачать смотреть  Гетероциклические соединения
Гетероциклические соединения Презентация по Химии "Классификация и применение сталей" - скачать смотреть
Презентация по Химии "Классификация и применение сталей" - скачать смотреть  Зат алмасу (көмірсу, май)
Зат алмасу (көмірсу, май) Элементы VII группы периодической таблицы Д.И. Менделеева
Элементы VII группы периодической таблицы Д.И. Менделеева Презентация по Химии "Химия неметаллов. Общая характеристика" - скачать смотреть
Презентация по Химии "Химия неметаллов. Общая характеристика" - скачать смотреть  Evolution of Isoconversional Methods
Evolution of Isoconversional Methods Альдегиды и кетоны. Карбоновые и дикарбоновые кислоты
Альдегиды и кетоны. Карбоновые и дикарбоновые кислоты Біохімічний рівень організації
Біохімічний рівень організації Дисперсные системы. Строение коллоидных частиц лиофобных золей
Дисперсные системы. Строение коллоидных частиц лиофобных золей Мыло. Компоненты мыла
Мыло. Компоненты мыла Марганец. Калий
Марганец. Калий Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Презентация по Химии "Хімія в медицині" - скачать смотреть бесплатно
Презентация по Химии "Хімія в медицині" - скачать смотреть бесплатно Азотная кислота
Азотная кислота Миметик глицина на основе производного Гераниола
Миметик глицина на основе производного Гераниола Сколько нужно чистого белка
Сколько нужно чистого белка Скло, його різновиди та застосування Робота Учениці 10-А класу Баранюк Надії
Скло, його різновиди та застосування Робота Учениці 10-А класу Баранюк Надії  Химическая связь
Химическая связь Наличие 2 х сигналов в ЯМР 1Н (задача)
Наличие 2 х сигналов в ЯМР 1Н (задача) Соли
Соли Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготувал
Органічні речовини як основа сучасних матеріалів. Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Підготувал Липиды. Классификация липидов
Липиды. Классификация липидов Пищевые добавки Они повсюду…
Пищевые добавки Они повсюду…  Специфическое поведение гетерофункциональных соединений как результат взаимного влияния атомов
Специфическое поведение гетерофункциональных соединений как результат взаимного влияния атомов