Содержание
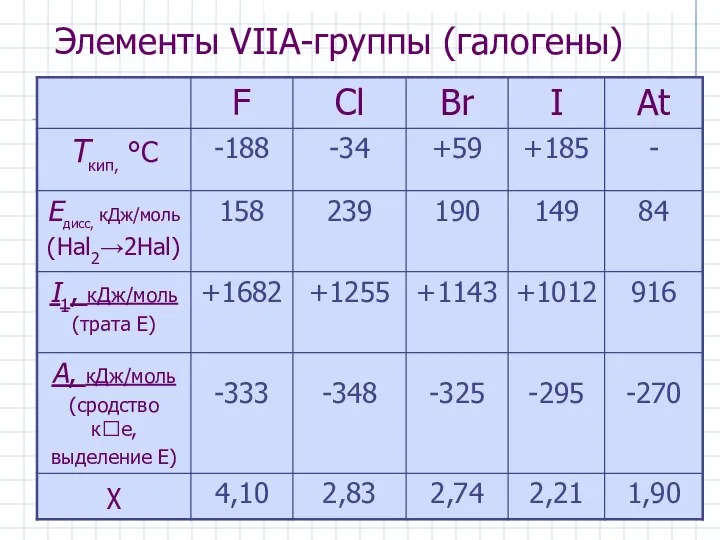
- 2. Элементы VIIА-группы (галогены)
- 3. Простые вещества: F2, Cl2, Br2, I2, At2 Иод Бром Фтор Хлор
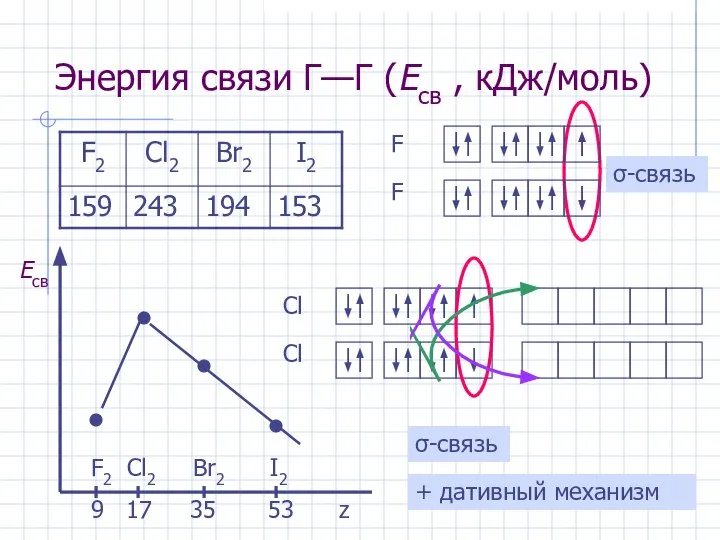
- 4. Энергия связи Г—Г (Eсв , кДж/моль) F2 Cl2 Br2 I2 9 17 35 53 z σ-связь
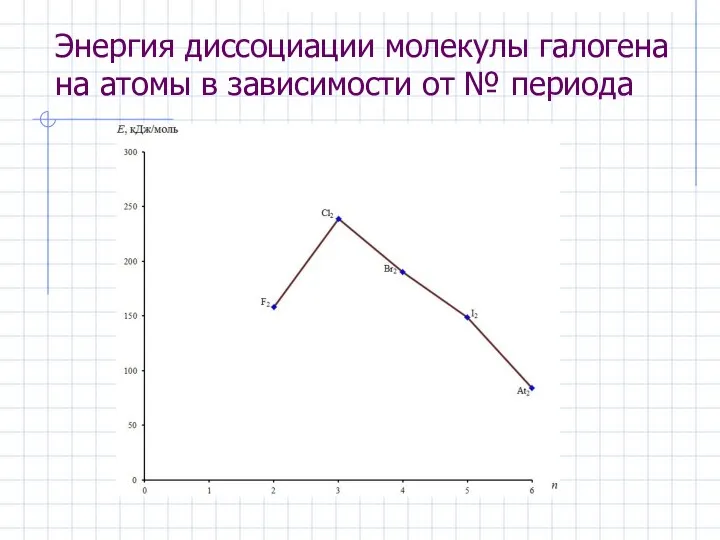
- 5. Энергия диссоциации молекулы галогена на атомы в зависимости от № периода
- 6. Кристаллы флюорита
- 7. Фтор F2 т.пл. –220 °С, т.кип. –183 °С Э + F2 → Э+νFν–I (ν - высокая,
- 8. Соединения фтора. Фтороводород Фтороводород HF : (HF)n т.кип. +19,5 °С, неограниченно растворим в воде Автопротолиз: H2F2
- 9. Фтороводород SiO2 + 4HF газ = SiF4↑ + 2H2O (травление стекла) SiO2 + 6HF изб. =
- 10. Открытие фтора Фтор впервые получен в 1886 г. (А. Муассан, электролиз HF+KF (≈KHF2)
- 11. Получение фтора и фтороводорода В промышленности: электролиз расплава KHF2 (т. пл. 239 °C) или KH2F3 (т.
- 12. Фтороводородная (плавиковая) кислота [H3O]+F- [H3O]+[HF2]- [H3O]+[H3F4]- Специфическая ионизация р-ров HF и специфический гидролиз водных р-ров фторидов:
- 13. Применение Водоподготовка (обеззараживание воды фторированием) Фторуглеродные соединения (фреоны, фторкаучуки, фторопласты (тефлоны) и т.п. HF: получение синтетического
- 15. Скачать презентацию







![Фтороводородная (плавиковая) кислота [H3O]+F- [H3O]+[HF2]- [H3O]+[H3F4]- Специфическая ионизация р-ров HF и](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396750/slide-11.jpg)

 Классификация топлива. Показатели качества топлива (Лекция 1)
Классификация топлива. Показатели качества топлива (Лекция 1) Значение периодического закона и периодической системы химических элементов Д.И. Менделеева
Значение периодического закона и периодической системы химических элементов Д.И. Менделеева Яды и химикаты
Яды и химикаты История развития химии
История развития химии Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері
Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері Свойства ковалентной связи Гибридизация Поляризация Направленность Насыщаемость
Свойства ковалентной связи Гибридизация Поляризация Направленность Насыщаемость Строение и свойства белков
Строение и свойства белков Алкалоиды
Алкалоиды Анализ качества лекарственных средств, производных алифатических и ароматических аминов
Анализ качества лекарственных средств, производных алифатических и ароматических аминов Химия и производство
Химия и производство Курс лекций по химии
Курс лекций по химии Химическая техника. Экстракция
Химическая техника. Экстракция Бытовая химия. Правила обращения с бытовыми химикатами
Бытовая химия. Правила обращения с бытовыми химикатами Детонаційна стійкість бензину
Детонаційна стійкість бензину Определение качества нефтепродуктов (на примере бензинов и дизельного топлива)
Определение качества нефтепродуктов (на примере бензинов и дизельного топлива) Тема урока Атомы химических элементов Задачи урока: повторить, обобщить и закрепить знания о строении атомов химических элемент
Тема урока Атомы химических элементов Задачи урока: повторить, обобщить и закрепить знания о строении атомов химических элемент Периодический закон химических элементов Д. И. Менделеева и периодическая система
Периодический закон химических элементов Д. И. Менделеева и периодическая система Изотермический процесс в реакционном объеме. (Тема 6.2)
Изотермический процесс в реакционном объеме. (Тема 6.2) Диффузия
Диффузия Физические и химические свойства кислот
Физические и химические свойства кислот Многоатомные спирты
Многоатомные спирты Особенности связей и строение фосфазенов
Особенности связей и строение фосфазенов Предмет органической химии
Предмет органической химии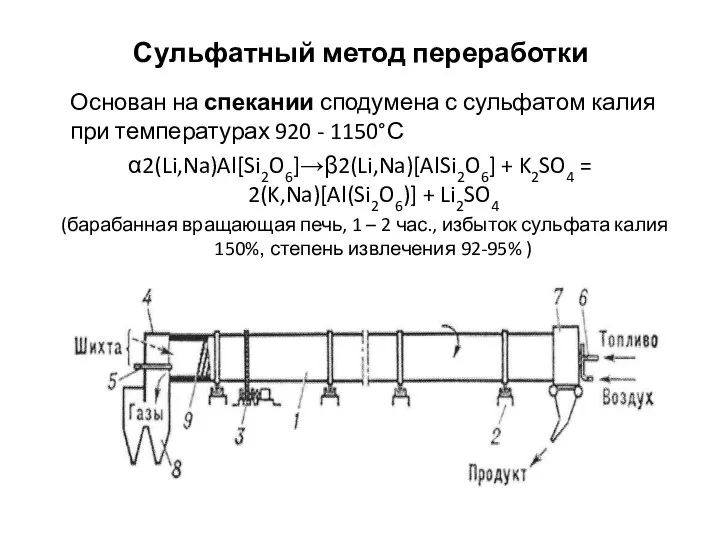 Сульфатный метод переработки
Сульфатный метод переработки Арены и ароматичность
Арены и ароматичность Соли в свете теории электролитической диссоциации
Соли в свете теории электролитической диссоциации Именные реакции в органической химии. Органический синтез. Механизмы химических процессов
Именные реакции в органической химии. Органический синтез. Механизмы химических процессов Использование химии в медицине
Использование химии в медицине