Содержание
- 2. 1. Історія вчення про ферменти. 2. Хімічна природа ферментів. 3. Фізико-хімічна характеристика ферментів. 4. Механізм дії
- 3. Розділ біохімії, який вивчає ферменти називається ензимологією. Ензими-ферменти. Розвиток вчення про ферменти можна умовно розбити на
- 4. Етапи розвитку вчення про ферменти Перший (до XVII ст.) характеризується використанням ферментів у практичній діяльності людини
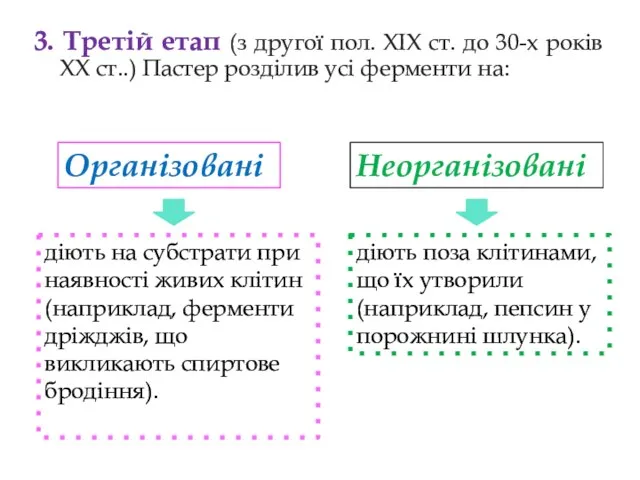
- 5. 3. Третій етап (з другої пол. XIX ст. до 30-х років XX ст..) Пастер розділив усі
- 6. Наприкінці XIX ст. виникла необхідність у систематизації їх назв. Е. Дюкло запропонував при найменуванні ферментів до
- 7. Дж. Самнер у 1926 р. виділяє перший фермент у кристалічному вигляді – уреазу. З цього часу
- 8. Ферменти – це біологічні каталізатори білкової природи, які синтезуються в живих клітинах і мають властивість прискорювати
- 9. Порівняльні розміри білків та пептидів: Зліва направо: Антитіло(IGG), гемоглобін, інсулін (гормон), аденілаткіназа (фермент) і глютамінсинтетаза (фермент).
- 10. Каталітичний центр - динамічне утворення, яке являє собою різні групування, які зумовлюють акт каталізу (фермент реакції
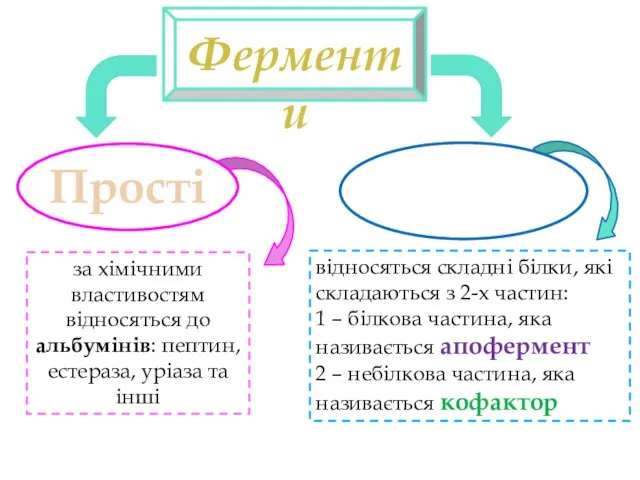
- 11. Прості Складні Ферменти за хімічними властивостям відносяться до альбумінів: пептин, естераза, уріаза та інші відносяться складні
- 12. 1). Якщо зв’язок з апоферментом не дуже міцний і утворюється в момент каталітичного акту, тоді у
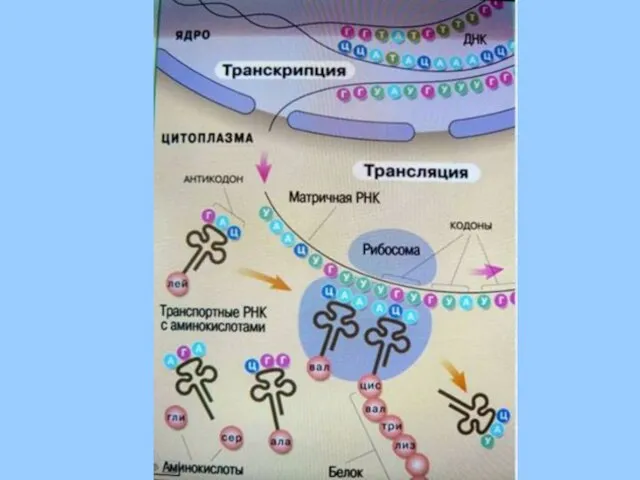
- 13. Формування активного центру. Здійснення контакту між ферментом та субстратом. Переніс атомних груп ( атомів, протонів, електронів
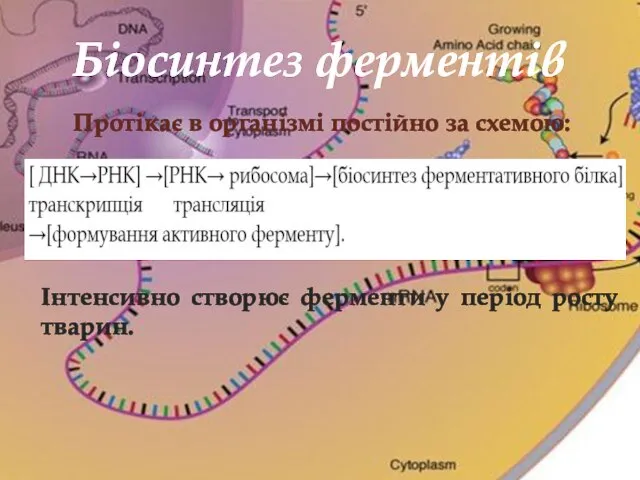
- 14. Протікає в організмі постійно за схемою: Інтенсивно створює ферменти у період росту тварин. Біосинтез ферментів
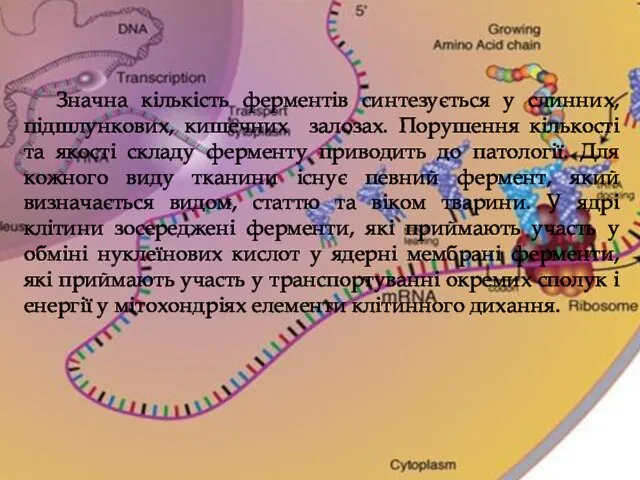
- 16. Значна кількість ферментів синтезується у слинних, підшлункових, кишечних залозах. Порушення кількості та якості складу ферменту приводить
- 17. 1. Термолабільність (вплив температури). Висока - знижає активність ферменту, ферменти денатурують і втрачають активність. Низькі температури
- 18. 2. Вплив рН – оптимум ферментів, таке значення рН при якому проявляється найбільша активність: рН трипсин
- 19. 3. Специфічність ферментів – визначається набором структур, які можуть перетворюватися під дією ферменту. Специфічність дії ферментів
- 20. Активатори – це речовини, які підвищують активність ферментів Бувають: Специфічні – це ферментні білки, дія яких
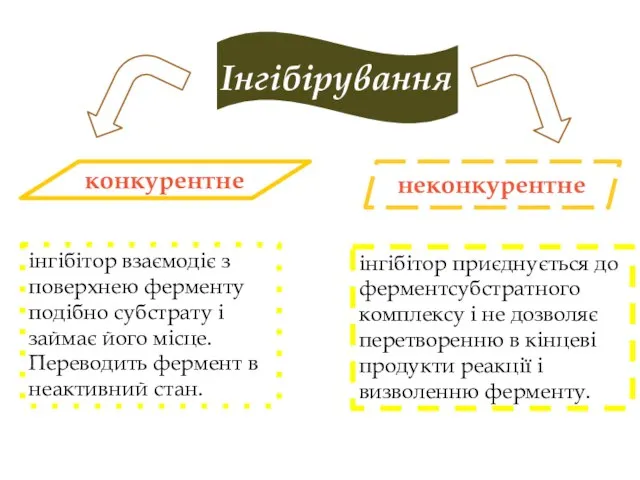
- 21. Інгібірування конкурентне інгібітор взаємодіє з поверхнею ферменту подібно субстрату і займає його місце. Переводить фермент в
- 22. Ферменти каталізують прямі і обратимі реакції. Наприклад, пепсин при рН = 1,5-2,5 розщеплює пептидні зв’язки, а
- 23. Ферментативна реакція підкоряється закону дії мас. Підвищується швидкість реакції, відбувається у наслідок зміни активації молекул субстрату.
- 24. Теорія ферментативного каталізу: (розроблена Михаелісом-Ментеном) між субстратом і ферментом виникає зв’язок, в результаті чого виникає фермент-субстратний
- 25. Е + S →ES →E + P ← розщеплений субстрат Субстрат має свій енергетичний бар’єр. Задача
- 26. Кінетика ферментативної реакції. Кожна хімічна реакція відбувається з певною швидкістю. Ферментативна кінетика – розділ хімічної кінетики,
- 27. Розрізняють кілька типів ферментативних реакцій: необоротні реакції з одним субстратом, необоротні реакції з двома субстратами і
- 28. У другій фазі ферментативного каталізу фермент-субстратний комплекс розпадається на фермент Е і продукт реакції Р Для
- 29. Швидкість ферментативної реакції визначається умовами її перебігу V = k + 2 [ E ], якщо
- 30. Застосовуючи константу Михаеліса-Ментена Коли [S] › km , то V = k+2[Eо] ≈ Vmax ,
- 31. За основу взятий принцип класифікації ферментів за типом хімічної реакції, які вони каталізують. Усі відомі ферменти
- 32. Кожний клас поділяється на підкласи, які діляться на підпідкласи, що складаються з окремих представників. Єдина система
- 33. 1. Оксидоредуктази - ферменти, які прискорюють окисно-відновні процеси. До них належать пероксидази, оксидази, каталази. 2. Трансферази
- 34. 3. Гідролази – каталізують розщеплення з участю води, внутрішньомолекулярні зв’язки в білках, вуглеводах, жирах на прості
- 36. Скачать презентацию





















![Застосовуючи константу Михаеліса-Ментена Коли [S] › km , то V = k+2[Eо] ≈ Vmax ,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/516847/slide-29.jpg)




 Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) Нефть, классификация, применение, основные показатели ,особенности кодировки
Нефть, классификация, применение, основные показатели ,особенности кодировки Композиты на основе полибензоксазинов
Композиты на основе полибензоксазинов Презентация по Химии "Полімери" - скачать смотреть бесплатно
Презентация по Химии "Полімери" - скачать смотреть бесплатно Основні класи неорганічних речовин
Основні класи неорганічних речовин Химические формулы. Классы неорганических веществ. Урок №1
Химические формулы. Классы неорганических веществ. Урок №1 Методология, принципы и методы изучения МПИ
Методология, принципы и методы изучения МПИ Минералы и Близнецы
Минералы и Близнецы 8 класс
8 класс  Эмульсии и эмульгаторы
Эмульсии и эмульгаторы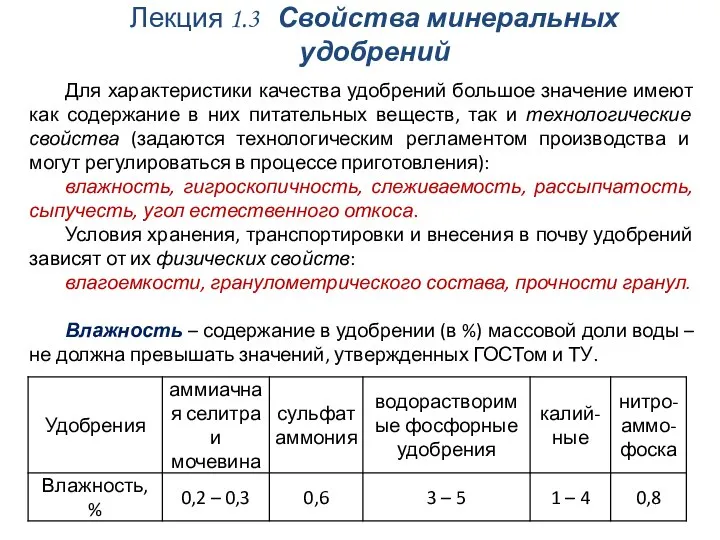 Свойства минеральных удобрений
Свойства минеральных удобрений Электрическая проводимость растворов
Электрическая проводимость растворов Презентация по Химии "Показатели воды: её жесткость и кислотность" - скачать смотреть
Презентация по Химии "Показатели воды: её жесткость и кислотность" - скачать смотреть  Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева
Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева Силикатная промышленность
Силикатная промышленность Кислотные дожди
Кислотные дожди Общая и неорганическая химия
Общая и неорганическая химия Білки. Функції білків в організмі
Білки. Функції білків в організмі Органические вещества
Органические вещества Безопасная пластмасса
Безопасная пластмасса Этиленовые, олефины, непредельные алкены
Этиленовые, олефины, непредельные алкены Методы диффузионной металлизации
Методы диффузионной металлизации Гипоксия
Гипоксия Презентация по Химии "Етери та естери" - скачать смотреть бесплатно
Презентация по Химии "Етери та естери" - скачать смотреть бесплатно Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно
Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно Химия в нашей жизни
Химия в нашей жизни Поверхностные явления. Лекция 15
Поверхностные явления. Лекция 15 Хімічні речовини у побуті підготували Стебко Марія, Бондар Аліна 11-Ф
Хімічні речовини у побуті підготували Стебко Марія, Бондар Аліна 11-Ф