Содержание
- 6. ОТНОСИТЕЛЬНАЯ АТОМНАЯ МАССА AR
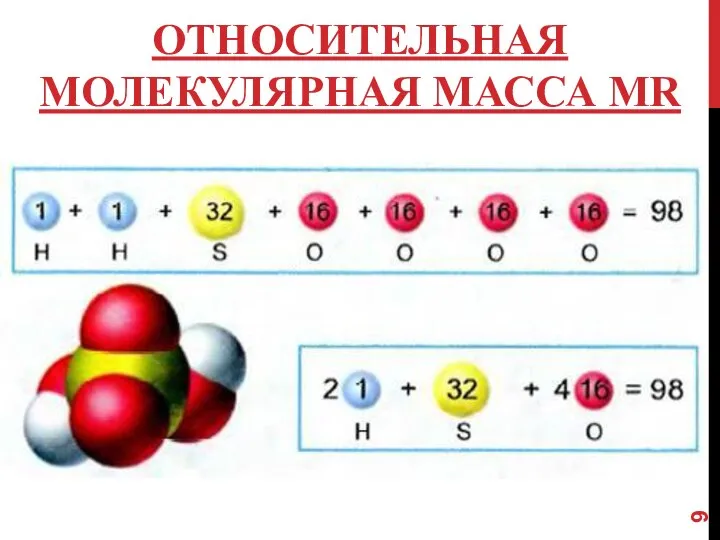
- 9. ОТНОСИТЕЛЬНАЯ МОЛЕКУЛЯРНАЯ МАССА МR
- 17. Молярная масса М m – масса вещества; n – число молей вещества.
- 18. Молярная масса М
- 20. Нормальные условия: T = 0o C или 273 К P = 1 атм. = 760 мм.рт.ст.
- 21. Молярный объем газа Vm (л/моль)
- 24. D =
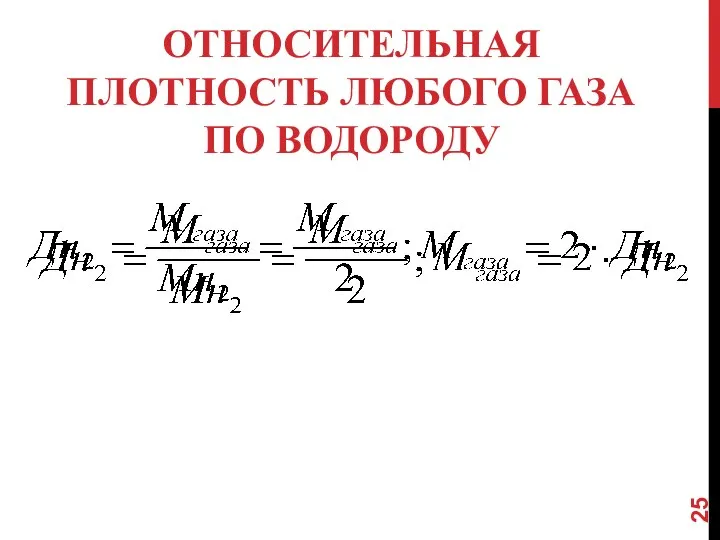
- 25. ОТНОСИТЕЛЬНАЯ ПЛОТНОСТЬ ЛЮБОГО ГАЗА ПО ВОДОРОДУ
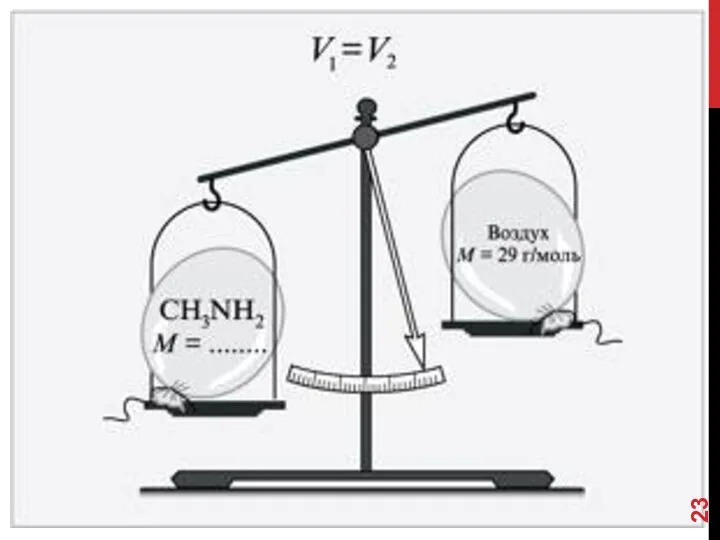
- 26. ОТНОСИТЕЛЬНАЯ ПЛОТНОСТЬ ПО ВОЗДУХУ
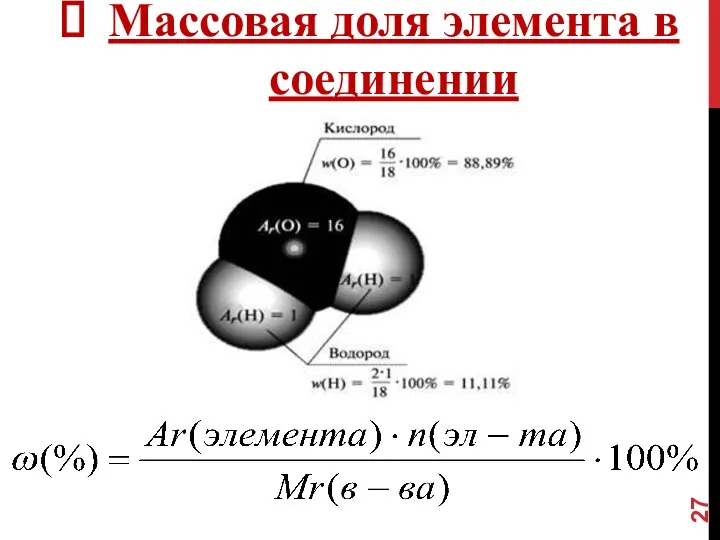
- 27. Массовая доля элемента в соединении
- 28. Основное уравнение газового состояния (уравнение объединенного закона Клайперона): P, V, T – при данных условиях P0,
- 29. Уравнение Клайперона-Менделеева
- 30. (если P в Па, а V в м3) R – универсальная газовая постоянная
- 32. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА (МЭ) ВЕЩЕСТВА это масса 1 моль эквивалента вещества, она равна произведению фактора эквивалентности
- 33. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА (МЭ) ВЕЩЕСТВА Мэ (в-ва) = fэ *М (в-ва)
- 34. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА ЭЛЕМЕНТА равна отношению молярной массы элемента к его валентности.
- 35. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА ОСНОВАНИЯ равна отношению молярной массы основания к числу замещенных гидроксогрупп (ч3ОН-):
- 36. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА КИСЛОТЫ равна отношению молярной массы кислоты к числу замещенных катионов водорода (ч3Н+).
- 37. МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА СОЛИ в обменных реакциях равна отношению молярной массы соли к произведению числа катионов
- 46. Скачать презентацию



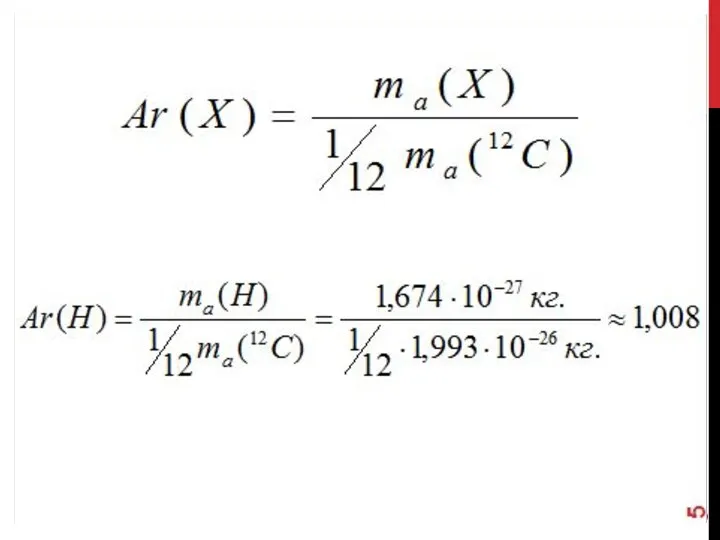


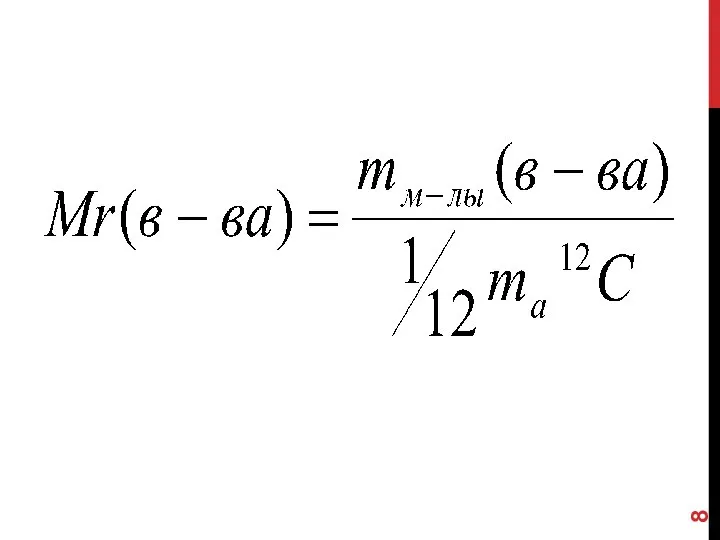












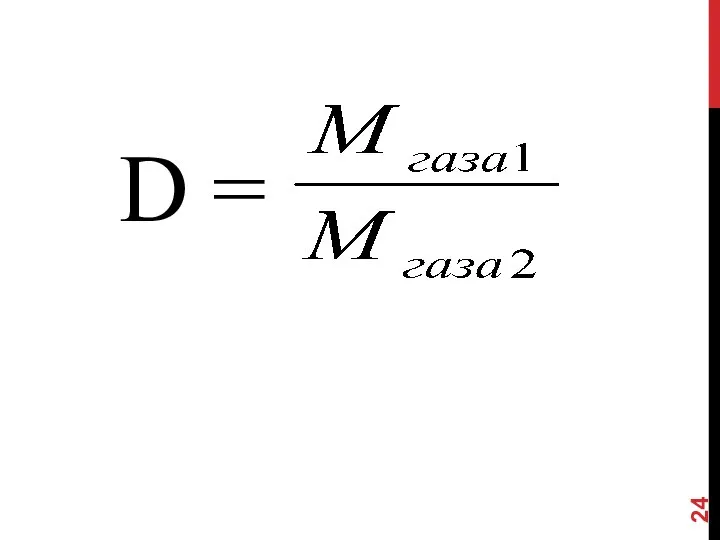

















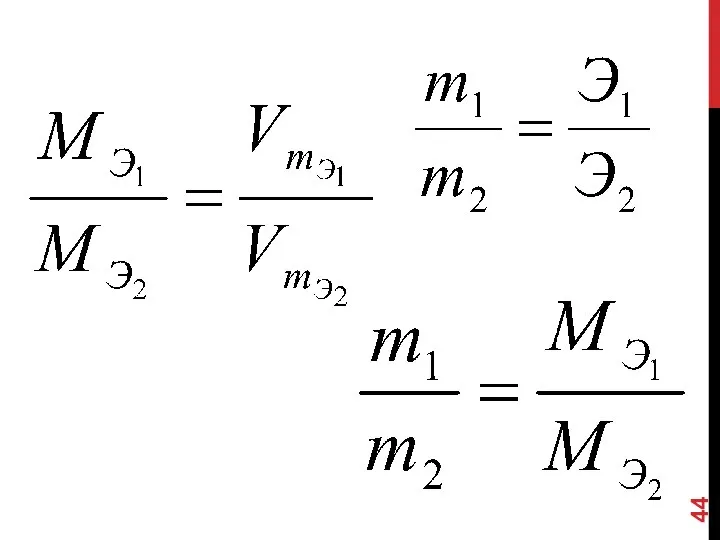
 Закон сохранения массы веществ
Закон сохранения массы веществ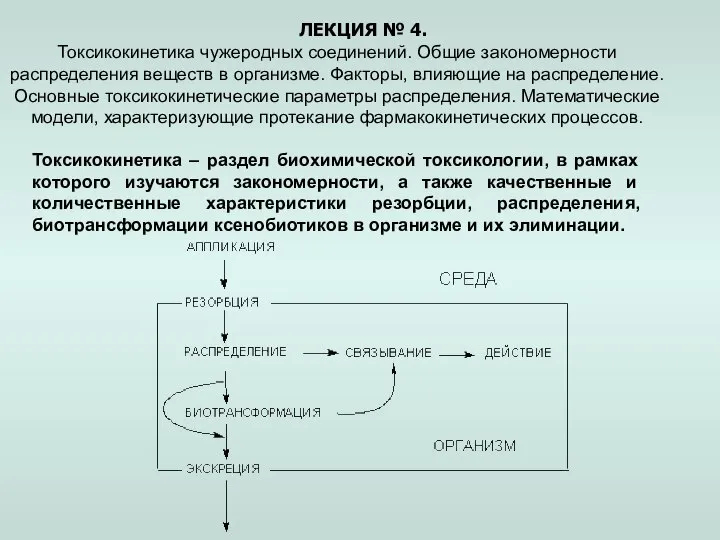 Токсикокинетика чужеродных соединений. Закономерности распределения веществ в организме. (Лекция 4)
Токсикокинетика чужеродных соединений. Закономерности распределения веществ в организме. (Лекция 4) Натрій. Знаходження в періодичній системі і основні характеристики
Натрій. Знаходження в періодичній системі і основні характеристики Простые вещества-металлы 9 класс
Простые вещества-металлы 9 класс Оксиды
Оксиды «Строение атома и периодическая система» Химический диктант в 8 классе
«Строение атома и периодическая система» Химический диктант в 8 классе Діагностика за показами газоаналізатора. Типи газоаналізаторів
Діагностика за показами газоаналізатора. Типи газоаналізаторів Термический анализ. Прибор синхронного термического анализа
Термический анализ. Прибор синхронного термического анализа Реология расплавов и растворов полимеров
Реология расплавов и растворов полимеров Номенклатура органических соединений Практическое приложение
Номенклатура органических соединений Практическое приложение  Лигандообменные равновесия и процессы
Лигандообменные равновесия и процессы Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн
Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн Избыток-недостаток, состав раствора.Типология задач ЕГЭ. Задание 34
Избыток-недостаток, состав раствора.Типология задач ЕГЭ. Задание 34 Полимеры
Полимеры Применение гибридного биосорбента для очистки промышленных сточных вод от радиоактивных примесей
Применение гибридного биосорбента для очистки промышленных сточных вод от радиоактивных примесей Роль воды в организме человека
Роль воды в организме человека Химическая термодинамика. Лекция 3
Химическая термодинамика. Лекция 3 Оксид кремния
Оксид кремния Растворение как физико-химический процесс
Растворение как физико-химический процесс Этилен
Этилен Обмен веществ и энергии, основа существования клетки
Обмен веществ и энергии, основа существования клетки Презентация по Химии "КОРРОЗИЯ МЕТАЛЛОВ" - скачать смотреть бесплатно
Презентация по Химии "КОРРОЗИЯ МЕТАЛЛОВ" - скачать смотреть бесплатно Химическое сопротивление пластмасс
Химическое сопротивление пластмасс ОВР в органической химии Автор: Тятин Павел Владимирович, 11М класс, МОУ лицей №6 Руководитель: Дробот Светлана Сергеевна , учит
ОВР в органической химии Автор: Тятин Павел Владимирович, 11М класс, МОУ лицей №6 Руководитель: Дробот Светлана Сергеевна , учит Синтетические волокна
Синтетические волокна  Сульфаниламидные препараты. Хинолоны
Сульфаниламидные препараты. Хинолоны Алюминиевые сплавы
Алюминиевые сплавы Полиморфизм. Аллотропия
Полиморфизм. Аллотропия