Содержание
- 2. Джерела амінокислот 1. Білки корму (екзогенні амінокислоти). 2. Білки тканин при розпаді в процесі їх оновлення
- 3. Шляхи використання амінокислот в організмі Біосинтез білків, специфічних для даного організму. Синтез біологічно активних речовин (ферментів,
- 5. КАТАБОЛІЗМ АМІНОКИСЛОТ Амінокислоти, які утворилися в результаті перетравлення білків і потрапили в клітини тканин, підлягають катаболізму
- 6. Дезамінування Найбільш розповсюдженим видом перетворення амінокислот є їх дезамінування з утворенням кетокислот і амоніаку. Амоніак є
- 7. 1. Відновлювальне дезамінування
- 8. 2. Гідролітичне дезамінування Ці два шляхи дезамінування характерні для більшості бактерій, особливо тих, які містяться в
- 9. 3. Внутрішньомолекулярне дезамінування Цей вид дезамінування є характерним для деяких рослин і бактерій, а в тваринному
- 10. В печінці уроканінова кислота перетворюється в імідазолонпропіонову кислоту при дії уроканінази. Подальші перетворення в ході серії
- 11. 4. Окисне дезамінування Окисне дезамінування – переважний тип дезамінування амінокислот в організмі ссавців та більшості аеробних
- 12. Процес окисного дезамінування відбувається в два етапи.
- 13. В тканинах достатньо активною є дегідрогеназа, яка специфічно дезамінує α-глутамінову кислоту, перетворюючи її в α-кетоглутарову кислоту
- 14. Трансамінування – непрямий шлях дезамінування Трансамінування ‒ реакція перенесення α-аміногрупи з амінокислоти на α-кетокислоту, в результаті
- 15. Найчастіше за все в реакціях трансамінування приймають участь амінокислоти, вміст яких у тканинах значно вище за
- 16. Вступати в реакції трансамінування можуть майже всі амінокислоти, за винятком лізину, треоніну та проліну.
- 17. Для амінотрансфераз характерною є субстратна специфічність до різних амінокислот. В тканинах людини виявлено більше 10 різних
- 18. Аланінамінотрансфераза АЛТ (АлАТ) каталізує реакцію трансамінування між аланіном і α-кетоглутаратом. Локалізований цей фермент у цитозолі клітин
- 19. ACT (АсАТ) каталізує реакцію трансамінування між аспартатом та α-кетоглутаратом аналогічно попередній. В результаті утворюються оксалоацетат і
- 20. Біологічне значення трансамінування Реакції трансамінування відіграють велику роль в обміні амінокислот. Оскільки цей процес є зворотним,
- 21. Специфічні шляхи катаболізму амінокислот
- 22. Синтез креатиніну Креатин є необхідним для утворення в м'язах високоенергетичної сполуки – креатинфосфату. Синтез креатину проходить
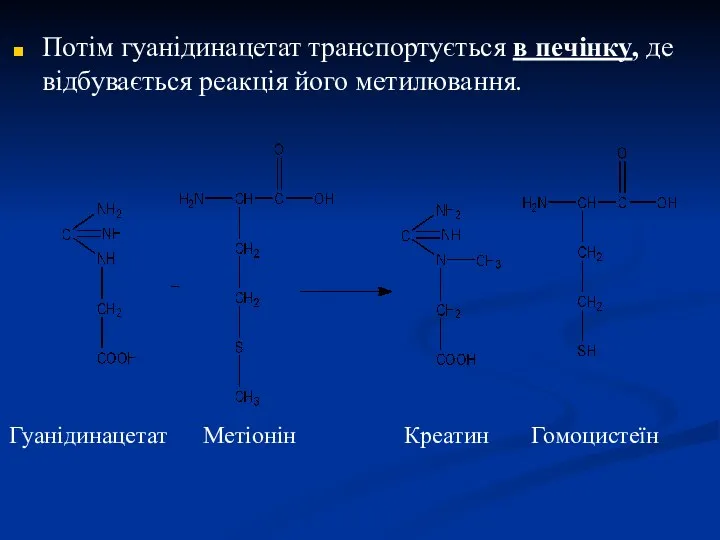
- 23. Потім гуанідинацетат транспортується в печінку, де відбувається реакція його метилювання. Гуанідинацетат Метіонін Креатин Гомоцистеїн
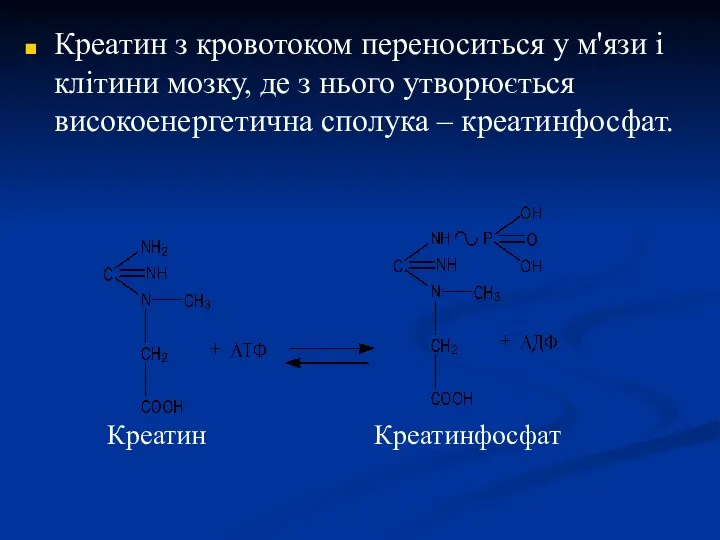
- 24. Креатин з кровотоком переноситься у м'язи і клітини мозку, де з нього утворюється високоенергетична сполука –
- 25. Якщо потреба в енергії стає великою (при м'язовому скороченні) креатинфосфат передає свій фосфат на АДФ для
- 26. Креатинфосфат відіграє важливу роль у забезпеченні енергією м'язу, що працює, в початковий період. В результаті неферментативного
- 27. Визначення вмісту креатину і креатиніну в крові та сечі використовується для характеристики інтенсивності роботи м'язів у
- 28. Глікогенні і кетогенні амінокислоти Амінокислоти, які в процесі катаболізму перетворюються в піруват, оксалоацетат (ЩОК) і фосфоєнолпіруват,
- 30. ДЕКАРБОКСИЛУВАННЯ АМІНОКИСЛОТ Процес відщеплення карбоксильної групи амінокислот у вигляді СО2 одержав назву декарбоксилування. Продукти реакції, що
- 31. Декарбоксилування амінокислот відбувається під впливом декарбоксилаз, коферментом яких є переважно фосфопіридоксаль (вітамін В6). Декарбоксилуванню підлягають лише
- 32. При декарбоксилуванні гістидину утворюється гістамін, який має сильну фармакологічну дію на кровоносні судини та кров'яний тиск
- 33. Біологічна роль гістаміну Багато синтезується в місці запалення: має судинорозширюючу дію, прискорює приплив лейкоцитів і активує
- 34. В результаті декарбоксилування глутамінової кислоти утворюється γ‑аміномасляна кислота, метаболіт, який синтезується в нервовій тканині, необхідний для
- 35. В організмі аміни окиснюються моноамінооксигеназами до альдегідів і виводяться нирками. В результаті декарбоксилування амінокислот виділяється третій
- 36. Токсичність амоніаку Амоніак легко проникає через мембрани в клітини і в мітохондріях змінює напрям реакції, яка
- 37. Підвищення концентрації амоніаку в крові змінює рН у лужну сторону (виникає алкалоз). Це, в свою чергу,
- 38. Шляхи знезараження амоніаку Тимчасове знезараження (у всіх тканинах): - утворення амонійних солей; - утворення амідів дикарбонових
- 39. Синтез амонійних солей органічних кислот відбувається тільки в нирках і займає незначне місце у всьому процесі
- 40. Знезараження амоніаку в місці його утворення (печінка, нирки, мозок, м'язи та ін.) відбувається, головним чином, за
- 41. Амоніак у складі аспарагіну і глутаміну надходить до печінки, де використовується для синтезу сечовини.
- 42. Глутамін — основний донор Нітрогену в організмі. Високий рівень глутаміну в крові та легкість його надходження
- 43. Орнітиновий цикл Сечовина − основний кінцевий продукт азотистого обміну, в складі якого з організму виділяється до
- 44. Перша стадія синтезу сечовини заключається в утворенні карбамоїлфосфату за участі АТФ і N-ацетилглутамінової кислоти, яка є
- 45. Карбамоїлфосфат за участі ферменту орнітинкарбамоїл-трансферази перетворюється в амінокислоту цитрулін:
- 46. В присутності ферменту аргінінсукцинатсинтетази і АТФ цитрулін вступає в реакцію конденсації з аспарагіновою кислотою, в результаті
- 47. Аргінінянтарна кислота при дії ферменту аргінінсукцинат-ліази розщеплюється на аргінін і фумарову кислоту:
- 48. Аргінін при дії аргінази перетворюється в орнітин і сечовину. Орнітин може включатися в новий цикл знезараження
- 49. Фумарова кислота при цьому перетворюється в яблучну і щавлевооцтову, а остання в результаті трансамінування або відновлювального
- 50. У жуйних частина її виділяється із сечею, а інша частина через слинні залози в складі слини
- 51. При утворенні сечовини використовується А) амоніак – одна молекула Б) СО2 – одна молекула В) аміногрупа
- 53. Анаболічна фаза обміну білків Синтез замінних амінокислот. Синтез специфічних білків. Синтез азотвмісних речовин: - біогенні аміни;
- 54. Синтез замінних амінокислот Вуглецевий скелет замінних амінокислот утворюється з проміжних метаболітів гліколізу, пентозофосфатного шляху, циклу трикарбонових
- 55. Відновлювальне амінування α-кетокислот
- 56. Трансамінування
- 57. Попередники замінних амінокислот
- 59. Скачать презентацию






















































 Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Классификация минералов
Классификация минералов Водород- зеленое топливо
Водород- зеленое топливо Основы строения сплавов. (3)
Основы строения сплавов. (3) Основы физической органической химии. Сигма-ро анализ
Основы физической органической химии. Сигма-ро анализ Соли, их классификация и свойства
Соли, их классификация и свойства Химическая связь
Химическая связь Смеси и растворы
Смеси и растворы Окисно-відновні реакції у природі і промисловості
Окисно-відновні реакції у природі і промисловості Уравнения химических реакций
Уравнения химических реакций Сера в таблице Д.И. Менделеева
Сера в таблице Д.И. Менделеева Основания, их классификация, способы получения и свойства. 8 класс
Основания, их классификация, способы получения и свойства. 8 класс Презентация по Химии "Готовимся к экзамену по химии" - скачать смотреть бесплатно
Презентация по Химии "Готовимся к экзамену по химии" - скачать смотреть бесплатно Химическая связь и ее типы
Химическая связь и ее типы Вдоль по радуге
Вдоль по радуге Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии»
Викторина на тему: «Щелочные и щелочноземельные металлы в гомеопатии» Презентация Степень окисления
Презентация Степень окисления  Молекулярно-механическое изнашивание
Молекулярно-механическое изнашивание Терпены и стероиды
Терпены и стероиды Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона
Геохимия природных процессов. Геохимическая типизация гранитоидов Л.В. Таусона Предмет химии. Основные задачи курса
Предмет химии. Основные задачи курса Горение твердого топлива
Горение твердого топлива Природні й синтетичні органічні сполуки в житті людини
Природні й синтетичні органічні сполуки в житті людини Химия и сельское хозяйство
Химия и сельское хозяйство  Кривые титрования
Кривые титрования Основания и их свойства
Основания и их свойства Аппаратура ионообменных процессов
Аппаратура ионообменных процессов История микроскопа
История микроскопа