Содержание
- 2. ТЕМА: АМФОТЕРНЫЕ ОКСИДЫ И ГИДРОКСИДЫ
- 3. Вещества - «хамелеоны». При добавлении к таким веществам кислоты, они проявляют основные свойства, а при добавлении
- 4. Амфотерность способность соединений проявлять либо кислотные либо основные свойства, в зависимости от того с чем они
- 5. Амфотерный характер носят оксиды и гидроксиды большинства переходных элементов и многих элементов побочных подгрупп.
- 6. Амфотерные соединения К амфотерным соединениям относят оксиды и гидроксиды некоторых металлов (в них металл чаще всего
- 7. Амфотерные оксиды Из оксидов двойственными свойствами обладают: оксид бериллия BeO, оксид цинка ZnO, оксид алюминия Al2O3,
- 8. Химические свойства амфотерных оксидов При реакции с соляной кислотой оксида цинка образуются соль хлорид цинка и
- 9. Амфотерные гидроксиды
- 10. Физические свойства амфотерных гидроксидов Амфотерные гидроксиды – это нерастворимые в воде твердые вещества, как правило, белого
- 11. Химические свойства амфотерных гидроксидов Zn(OH)2+2HCl=ZnCl2+2H2O Zn(OH)2+2KOH=K2ZnO2+2H2O Амфотерный гидроксид цинка в реакции со щелочью гидроксидом калия образовал
- 12. Задание Закончите уравнения реакций: Cr(OH)3 + 6HCl = ? Cr(OH)3 + NaOH = ?
- 13. Какие из групп веществ проявляют амфотерные свойства? Ca(ОН)2, Cu(ОН)2, NaОН, Fe(OН)2 Fe2O3, Al2O3, Fe(OН)3 , ZnO,
- 14. Допишите уравнение реакции: Zn(OH)2 + 2NaOH в результате образуются Na2ZnO2 + 2H2O Zn(OH)2 + Na2O ZnSO4
- 15. Совершенно верно!!!
- 16. Спасибо за внимание!
- 18. Скачать презентацию















 Алюминий - презентация скачать
Алюминий - презентация скачать  Кислоты, их состав, свойства и применение
Кислоты, их состав, свойства и применение Масс-спектрометрия в органической химии
Масс-спектрометрия в органической химии Сложные эфиры Урок химии в 10 классе
Сложные эфиры Урок химии в 10 классе Периодическая таблица Д.И. Менделеева. Своя игра
Периодическая таблица Д.И. Менделеева. Своя игра Минералы и горные породы, методы их определения
Минералы и горные породы, методы их определения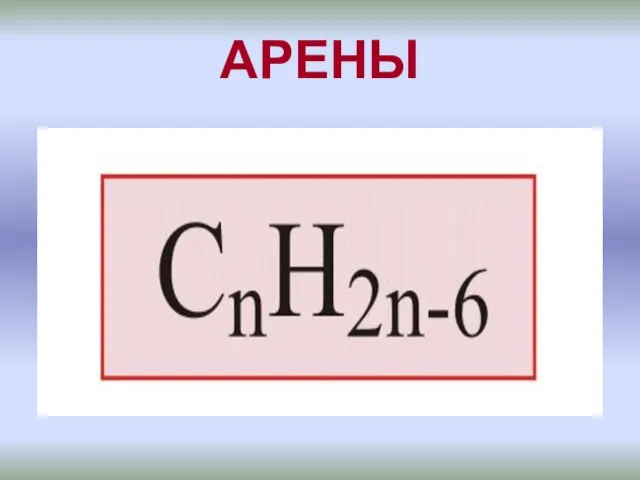 Бензоидные ароматические углеводороды - арены
Бензоидные ароматические углеводороды - арены Состав и основные свойства янтаря и древесных смол
Состав и основные свойства янтаря и древесных смол Производные кислородсодержащих гетероциклов - пиранов
Производные кислородсодержащих гетероциклов - пиранов Крахмал. Физические свойства
Крахмал. Физические свойства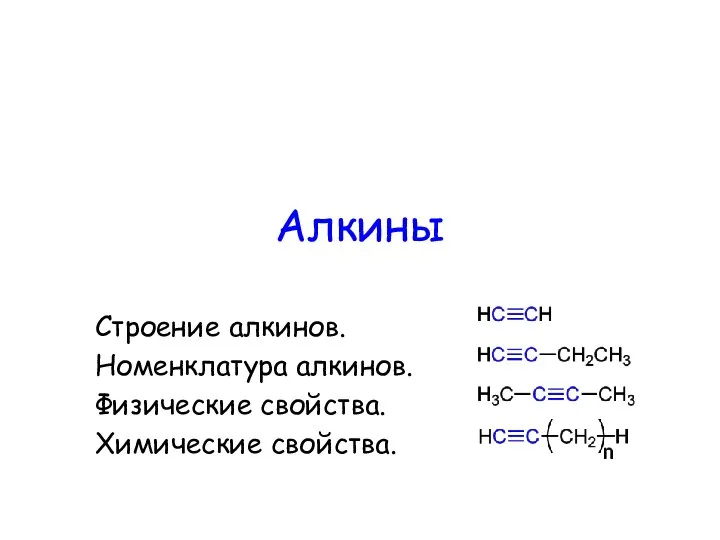 Алкины. Строение алкинов. Номенклатура алкинов. Физические свойства. Химические свойства
Алкины. Строение алкинов. Номенклатура алкинов. Физические свойства. Химические свойства Реакция соединения
Реакция соединения Химическая связь. Урок 34-37
Химическая связь. Урок 34-37 Углеводы (10 класс) - Презентация по Химии_
Углеводы (10 класс) - Презентация по Химии_ Целлюлоза
Целлюлоза  Композитные материалы
Композитные материалы Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих Презентация на тему: Кремний и его соединения
Презентация на тему: Кремний и его соединения Введение в биохимию
Введение в биохимию Химическая термодинамика
Химическая термодинамика Фармацевтичний аналіз
Фармацевтичний аналіз Химический состав фракций нефти
Химический состав фракций нефти Fuel cells
Fuel cells Характеристика ядов, изолируемых минерализацией в клинической фармации
Характеристика ядов, изолируемых минерализацией в клинической фармации Подготовка к ЕГЭ: КИСЛОРОДСОДЕРЖАЩИЕ. УГЛЕВОДЫ. Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразоват
Подготовка к ЕГЭ: КИСЛОРОДСОДЕРЖАЩИЕ. УГЛЕВОДЫ. Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразоват Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері
Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері Термодинамическое равновесие
Термодинамическое равновесие Сулы ерітінділер. Тірі ағза сұйықтықтарындағы тепе-теңдік
Сулы ерітінділер. Тірі ағза сұйықтықтарындағы тепе-теңдік