Содержание
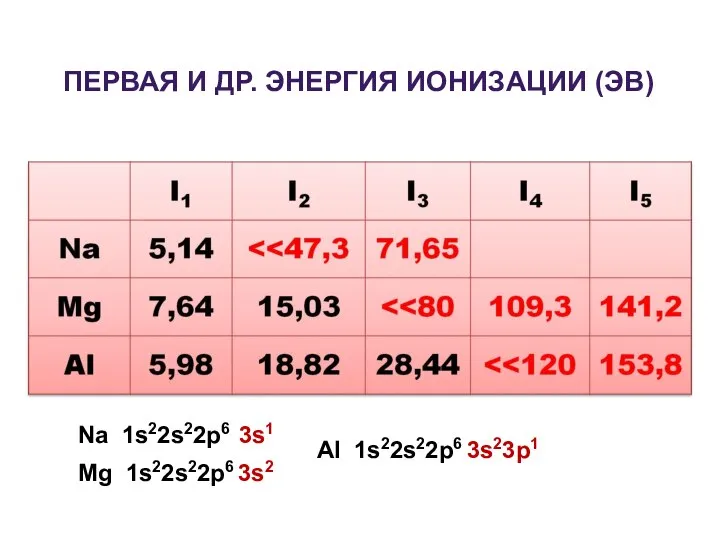
- 2. ПЕРВАЯ И ДР. ЭНЕРГИЯ ИОНИЗАЦИИ (ЭВ) Na 1s22s22p6 3s1 Mg 1s22s22p6 3s2 Al 1s22s22p6 3s23p1
- 3. e–1 r12 e–2 А rАВ В Молекула Н2: А и В – ядра; е1 и е2
- 4. ⮀ ⮅ Ψмол= Ψ1(1)Ψ2(2), при обмене электронами Ψмол= Ψ1(2)Ψ2(1) Ψмол= Ψ1(1)Ψ2(2) − Ψ1(2)Ψ2(1) Ψмол= Ψ1(1)Ψ2(2) +
- 5. РЕЗУЛЬТАТЫ КВАНТОВО-МЕХ. РАСЧЁТА МОЛ-ЛЫ Н2
- 6. Свойства ковалентной связи а) насыщаемость б) направленность в) поляризуемость Типы ковалентной связи сигма σ пи π
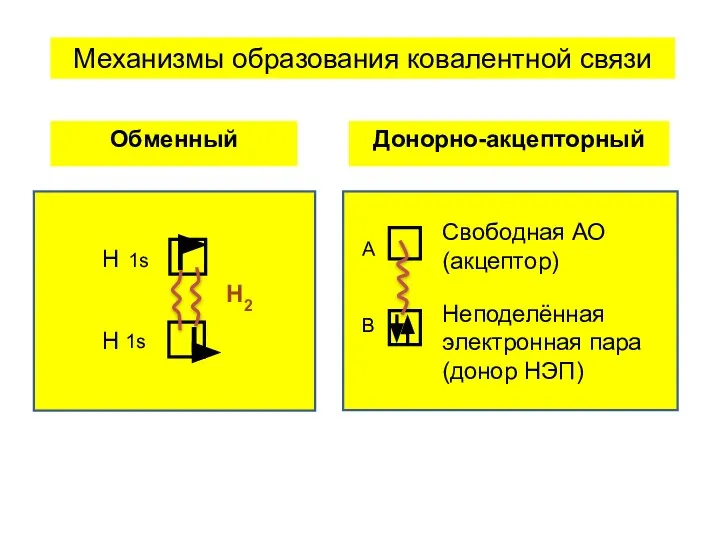
- 7. Н Н Н2 1s 1s Обменный А В Свободная АО (акцептор) Неподелённая электронная пара (донор НЭП)
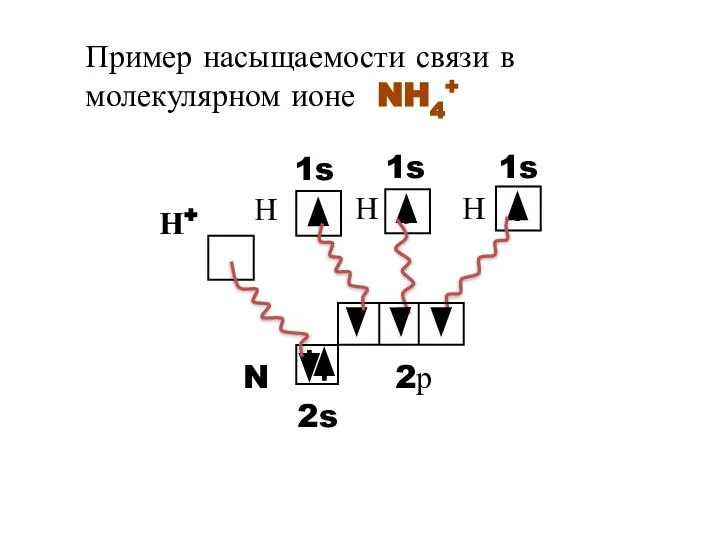
- 8. Пример насыщаемости связи в молекулярном ионе NH4+
- 9. s s σ-связь s s s p σ-связь 1 2 А) Б) Рис. Перекрывание атомных орбиталей
- 10. А) Б) d p p p d d В) Рис. Перекрывание АО при образовании π-связей. d
- 11. б) Направленность ковалентной связи. s ВеН2 возбуждённое нормальное
- 12. Образование sp-гибридных орбиталей. Гибридизация АО sp
- 13. Условия гибридизации АО. АО должны быть обязательно разного типа (s, p, и/или d), причём участие s-орбиталей
- 14. sp2 sp3
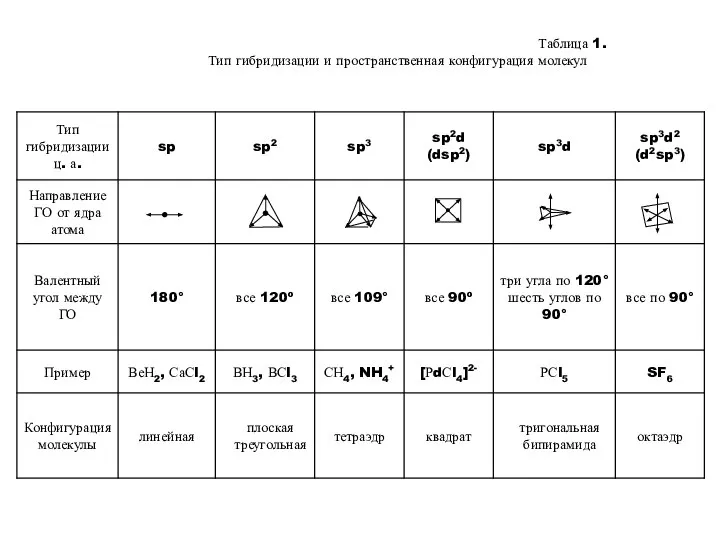
- 15. Таблица 1. Тип гибридизации и пространственная конфигурация молекул
- 16. 109,5° Рис.10. Форма молекул и влияние НЭП на величину валентного угла в молекуле (на примере sp3-гибридизации).
- 17. Молекулы с π - связями. π – связь π - связь О‾ О‾ О О ↔
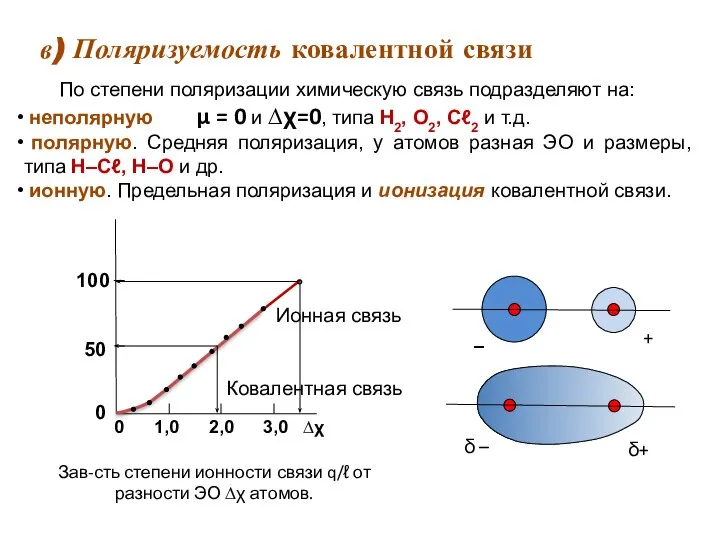
- 18. в) Поляризуемость ковалентной связи Ковалентная связь По степени поляризации химическую связь подразделяют на: неполярную μ =
- 19. Ионная связь. Свойства – неспецифичность ненасыщаемость ненаправленность. Ионные соединения не образуют молекул. координационное число – к.ч.
- 20. к.ч. = 6 к.ч. = 8
- 21. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ (ММО) 1927-29 гг. Ф. Гунд, Р. Малликен, Р. Ленард-Джонс и др. Основные положения
- 22. Имеются различные варианты ММО. Наиболее широкое использование получил метод МО ЛКАО «молекулярная орбиталь – есть линейная
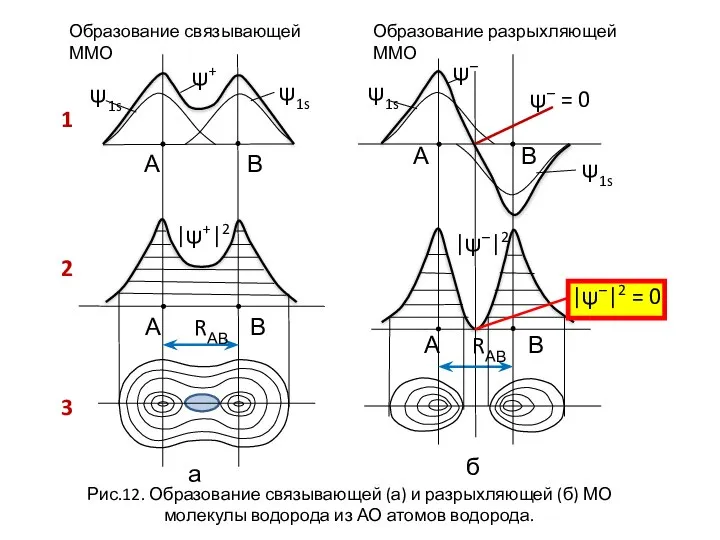
- 23. Образование связывающей ММО Образование разрыхляющей ММО
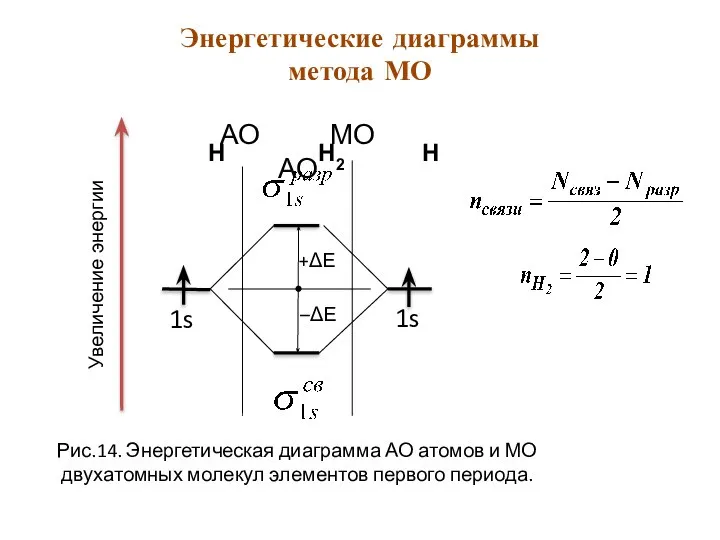
- 25. АО МО АО 1s 1s Увеличение энергии Рис.14. Энергетическая диаграмма АО атомов и МО двухатомных молекул
- 26. АОН диамагнит парамагнит
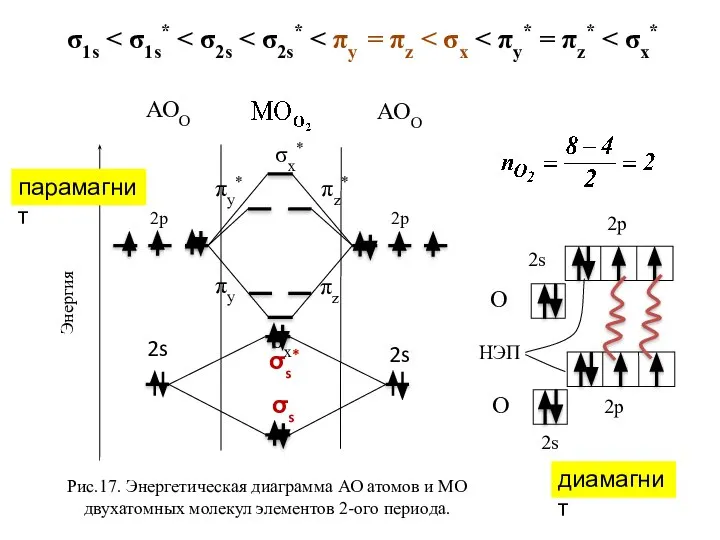
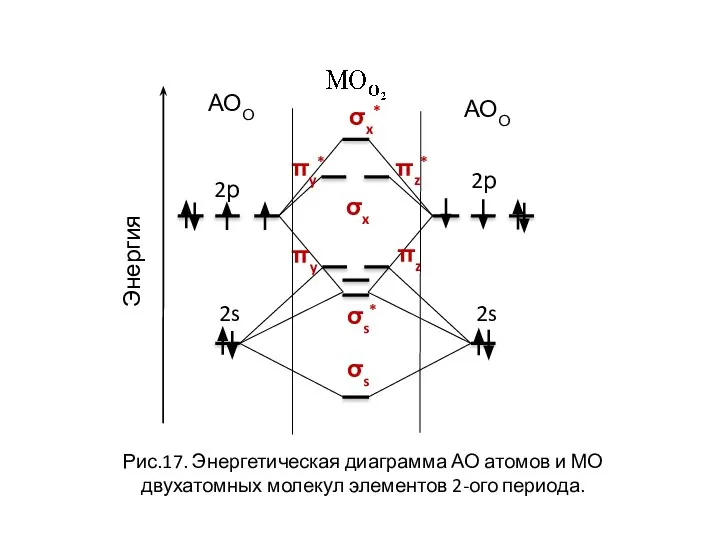
- 27. σx* σx πy πz πy* πz* Рис.17. Энергетическая диаграмма АО атомов и МО двухатомных молекул элементов
- 28. σs σs* σx* σx πy πz πy* πz* 2р 2s АОО Рис.17. Энергетическая диаграмма АО атомов
- 29. Метод МО при описании металлической связи. N (для 1 см3 порядка 1022–1023) ММО рассматривает металлическую связь
- 31. (а) ориентационное + ─ + ─ + ─ + ─ + ─ + ─ ± +
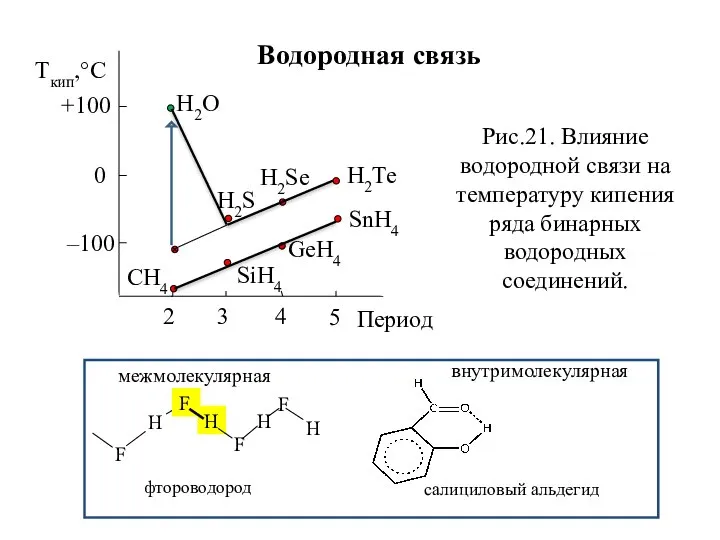
- 32. Водородная связь Н2О Н2Те Н2Sе Н2S СН4 SiН4 GеН4 SnН4 Ткип,°C +100 0 –100 2 3
- 33. Рис.22. Водородная связь в ионе НF2− и форма молекулярных орбиталей. + − + + − σs*
- 35. Скачать презентацию






















 Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1)
Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1) Штучні і синтетичні волокна
Штучні і синтетичні волокна  Химиялық реакция белгілерін атаңыз
Химиялық реакция белгілерін атаңыз Металлы и сплавы с высокой удельной прочностью
Металлы и сплавы с высокой удельной прочностью Физические и химические явления
Физические и химические явления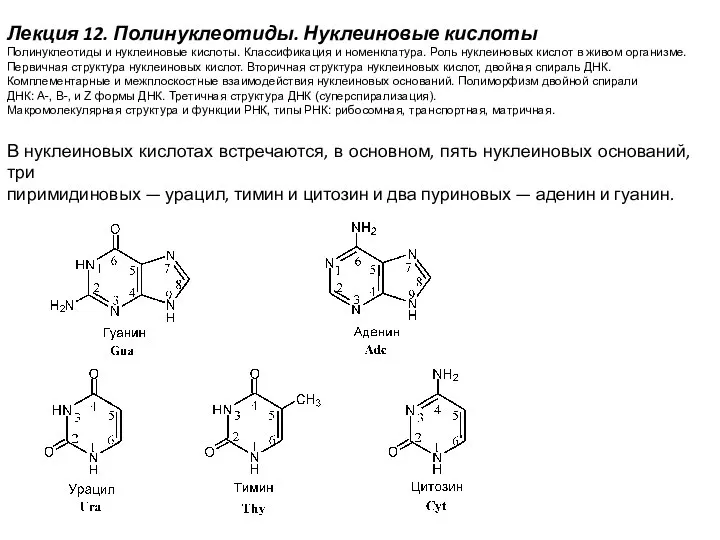 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты Выдающиеся ученые - химики и их заслуги
Выдающиеся ученые - химики и их заслуги Классификация моющих средств
Классификация моющих средств Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы Молярный объём газообразного вещества
Молярный объём газообразного вещества Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Тыңайтқыштар
Тыңайтқыштар Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат
Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат Неидеальные растворы
Неидеальные растворы Introduction to metabolism
Introduction to metabolism Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.
Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов. Алкены
Алкены Презентация Лекарства дома
Презентация Лекарства дома Химия (Органическая химия)
Химия (Органическая химия) Цикли трикарбонових кислот
Цикли трикарбонових кислот Алкадиены
Алкадиены Оксиды азота.
Оксиды азота. Общая химия, понятия
Общая химия, понятия Р-элементы IV группы: C, Si, Ge, Sn, Pb
Р-элементы IV группы: C, Si, Ge, Sn, Pb Основні класи неорганічних сполук
Основні класи неорганічних сполук Общая и неорганическая химия
Общая и неорганическая химия Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще
Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии
Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии