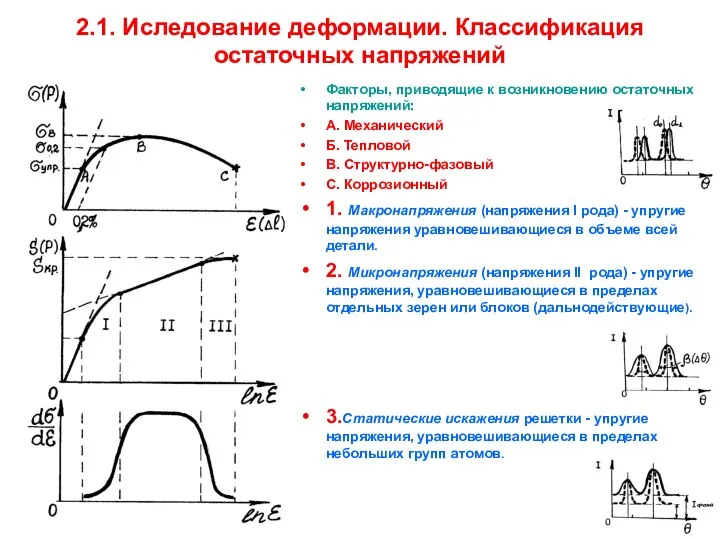
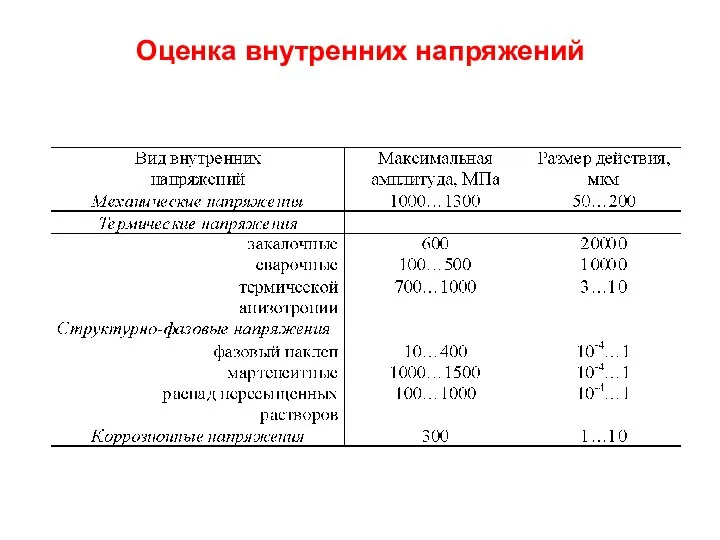
2.5. Коррозионные напряжения
Анодные процессы - заключаются в том, что металлы с
более отрицательным потенциалом в результате взаимодействия с токопроводящей средой (электролитом), содержащей атомы кислорода, водорода, хлора и др., будут окисляться (растворяться), переходя в раствор в виде ионов при соответствующих таблице разностях потенциалов по реакциям:
H2 → 2H+ + 2e− Cr → Cr3+ + 3e−
Fe → Fe2+ + 2e− Al → Al3+ + 3e−
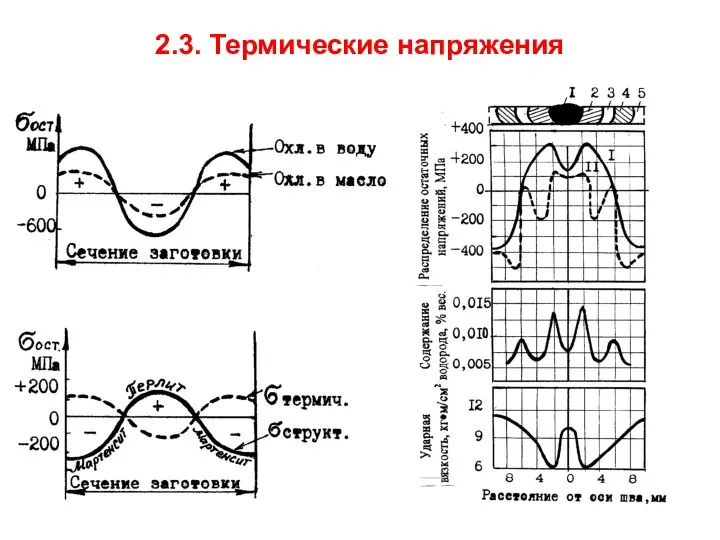
Катодные процессы - заключаются в том, что ионы металлов с более положительным потенциалом в результате взаимодействия с электролитом будут восстанавливаться (электролитически осаждаться) с участием электронов по реакции:
Ме2++ 2е− → 2 Ме например: Cu2+ + 2e- → Cu
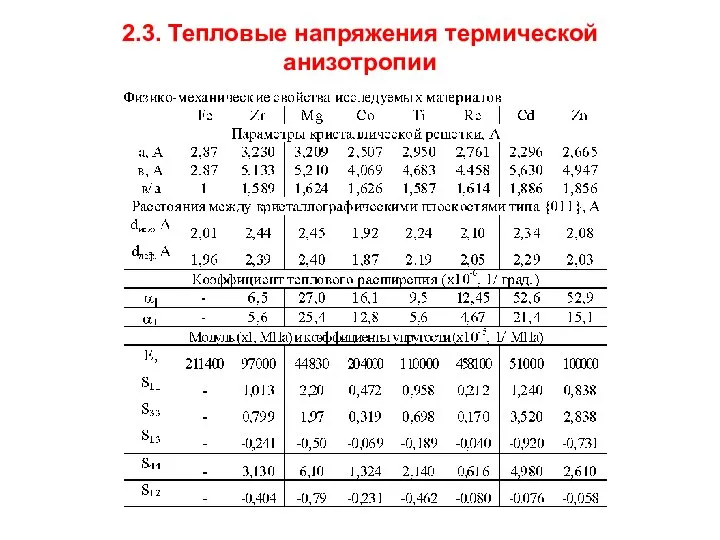
Электродные потенциалы, Е,В , 20°С.
низкая коррозионная стойкость
высокая коррозионная стойкость




![2.3. Тепловые напряжения термической анизотропии (α|| −α⊥) [cos2β − cos2(β+ψ)]___________________ S11[sin4β+sin4(β+ψ)]+S33[cos4β+cos4(β+ψ)]+(2S13+S44)[cos2β⋅sin2β+cos2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1337747/slide-8.jpg)


 Этиленовые, олефины, непредельные алкены
Этиленовые, олефины, непредельные алкены Химия вокруг нас
Химия вокруг нас Неравновесные явления в сложных химических процессах. Часть 1: электрохимия
Неравновесные явления в сложных химических процессах. Часть 1: электрохимия Липиды. Элементарный химический состав, содержание, строение, разнообразие, функции
Липиды. Элементарный химический состав, содержание, строение, разнообразие, функции Диазины. Характеристика диазинов. (Лекция 8)
Диазины. Характеристика диазинов. (Лекция 8) Презентация по химии Металлы
Презентация по химии Металлы  Презентация по химии Углерод
Презентация по химии Углерод Физика древесины
Физика древесины Органическая химия Скорость химических реакций
Органическая химия Скорость химических реакций Анилин. Физические свойства
Анилин. Физические свойства Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Аммиак
Аммиак Mechanistic insights into the aminolysis of 3,4-epoxysulfolane
Mechanistic insights into the aminolysis of 3,4-epoxysulfolane Презентация по Химии "Изучение характеристик мороженого как продукта питания" - скачать смотреть
Презентация по Химии "Изучение характеристик мороженого как продукта питания" - скачать смотреть  Презентация по Химии "Органічні сполуки і здоров’я людини." - скачать смотреть бесплатно
Презентация по Химии "Органічні сполуки і здоров’я людини." - скачать смотреть бесплатно II группа периодической системы Д. И. Менделеева. Магния сульфат. Кальция хлорид
II группа периодической системы Д. И. Менделеева. Магния сульфат. Кальция хлорид Кислородсодержащие органические соединения. Спирты. Фенолы. Альдегиды
Кислородсодержащие органические соединения. Спирты. Фенолы. Альдегиды Альдегиды. Раствор формальдегида. Гексаметилентетрамин (метенамин)
Альдегиды. Раствор формальдегида. Гексаметилентетрамин (метенамин) Простые вещества, металлы
Простые вещества, металлы Средние породы. Типичный андезитовый вулкан
Средние породы. Типичный андезитовый вулкан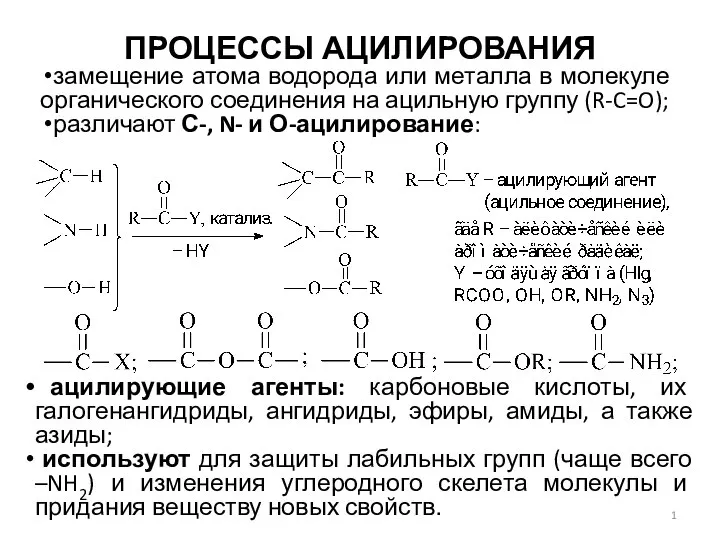 Процессы ацилирования
Процессы ацилирования Основные классы неорганических соединений
Основные классы неорганических соединений Значение теории химического строения А.М.Бутлерова
Значение теории химического строения А.М.Бутлерова  Антиоксидантная защита мозга
Антиоксидантная защита мозга Водород. Получение водорода
Водород. Получение водорода Буферные растворы. Буферная емкость
Буферные растворы. Буферная емкость Titration and Acid-Base Neutralization
Titration and Acid-Base Neutralization Неорганическая химия Сероводород
Неорганическая химия Сероводород