Содержание
- 2. К классу гетероциклов относят производные органических соединений, имеющих циклический скелет, в составе которого присутствуют атомы других
- 3. Гетероциклические соединения, как и карбоциклические, могут быть насыщенными и ненасыщенными Насыщенные гетероциклы по химическим свойствам почти
- 4. Распространение в природе Значимость Ароматические азотсодержащие гетероциклы широко распространены в природе; некоторые из них являются основой
- 5. Гетероциклические фрагменты входят в состав многих α-аминокислот
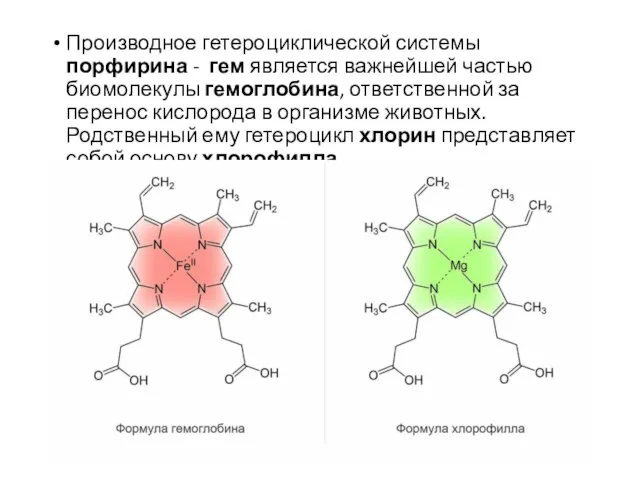
- 6. Производное гетероциклической системы порфирина - гем является важнейшей частью биомолекулы гемоглобина, ответственной за перенос кислорода в
- 7. Самые разнообразные системы гетероциклического ряда являются основой молекул витаминов молекула витамина B12 (цианокобаламина), представляет собой производное
- 8. Большое число производных гетероциклов применяется в качестве лекарственных средств
- 9. На основе гетероциклов синтезировано большое количество красителей. К синтетическим относятся синий индиго и метиленовый синий, красный
- 10. В растительном мире весьма распространены флавоны, флавонолы и антоцианидины. Окраска этих соединений варьируется в широком интервале
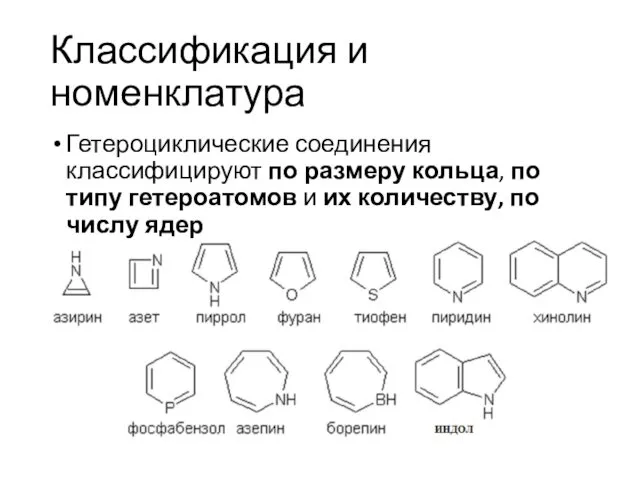
- 11. Классификация и номенклатура Гетероциклические соединения классифицируют по размеру кольца, по типу гетероатомов и их количеству, по
- 12. Ароматические шестичленные гетероциклы, содержащие хотя бы один атом азота, называют азины; в соответствии с количеством гетероатомов
- 13. Широко применяется также более старая номенклатура гетероциклов. Атомы ядра обозначают буквами греческого алфавита, начиная от соседнего
- 14. Типы гетероатомов Если гибридный атом образует максимально возможное количество σ-связей. При этом у него остаются неподеленные
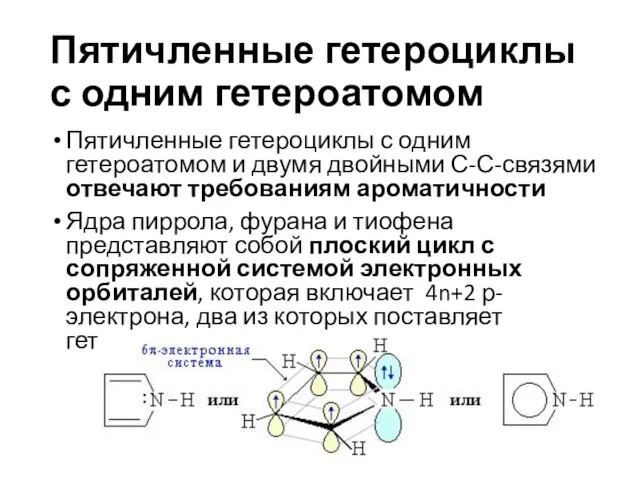
- 15. Пятичленные гетероциклы с одним гетероатомом Пятичленные гетероциклы с одним гетероатомом и двумя двойными С-С-связями отвечают требованиям
- 16. Атомы кислорода и серы, как и атом азота, способны выступать в качестве донора неподеленной пары электронов,
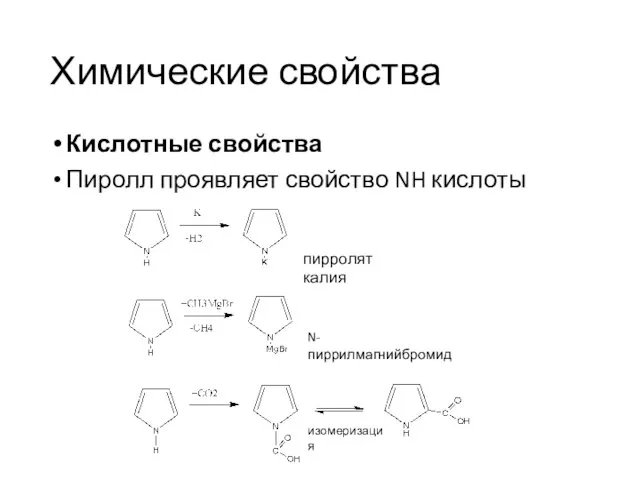
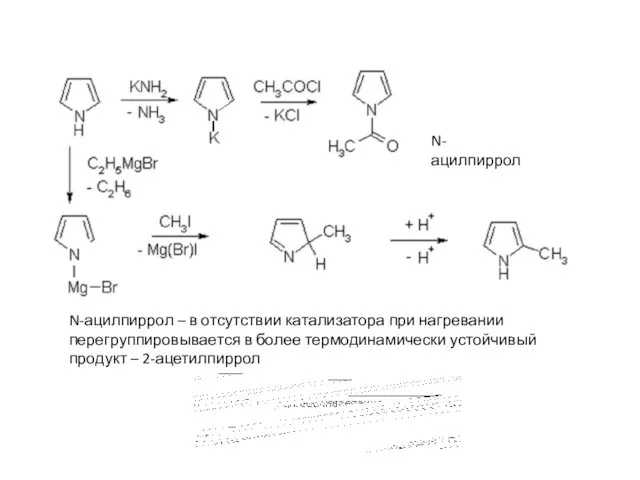
- 17. Химические свойства Кислотные свойства Пиролл проявляет свойство NH кислоты пирролят калия изомеризация N-пиррилмагнийбромид
- 18. N-ацилпиррол – в отсутствии катализатора при нагревании перегруппировывается в более термодинамически устойчивый продукт – 2-ацетилпиррол N-ацилпиррол
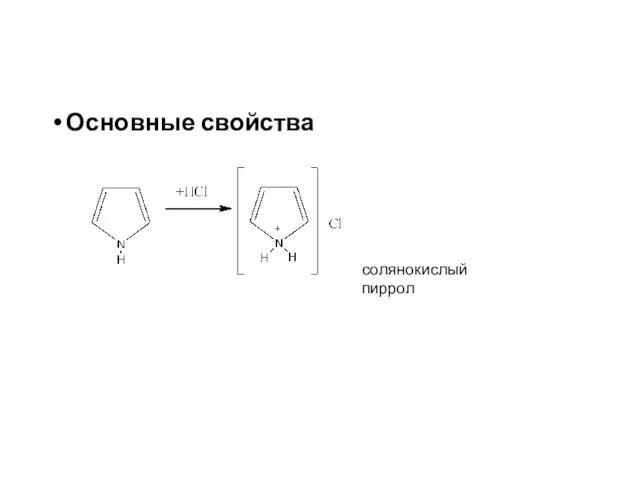
- 19. Основные свойства солянокислый пиррол
- 20. Реакции ядра Нитрование. Нитрующая смесь вызывают быстрое разложение пиррола, поэтому для нитрования используют специальные реагенты: ацетилнитрат,
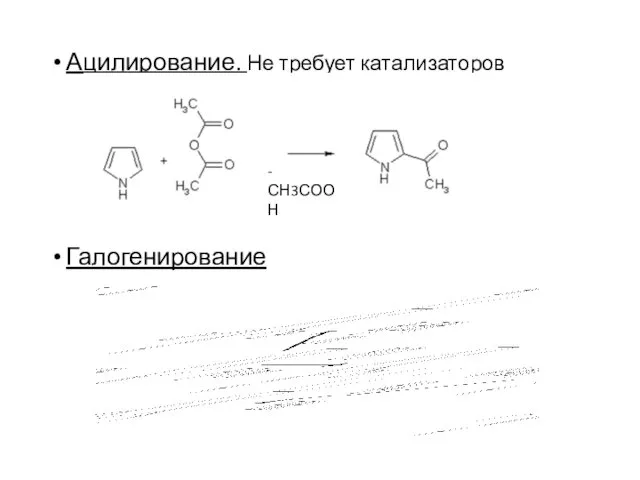
- 21. Ацилирование. Не требует катализаторов Галогенирование -СН3СООН
- 22. Карбоксилирование по Кольбе с карбонатом аммония Реакция азосочетания
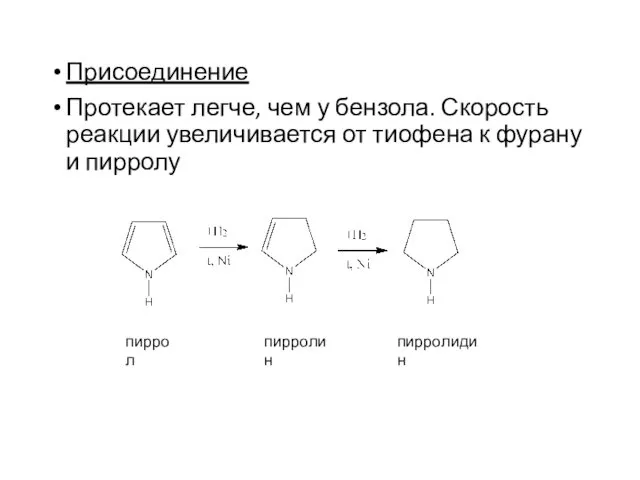
- 23. Присоединение Протекает легче, чем у бензола. Скорость реакции увеличивается от тиофена к фурану и пирролу пиррол
- 24. Взаимопревращение пятичленных гетероциклов Реакция Юрьева. В жестких условиях пиррол, фуран и тиофен способны к раскрытию кольца
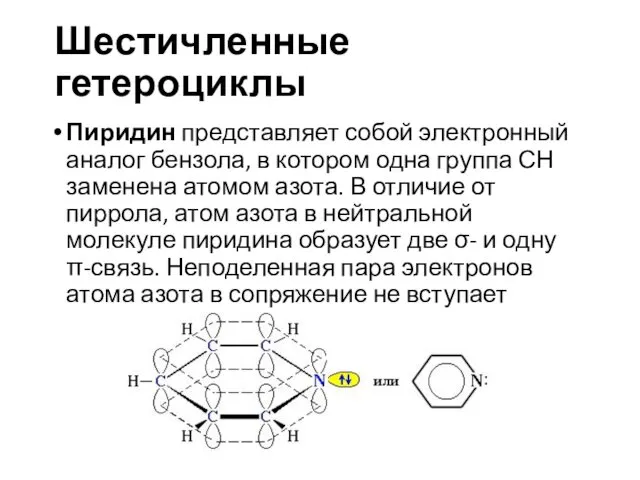
- 25. Шестичленные гетероциклы Пиридин представляет собой электронный аналог бензола, в котором одна группа СН заменена атомом азота.
- 26. Химические свойства Превращения по атому азота Основные свойства. Пиридин – основание средней силы Нуклеофильные свойства
- 27. Реакции по кольцу Эти реакции протекают значительно труднее, чем в бензоле. Пиридин атакуется только сильнейшими электрофилами,
- 28. 2) Сульфирование 3) Галогенирование
- 29. Нуклеофильное замещение Более характерными превращениями пиридина являются реакции нуклеофильного замещения. Замещение атома водорода на аминогруппу протекает
- 30. Свободнорадикальные реакции При действии атомарных хлора и брома на пиридин происходит свободнорадикальное галогенирование, которое, в отличие
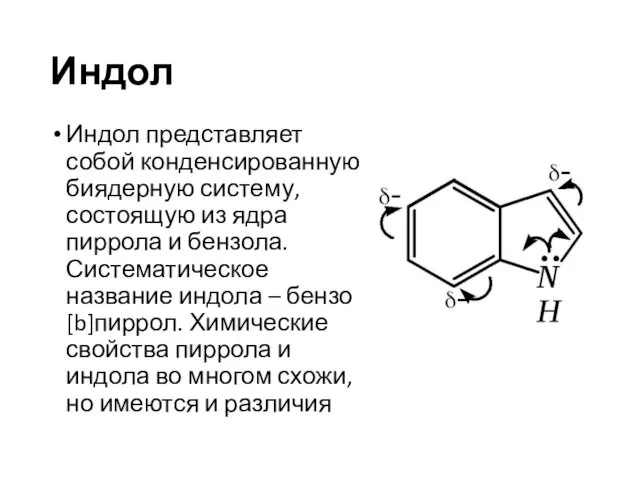
- 31. Индол Индол представляет собой конденсированную биядерную систему, состоящую из ядра пиррола и бензола. Систематическое название индола
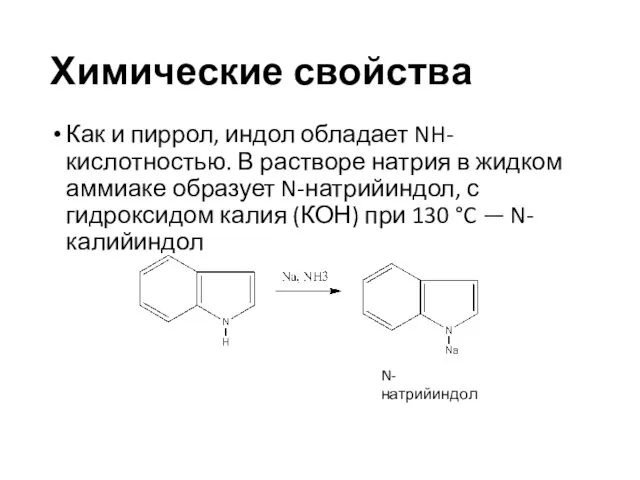
- 32. Химические свойства Как и пиррол, индол обладает NH-кислотностью. В растворе натрия в жидком аммиаке образует N-натрийиндол,
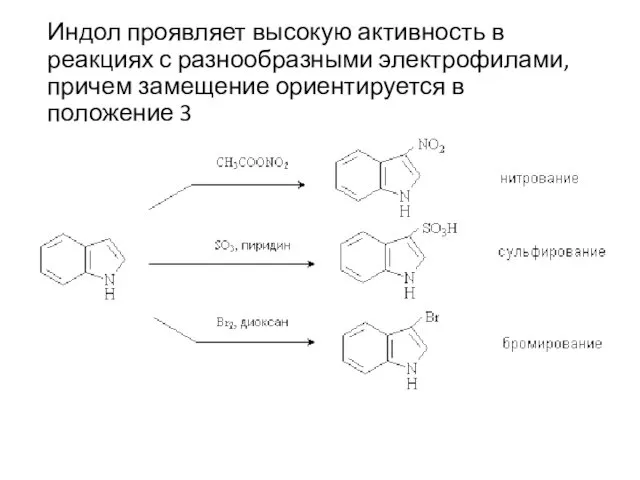
- 33. Индол проявляет высокую активность в реакциях с разнообразными электрофилами, причем замещение ориентируется в положение 3
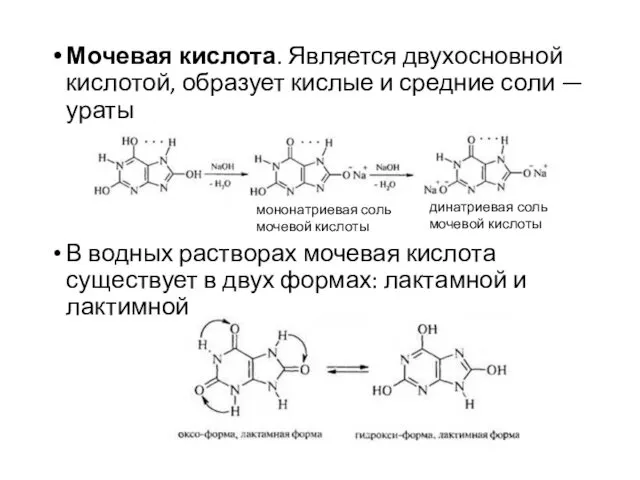
- 34. Мочевая кислота. Является двухосновной кислотой, образует кислые и средние соли — ураты В водных растворах мочевая
- 36. Скачать презентацию




















 Лекция 8. Стационарная кинетика (продолжение). Сложные ферментативные реакции
Лекция 8. Стационарная кинетика (продолжение). Сложные ферментативные реакции Химиялық реакциялардың типтері
Химиялық реакциялардың типтері Структура електронної оболонки атома
Структура електронної оболонки атома Природные источники углеводородов
Природные источники углеводородов Презентация по Химии "Ферменты" - скачать смотреть
Презентация по Химии "Ферменты" - скачать смотреть  Моделирование химико-технологических процессов
Моделирование химико-технологических процессов Металдарға жалпы сипаттама
Металдарға жалпы сипаттама Кинетическое лимитирование роста и жизненные стратегии микроорганизмов
Кинетическое лимитирование роста и жизненные стратегии микроорганизмов Магматические формации
Магматические формации Производные фенола: танины
Производные фенола: танины Синтез Aspergillin PZ
Синтез Aspergillin PZ Обменные реакции в растворах электролитов
Обменные реакции в растворах электролитов ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар
ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар Подготовка нефти и газового конденсата к переработке. Атмосферная и вакуумная перегонка
Подготовка нефти и газового конденсата к переработке. Атмосферная и вакуумная перегонка Кремний и его соединения
Кремний и его соединения Dzeramā ūdens sagatavošanas shēma
Dzeramā ūdens sagatavošanas shēma Биодеградируемые полимеры – продукты биотехнологии
Биодеградируемые полимеры – продукты биотехнологии Клетка. Химический состав клеток
Клетка. Химический состав клеток Полистирол өндірісі
Полистирол өндірісі Превращения веществ. Роль химии в жизни человека
Превращения веществ. Роль химии в жизни человека Механические свойства минералов
Механические свойства минералов Химия 9 класс Химия 9 класс Приходько Альбина Анатольевна Учитель химии и биологии МОУ «Дубровская СОШ»
Химия 9 класс Химия 9 класс Приходько Альбина Анатольевна Учитель химии и биологии МОУ «Дубровская СОШ»  ЗАСТОСУВАННЯ РІДКИХ КРИСТАЛІВ Виконала учениця 10 класу Гаєвська Зоряна
ЗАСТОСУВАННЯ РІДКИХ КРИСТАЛІВ Виконала учениця 10 класу Гаєвська Зоряна  Электронное и пространственное строение молекул органических соединений – основа их биологической активности
Электронное и пространственное строение молекул органических соединений – основа их биологической активности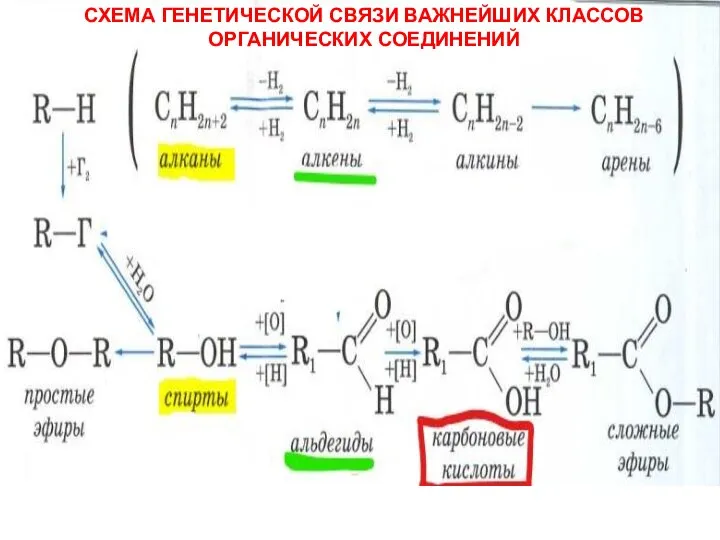 Схема генетической связи важнейших классов органических соединений
Схема генетической связи важнейших классов органических соединений Почему протекают химические реакции Учитель химии ГОУ средняя общеобразовательная школа №10 с углубленным изучением химии
Почему протекают химические реакции Учитель химии ГОУ средняя общеобразовательная школа №10 с углубленным изучением химии  Факторы и процессы формирования химического состава подземных вод
Факторы и процессы формирования химического состава подземных вод Кремний и его соединения. Силикатная промышленность
Кремний и его соединения. Силикатная промышленность