Содержание
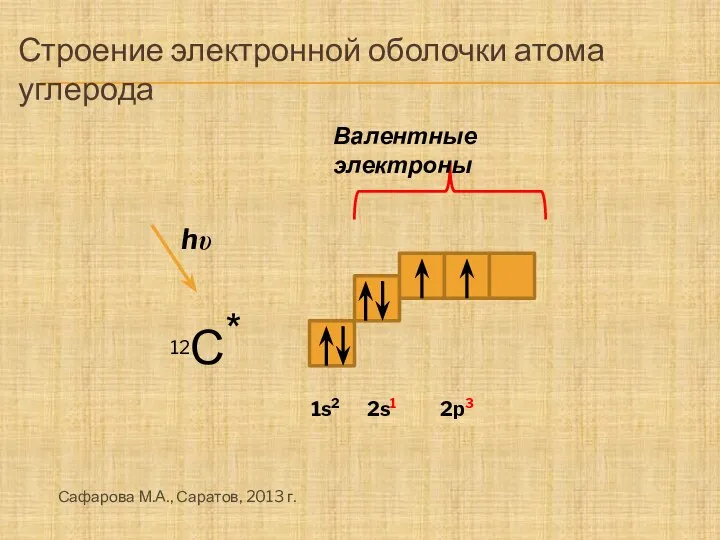
- 2. Строение электронной оболочки атома углерода 12С * hυ Валентные электроны 1s2 2s2 2p2 2s1 2p3 Сафарова
- 3. ГИБРИДИЗАЦИЯ АТОМА УГЛЕРОДА В зависимости от количества орбиталей, принимающих участие в гибридизации, различают sp3-, sp2- и
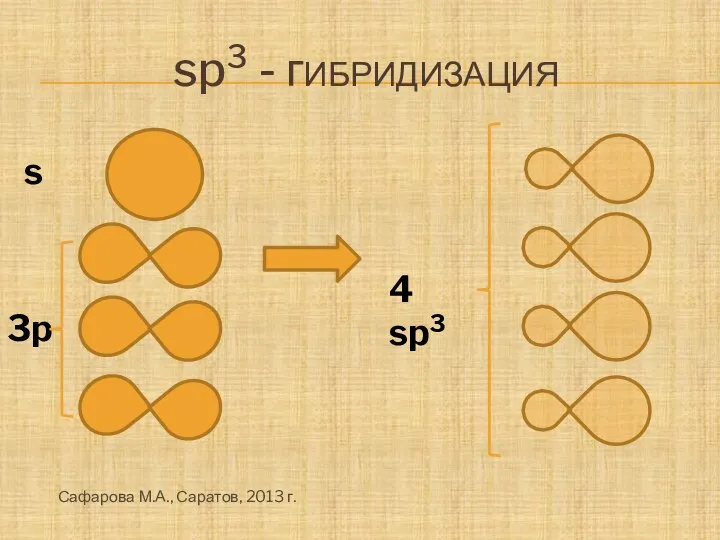
- 4. sp3 - гибридизация 3p s 4 sp3 Сафарова М.А., Саратов, 2013 г.
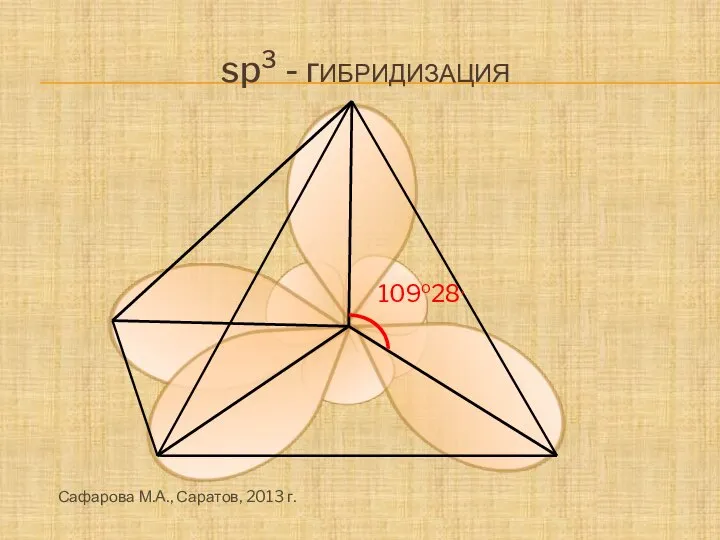
- 5. 109o28, sp3 - гибридизация Сафарова М.А., Саратов, 2013 г.
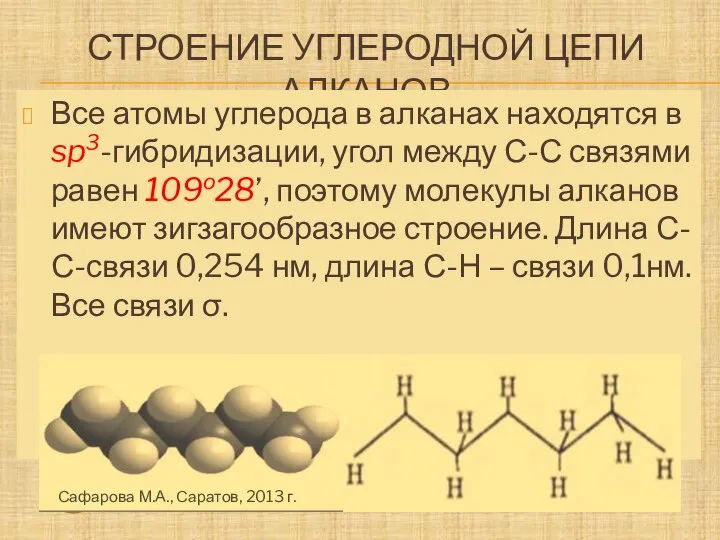
- 6. СТРОЕНИЕ УГЛЕРОДНОЙ ЦЕПИ АЛКАНОВ Молекула метана Молекула этана - Атомы водорода Все атомы углерода в алканах
- 7. В алмазе атомы углерода находятся в sp3 – гибридизации. Сафарова М.А., Саратов, 2013 г.
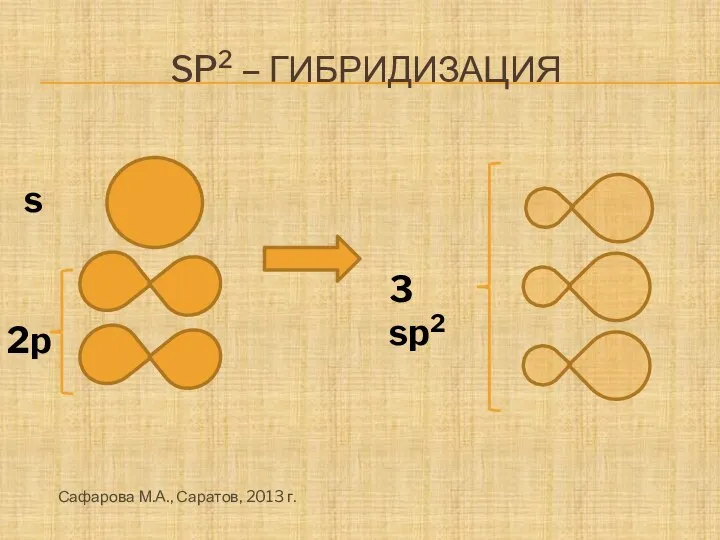
- 8. SP2 – ГИБРИДИЗАЦИЯ s 3 sp2 2p Сафарова М.А., Саратов, 2013 г.
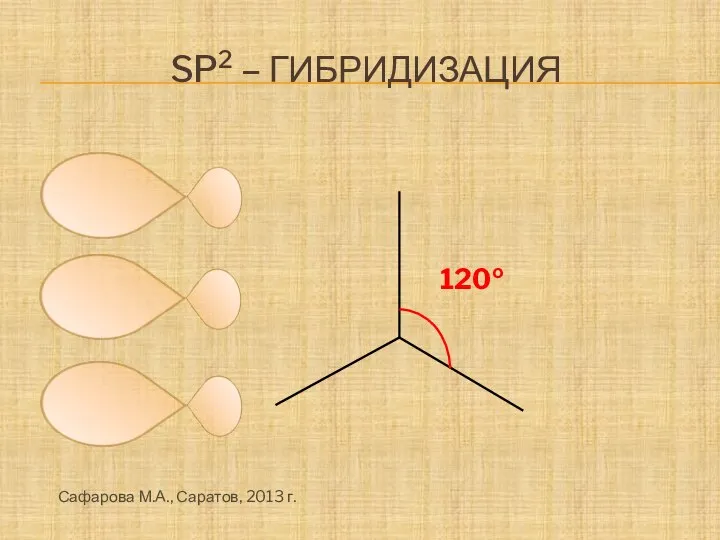
- 9. SP2 – ГИБРИДИЗАЦИЯ 120о Сафарова М.А., Саратов, 2013 г.
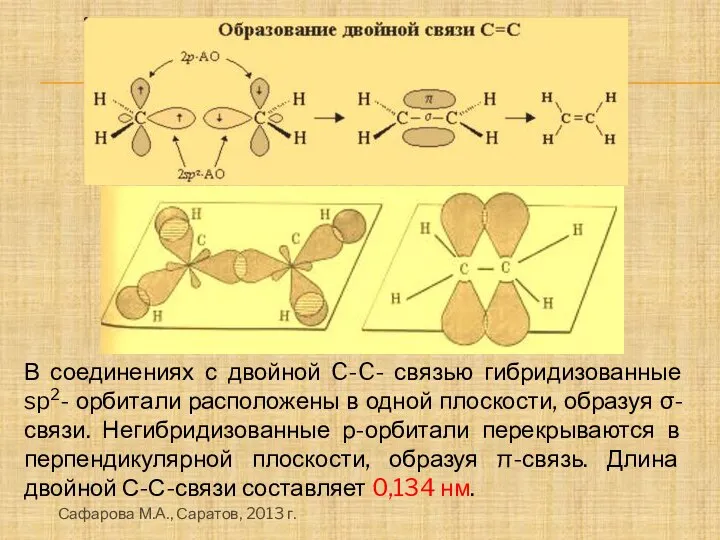
- 10. В соединениях с двойной C-C- связью гибридизованные sp2- орбитали расположены в одной плоскости, образуя σ-связи. Негибридизованные
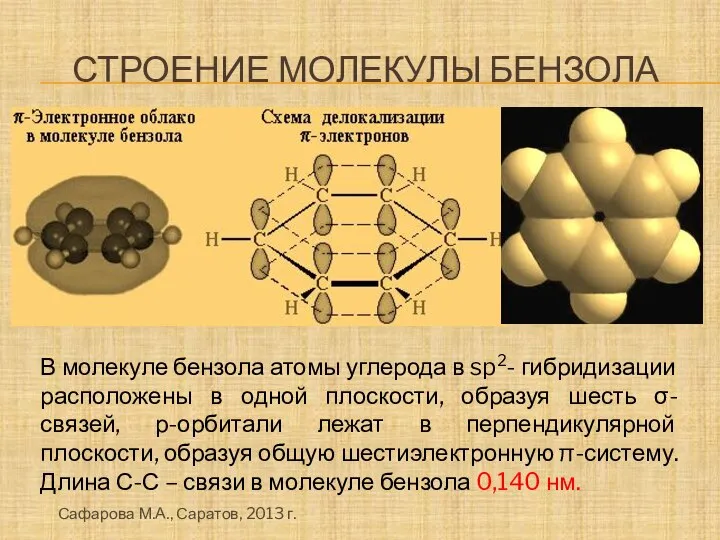
- 11. СТРОЕНИЕ МОЛЕКУЛЫ БЕНЗОЛА В молекуле бензола атомы углерода в sp2- гибридизации расположены в одной плоскости, образуя
- 12. В молекуле графита атомы углерода находятся в sp2- гибридизации. Бензольное кольцо можно рассматривать как структурную единицу
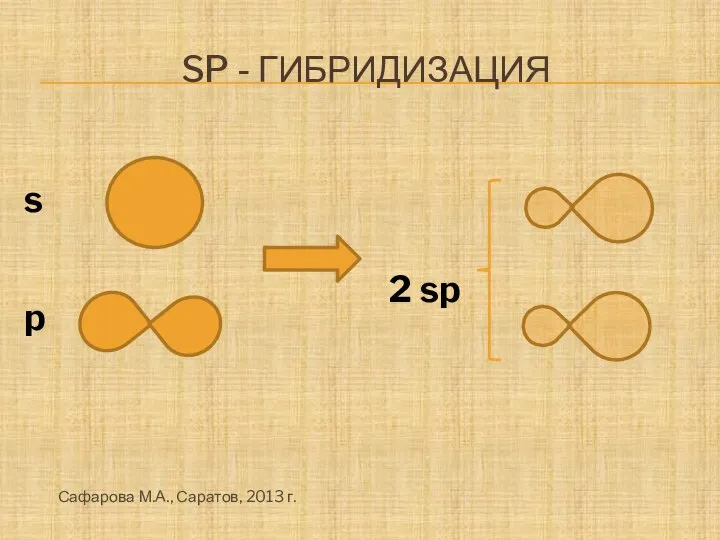
- 13. SP - ГИБРИДИЗАЦИЯ s 2 sp p Сафарова М.А., Саратов, 2013 г.
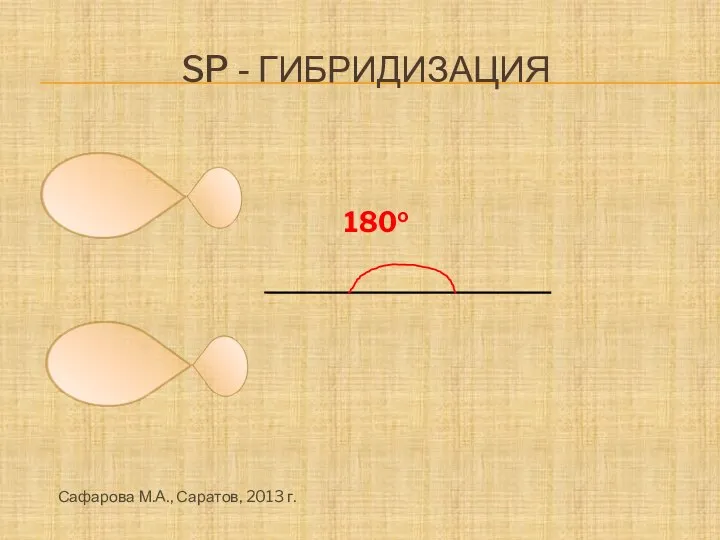
- 14. SP - ГИБРИДИЗАЦИЯ 180о Сафарова М.А., Саратов, 2013 г.
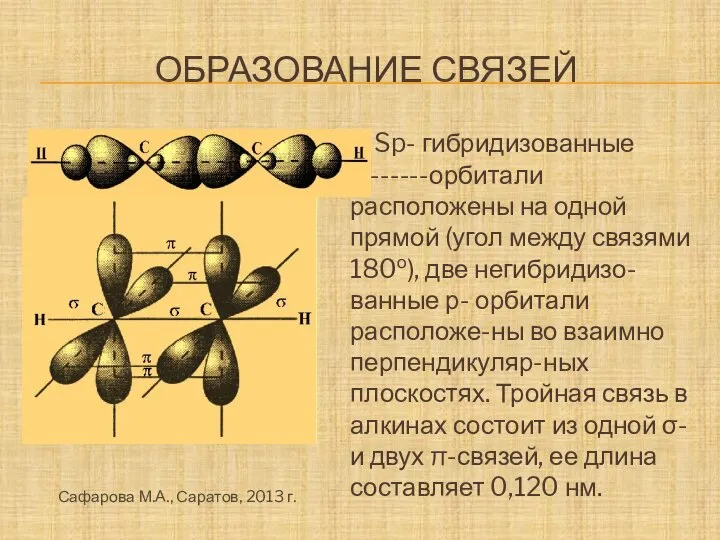
- 15. ОБРАЗОВАНИЕ СВЯЗЕЙ Sp- гибридизованные --------орбитали расположены на одной прямой (угол между связями 180о), две негибридизо-ванные р-
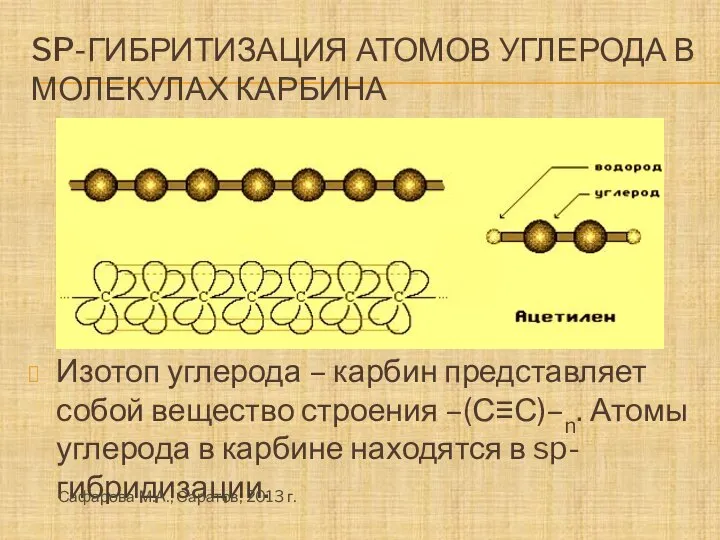
- 16. SP-ГИБРИТИЗАЦИЯ АТОМОВ УГЛЕРОДА В МОЛЕКУЛАХ КАРБИНА Изотоп углерода – карбин представляет собой вещество строения –(С≡С)–n. Атомы
- 18. Скачать презентацию



 «Е у шкільному буфеті?!»
«Е у шкільному буфеті?!»  Общие сведения о комплексных соединениях
Общие сведения о комплексных соединениях Супрамолекулярные системы – мост между неживой и живой материей
Супрамолекулярные системы – мост между неживой и живой материей Метали
Метали  Тағамдық қоспалар. Тағамдық бояулар. Антиоксиданттар. Эмульгаторлар
Тағамдық қоспалар. Тағамдық бояулар. Антиоксиданттар. Эмульгаторлар Gmp – тиісті өндірістік тәжірибе
Gmp – тиісті өндірістік тәжірибе Закономерности протекания химических процессов. Основы химической термодинамики. (Лекция 2)
Закономерности протекания химических процессов. Основы химической термодинамики. (Лекция 2) История спички Выполнил ученик 9 б класса МОУ Навлинская СОШ №1 Фролов Кирилл
История спички Выполнил ученик 9 б класса МОУ Навлинская СОШ №1 Фролов Кирилл Строение вещества
Строение вещества Высшие жирные кислоты. Липиды
Высшие жирные кислоты. Липиды Реакции ионного обмена. Свойства ионов
Реакции ионного обмена. Свойства ионов Крахмал
Крахмал Химия. Лекция 1. Термодинамика и кинетика
Химия. Лекция 1. Термодинамика и кинетика Применение CVD алмаза в технологии лавинно-пролётных диодов
Применение CVD алмаза в технологии лавинно-пролётных диодов Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Основания. Гидроксид железа (II)
Основания. Гидроксид железа (II) Основные задачи токсикологической химии в аналитической диагностике наркотических и психотропных веществ (Продолжение)
Основные задачи токсикологической химии в аналитической диагностике наркотических и психотропных веществ (Продолжение) Курс лекций по химии
Курс лекций по химии Химиялық технологияның басқа ғылыммен байланысы. Негізгі технологиялық түсініктер және анықтамалар
Химиялық технологияның басқа ғылыммен байланысы. Негізгі технологиялық түсініктер және анықтамалар Расчеты по химическим уравнениям
Расчеты по химическим уравнениям Все о чае
Все о чае  Алкины. Строение алкинов
Алкины. Строение алкинов Иридоиды. Классификация
Иридоиды. Классификация Термопластические полимеры
Термопластические полимеры Сапалық талдау. Сапалық аналитикалық реакциялар
Сапалық талдау. Сапалық аналитикалық реакциялар Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Титриметрические методы анализа
Титриметрические методы анализа Воздух - источник жизни на земле. (3 класс)
Воздух - источник жизни на земле. (3 класс)