Содержание
- 2. Гидроксиды. Основания: способы получения Что надо узнать: Состав и названия Классификация Способы получения
- 3. K2O + H2O → 2KOH Гидроксиды– это сложные вещества в состав которых входят атомы металлов и
- 4. Основания - это гидроксиды металлов IА и IIА (кроме Be), а также металлов в минимальной степени
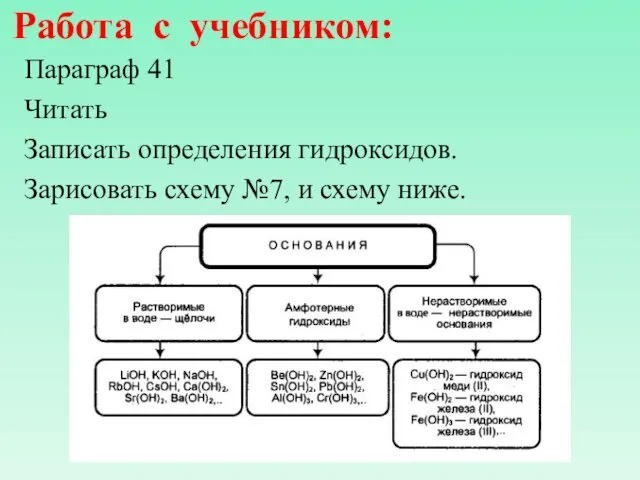
- 5. Работа с учебником: Параграф 41 Читать Записать определения гидроксидов. Зарисовать схему №7, и схему ниже.
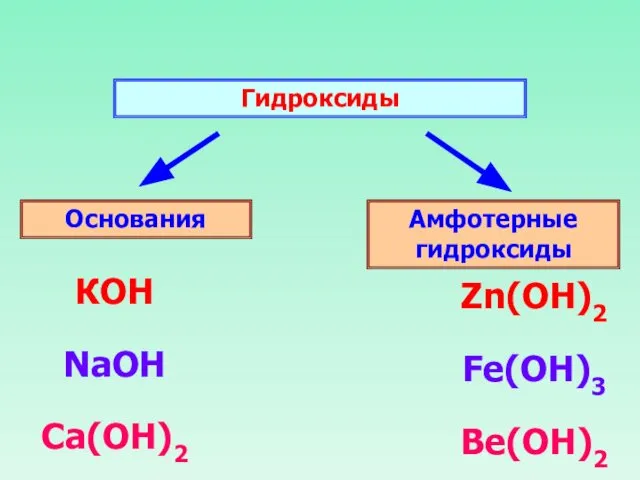
- 7. Гидроксиды Основания Амфотерные гидроксиды КОН NaOH Ca(OH)2 Zn(ОН)2 Fe(OH)3 Be(OH)2
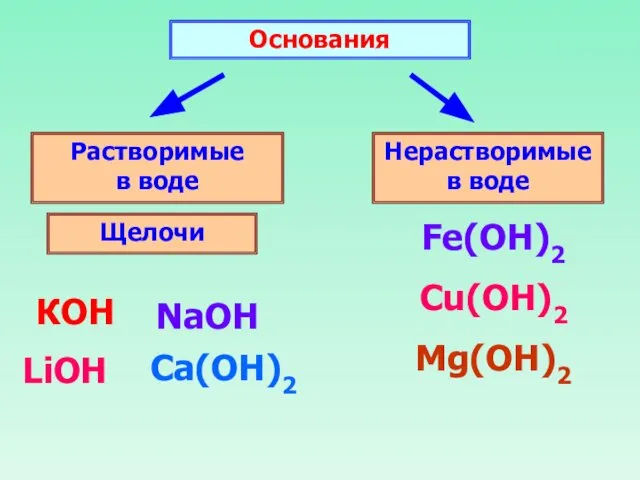
- 8. Основания Растворимые в воде Нерастворимые в воде Щелочи КОН NaOH Ca(ОН)2 LiOH Fe(OH)2 Cu(OH)2 Mg(ОН)2
- 9. NaOH – гидроксид натрия, едкий натр, каустическая сода
- 10. Записать по презентации и учебнику страница 139 получение оснований как словами так и формулами. Выписать физические
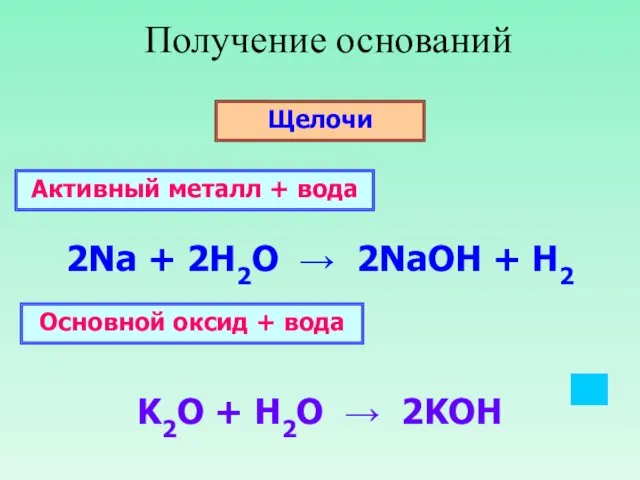
- 11. Получение оснований Щелочи 2Na + 2H2O → 2NaOH + H2 K2O + H2O → 2KOH Активный
- 12. Сильные и слабые основания
- 14. Скачать презентацию






 Презентация по химии Классы неорганических веществ
Презентация по химии Классы неорганических веществ Кислород. Электронное строение и свойства
Кислород. Электронное строение и свойства Душистые вещества животного и растительного происхождения
Душистые вещества животного и растительного происхождения Электролиз веществ
Электролиз веществ Гидролиз солей
Гидролиз солей Алкены
Алкены Пластические массы
Пластические массы Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Голубое золото
Голубое золото Химия: основные понятия
Химия: основные понятия Презентация по Химии "Скло Будівельний матеріал" - скачать смотреть бесплатно
Презентация по Химии "Скло Будівельний матеріал" - скачать смотреть бесплатно Презентация по Химии "Великие учёные, внёсшие значительный вклад в развитие химии." - скачать смотреть бесплатно
Презентация по Химии "Великие учёные, внёсшие значительный вклад в развитие химии." - скачать смотреть бесплатно Презентация по Химии "Проблеми використання відходів видобутку та переробки" - скачать смотреть бесплатно
Презентация по Химии "Проблеми використання відходів видобутку та переробки" - скачать смотреть бесплатно Производство минеральных удобрений
Производство минеральных удобрений Электролиз: опыты к заданиям ЕГЭ
Электролиз: опыты к заданиям ЕГЭ Новые катализаторы
Новые катализаторы Люди отличающиеся от нас
Люди отличающиеся от нас Синтез реакционноспособных олигомеров и полимеров на их основе
Синтез реакционноспособных олигомеров и полимеров на их основе Определение массы и объёма по плотности вещества
Определение массы и объёма по плотности вещества Презентация по химии по теме: «Гидролиз»
Презентация по химии по теме: «Гидролиз»  Пентозофосфатный цикл
Пентозофосфатный цикл Применение закона действующих масс к гетерогенным равновесиям. Ионное произведение растворимости. (Лекция 5)
Применение закона действующих масс к гетерогенным равновесиям. Ионное произведение растворимости. (Лекция 5) Нефть и способы её переработки.
Нефть и способы её переработки. МЕТАЛЛЫ Подготовила: преподаватель химии и биологии Уалихановского сельскохозяйственного колледжа Сыздыкова Карлыгаш Казбеков
МЕТАЛЛЫ Подготовила: преподаватель химии и биологии Уалихановского сельскохозяйственного колледжа Сыздыкова Карлыгаш Казбеков Властивості та застосування полімерів
Властивості та застосування полімерів Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9
Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9 Ocena zawartości mikotoksyn w wybranych produktach spożywczych
Ocena zawartości mikotoksyn w wybranych produktach spożywczych Презентация по химии Общая характеристика реакций органических соединений. Классификация органических реакций и реагентов.
Презентация по химии Общая характеристика реакций органических соединений. Классификация органических реакций и реагентов.