Содержание
- 2. Гидроксилпроизводные – это такие производные углеводородов, в состав молекулы которых входит одна или несколько гидроксильных групп.
- 3. Классификация В зависимости от количества гидроксильных групп различают: Одноатомные; Двухатомные; Трех- и многоатомные. В зависимости от
- 4. Номенклатура
- 5. Таким образом получаем, что различают следующие группы гидроксилпроизводных: Насыщенные (предельные) одноатомные спирты Ненасыщенные одноатомные спирты Гидроксилпрозводные
- 6. Гидроксилпроизводные алкиларенов с гидроксильной группой в боковой цепи Дигидроксилпроизводные – двухатомные спирты (диолы) классификация
- 7. Трёхатомные и многоатомные спирты Гидроксилпроизводные ароматическихуглеводородов - фенолы классификация
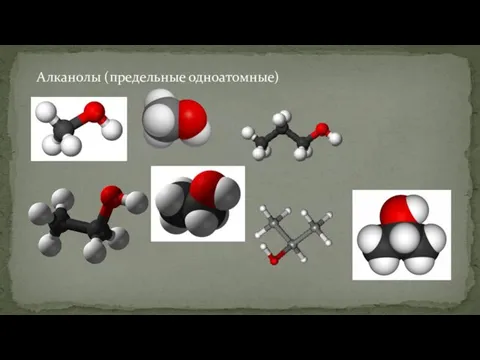
- 8. Алканолы (предельные одноатомные)
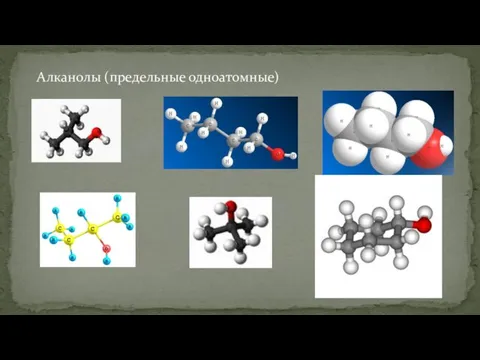
- 9. Алканолы (предельные одноатомные)
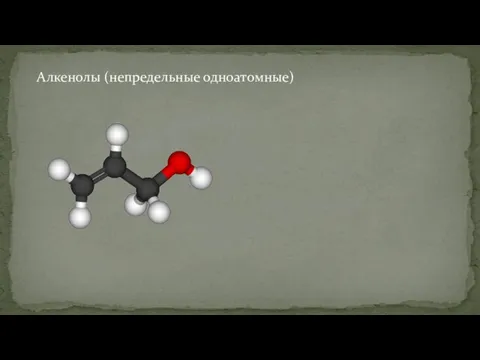
- 10. Алкенолы (непредельные одноатомные)
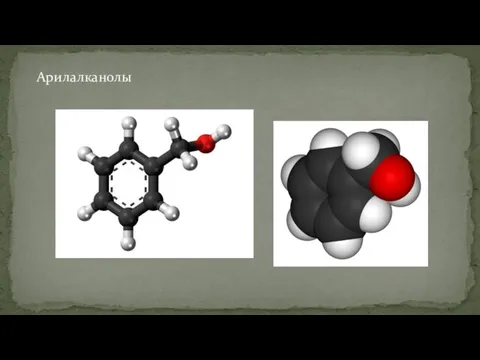
- 11. Арилалканолы
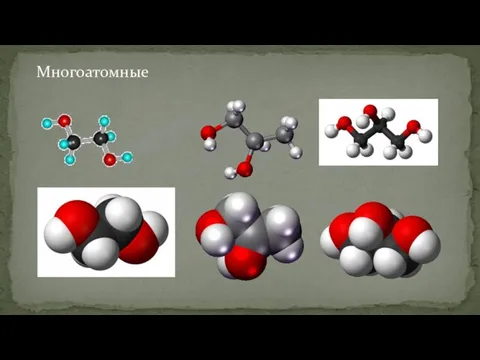
- 12. Многоатомные
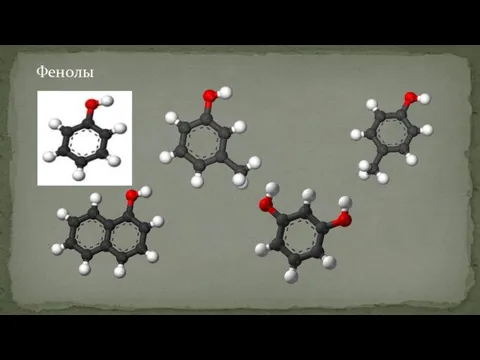
- 13. Фенолы
- 14. Спирты
- 15. Спирты - это производные углеводородов, содержащие одну или несколько гидроксильных групп (-O-H) R-OH
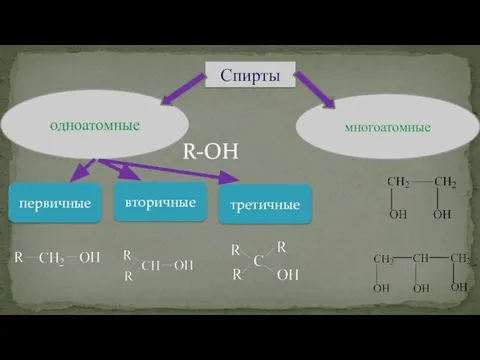
- 16. Классификация спиртов
- 17. третичные R-OH
- 18. Номенклатура спиртов
- 19. Название углеводородного радикала и окончание ОЛ CH3-OH метанол (метиловый спирт) CH3-CH2-OH этанол (этиловый спирт) CH3-CH2-CH2-OH пропанол-1
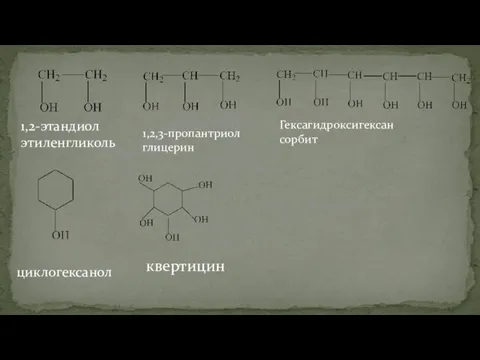
- 20. 1,2-этандиол этиленгликоль 1,2,3-пропантриол глицерин Гексагидроксигексан сорбит циклогексанол квертицин
- 21. ЩЕЛОЧНОЙ ГИДРОЛИЗ ГАЛОГЕНУГЛЕВОДОРОДОВ: при нагревании с водными растворами щелочей C-Hal F Методы получения спиртов
- 23. 2. ГИДРАТАЦИЯ АЛКЕНОВ
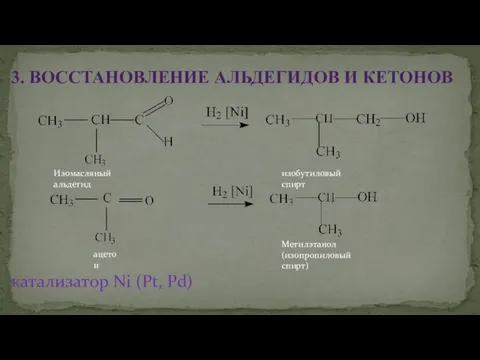
- 24. катализатор Ni (Pt, Pd) 3. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
- 25. 4. Синтез спиртов с помощью реактивов Гриньяра: Пропионовый альдегид метилмагнийиодид δ+ δ- δ- δ+ Алкоголят вторичный
- 26. Этанол получают из пищевого и непищевого органического сырья путем сбраживания: глюкоза ферменты
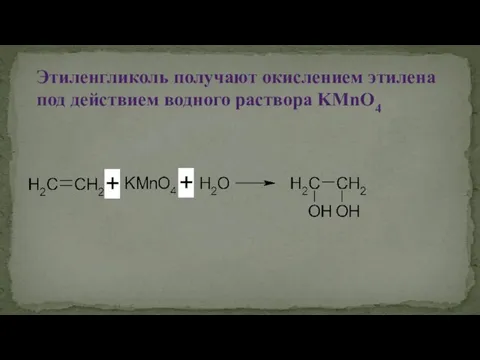
- 27. Этиленгликоль получают окислением этилена под действием водного раствора KMnO4
- 28. Условия: Нагревание, высокое давление, катализатор (Fe, Co) nCO +2nH2 → CnH2n+1OH + (n-1)H2O Получение смеси спиртов
- 29. В качестве окислителей применяют перекись водорода или щелочной раствор перманганата калия Кроме того многоатомные спирты получают
- 30. А так же многоатомные спирты получают из α-оксидов алкенов
- 31. Физические свойства спиртов Молекулы спиртов ассоциированы за счет образования межмолекулярных водородных связей: Низшие и средние предельные
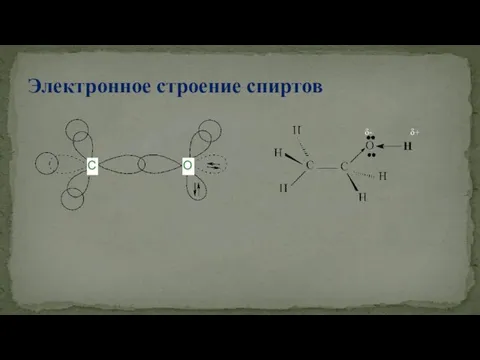
- 32. Электронное строение спиртов δ- δ+
- 33. Спирты очень слабые электролиты (слабее воды) CH3-CH2-O-H ↔CH3-CH2-O- + H+ Типы реакций Реакции с участием водорода
- 34. 1. Замещение гидроксильного атома водорода на металл. (Na,Mg,Al) 2R-O-H + 2Na →2R-O-Na + H2 Алкоголят натрия
- 35. 2. Реакция этерификации – образование сложных эфиров
- 36. 1. Замещение гидроксила на галоген: CH3OH +PBr5 ↔ CH3Br + POBr3 + РBr метанол бромметан C3H7OH
- 37. Условия: Нагревание с конц. H2SO4 или ZnCl2 (Al2O3) 2. Отщепление воды с образованием алкенов
- 38. Условия: нагревание избытка спирта с серной кислотой или пары спирта при 2000С через порошок сульфата алюминия
- 39. Условия: 3000С, Al2O3 R-O-H + NH3 → R-NH2 + HOH спирт амин 4. Замена гидроксила на
- 40. III. Реакции окисления, в которых одновременно принимают участие гидроксильная группа, α-водородные атомы или соседние связи С-С
- 41. Условие: пропускание паров спирта при 200 -3000С над мелкораздробленной медью или серебром α-H этиловый спирт уксусный
- 42. Условия : сильные окислители (H2SO4 +KMnO4; H2SO4+ K2Cr2O7) Первичные спирты: Этанол этаналь (альдегид) 2. Окисление
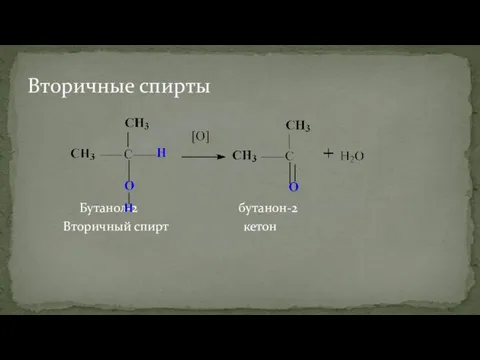
- 43. Бутанол-2 бутанон-2 Вторичный спирт кетон Вторичные спирты
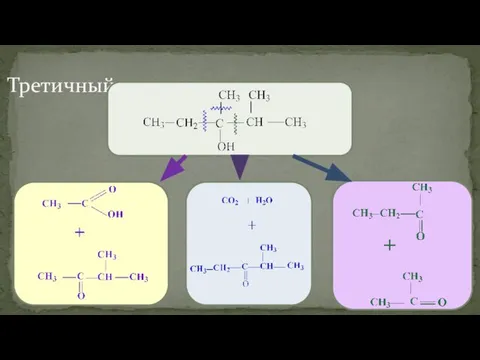
- 44. Третичный спирт
- 45. Взаимодействие с металлами (Na, K, Mg, Al) Многоатомные спирты
- 46. Взаимодействие с гидроксидами металлов Многоатомные спирты
- 47. Взаимодействие с гидроксидами металлов При взаимодействии с гидроксидами d-металлов образуются комплексные соединения Многоатомные спирты
- 48. Взаимодействие с кислотами (реакция этерефикации) протекает ступенчато Многоатомные спирты
- 49. Замещение гидроксила на галоген Многоатомные спирты
- 50. Дегидратация Межмолекулярная При нагревании со спиртами в присутствии сильных кислот (серной или ортофосфорной) Многоатомные спирты
- 51. Дегидратация Межмолекулярная При нагревании с сильными кислотами (серной или ортофосфорной) образуют циклические эфиры Многоатомные спирты
- 52. Дегидратация Внутримолекулярная В случае гликолей с изолированными гидроксогруппами (γ-гликоли и т.д.) происходит образование внутренних циклических эфиров
- 53. Дегидратация Внутримолекулярная В случае гликолей с изолированными гидроксогруппами (β-гликоли) происходит образование непредельных спиртов Многоатомные спирты
- 54. Дегидратация Особым образом происходит этот процесс в случае пинаконов (спиртов, в молекулах которых рядом находятся две
- 55. Окисление В общем виде окисление многоатомных спиртов на примере этиленгликоля может быть представлено следующим образом Многоатомные
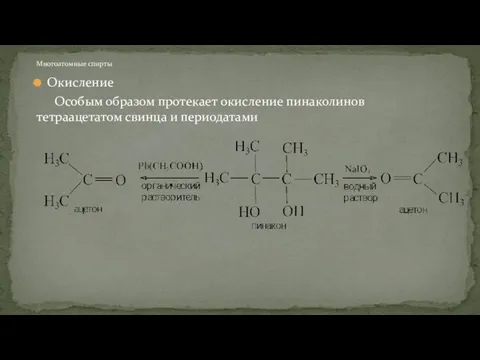
- 56. Окисление Особым образом протекает окисление пинаколинов тетраацетатом свинца и периодатами Многоатомные спирты
- 57. Отдельные представители спиртов
- 58. CH3OH Метанол — это первый представитель гомологического ряда предельных одноатомных спиртов. Общая формула СnH2n+1OH. Метанол (метиловый
- 59. Метанол -жидкость без цвета с температурой кипения 64 0С, с характерным запахом, легче воды, горит бесцветным
- 60. ПРИМЕНЕНИЕ метилового спирта
- 61. метанол Форм-альдегид (смолы) Уксусная кислота Изопрен Формалин Эфиры Растворитель в лакокрасочной промышленности Топливные элементы Добавка к
- 62. В газовой промышленности используется для борьбы с образованием гидратов. (При добыче газа гидраты могут образовываться в
- 63. Во многих странах метанол применяется в качестве добавки к этиловому спирту при производстве парфюмерии. В России
- 64. Метанол — опаснейший яд, приём внутрь 5—10 мл метанола приводит к тяжёлому отравлению и слепоте, а
- 65. Этиловый спирт (Этанол)
- 66. Этанол-бесцветная жидкость с характерным запахом и жгучим вкусом, температурой кипения78 0С. Легче воды. Смешивается с ней
- 67. Применение этанола
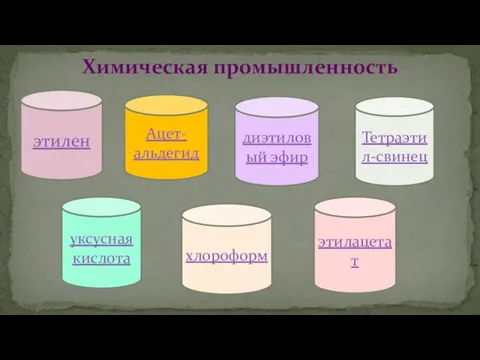
- 68. Химическая промышленность Ацет-альдегид диэтиловый эфир Тетраэтил-свинец уксусная кислота хлороформ этилацетат этилен
- 69. В лакокрасочной промышленности, в производстве товаров бытовой химии (в чистящих и моющих средствах, в особенности для
- 70. Является универсальным растворителем различных веществ и основным компонентом духов, аэрозолей. Входит в состав зубных паст, шампуни,
- 71. Этиловый спирт также используется как топливо. Применяется для консервирования биологических препаратов. Является наполнителем в спиртовых термометрах*.
- 72. антисептик; подсушивающие и дубящие свойства 96%-го этилового спирта используются для обработки операционного поля или для обработки
- 73. Является основным компонентом спиртных напитков. В небольших количествах содержится в ряде напитков, получаемых брожением, но не
- 74. Депресантом – психоактивным веществом, угнетающим центральную нервную систему. В зависимости от дозы, концентрации, пути попадания в
- 75. Этиленгликоль Прозрачная бесцветная жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Токсичен.
- 76. Как компонент автомобильных антифризов и тормозных жидкостей. Смесь 60 % этиленгликоля и 40 % воды замерзает
- 77. В органическом синтезе для получения многих веществ и как высокотемпературный растворитель Как компонент жидкости «И», используемой
- 78. Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C Этиленгликоль токсичен. По степени воздействия на организм
- 79. трехатомный предельный спирт. Бесцветная, вязкая, гигроскопичная, сладкая (гликос — сладкий) на вкус жидкость. Смешивается с водой
- 80. Применяется в производстве взрывчатых веществ нитроглицерина. При обработке кожи. Как компонент некоторых клеев. При производстве пластмасс
- 81. Фенолы
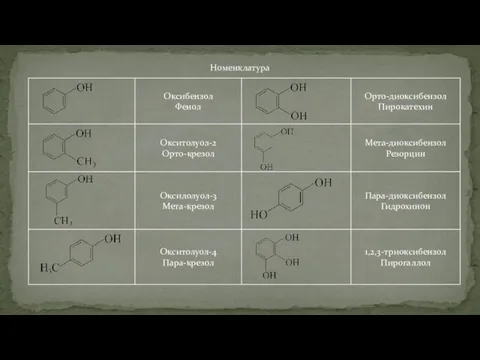
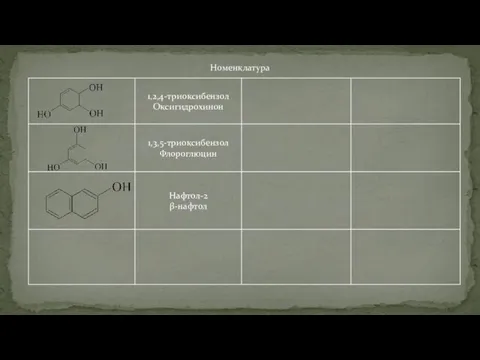
- 83. Номенклатура
- 84. Номенклатура
- 85. Номенклатура
- 86. Положения гидроксильных групп Строения и положения заместителей Межклассовая изомерия Изомерия
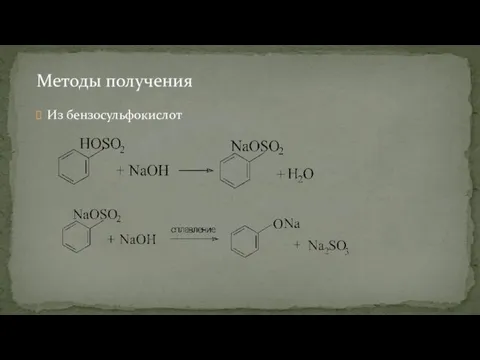
- 87. Из бензосульфокислот Методы получения
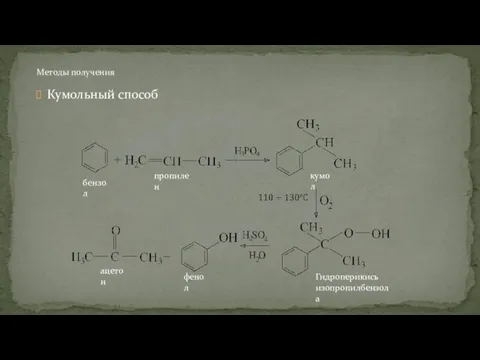
- 88. Кумольный способ Методы получения
- 89. Парофазный каталитический гидролиз бензолхлорида Методы получения
- 90. Фенолы при обычных условиях представляют собой жидкости или твёрдые вещества с очень своеобразным, сильным и устойчивым
- 91. Кислотность и реакции с участием атома кислорода. Фенолы являются слабыми кислотами, но значительно более сильными по
- 92. Фенолы имеют очень характерную цветную реакцию: в водных растворах с FeCl3 они дают красно-фиолетовое окрашивание, которое
- 93. Алкилирование Химические свойства. Кислотность и реакции с участием атома кислорода.
- 94. Ацилирование Химические свойства. Кислотность и реакции с участием атома кислорода.
- 95. Окисление. Химические свойства.
- 96. Реакции с электрофильными реагентами. Галогенирование. Химические свойства.
- 97. Нитрование. Химические свойства. Реакции с электрофильными реагентами.
- 98. Сульфирование. Химические свойства. Реакции с электрофильными реагентами.
- 99. Ацилирование. Химические свойства. Реакции с электрофильными реагентами.
- 100. Алкилирование. Химические свойства. Реакции с электрофильными реагентами.
- 102. Скачать презентацию














































































 Синтез 2,6-диметил-3,5-диэтоксикарбонилпиридина
Синтез 2,6-диметил-3,5-диэтоксикарбонилпиридина Адсорбция. Поглощение газов или паров из газовых смесей или растворов твердым веществом
Адсорбция. Поглощение газов или паров из газовых смесей или растворов твердым веществом История развития химии
История развития химии Презентация по Химии "Алгоритм решения задач" - скачать смотреть
Презентация по Химии "Алгоритм решения задач" - скачать смотреть  Ленточные силикаты
Ленточные силикаты Отримання кисню. Властивості кисню
Отримання кисню. Властивості кисню Термодинамика. Химическое равновесие. Кинетика
Термодинамика. Химическое равновесие. Кинетика Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Презентация по Химии "Полимеры" 10 класс
Презентация по Химии "Полимеры" 10 класс Термические процессы нефтепереработки
Термические процессы нефтепереработки Задачи на массовую долю растворённого вещества в растворе
Задачи на массовую долю растворённого вещества в растворе Отравляющие вещества
Отравляющие вещества  Особенности химического состава клетки
Особенности химического состава клетки Adaptive response of metal-oxide memristive nanostructures to periodic electric stimulation
Adaptive response of metal-oxide memristive nanostructures to periodic electric stimulation Композиционные или композитные материалы
Композиционные или композитные материалы Атомно-молекулярное учение. (Лекция 1)
Атомно-молекулярное учение. (Лекция 1) Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Ионный обмен или сорбция
Ионный обмен или сорбция Термодинамическое равновесие
Термодинамическое равновесие Аморфные сплавы
Аморфные сплавы Классификация моторных масел
Классификация моторных масел Комплексные соединения
Комплексные соединения Химические опасности. Токсичные элементы. Мышьяк. Свинец. Ртуть
Химические опасности. Токсичные элементы. Мышьяк. Свинец. Ртуть Подготовка к аттестации. ГОУ гимназия №1587ЮАО, Иванова Т.Ю.
Подготовка к аттестации. ГОУ гимназия №1587ЮАО, Иванова Т.Ю. Методы измерения и приборное обеспечение радиационно-экологического мониторинга. (Лекция 6)
Методы измерения и приборное обеспечение радиационно-экологического мониторинга. (Лекция 6)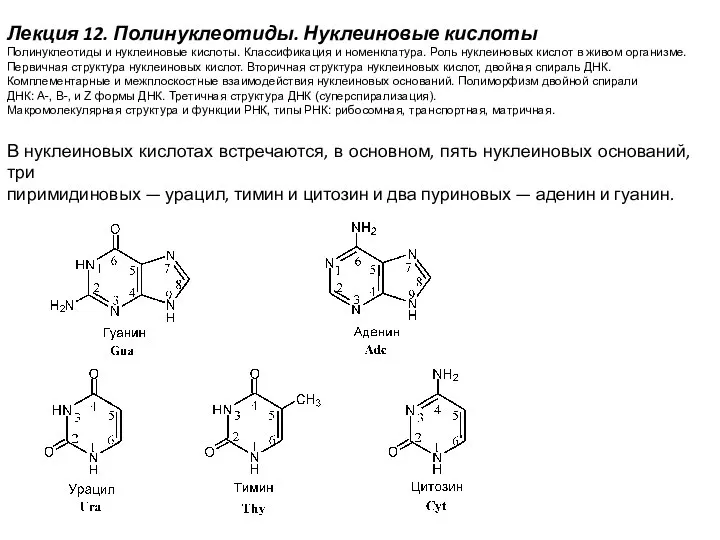 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты Противогололёдные реагенты. Вред или польза?
Противогололёдные реагенты. Вред или польза? Структура ЕГЭ по химии. Электролиз
Структура ЕГЭ по химии. Электролиз