Содержание
- 2. Урок химии в 11 классе Эпиграф урока: Учиться – это как грести против течения: стоит остановиться
- 3. 1. Какие вещества называются солями? 2. В результате реакций какого типа образуются соли? Почему эти реакции
- 4. Проведём эксперимент…
- 5. Окраска индикаторов
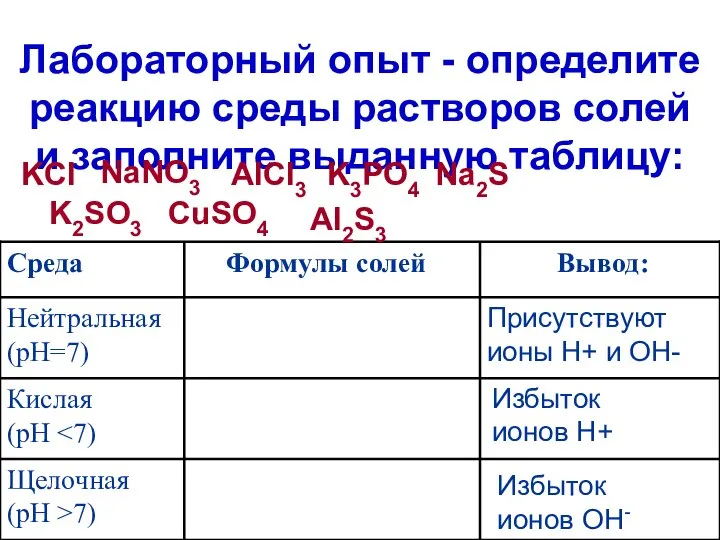
- 6. Лабораторный опыт - определите реакцию среды растворов солей и заполните выданную таблицу: KCl NaNO3 AlCl3 K3PO4
- 7. Проблемный вопрос: Почему растворы солей имеют не только нейтральную, но и кислую и щелочную среду?
- 8. Тема урока: Гидролиз неорганических и органических соединений
- 9. Цель урока: изучить сущность процесса гидролиза Задачи : - Сформулировать определение понятия «гидролиз» - научиться объяснять
- 10. Слово «гидролиз» означает разложение водой («гидро» вода, «лизис» - разложение) Гидролиз - одно из важнейших химических
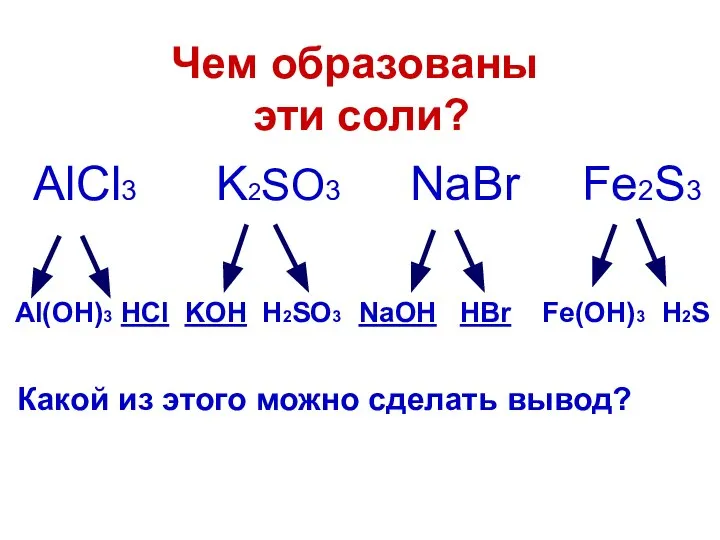
- 11. Чем образованы эти соли? AlCl3 K2SO3 NaBr Fe2S3 Al(OH)3 HCl KOH H2SO3 NaOH HBr Fe(OH)3 H2S
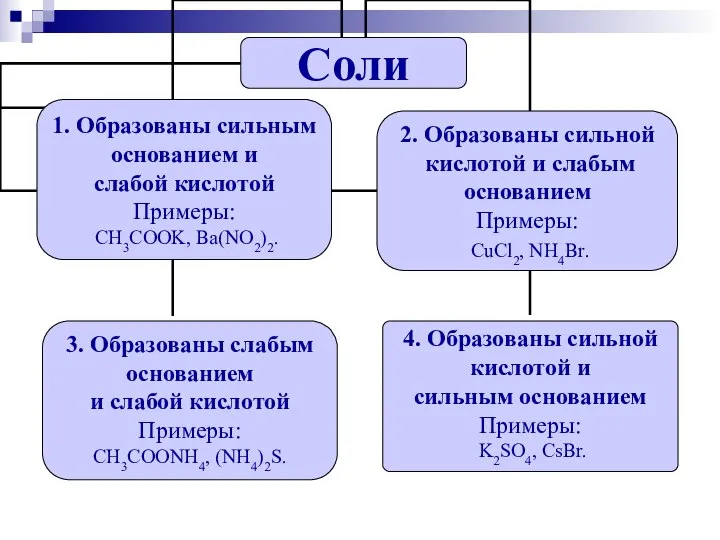
- 13. Алгоритм составления уравнений гидролиза: 1. Необходимо определить состав соли, указать, какими по силе основанием и какой
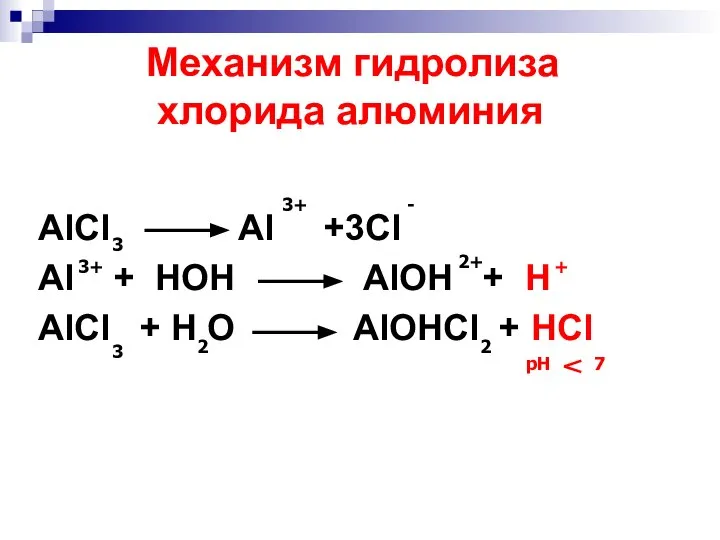
- 14. Механизм гидролиза хлорида алюминия AlCl Al +3Cl Al + HOH AlOH + H AlCl + H
- 15. Вывод: Раствор соли, образованной _________ , гидролизуется по _______ ,имеет _______ среду, так как в растворе
- 16. Вывод: Раствор соли, образованной _________ , гидролизуется по ____ и ___ ,имеет _______ среду, так как
- 17. Вывод: Раствор соли, образованной ________, не гидролизуется, имеет _____среду, так как в растворе присутствуют и ионы
- 18. Гидролизом соли называется взаимодействие ионов соли с водой, в результате которого образуются слабые электролиты
- 19. Степень гидролиза Как влияет температура на степень гидролиза? Как влияет разбавление на степень гидролиза?
- 20. Значение гидролиза
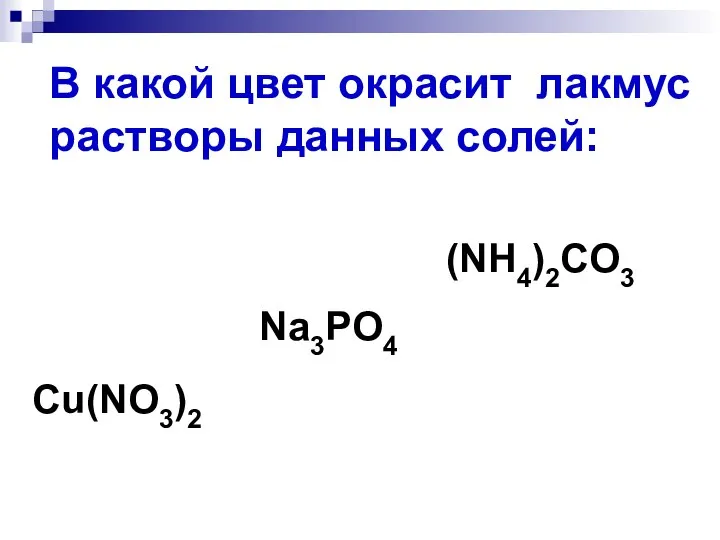
- 21. В какой цвет окрасит лакмус растворы данных солей: Cu(NO3)2 Na3PO4 (NH4)2CO3
- 22. Укажите, какие из следующих солей подвергаются гидролизу а) по аниону: б) по катиону: CuCl2 Mn(NO3)2 Na2CO3
- 23. Проблемный вопрос: Почему растворы солей имеют не только нейтральную, но и кислую и щелочную среду?
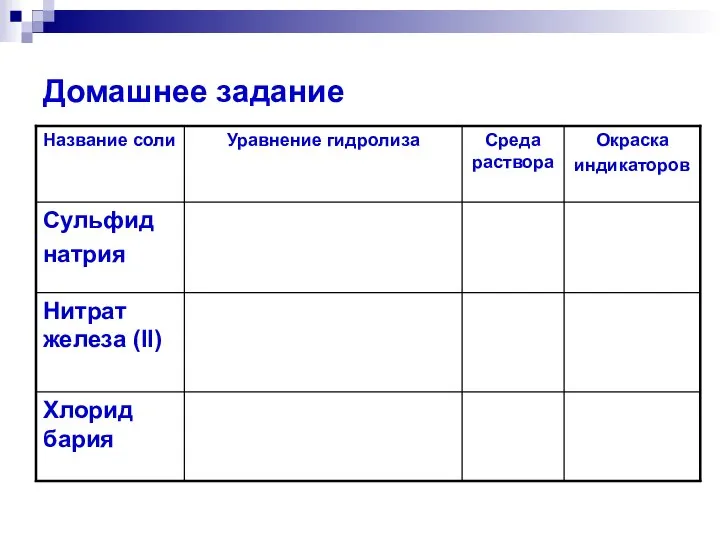
- 24. Домашнее задание
- 25. УЛЫБНИТЕСЬ!!! РАЗМЫШЛЕНИЯ О ГИДРОЛИЗЕ Лёжа дома на диване Про гидролиз думал Ваня. «Сколько в мире, -
- 27. Скачать презентацию
















 Предельные углеводороды. Метан как представитель предельных углеводородов
Предельные углеводороды. Метан как представитель предельных углеводородов Необратимые электродные процессы. Часть 2
Необратимые электродные процессы. Часть 2 Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы
Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы Строение и свойства углеводов и липидов
Строение и свойства углеводов и липидов Сопряжение и ароматичность – энергетический фактор стабилизации молекул биологически активных соединений
Сопряжение и ароматичность – энергетический фактор стабилизации молекул биологически активных соединений Железоуглеродистый сплав чугун
Железоуглеродистый сплав чугун Установление структуры биополимеров
Установление структуры биополимеров Магистры Тема 3б
Магистры Тема 3б Разделение и концентрирование методом осаждения и соосаждения. Различие осаждения и соосаждения. (Лекция 6)
Разделение и концентрирование методом осаждения и соосаждения. Различие осаждения и соосаждения. (Лекция 6) Методы познания химии
Методы познания химии Презентация по Химии "Карбоновые кислоты 9 класс" - скачать смотреть
Презентация по Химии "Карбоновые кислоты 9 класс" - скачать смотреть  Лабораторное оборудование, посуда и средства защиты
Лабораторное оборудование, посуда и средства защиты  Презентация по Химии "Решение задач по химическим уравнениям" - скачать смотреть
Презентация по Химии "Решение задач по химическим уравнениям" - скачать смотреть  Влияние давления на скорость химических реакций с участием газов
Влияние давления на скорость химических реакций с участием газов Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов
Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов Классификация неорганических веществ
Классификация неорганических веществ Ароматические амины
Ароматические амины Органическая химия
Органическая химия Презентация по Химии "Терпены и терпеноиды" - скачать смотреть
Презентация по Химии "Терпены и терпеноиды" - скачать смотреть  Вермикулитовый концентрат
Вермикулитовый концентрат Энергосиловое оборудование промышленных предприятий. Топливо и его виды
Энергосиловое оборудование промышленных предприятий. Топливо и его виды Типы химических реакций. Классификация химических реакций по числу и составу реагентов и продуктов ХР
Типы химических реакций. Классификация химических реакций по числу и составу реагентов и продуктов ХР Ароматические углеводороды. Гомологический ряд, изомерия
Ароматические углеводороды. Гомологический ряд, изомерия Білки. Функції білків в організмі
Білки. Функції білків в організмі Получение водорода
Получение водорода Свойства фосфора
Свойства фосфора Жири. Склад жирів, їх утворення. Жири у природі. Біологічна роль жирів
Жири. Склад жирів, їх утворення. Жири у природі. Біологічна роль жирів МОЛЬ. МОЛЯРНАЯ МАССА.
МОЛЬ. МОЛЯРНАЯ МАССА.