Содержание
- 2. РХТУ АЕК Кн. 1, с. 309-344, 376-385 Вопросы в экзаменационных билетах 1. Биохимические механизмы деградации ксенобиотиков.
- 3. РХТУ АЕК ОСНОВНЫЕ ЭТАПЫ МИКРОБИОЛОГИЧЕСКОЙ ТРАНСФОРМАЦИИ Основные стадии взаимодействия органического ксенобиотика и клетки
- 4. РХТУ АЕК Последовательная трансформация органического ксенобиотика в одно из соединений, вступающего затем в основные (центральные) пути
- 5. РХТУ АЕК Реакции окисления. В аэробных условиях подготовительный метаболизм начинается с реакций включения кислорода (гидроксилирования) в
- 6. РХТУ АЕК Метанмонооксигеназа – у метанокисляющих бактерий CH4 + NADH + H+ +O2 → CH3OH +
- 7. РХТУ АЕК В большинстве случаев субстратами ферментов, катализирующих разрыв бензольного кольца, являются соединения, имеющие как минимум
- 8. РХТУ АЕК Орто- или β-кетоадипатный путь расщепления (Pseudomonas putida и др.)
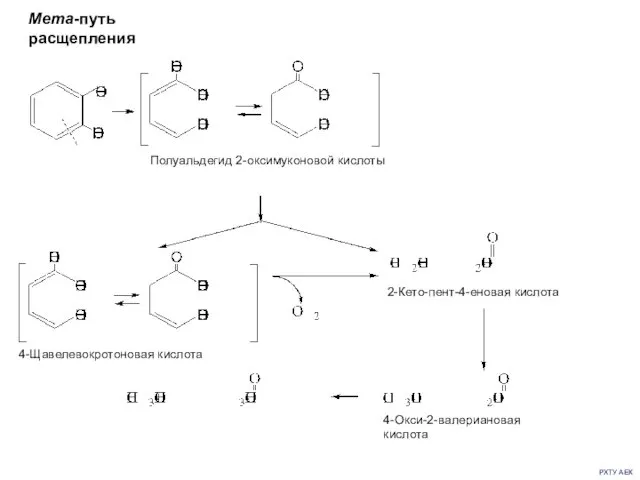
- 9. РХТУ АЕК Мета-путь расщепления
- 10. РХТУ АЕК При мета-расщеплении ароматических колец микроорганизмы, как правило, растут быстрее, чем при орто-расщеплении. Однако мета-расщепление
- 11. РХТУ АЕК Окисление ароматических соединений с небольшими боковыми группами Окисление соединений, содержащих длинные алкильные боковые цепи
- 12. РХТУ АЕК В анаэробных или аноксигенных условиях окисление восстановленных соединений-ксенобиотиков возможно нитратом, оксидами металлов, сульфатами, диоксидом
- 13. РХТУ АЕК Реакции восстановления. Протекают, как правило, в анаэробных условиях. При этом микроорганизмы могут использовать многие
- 14. РХТУ АЕК Реакции деградации. Примеры: гидролиз эфиров, амидов, гидразидов и нитрилов, фосфатных и полифосфатных групп; деалкилирование,
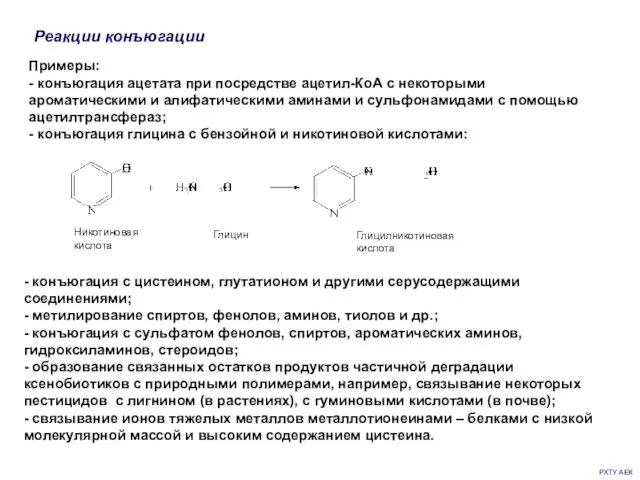
- 15. РХТУ АЕК Реакции конъюгации Примеры: - конъюгация ацетата при посредстве ацетил-КоА с некоторыми ароматическими и алифатическими
- 16. РХТУ АЕК Дегалогенирование Расщепление связи C-Hal: дегалогеназы; спонтанное дегалогенирование нестабильных интермедиатов; ферменты с ослабленной субстратной специфичностью.
- 17. РХТУ АЕК
- 18. РХТУ АЕК
- 19. РХТУ АЕК Чем выше редокс-потенциал, тем труднее вещество поддается окислению и легче восстановлению.
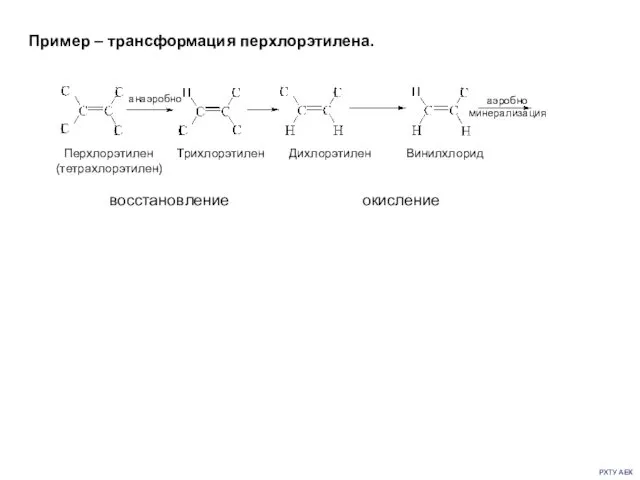
- 20. РХТУ АЕК Пример – трансформация перхлорэтилена. восстановление окисление
- 21. РХТУ АЕК ОСОБЕННОСТИ МИКРООРГАНИЗМОВ – ДЕСТРУКТОРОВ ОРГАНИЧЕСКИХ КСЕНОБИОТИКОВ Ведущая роль – гетеротрофные микроорганизмы, особенно бактерии (р.
- 22. РХТУ АЕК Более легко адаптируются к потреблению субстрата-ксенобиотика: микроорганизмы, у которых отсутствует только один из ферментов
- 23. РХТУ АЕК В зависимости от условий получения необходимой массы микроорганизмов-деструкторов возможны два варианта биоочистки и биоремедиации.
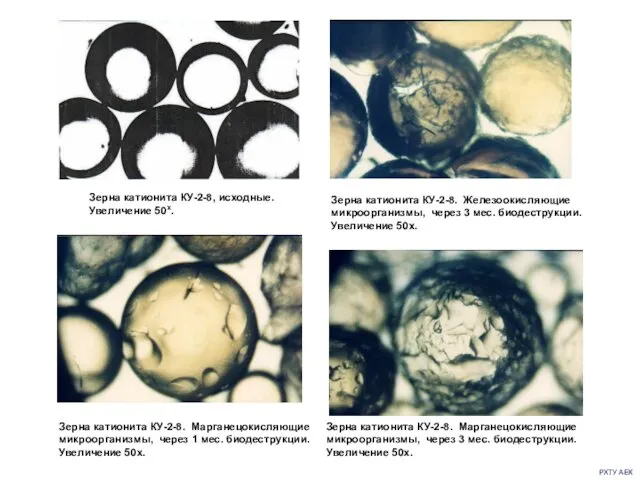
- 24. РХТУ АЕК Зерна катионита КУ-2-8, исходные. Увеличение 50х. Зерна катионита КУ-2-8. Железоокисляющие микроорганизмы, через 3 мес.
- 26. Скачать презентацию



















 Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты
Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты Хром және оның қосылыстары
Хром және оның қосылыстары Металл и ржавчина: взаимодействие и способы защиты
Металл и ржавчина: взаимодействие и способы защиты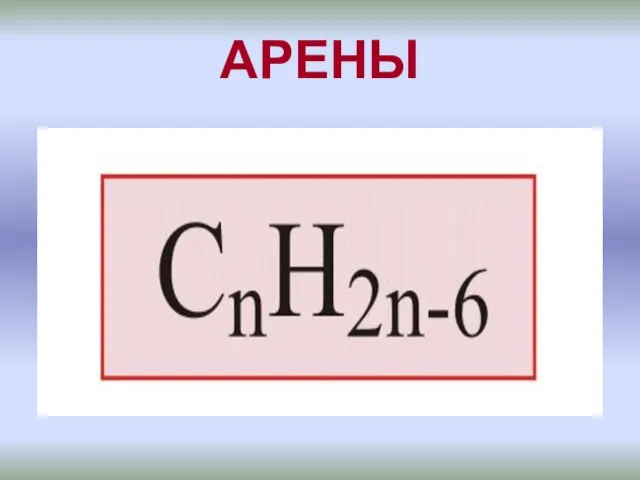 Бензоидные ароматические углеводороды - арены
Бензоидные ароматические углеводороды - арены Диссертация «Анализ и моделирование колебательно-вращательных спектров высокого разрешения молекулы двуокиси азота»
Диссертация «Анализ и моделирование колебательно-вращательных спектров высокого разрешения молекулы двуокиси азота» Отбор проб товаров для анализа. Химико-аналитический контроль
Отбор проб товаров для анализа. Химико-аналитический контроль Аттестационная работа. Задачи на смеси и сплавы
Аттестационная работа. Задачи на смеси и сплавы Способы получения полимеров (Лекция 3)
Способы получения полимеров (Лекция 3) Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений
Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений Сульфиды. Лекция 8
Сульфиды. Лекция 8 The alkali metals
The alkali metals Классификация химических реакций
Классификация химических реакций Оксиды углероды
Оксиды углероды Презентация по химии Применение кислорода
Презентация по химии Применение кислорода Дисперсные системы. Коллоидные растворы
Дисперсные системы. Коллоидные растворы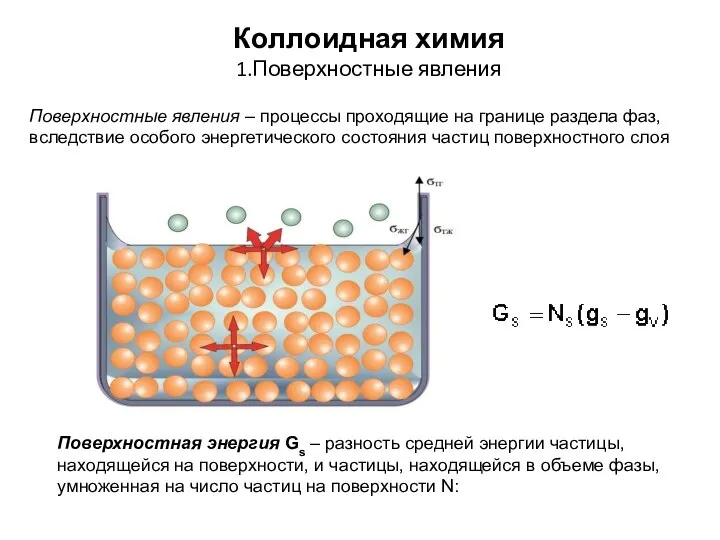 Коллоидная химия. Поверхностные явления
Коллоидная химия. Поверхностные явления Презентация по Химии "Степень окисления" - скачать смотреть
Презентация по Химии "Степень окисления" - скачать смотреть  Состав, строение, классификация кислот
Состав, строение, классификация кислот Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу
Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу Пральні порошки. Мила
Пральні порошки. Мила  Особенности строения, реакционной способности и методы синтеза галогенпроизводных углеводородов
Особенности строения, реакционной способности и методы синтеза галогенпроизводных углеводородов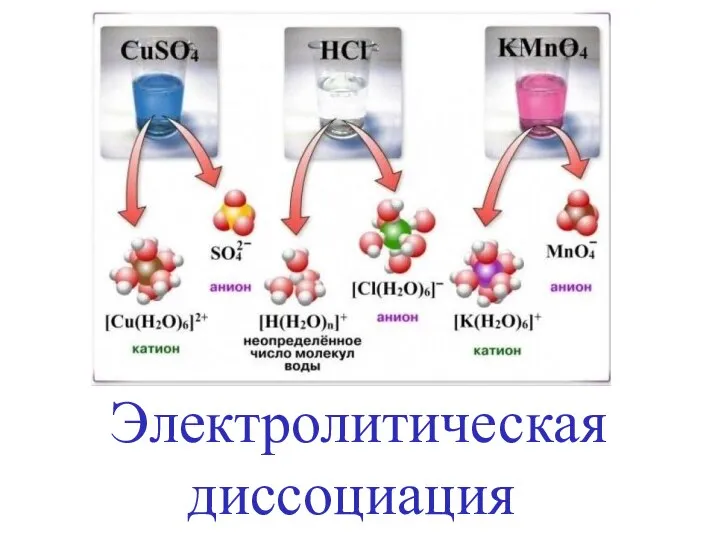 Электролитическая диссоциация
Электролитическая диссоциация Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Окислительно-восстановительные реакции с участием органических веществ
Окислительно-восстановительные реакции с участием органических веществ Ионизирующее излучение и окружающая среда
Ионизирующее излучение и окружающая среда Елементи VІ групи головної підгрупи
Елементи VІ групи головної підгрупи Підготувала учениця 11-А класу Білецька Олеся
Підготувала учениця 11-А класу Білецька Олеся