Содержание
- 2. Гидролиз солей - процесс взаимодействия ионов некоторых солей с водой.
- 3. СОЛЬ (КBr) кислота + основание HBr KOH
- 4. Типы солей Сильная кислота и слабое основание Сильная кислота и сильное основание Слабая кислота и слабое
- 5. Алгоритм составления ионного и молекулярного уравнения гидролиза соли 1. Составляем уравнение электролитической диссоциации соли. 2. Определяем
- 6. З А П О М Н И Т Е ГИДРОЛИЗ – ОБРАТИМЫЙ ПРОЦЕСС
- 7. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону) AlCl3 Al3++3Cl- Al3++ 3CL- + -HO-H+
- 8. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону) Na2CO3 2Na+ + CO32- 2Na+ +
- 9. запомните Гидролиз протекает по «слабому»; Среда определяется «сильным»
- 10. Гидролиз соли сильной кислоты и сильного основания (гидролиз по аниону и катиону) NaCL Na+ + CL-
- 11. Сделайте выводы: Какие соли могут подвергаться гидролизу? Почему они подвергаются гидролизу? Как определить реакцию среды соли?
- 12. Запомните Соли, образованные сильной кислотой и сильным основанием гидролизу не подвергаются
- 14. Скачать презентацию









 Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Новогаленовые. Максимально очищенные экстракционные препараты
Новогаленовые. Максимально очищенные экстракционные препараты Возбудители колибактериоза
Возбудители колибактериоза Кислотно-основные взаимодействия. Принцип ЖМКО Пирсона
Кислотно-основные взаимодействия. Принцип ЖМКО Пирсона Физико-химические свойства жиров
Физико-химические свойства жиров Презентация Дисперсные системы
Презентация Дисперсные системы  Газы, применяемые при сварке
Газы, применяемые при сварке Анализ качества лекарственных и косметических лекарственных средств из группы галогенидов щелочных металлов
Анализ качества лекарственных и косметических лекарственных средств из группы галогенидов щелочных металлов Коррозия металлов
Коррозия металлов Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері
Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері Эндогенная серия. Гидротермальная группа
Эндогенная серия. Гидротермальная группа Масс-спектры спиртов и фенолов
Масс-спектры спиртов и фенолов Газообразные вещества. Парниковый эффект
Газообразные вещества. Парниковый эффект Вплив фосфатної побутової хімії на організм людини.
Вплив фосфатної побутової хімії на організм людини.  Минералы натрия
Минералы натрия Хлориды. Химические свойства
Хлориды. Химические свойства Иондық және ковалентті байланысы бар қосылыстардың электролиттік диссоциациясы
Иондық және ковалентті байланысы бар қосылыстардың электролиттік диссоциациясы Свойства и способы получения аминокислот. Их значение и применение.
Свойства и способы получения аминокислот. Их значение и применение.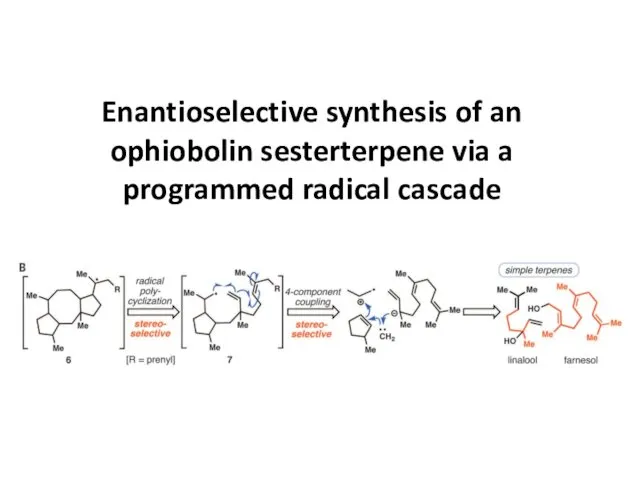 Enantioselective synthesis of an ophiobolin sesterterpene via a programmed radical cascade
Enantioselective synthesis of an ophiobolin sesterterpene via a programmed radical cascade Фильтрационные свойства.Решение уравнений Стокса для несжимаемой жидкости
Фильтрационные свойства.Решение уравнений Стокса для несжимаемой жидкости Некрохмалисті полісахариди
Некрохмалисті полісахариди Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Электронное строение атомов элементов
Электронное строение атомов элементов Природные (натуральные) полимеры. Композиционные материалы
Природные (натуральные) полимеры. Композиционные материалы Химические реакции. Тепловой эффект
Химические реакции. Тепловой эффект Занимательные опыты по химии
Занимательные опыты по химии Очистка масляных фракций от смолистых веществ
Очистка масляных фракций от смолистых веществ Презентация по Химии "Д.И.Менделеев – гордость России" - скачать смотреть
Презентация по Химии "Д.И.Менделеев – гордость России" - скачать смотреть