Содержание
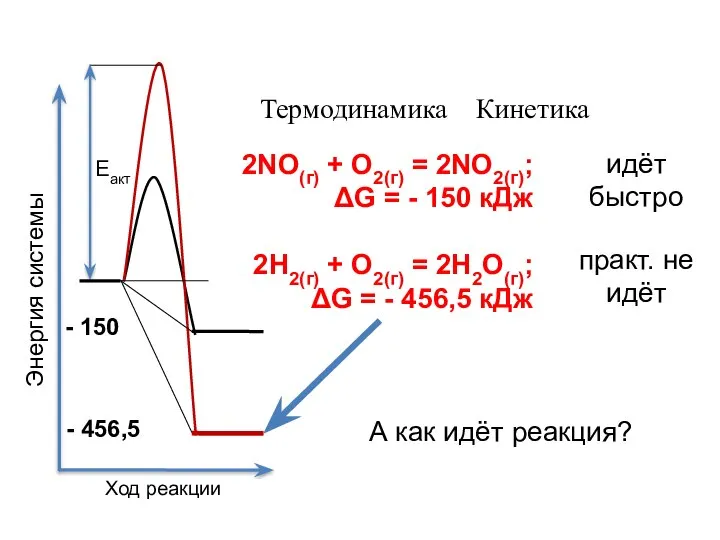
- 2. Еакт 2NO(г) + О2(г) = 2NO2(г); ΔG = - 150 кДж 2Н2(г) + О2(г) = 2Н2О(г);
- 3. Механизм химической реакции - совокупность элементарных стадий, из к-рых складывается хим. реакция Большинство р-ций осуществляется не
- 4. По числу ч-ц или мол-л, участвующих в элем. акте, судят о молекулярности реакции. 2А + В
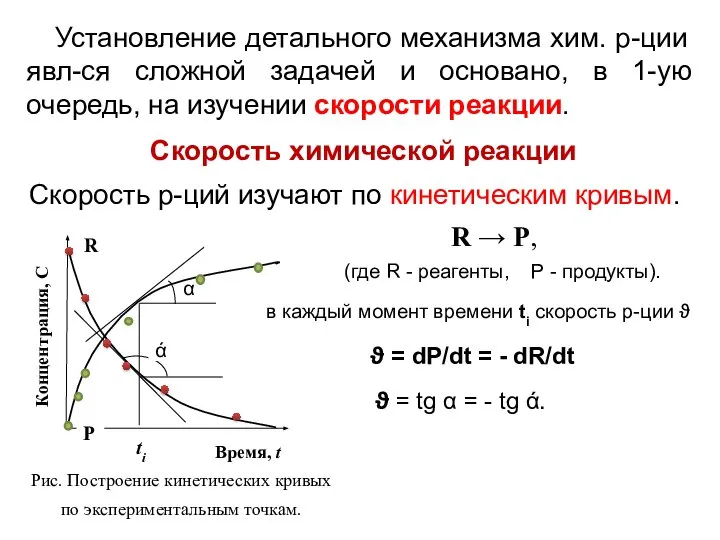
- 5. Установление детального механизма хим. р-ции явл-ся сложной задачей и основано, в 1-ую очередь, на изучении скорости
- 6. при V=Const : где С – конц-ция. Влияние концентрации реагентов. Основной закон кинетики Давно известно, что
- 7. Математически ОЗК даётся в виде кинетическо-го ур-ния р-ции: ϑ = К·[A1]p·[A2]q····[Aℓ]r. К - константа скорости р-ции,
- 8. Для них кинетич. ур-ние р-ции выражает сущность основного постулата хим. кинетики – закона действия (действующих) масс
- 9. 3. если мех-зм простой (одна стадия), то ϑр-ции = К·[A]2·[В] если ϑ1 ϑр-ции = ϑ1 =
- 10. Влияние т-ры. Энергия активации процесса. Впервые количественная зав-сть скорости р-ции от т-ры была дана ≈ в
- 11. В чём причина зависимости? Впервые это сделал Аррениус (1889 г). Суть гипотезы Аррениуса: в эффективном столкновении
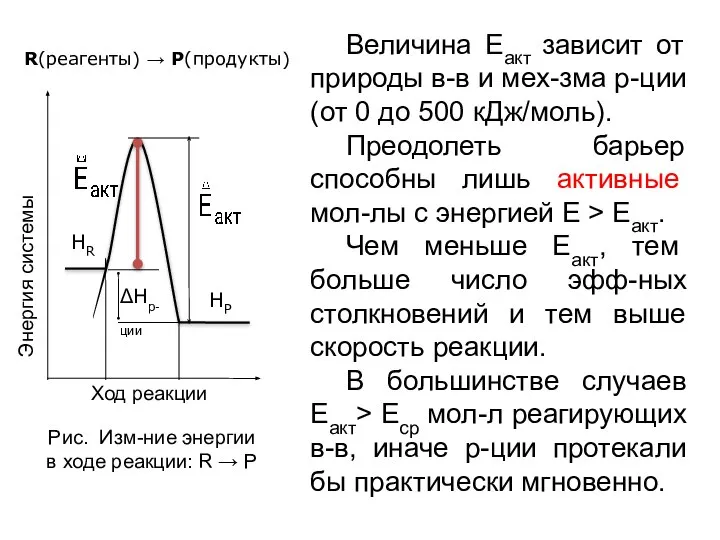
- 12. Величина Еакт зависит от природы в-в и мех-зма р-ции (от 0 до 500 кДж/моль). Преодолеть барьер
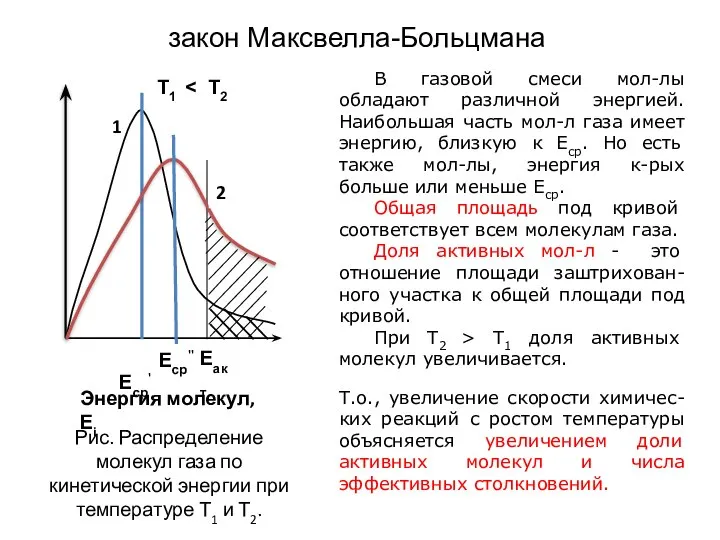
- 13. закон Максвелла-Больцмана В газовой смеси мол-лы обладают различной энергией. Наибольшая часть мол-л газа имеет энергию, близкую
- 15. Влияние катализатора. Понятие о катализе Поскольку кат-р после р-ции остаётся в неизменном состоянии и количестве, то
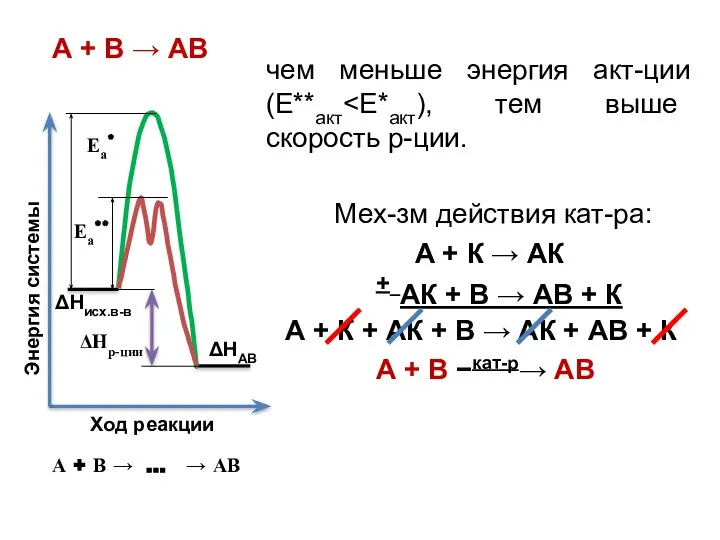
- 16. чем меньше энергия акт-ции (Е**акт А + В → АВ Мех-зм действия кат-ра: А + К
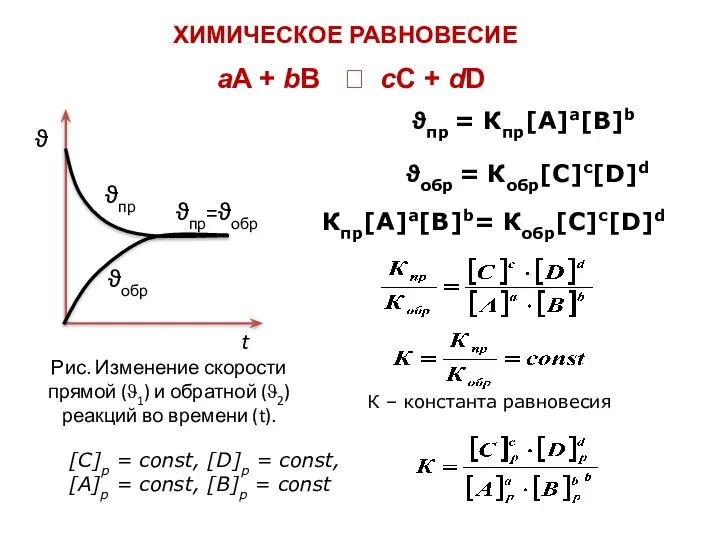
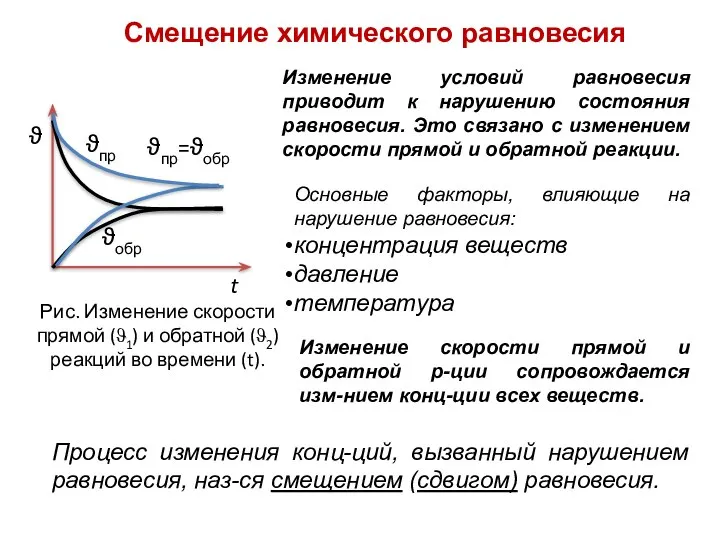
- 17. ϑ ϑпр ϑобр ϑпр=ϑобр t Рис. Изменение скорости прямой (ϑ1) и обратной (ϑ2) реакций во времени
- 18. МОДЕЛЬ ХИМИЧЕСКОГО РАВНОВЕСИЯ
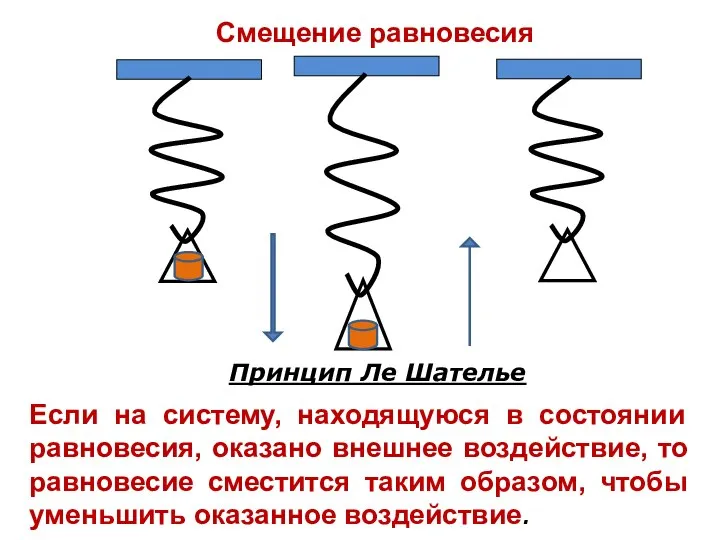
- 19. Смещение равновесия Принцип Ле Шателье Если на систему, находящуюся в состоянии равновесия, оказано внешнее воздействие, то
- 20. Основные факторы, влияющие на нарушение равновесия: концентрация веществ давление температура Процесс изменения конц-ций, вызванный нарушением равновесия,
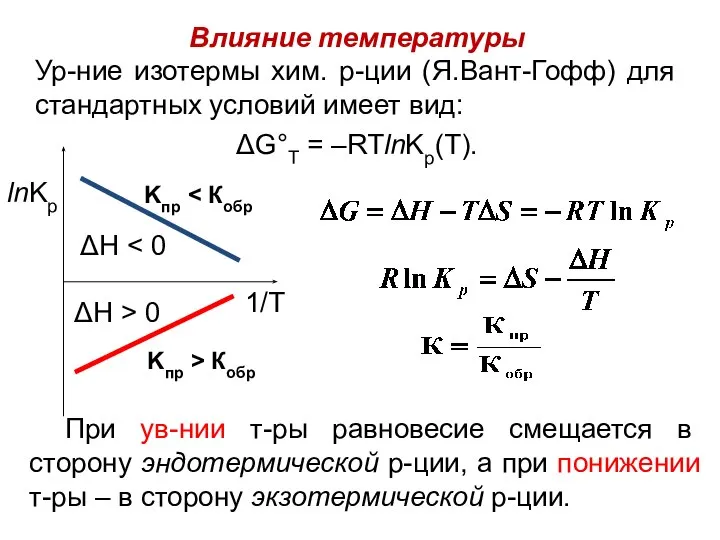
- 21. Влияние температуры Ур-ние изотермы хим. р-ции (Я.Вант-Гофф) для стандартных условий имеет вид: ΔG°Т = –RTlnKp(T). При
- 22. Закономерности сдвига равновесия в химических системах есть частный случай общего принципа поведения равновесных систем. Это принцип
- 24. Скачать презентацию



![Математически ОЗК даётся в виде кинетическо-го ур-ния р-ции: ϑ = К·[A1]p·[A2]q····[Aℓ]r.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/706119/slide-6.jpg)

![3. если мех-зм простой (одна стадия), то ϑр-ции = К·[A]2·[В] если](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/706119/slide-8.jpg)





 Термическая переработка газов, нефтяных фракций и остатков нефтепереработки
Термическая переработка газов, нефтяных фракций и остатков нефтепереработки Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Жирорастворимые витамины. (Лекция 12)
Жирорастворимые витамины. (Лекция 12) Презентация по Химии "Значение химии" - скачать смотреть бесплатно
Презентация по Химии "Значение химии" - скачать смотреть бесплатно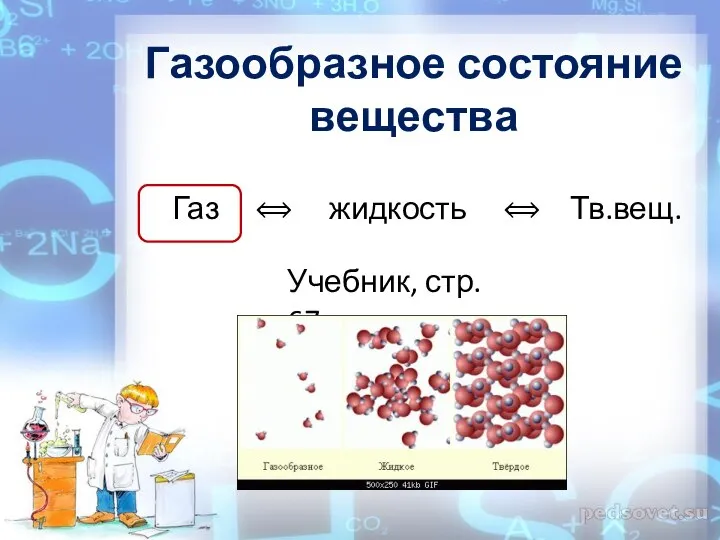 Газообразное состояние вещества
Газообразное состояние вещества Радиофармацевтическая химия
Радиофармацевтическая химия Влияние нанокомпозитов платина/Нафион на электрокаталитическую активность реакции восстановления водорода и окисления кислорода
Влияние нанокомпозитов платина/Нафион на электрокаталитическую активность реакции восстановления водорода и окисления кислорода Периодический закон Д.И. Менделеева. Строение атома
Периодический закон Д.И. Менделеева. Строение атома Крем
Крем  Кристаллические решетки
Кристаллические решетки Растворы. Основные понятия. Концентрация. Законы Рауля
Растворы. Основные понятия. Концентрация. Законы Рауля Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов
Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов Nucleic acids
Nucleic acids Коррозия металла
Коррозия металла Викторина. Химический Элементариум
Викторина. Химический Элементариум Полимеры
Полимеры Химическое сопротивление алюминий и его сплавов
Химическое сопротивление алюминий и его сплавов Непредельные, ненасыщенные, ацетиленовые алкины
Непредельные, ненасыщенные, ацетиленовые алкины Химический элемент медь. (11 класс)
Химический элемент медь. (11 класс) Характеристика липидов. Углеводы. Моносахариды. Дисахариды. Полисахариды
Характеристика липидов. Углеводы. Моносахариды. Дисахариды. Полисахариды Radiation dosimetry
Radiation dosimetry Насыщенные (предельные) углеводороды. Алканы (парафины)
Насыщенные (предельные) углеводороды. Алканы (парафины) Энергетический обмен. Биологическое окисление
Энергетический обмен. Биологическое окисление Титан. Структура, применение, свойства (11 класс)
Титан. Структура, применение, свойства (11 класс) Катализатор Уилкинсона
Катализатор Уилкинсона Окислительно- восстановительные процессы
Окислительно- восстановительные процессы Презентация Щелочные металлы
Презентация Щелочные металлы  Марганец и его свойства
Марганец и его свойства