Содержание
- 2. Химическая связь – совокупность сил, удерживающих два и более атома в многоатомной системе. Ковалентная связь –
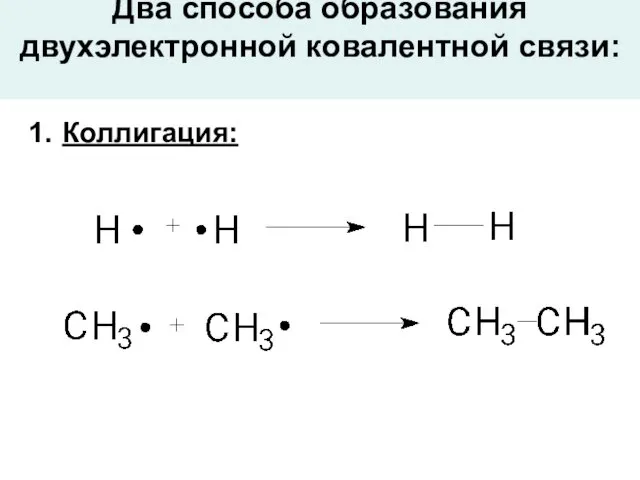
- 3. Два способа образования двухэлектронной ковалентной связи: Коллигация:
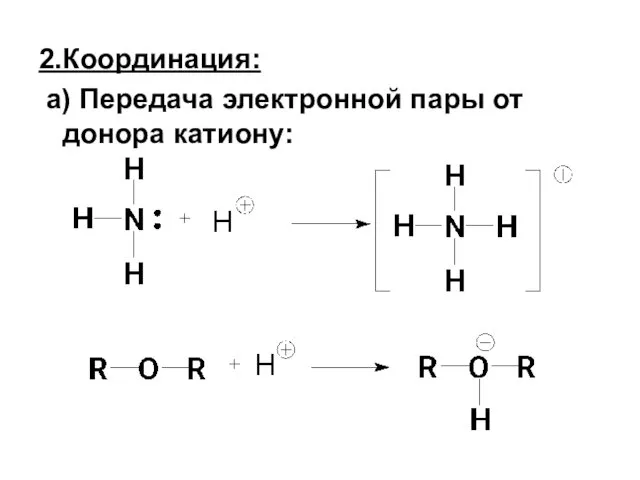
- 4. 2.Координация: а) Передача электронной пары от донора катиону:
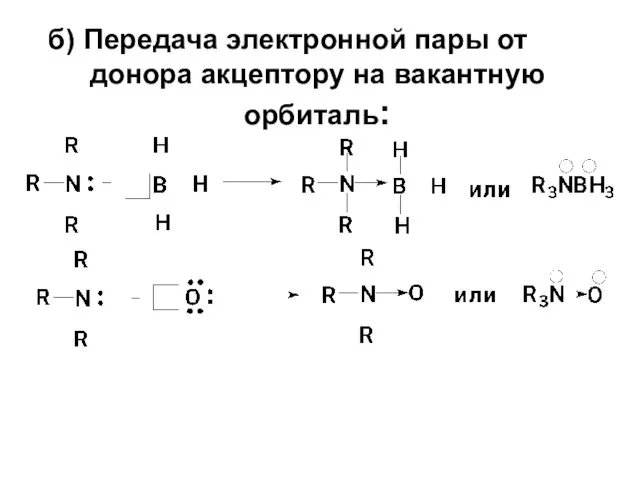
- 5. б) Передача электронной пары от донора акцептору на вакантную орбиталь:
- 6. В основе теории хим. связи лежит волновая теория – квантовая механика. Движение электрона описывается волновой функцией
- 7. оператор Гамильтона. h-постоянная планка. m-масса электрона. r-расстояние между электроном и ядром. E-собственная энергия системы.
- 8. Решение уравнения Шредингера возможно только для простейших систем: для H и H2+. для решения более сложных
- 9. - каждый электрон принадлежит молекуле в целом и движется в поле всех атомных ядер; - каждому
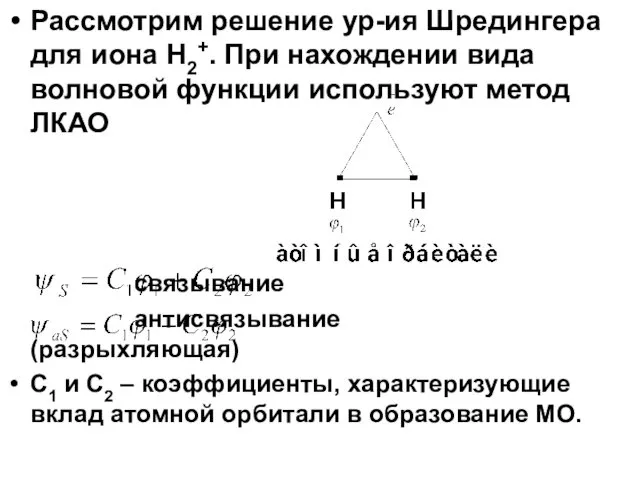
- 10. Рассмотрим решение ур-ия Шредингера для иона H2+. При нахождении вида волновой функции используют метод ЛКАО связывание
- 11. Таким образом, метод МО показывает следующее: Природа сил, обеспечивающих хим. связь носит электрический характер. Движущей силой
- 12. Условия образования МО: Комбинируемые МО близки по энергии. АО, участвующие в образовании МО, должны перекрываться max.
- 13. Классификация МО В зависимости от критерия существует несколько способов классификации: по способу комбинирования АО различают связывающие
- 14. Энергия связывания будет равна: S-интеграл перекрывания S
- 15. Энергия антисвязывания будет равна:
- 16. -кулоновский интеграл, который характеризует кулоновское взаимодействие частиц и включает Е электрона в атоме в основном состоянии,
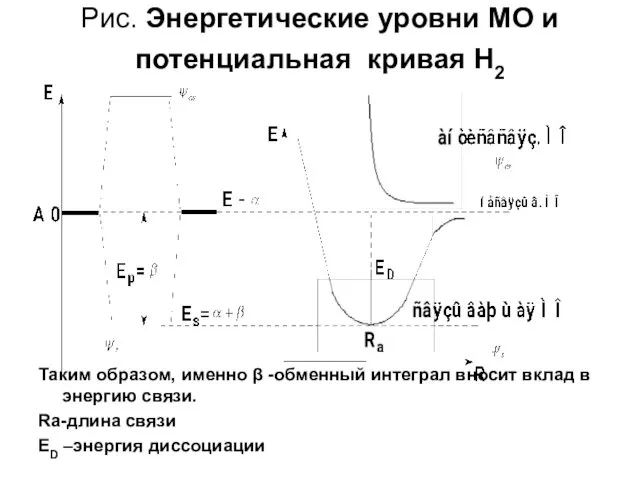
- 17. Рис. Энергетические уровни МО и потенциальная кривая H2 Таким образом, именно β -обменный интеграл вносит вклад
- 18. СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА СВЯЗЫВАЮЩИХ И РАЗРЫХЛЯЮЩИХ МО
- 19. СРАВНИТЕЛЬНАЯ ТАБЛИЦА σ- и π-МО
- 21. Ковалентная связь характеризуется: длиной, энергией, полярностью, поляризуемостью и направленностью ДЛИНА СВЯЗИ – равновесное расстояние между центрами
- 22. ЭНЕРГИЯ СВЯЗИ – энергия, которую необходимо затратить, чтобы разорвать химическую связь ( или выделяется при образовании
- 23. Средняя энергия связи Ес – приближенная усредненная величина, получаемая расчетным путем на основе допущения, что все
- 24. Для оценки стабильности молекулы исп. также: ∆На – теплота образования соединений из атомов. Это сумма энергий
- 25. ∆Нс – теплота сгорания соединения. Чем меньше ∆Нс, тем устойчивее молекула, т.е. меньше тепла выделяется при
- 26. ПОЛЯРНОСТЬ СВЯЗИ – асимметрия распределения электронной плотности между атомами вследствие различия их в электроотрицательности. Шкала электроотрицательности
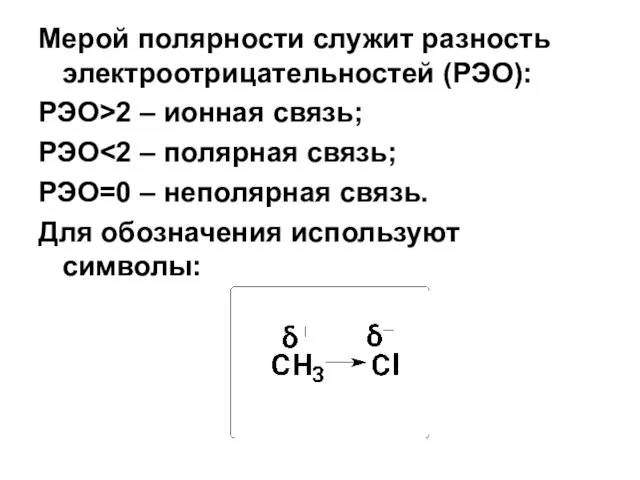
- 27. Мерой полярности служит разность электроотрицательностей (РЭО): РЭО>2 – ионная связь; РЭО РЭО=0 – неполярная связь. Для
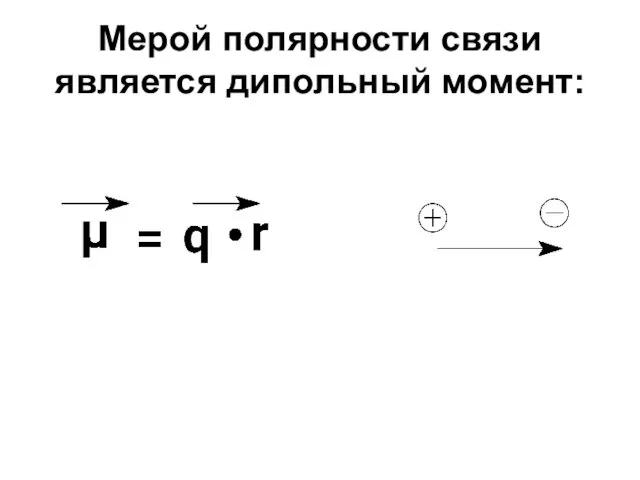
- 28. Мерой полярности связи является дипольный момент:
- 29. ПОЛЯРИЗУЕМОСТЬ – способность изменять свою полярность под действием внешнего поля ( как правило, реагента). Порляризуемость растет
- 30. НАПРАВЛЕННОСТЬ СВЯЗИ определяется гибридным состоянием атома С.
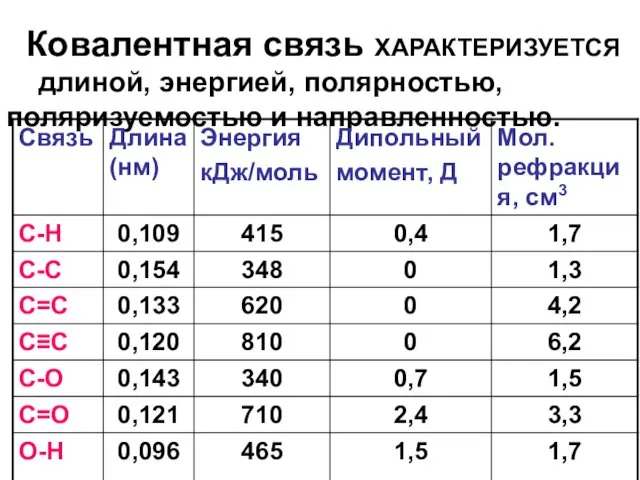
- 31. Ковалентная связь ХАРАКТЕРИЗУЕТСЯ длиной, энергией, полярностью, поляризуемостью и направленностью.
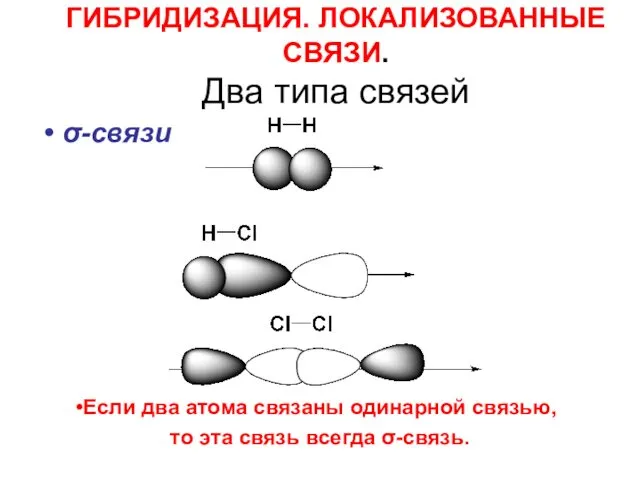
- 32. ГИБРИДИЗАЦИЯ. ЛОКАЛИЗОВАННЫЕ СВЯЗИ. Два типа связей σ-связи Если два атома связаны одинарной связью, то эта связь
- 33. σ - связь это связь, при образовании которой мах. электронная плотность лежит на линии, соединяющей центры
- 34. При образовании кратной связи ( двойной, тройной ) кратность связи повышается за счет π-связывания, то есть
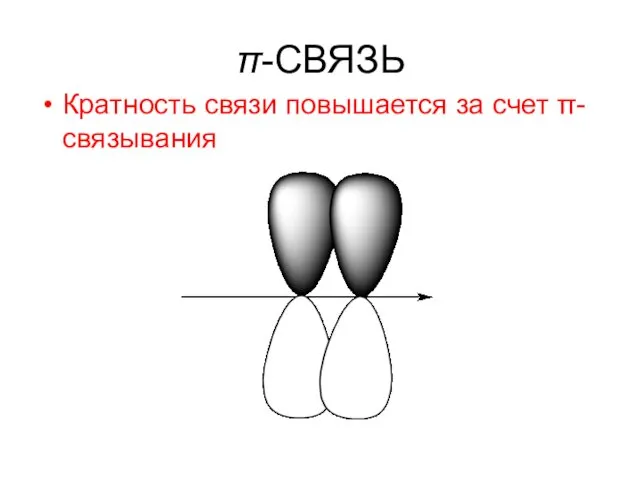
- 35. π-СВЯЗЬ Кратность связи повышается за счет π-связывания
- 36. π - связь - это связь, при образовании которой мах. электронная плотность лежит над и под
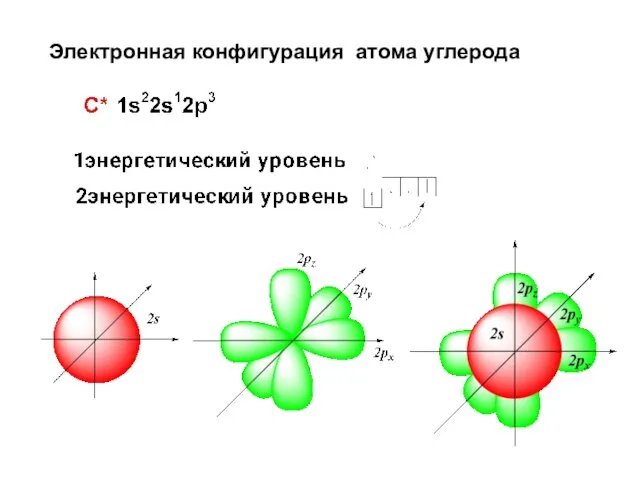
- 37. Электронная конфигурация атома углерода
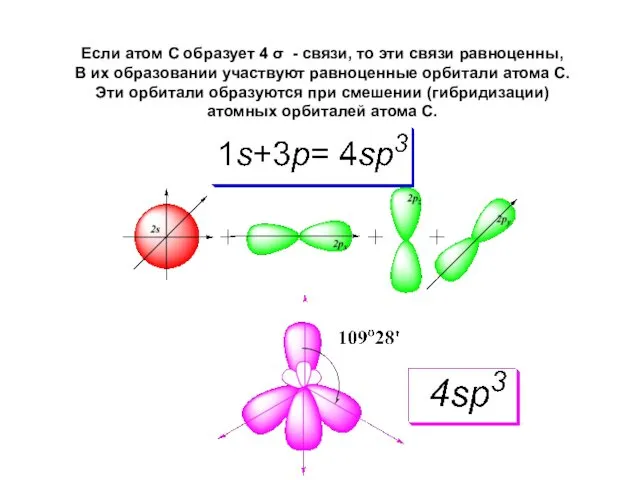
- 38. Если атом С образует 4 σ - связи, то эти связи равноценны, В их образовании участвуют
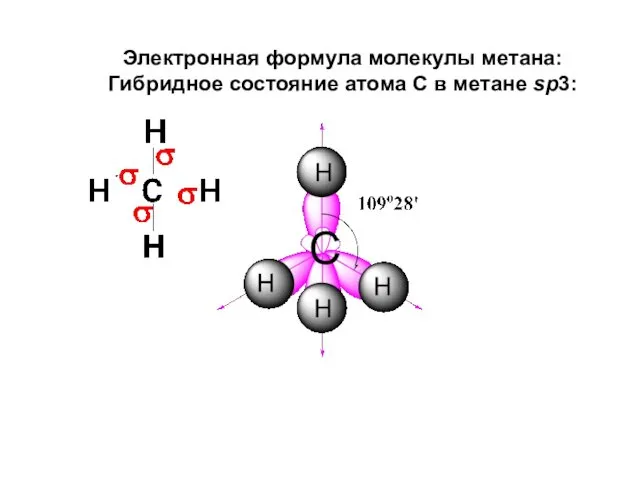
- 39. Электронная формула молекулы метана: Гибридное состояние атома С в метане sp3:
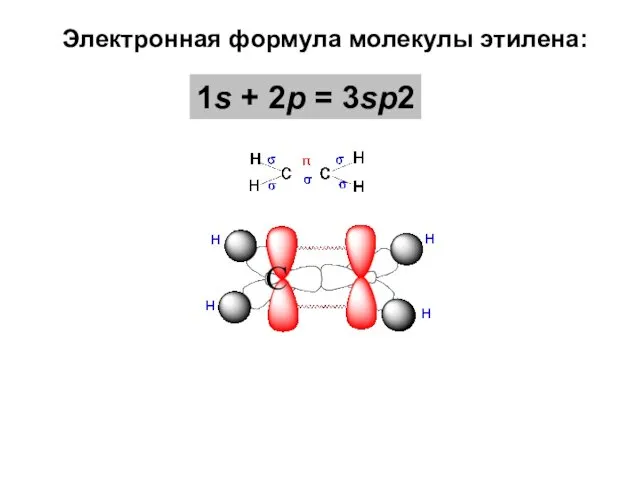
- 41. Электронная формула молекулы этилена: 1s + 2p = 3sp2
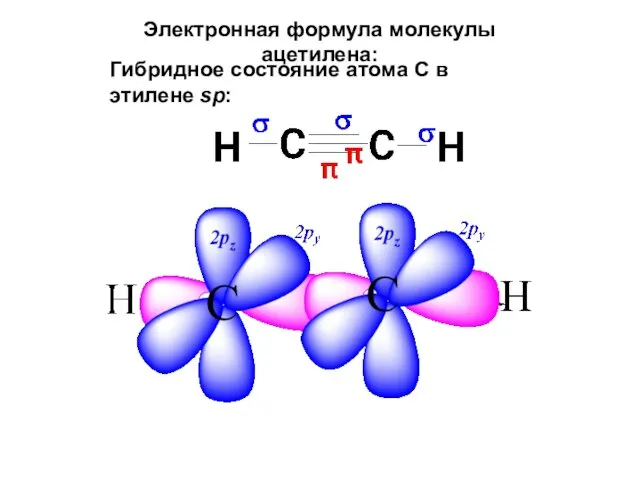
- 43. Электронная формула молекулы ацетилена: Гибридное состояние атома С в этилене sp:
- 44. Электроотрицательность С зависит от его гибридного состояния: sp3 – 2,51 sp2 – 2,59 sp– 2,75
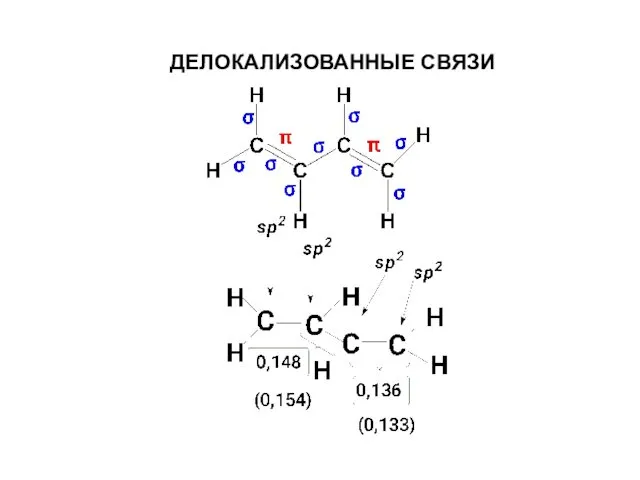
- 45. ДЕЛОКАЛИЗОВАННЫЕ СВЯЗИ
- 46. Отклонение от принципов аддитивности длин и энергий связи ( теплота гидрирования меньше на 3,1 ккал/моль, чем
- 49. Под сопряжением (мезомерией) понимают двустороннее перекрывание электронных облаков π-связей с образованием как бы единого электронного облака,
- 50. Классическая формула не полностью отражает строение бутадиена. Предлагается изображать ее набором валентных схем (мезомерных структур):
- 51. Отклонение от принципов аддитивности у сопряженных систем Зная структурную формулу молекулы можно рассчитать согласно принципу аддитивности
- 52. R C=C расч. R C-C расч. > R C-C эксп. – говорит о перераспределении электронной плотности
- 53. ЭЛЕКТРОННЫЕ ЭФФЕКТЫ (СМЕЩЕНИЯ) В ОРГАНИЧЕСКИХ МОЛЕКУЛАХ Индуктивный (или индукционный) эффект I-эффект – обусловлен асимметрией распределения электронного
- 54. I-эффект быстро затухает по цепи σ - связей. I-эффект может быть +I-эффект и -I-эффект. -I-эффект: а)
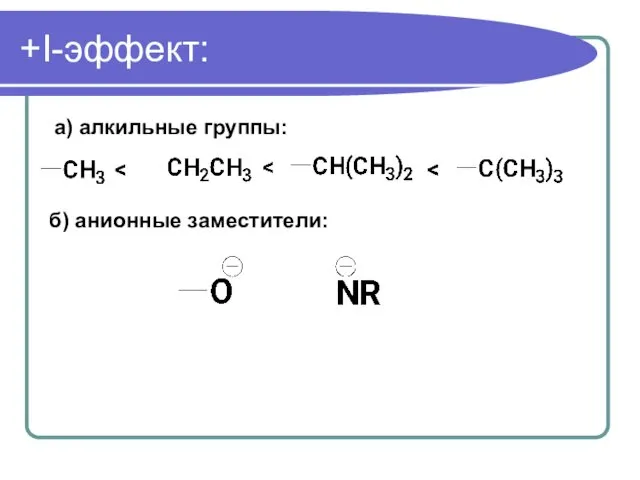
- 55. +I-эффект: а) алкильные группы: б) анионные заместители:
- 56. Мезомерный эффект (М-эффект) –электронные смещения по системе полярных делокализованных π-связей. Изображение:
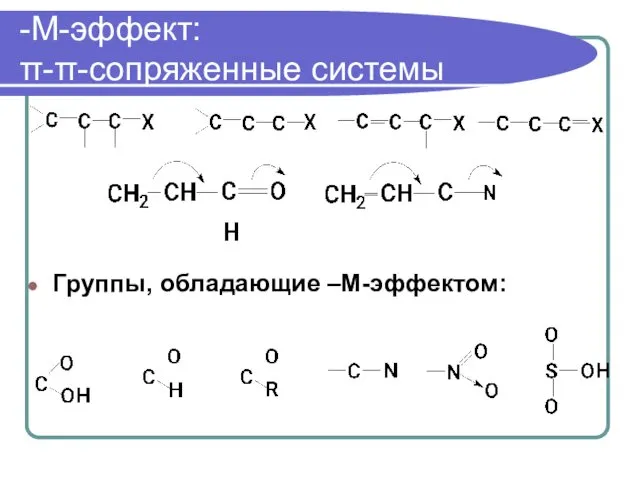
- 57. -М-эффект: π-π-сопряженные системы Группы, обладающие –М-эффектом:
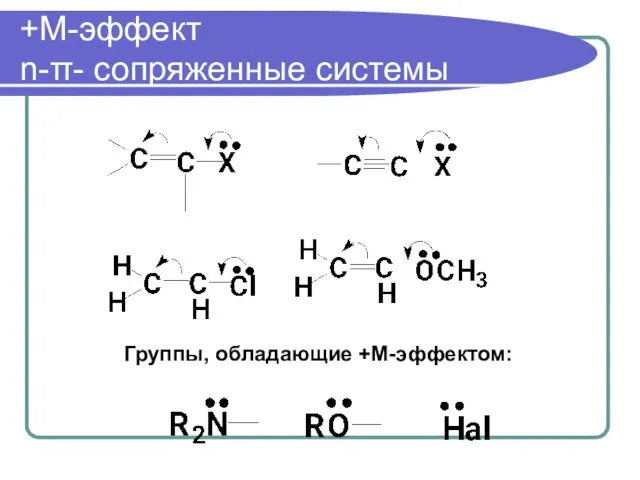
- 58. +М-эффект n-π- сопряженные системы Группы, обладающие +М-эффектом:
- 60. Скачать презентацию






































 Презентация по химии Галогены в организме человека
Презентация по химии Галогены в организме человека Определение крахмала в продуктах
Определение крахмала в продуктах Химия 8 класс
Химия 8 класс  Витамины алифатического ряда, пангамовая и пантотеновая кислоты. Витамины алициклического ряда, витамины А и D. (Тема 3)
Витамины алифатического ряда, пангамовая и пантотеновая кислоты. Витамины алициклического ряда, витамины А и D. (Тема 3) Производство стекла
Производство стекла Неорганическая химия. Соединение химических элементов
Неорганическая химия. Соединение химических элементов Методы экстрагирования ЛРС и оборудование
Методы экстрагирования ЛРС и оборудование Вакуумное фильтрование
Вакуумное фильтрование Газохроматографический анализ летучих ядов
Газохроматографический анализ летучих ядов Классификации ПАВ
Классификации ПАВ Металлы и сплавы с высокой удельной прочностью
Металлы и сплавы с высокой удельной прочностью Коды Менделеева
Коды Менделеева Спін-спінова взаємодія в спектрах ямр
Спін-спінова взаємодія в спектрах ямр Химическая посуда и ее назначения (5)
Химическая посуда и ее назначения (5) Волшебница вода
Волшебница вода Colligative properties of solutions
Colligative properties of solutions Степень диссоциации. 9 класс
Степень диссоциации. 9 класс Презентация по химии Эпоха теории флогистона Пневматическая химия Развитие аналитической химии
Презентация по химии Эпоха теории флогистона Пневматическая химия Развитие аналитической химии  Matter - Its Properties and Measurement
Matter - Its Properties and Measurement Натрия и калия иодиды. Йод, раствор иода спиртовый 5%
Натрия и калия иодиды. Йод, раствор иода спиртовый 5% Тест для подготовки к ЕГЭ по химии 2017
Тест для подготовки к ЕГЭ по химии 2017 Шунгит: минерал, творящий чудеса МОУ «Осташевская СОШ»
Шунгит: минерал, творящий чудеса МОУ «Осташевская СОШ» Основы химической кинетики и химическое равновесие (лекция 5)
Основы химической кинетики и химическое равновесие (лекция 5) Қатты күйдегі препараттар
Қатты күйдегі препараттар Олимпиада по фармацевтической химии. Своя игра
Олимпиада по фармацевтической химии. Своя игра Mohs scale of mineral hardness
Mohs scale of mineral hardness Алкандар. (қаныққан көмірсутектер. Парафиндер.)
Алкандар. (қаныққан көмірсутектер. Парафиндер.) Основания. Классификация оснований
Основания. Классификация оснований