Содержание
- 3. Малополярные связи C-H в алканах относительно легко подвергаются гомолитическому разрыву по механизму радикального замещения (галогенирования, нитрования.
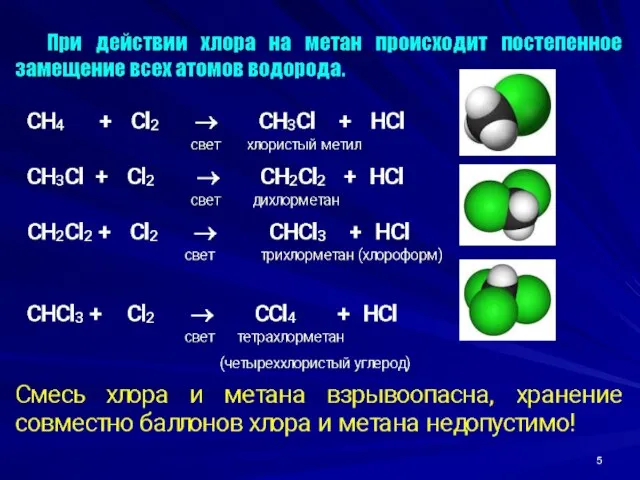
- 6. В.В. Марковников установил, что после замещения одного атома водорода хлором облегчается замещение оставшихся водородных атомов. Обычно
- 7. Галогеналканы очень хорошо растворяют жиры и масла, и являются фреонами (хладагентами). Легко сжижаемые смешанные галогеналканы (CCl3F,
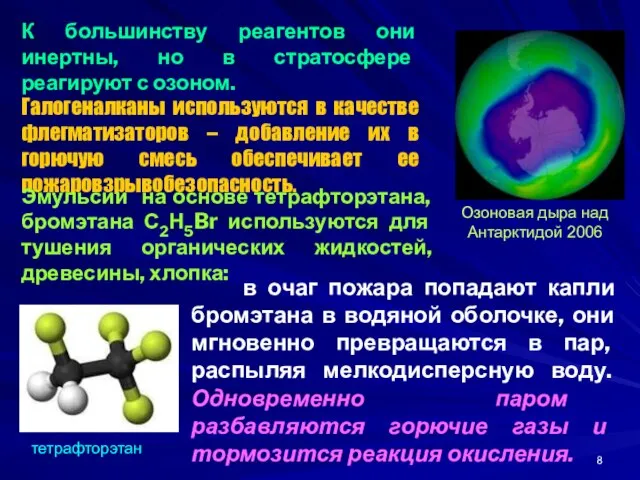
- 8. в очаг пожара попадают капли бромэтана в водяной оболочке, они мгновенно превращаются в пар, распыляя мелкодисперсную
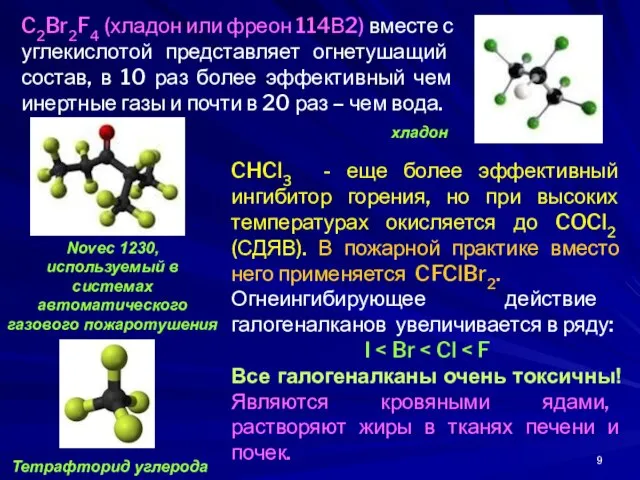
- 9. CHCl3 - еще более эффективный ингибитор горения, но при высоких температурах окисляется до COCl2 (СДЯВ). В
- 11. Реакция нитрования протекает по радикальному механизму. Ее инициатором является двуокись азота с неспаренным электроном, образующаяся при
- 13. Нитроалканы – высококипящие, плохо растворимые в воде, легко воспламеняемые и взрывоопасные жидкости. Способны к взрывному горению
- 15. Как и при нитровании, в случае сульфирования водородные атомы у вторичных и третичных атомов углерода замещаются
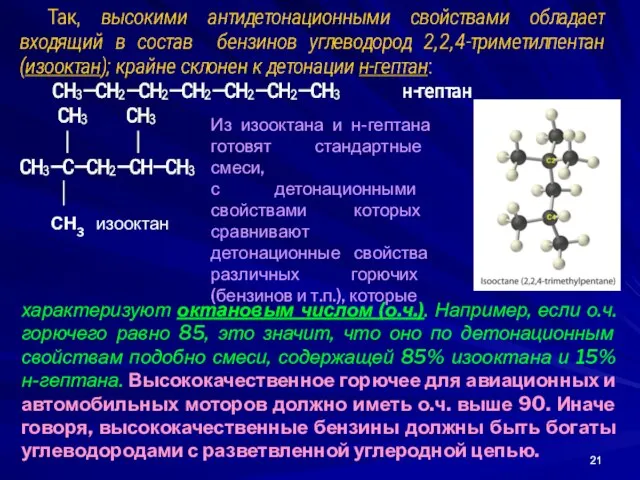
- 21. Из изооктана и н-гептана готовят стандартные смеси, с детонационными свойствами которых сравнивают детонационные свойства различных горючих
- 32. Было выдвинуто много теорий, объясняющих происхождение нефти. Из них основными являются: неорганическая, космическая и органическая. Согласно
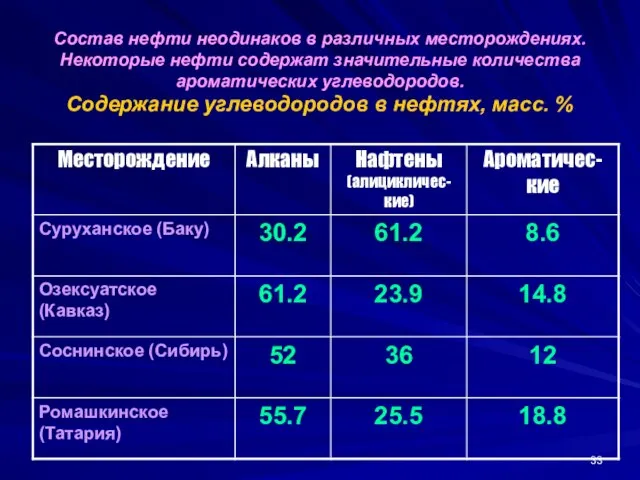
- 33. Состав нефти неодинаков в различных месторождениях. Некоторые нефти содержат значительные количества ароматических углеводородов. Содержание углеводородов в
- 34. Путем перегонки из нефти получают продукты различного назначения. Главный способ переработки нефти – фракционирование (перегонка), при
- 35. При окислении хорошо очищенного парафина воздухом в присутствии катализаторов образуются карбоновые кислоты, применяемые в мыловарении как
- 39. Скачать презентацию































 Аттестационная работа. Повышение квалификации учителей химии и биологии в организации проектно-исследовательской деятельности
Аттестационная работа. Повышение квалификации учителей химии и биологии в организации проектно-исследовательской деятельности Изготовление индикаторной бумаги
Изготовление индикаторной бумаги Органічні сполуки і здоров’я людини. Жири, білки, вуглеводи, як компоненти їжі Виконали учні 7-А (г.) класу ЛНВК ім. В. Симоненка
Органічні сполуки і здоров’я людини. Жири, білки, вуглеводи, як компоненти їжі Виконали учні 7-А (г.) класу ЛНВК ім. В. Симоненка Презентація уроку «Чисті речовини і суміші. Основні способи розділення сумішей» Підготувала: учитель хімії вищої категорії Хри
Презентація уроку «Чисті речовини і суміші. Основні способи розділення сумішей» Підготувала: учитель хімії вищої категорії Хри Штучні волокна Підготували учениці 7(11) – А класу Єзерська В., Крамарук М.
Штучні волокна Підготували учениці 7(11) – А класу Єзерська В., Крамарук М.  Презентация по Химии "Таблица Периодическая система химических элементов Д.И. Менделеева" - скачать смотреть
Презентация по Химии "Таблица Периодическая система химических элементов Д.И. Менделеева" - скачать смотреть  Чистые вещества и смеси. Способы разделения смесей. 8 класс
Чистые вещества и смеси. Способы разделения смесей. 8 класс Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості Оксид металлов
Оксид металлов Презентация по химии Удобрения и их классификация
Презентация по химии Удобрения и их классификация Ароматты галогентуындылар. Айырылу-қосылу және қосылу айырылу реакциясының механизмі
Ароматты галогентуындылар. Айырылу-қосылу және қосылу айырылу реакциясының механизмі Химические элементы и организм человека
Химические элементы и организм человека Теплота сгорания топлива
Теплота сгорания топлива Готовимся к контрольной работе по химии
Готовимся к контрольной работе по химии Аттестационная работа. Элективный курс Химия в доме
Аттестационная работа. Элективный курс Химия в доме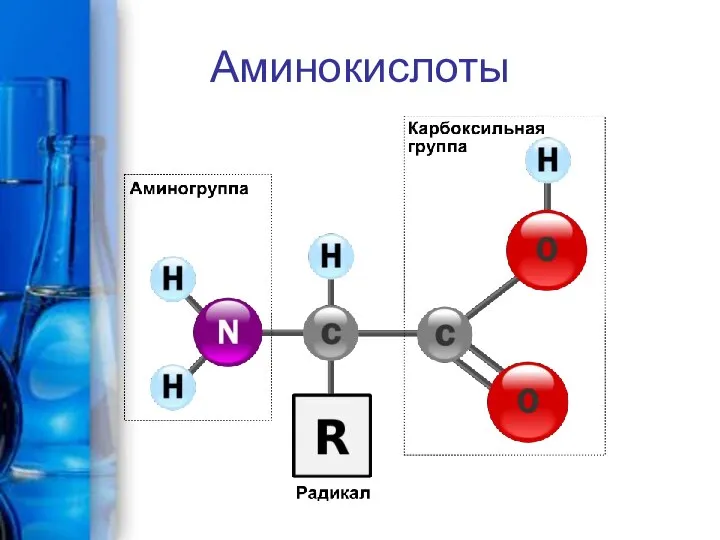 Аминокислоты и белки
Аминокислоты и белки Химический состав клетки
Химический состав клетки Органика – 4 галогенпроизводные
Органика – 4 галогенпроизводные Необычные минералы
Необычные минералы ПОДГОТОВКА К КОНТРОЛЬНОЙ РАБОТЕ ПО ТЕМЕ « Углеводороды» 10 класс. Автор: Ким Н.В. Учитель химии МБОУ «СОШ № 6» г.Нягань ХМАО-Югры
ПОДГОТОВКА К КОНТРОЛЬНОЙ РАБОТЕ ПО ТЕМЕ « Углеводороды» 10 класс. Автор: Ким Н.В. Учитель химии МБОУ «СОШ № 6» г.Нягань ХМАО-Югры Медико-биологическое значение соединений алюминия
Медико-биологическое значение соединений алюминия Игра-квест на уроке химии
Игра-квест на уроке химии Адсорбционные явления. Общая характеристика адсорбции
Адсорбционные явления. Общая характеристика адсорбции Crystal Defects and Noncrystalline Structure–Imperfection
Crystal Defects and Noncrystalline Structure–Imperfection Водород. Получение и свойства водорода
Водород. Получение и свойства водорода Введение. Классификация минеральных удобрений
Введение. Классификация минеральных удобрений Сера
Сера Самоорганизация на межфазных границах, метод Ленгмюра-Блоджетт. Объекты исследования коллоидной химии
Самоорганизация на межфазных границах, метод Ленгмюра-Блоджетт. Объекты исследования коллоидной химии