Содержание
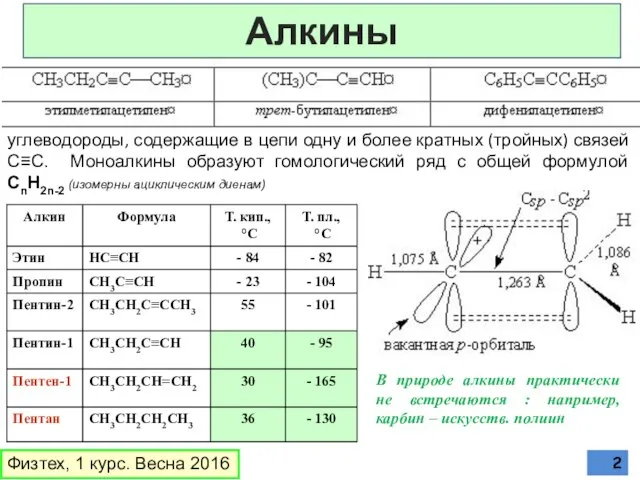
- 2. Алкины Физтех, 1 курс. Весна 2016 углеводороды, содержащие в цепи одну и более кратных (тройных) связей
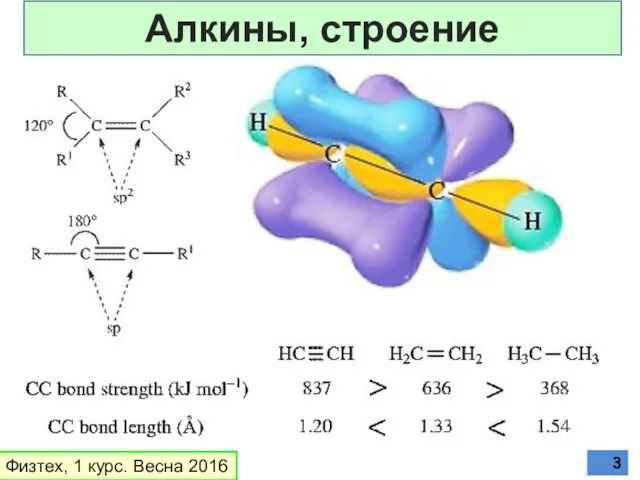
- 3. Физтех, 1 курс. Весна 2016 Алкины, строение
- 4. Факторы, ответственные за меньшую активность алкинов ВЗМО алкина располагается ниже, чем ВЗМО алкена Физтех, 1 курс.
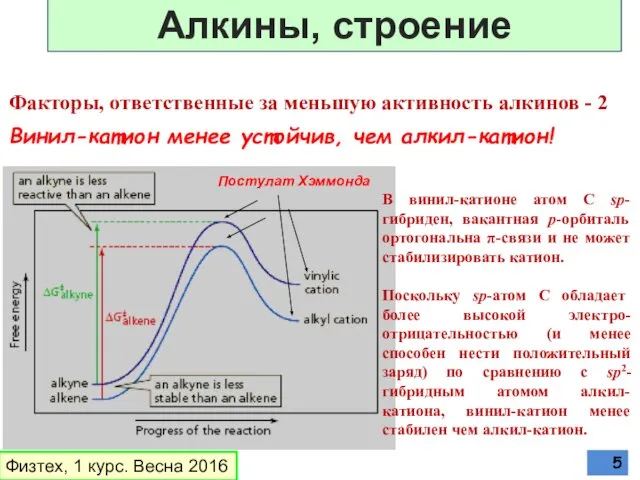
- 5. В винил-катионе атом С sp-гибриден, вакантная р-орбиталь ортогональна π-связи и не может стабилизировать катион. Поскольку sp-атом
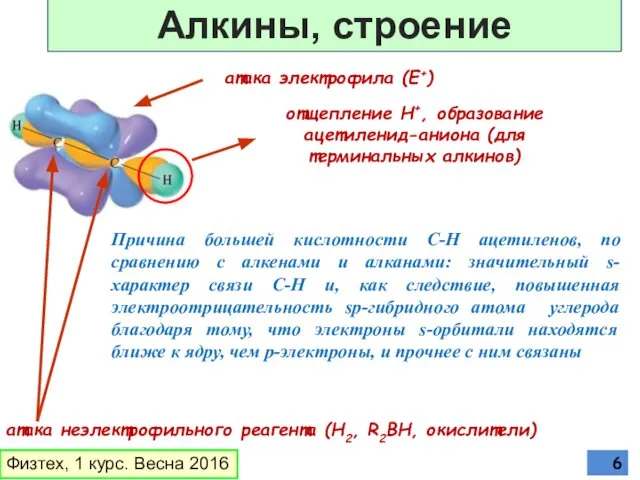
- 6. атака электрофила (E+) отщепление Н+, образование ацетиленид-аниона (для терминальных алкинов) атака неэлектрофильного реагента (Н2, R2BH, окислители)
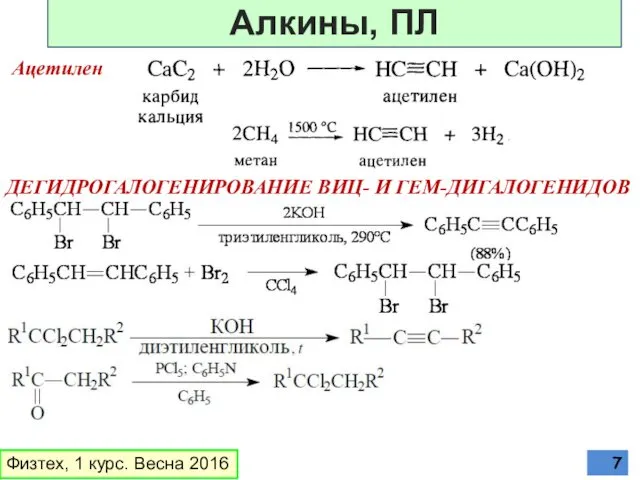
- 7. ДЕГИДРОГАЛОГЕНИРОВАНИЕ ВИЦ- И ГЕМ-ДИГАЛОГЕНИДОВ Ацетилен Физтех, 1 курс. Весна 2016 Алкины, ПЛ
- 8. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ К АЛКИНАМ Как следует из опыта химии алкенов, повышение электронной плотности в области двойной
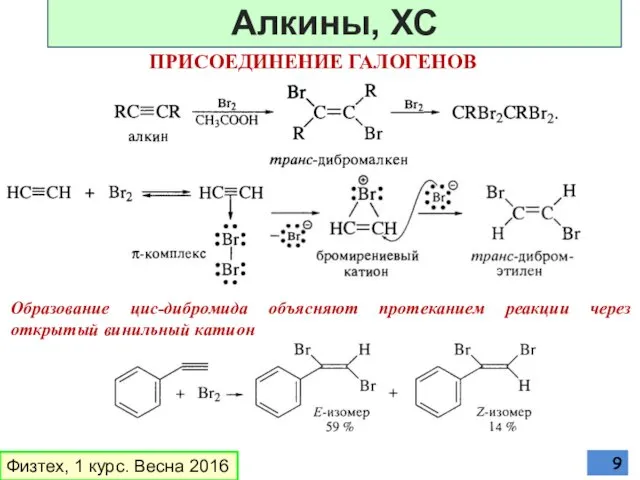
- 9. ПРИСОЕДИНЕНИЕ ГАЛОГЕНОВ Образование цис-дибромида объясняют протеканием реакции через открытый винильный катион Физтех, 1 курс. Весна 2016
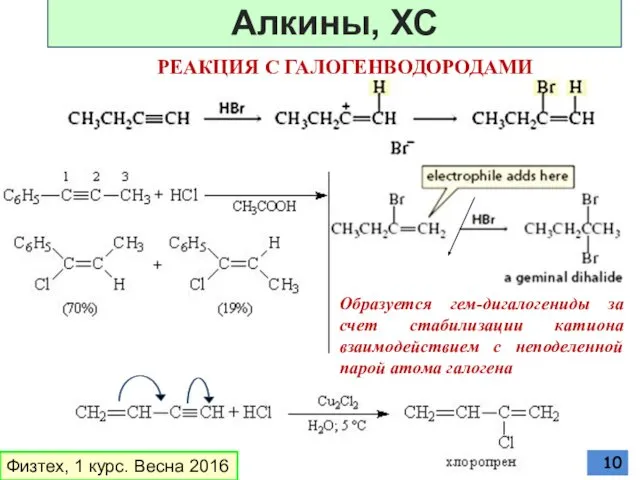
- 10. РЕАКЦИЯ С ГАЛОГЕНВОДОРОДАМИ Образуется гем-дигалогениды за счет стабилизации катиона взаимодействием с неподеленной парой атома галогена Физтех,
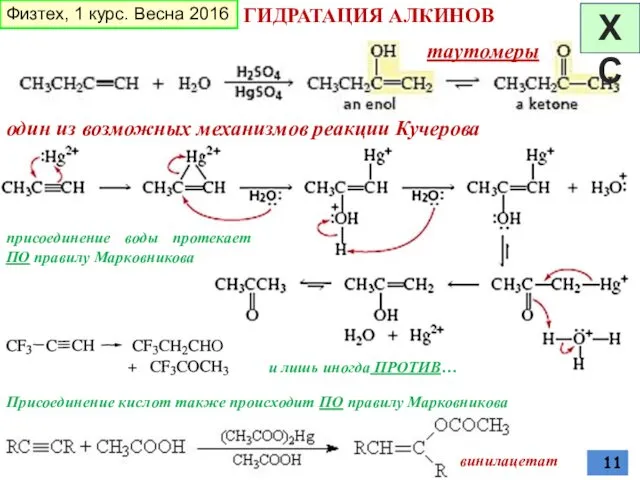
- 11. ГИДРАТАЦИЯ АЛКИНОВ один из возможных механизмов реакции Кучерова таутомеры присоединение воды протекает ПО правилу Марковникова Присоединение
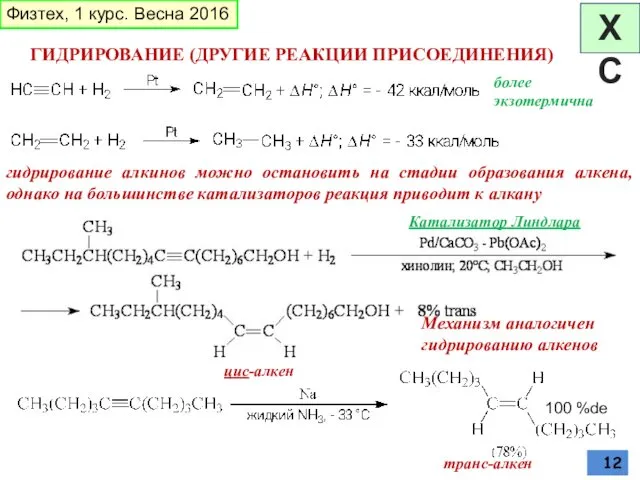
- 12. ГИДРИРОВАНИЕ (ДРУГИЕ РЕАКЦИИ ПРИСОЕДИНЕНИЯ) более экзотермична гидрирование алкинов можно остановить на стадии образования алкена, однако на
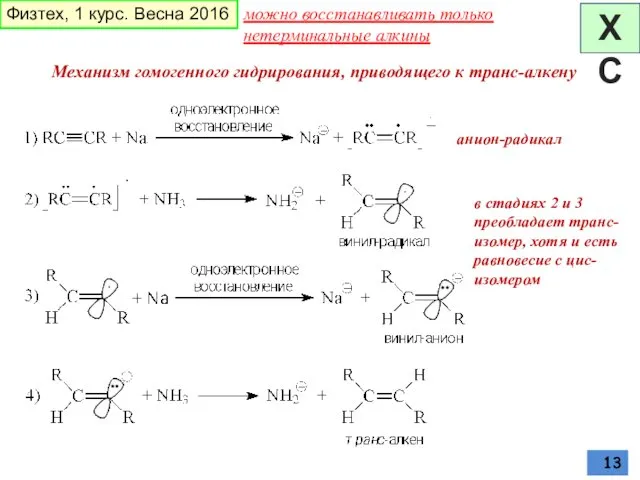
- 13. в стадиях 2 и 3 преобладает транс-изомер, хотя и есть равновесие с цис-изомером анион-радикал Механизм гомогенного
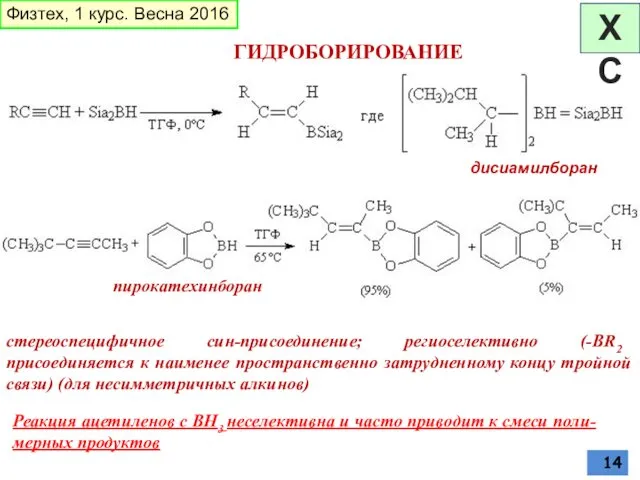
- 14. ГИДРОБОРИРОВАНИЕ дисиамилборан Реакция ацетиленов с BH3 неселективна и часто приводит к смеси поли-мерных продуктов стереоспецифичное син-присоединение;
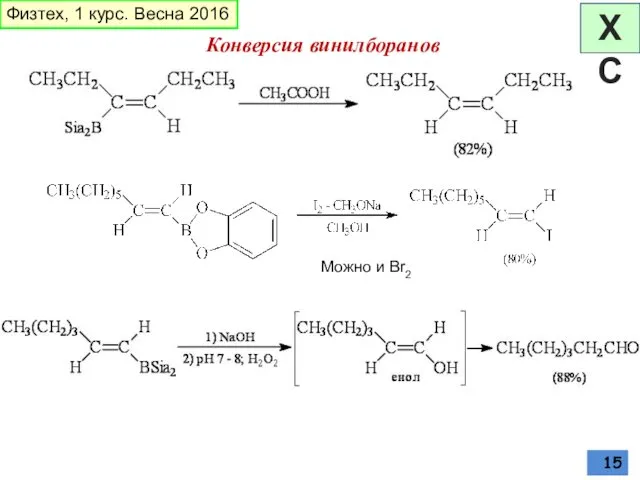
- 15. Можно и Br2 Конверсия винилборанов Физтех, 1 курс. Весна 2016 ХС
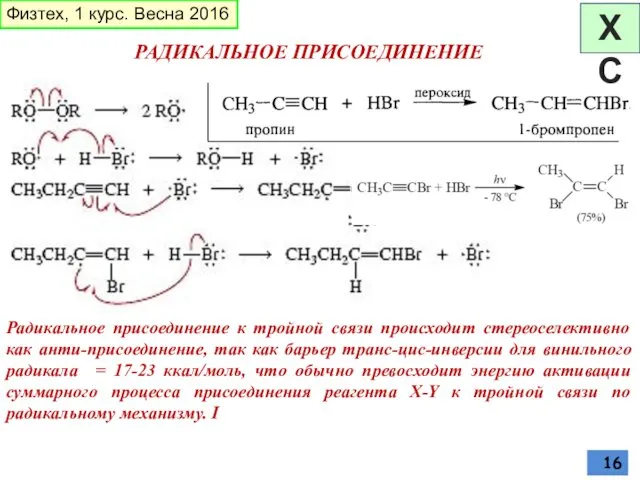
- 16. РАДИКАЛЬНОЕ ПРИСОЕДИНЕНИЕ Радикальное присоединение к тройной связи происходит стереоселективно как анти-присоединение, так как барьер транс-цис-инверсии для
- 17. НУКЛЕОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ атака цианид-ионом Уровень НСМО в алкинах ниже чем в алкенах; винильный анион более стабилен,
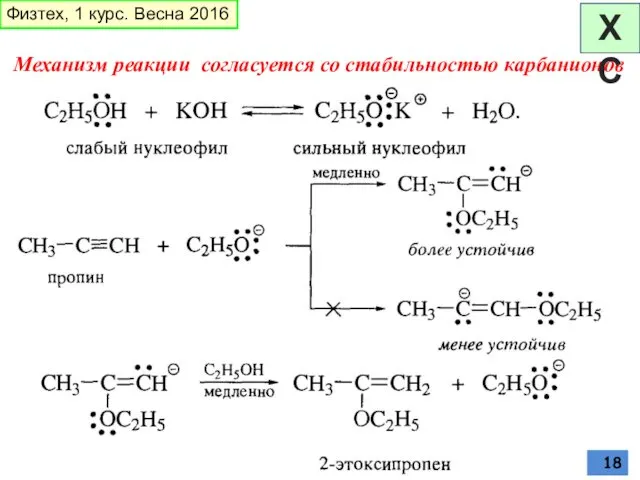
- 18. Механизм реакции согласуется со стабильностью карбанионов Физтех, 1 курс. Весна 2016 ХС
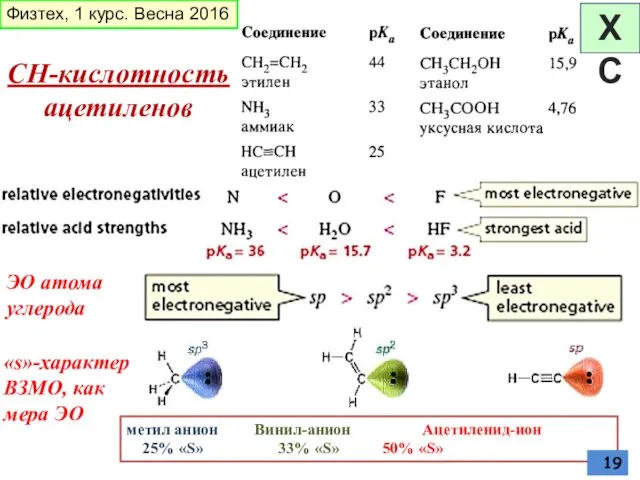
- 19. СН-кислотность ацетиленов ЭО атома углерода Физтех, 1 курс. Весна 2016 «s»-характер ВЗМО, как мера ЭО метил
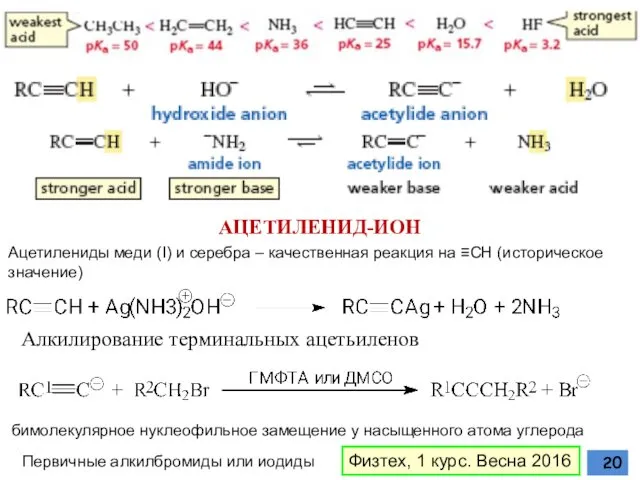
- 20. АЦЕТИЛЕНИД-ИОН бимолекулярное нуклеофильное замещение у насыщенного атома углерода Первичные алкилбромиды или иодиды Ацетилениды меди (I) и
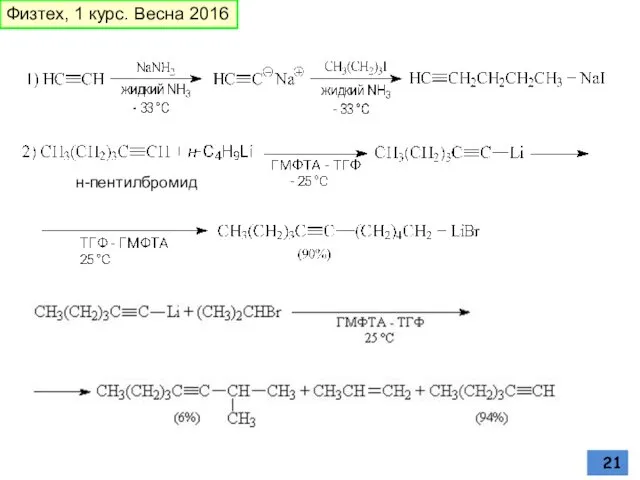
- 21. н-пентилбромид Физтех, 1 курс. Весна 2016
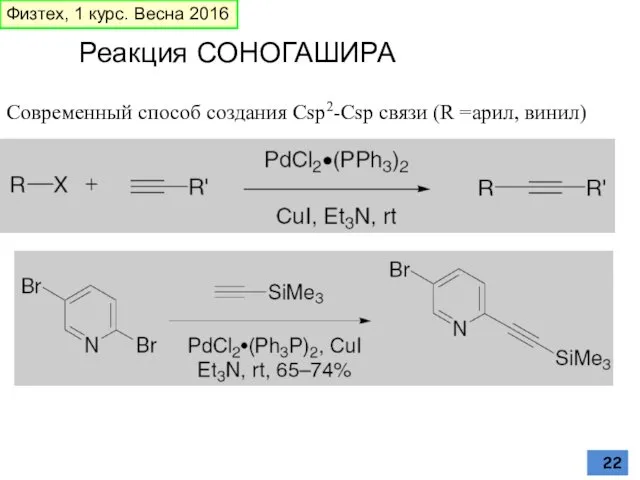
- 22. Реакция СОНОГАШИРА Современный способ создания Csp2-Csp связи (R =арил, винил) Физтех, 1 курс. Весна 2016
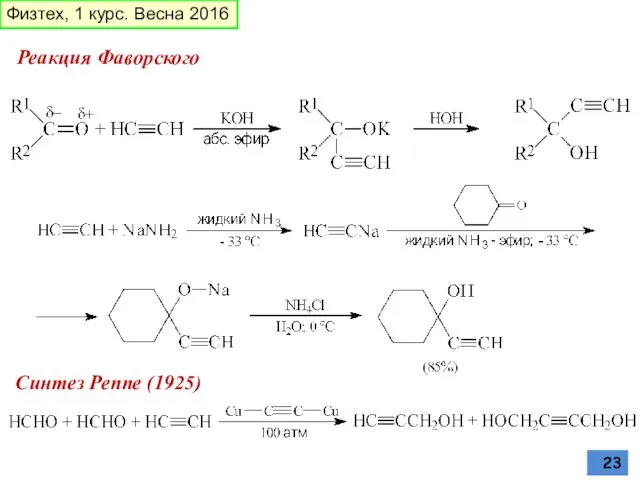
- 23. Реакция Фаворского Синтез Реппе (1925) Физтех, 1 курс. Весна 2016
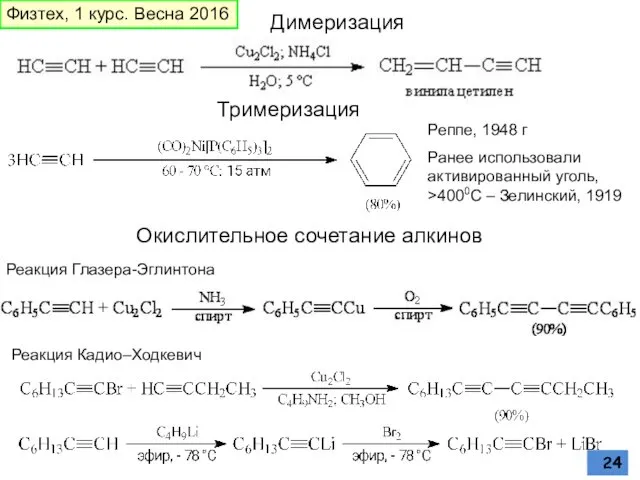
- 24. Окислительное сочетание алкинов Реакция Глазера-Эглинтона Димеризация Реппе, 1948 г Ранее использовали активированный уголь, >4000С – Зелинский,
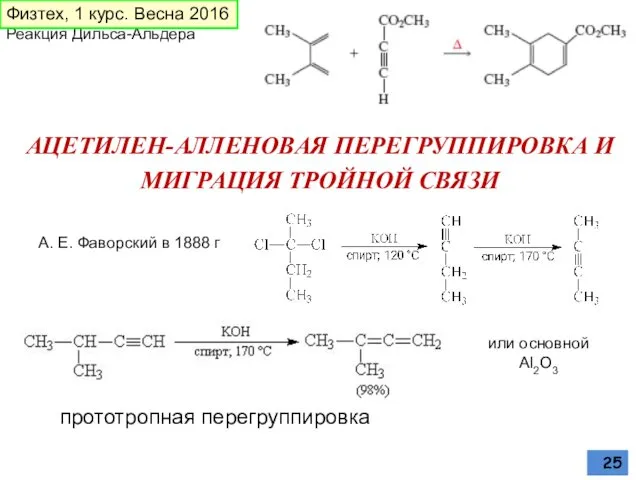
- 25. АЦЕТИЛЕН-АЛЛЕНОВАЯ ПЕРЕГРУППИРОВКА И МИГРАЦИЯ ТРОЙНОЙ СВЯЗИ А. Е. Фаворский в 1888 г или основной Al2O3 прототропная
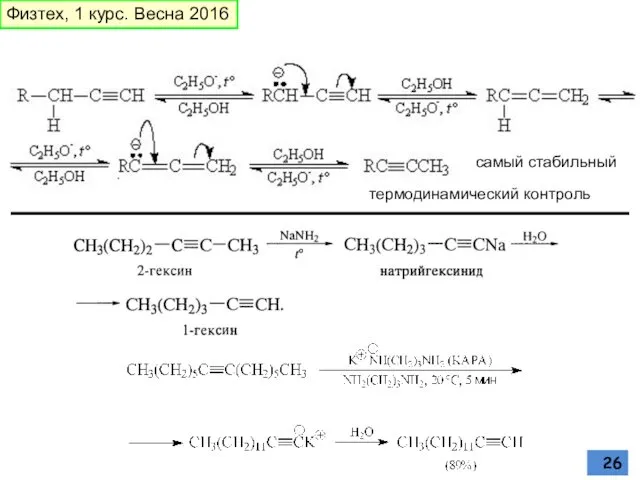
- 26. самый стабильный термодинамический контроль Физтех, 1 курс. Весна 2016
- 27. СПЕКТРАЛЬНЫЕ ХАРАКТЕРИСТИКИ Физтех, 1 курс. Весна 2016
- 28. 1825 г.: бензол - выделен М.Фарадеем из светильной жидкости, установлена эмпирическая формула СnНn. 1833 г.: Э.Мичерлих
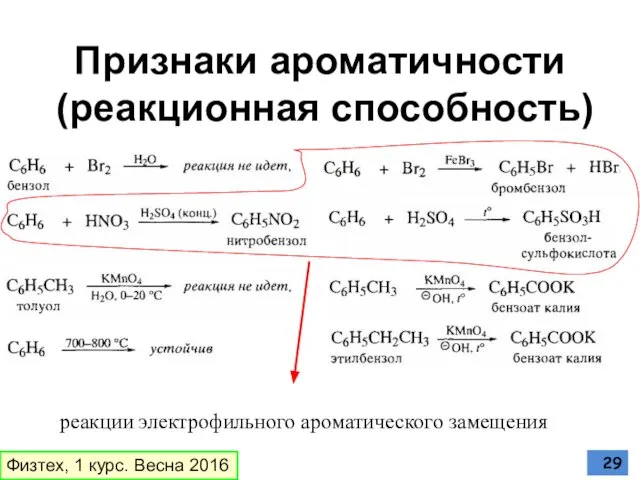
- 29. Признаки ароматичности (реакционная способность) реакции электрофильного ароматического замещения Физтех, 1 курс. Весна 2016
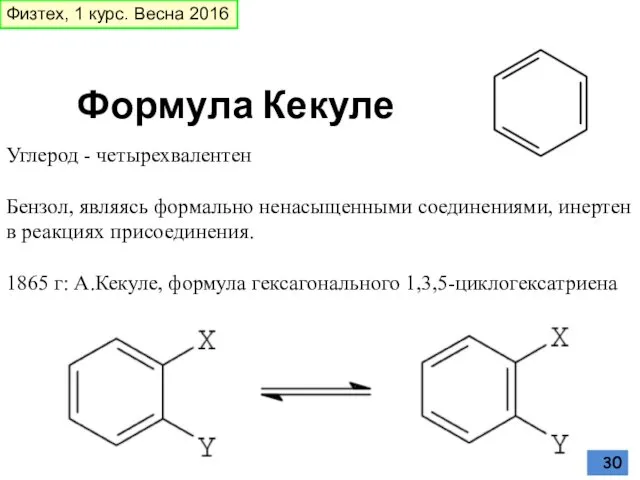
- 30. Углерод - четырехвалентен Бензол, являясь формально ненасыщенными соединениями, инертен в реакциях присоединения. 1865 г: А.Кекуле, формула
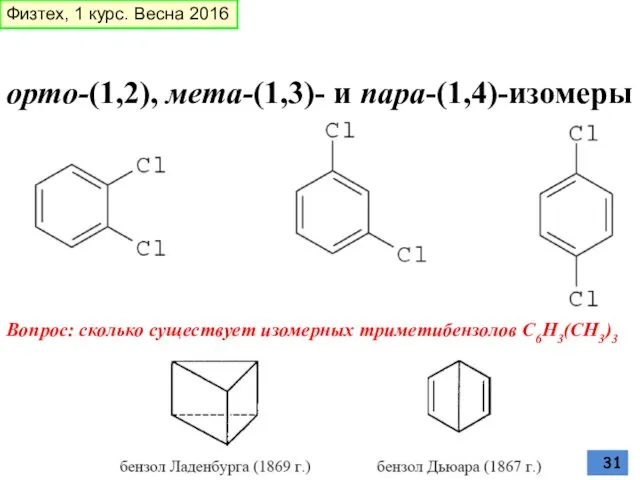
- 31. орто-(1,2), мета-(1,3)- и пара-(1,4)-изомеры Вопрос: сколько существует изомерных триметибензолов С6Н3(СН3)3 Физтех, 1 курс. Весна 2016
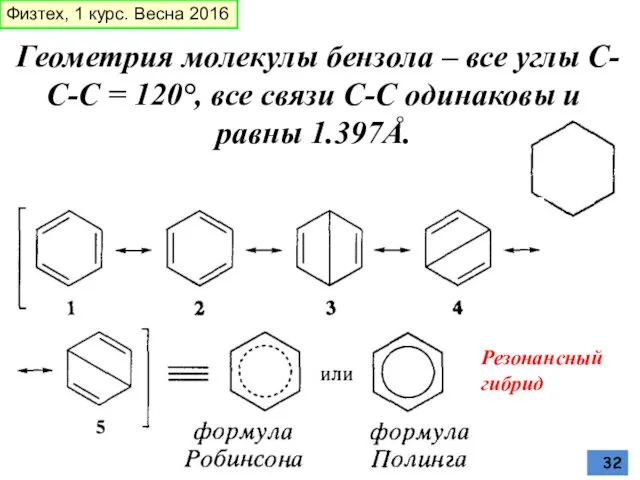
- 32. Геометрия молекулы бензола – все углы С-С-С = 120°, все связи С-С одинаковы и равны 1.397Å.
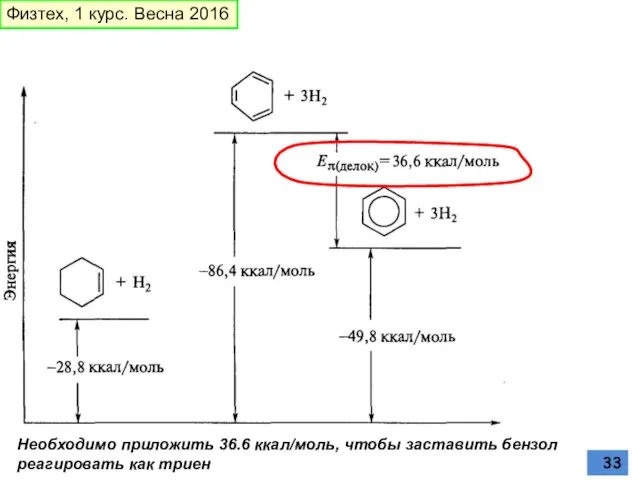
- 33. Необходимо приложить 36.6 ккал/моль, чтобы заставить бензол реагировать как триен Физтех, 1 курс. Весна 2016
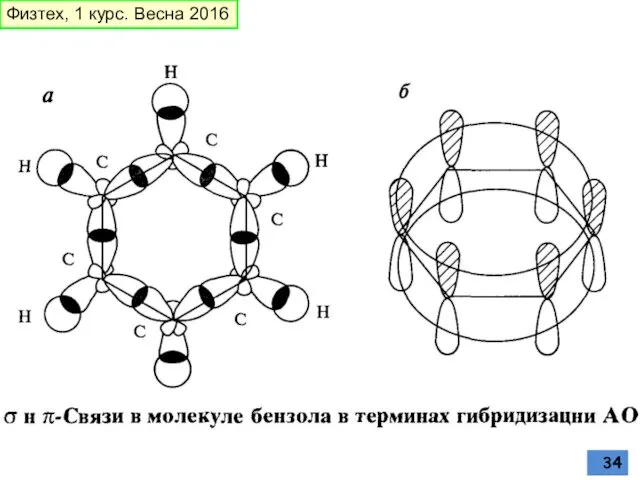
- 34. Физтех, 1 курс. Весна 2016
- 35. Правила ароматичности Правило Хюккеля 1930 г. Плоские моноциклические сопряженные углеводороды будут ароматическими, если цикл содержит (4п
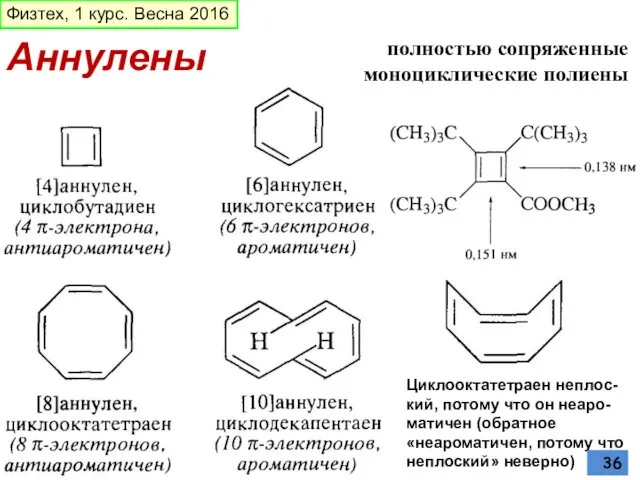
- 36. Аннулены полностью сопряженные моноциклические полиены Циклооктатетраен нeплос-кий, потому что он неаро-матичен (обратное «неароматичен, потому что неплоский»
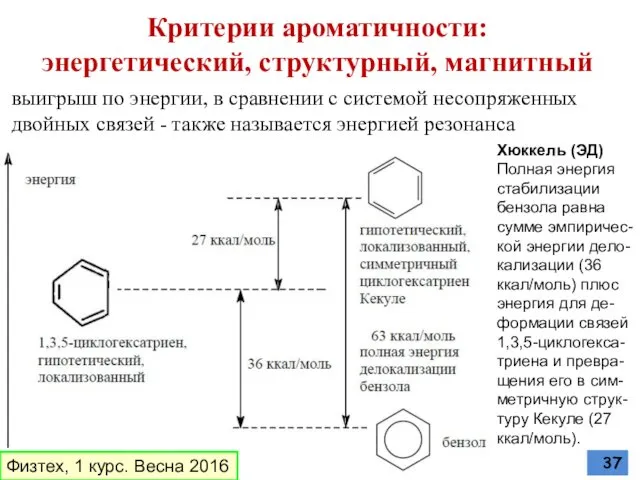
- 37. Критерии ароматичности: энергетический, структурный, магнитный Хюккель (ЭД) Полная энергия стабилизации бензола равна сумме эмпиричес-кой энергии дело-кализации
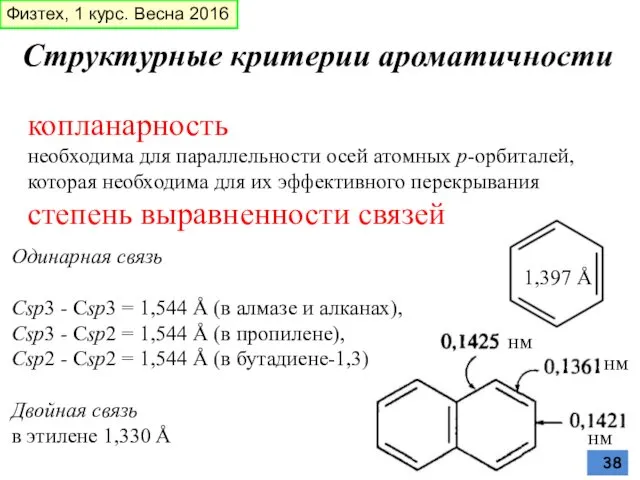
- 38. Структурные критерии ароматичности копланарность необходима для параллельности осей атомных p-орбиталей, которая необходима для их эффективного перекрывания
- 39. Магнитный критерии ароматичности При помещении ароматического вещества в однородное магнитное поле (ЯМР спектроскопия) возникает так называемый
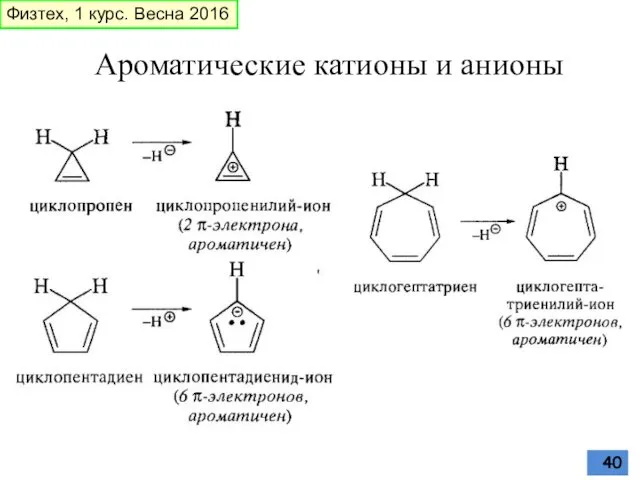
- 40. Ароматические катионы и анионы Физтех, 1 курс. Весна 2016
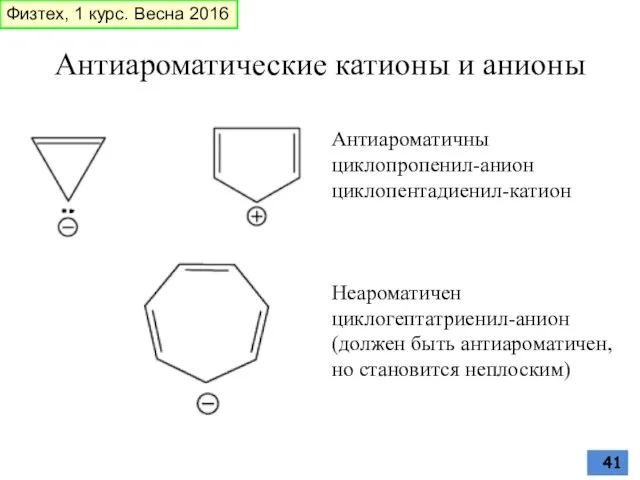
- 41. Антиароматические катионы и анионы Антиароматичны циклопропенил-анион циклопентадиенил-катион Неароматичен циклогептатриенил-анион (должен быть антиароматичен, но становится неплоским) Физтех,
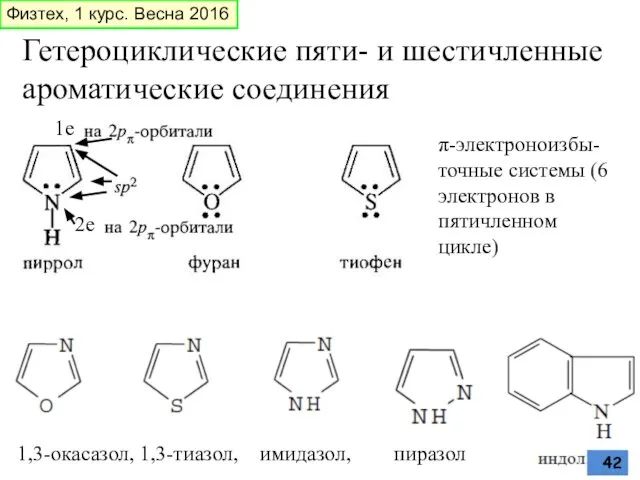
- 42. Гетероциклические пяти- и шестичленные ароматические соединения 1,3-окасазол, 1,3-тиазол, имидазол, пиразол π-электроноизбы-точные системы (6 электронов в пятичленном
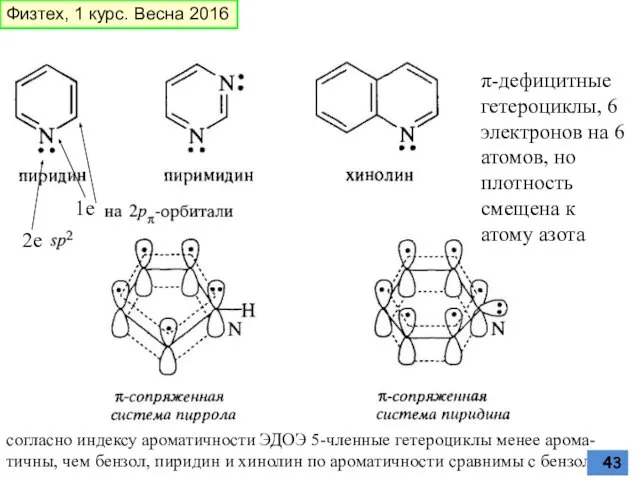
- 43. π-дефицитные гетероциклы, 6 электронов на 6 атомов, но плотность смещена к атому азота 2е 1е согласно
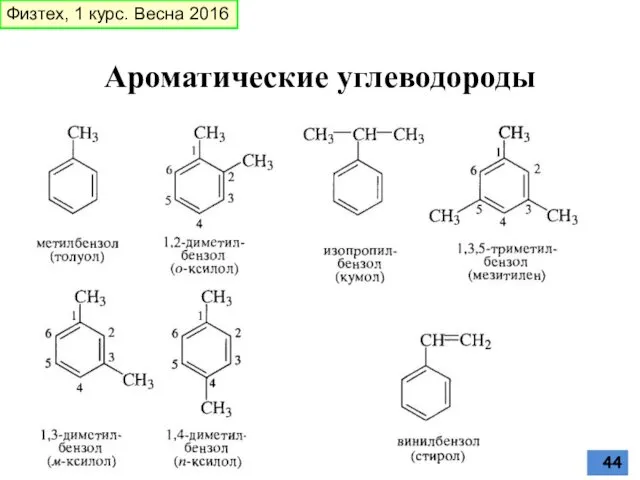
- 44. Ароматические углеводороды Физтех, 1 курс. Весна 2016
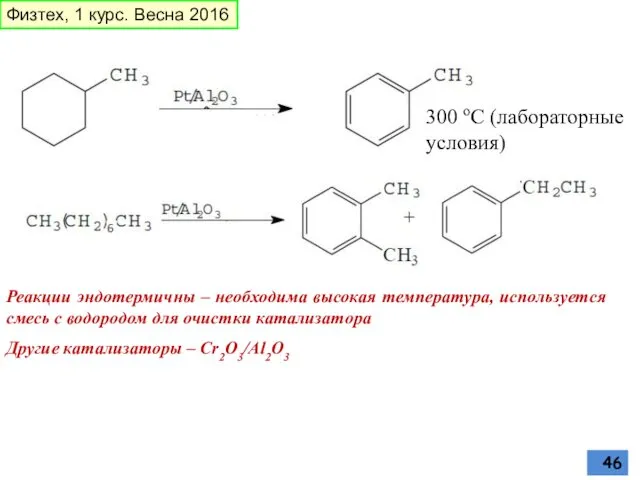
- 45. Промышленные источники ароматических углеводородов. Риформинг Реакции дегидрирования циклоалканов и дегидроциклизации алканов на катализаторе - каталитический риформинг
- 46. Реакции эндотермичны – необходима высокая температура, используется смесь с водородом для очистки катализатора Другие катализаторы –
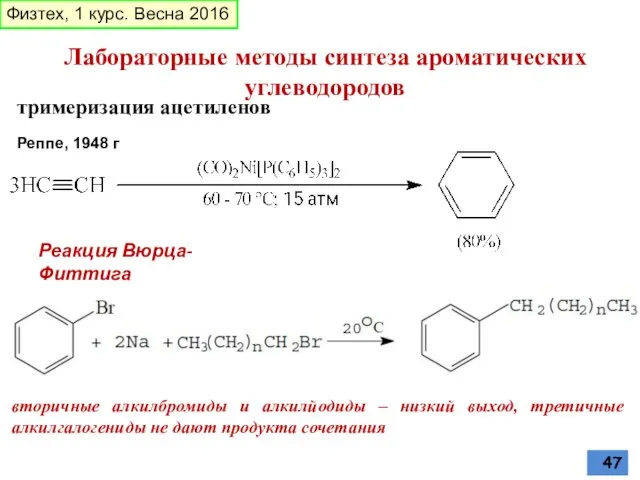
- 47. тримеризация ацетиленов Реппе, 1948 г Лабораторные методы синтеза ароматических углеводородов Реакция Вюрца-Фиттига вторичные алкилбромиды и алкилйодиды
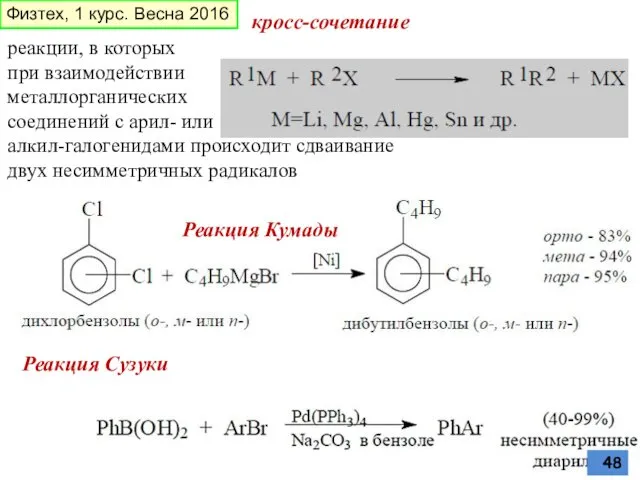
- 48. кросс-сочетание реакции, в которых при взаимодействии металлорганических соединений с арил- или алкил-галогенидами происходит сдваивание двух несимметричных
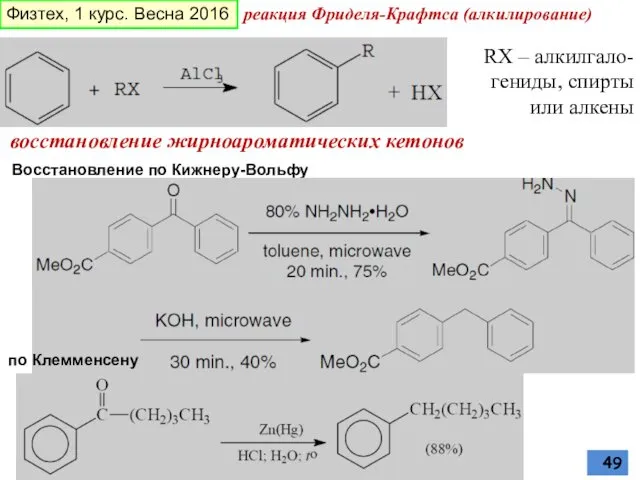
- 49. восстановление жирноароматических кетонов Восстановление по Кижнеру-Вольфу по Клемменсену реакция Фриделя-Крафтса (алкилирование) RX – алкилгало-гениды, спирты или
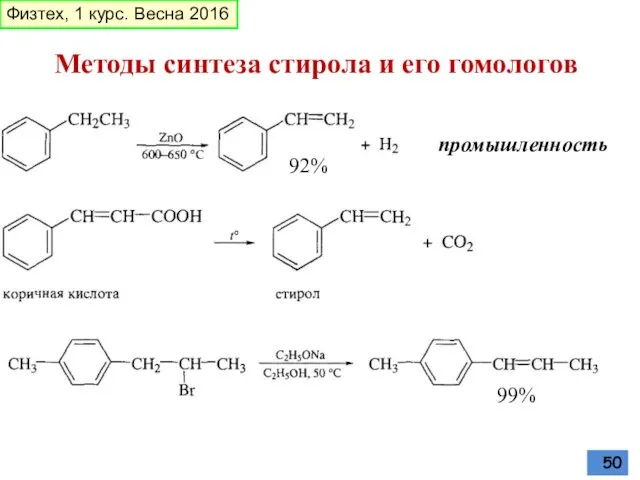
- 50. Методы синтеза стирола и его гомологов 92% промышленность 99% Физтех, 1 курс. Весна 2016
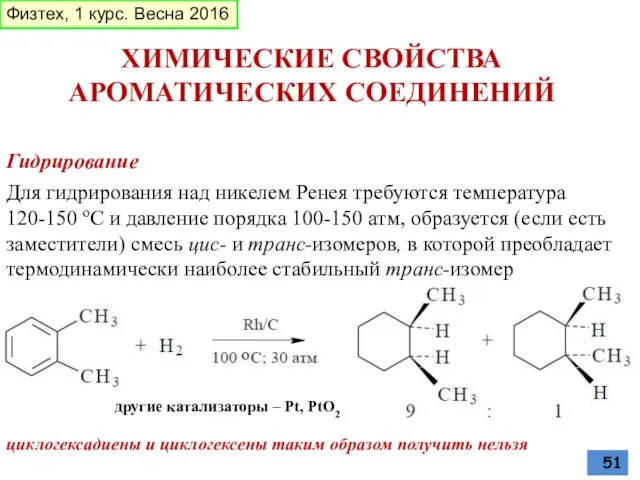
- 51. Гидрирование ХИМИЧЕСКИЕ СВОЙСТВА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ Для гидрирования над никелем Ренея требуются температура 120-150 oС и давление
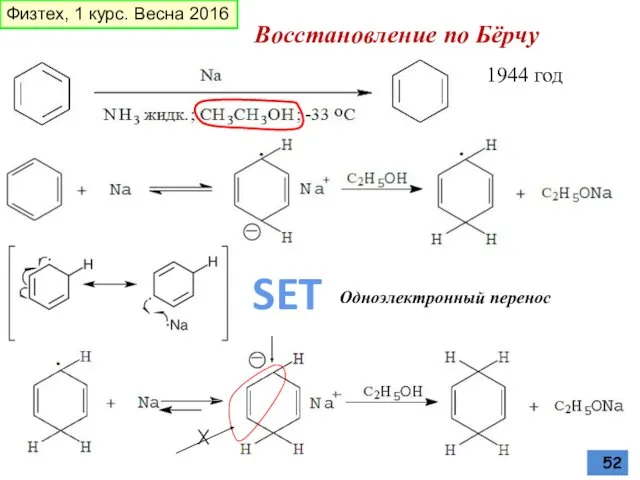
- 52. Восстановление по Бёрчу 1944 год Х Физтех, 1 курс. Весна 2016 SET Одноэлектронный перенос
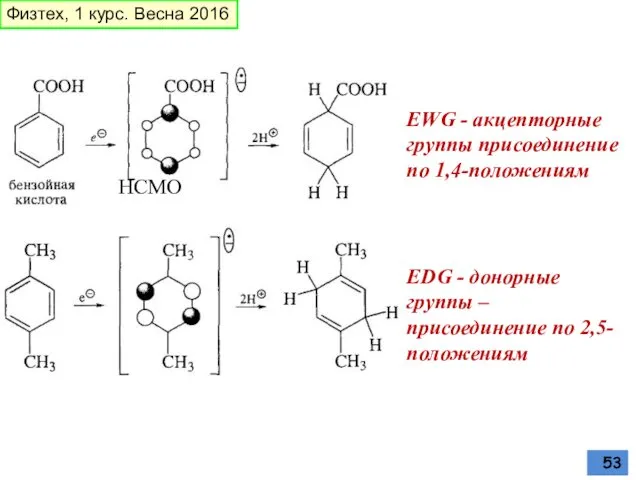
- 53. EWG - акцепторные группы присоединение по 1,4-положениям EDG - донорные группы – присоединение по 2,5-положениям НСМО
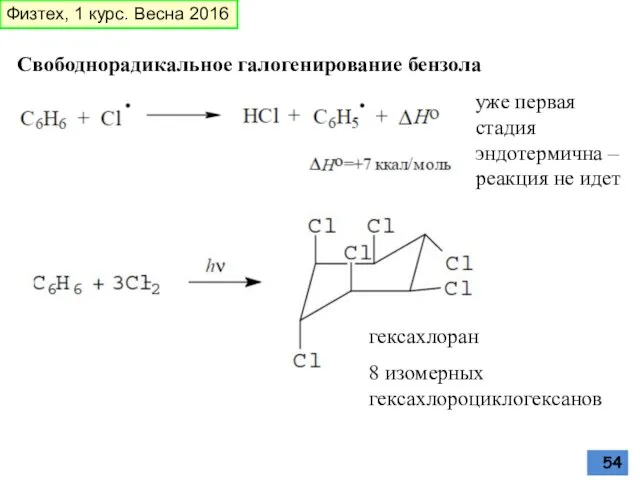
- 54. Свободнорадикальное галогенирование бензола уже первая стадия эндотермична – реакция не идет гексахлоран 8 изомерных гексахлороциклогексанов Физтех,
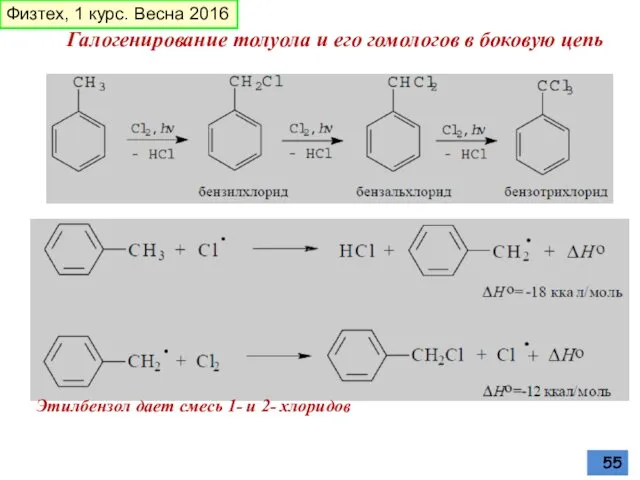
- 55. Галогенирование толуола и его гомологов в боковую цепь Этилбензол дает смесь 1- и 2- хлоридов Физтех,
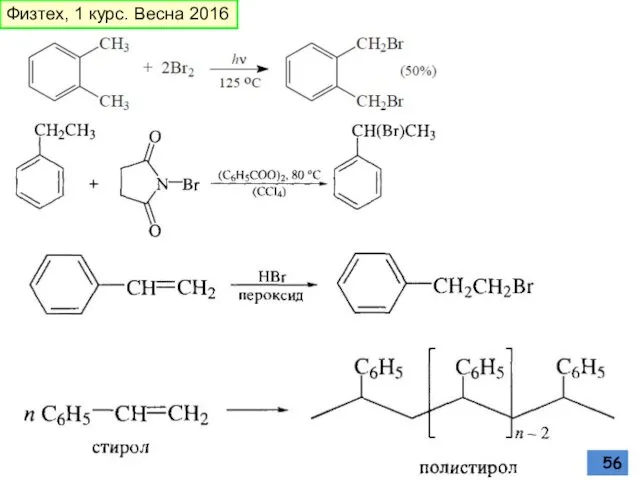
- 56. Физтех, 1 курс. Весна 2016
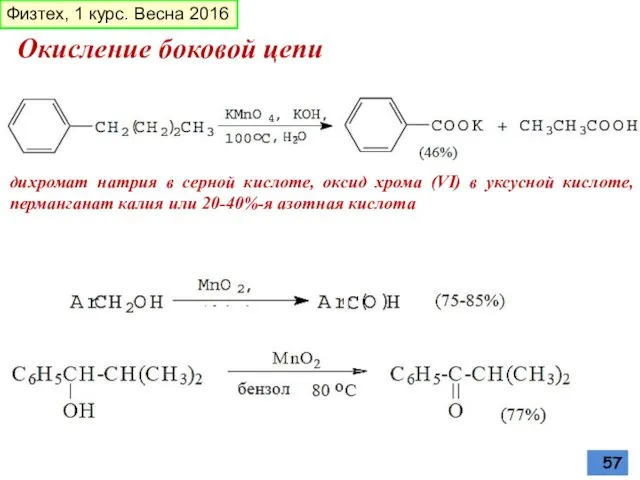
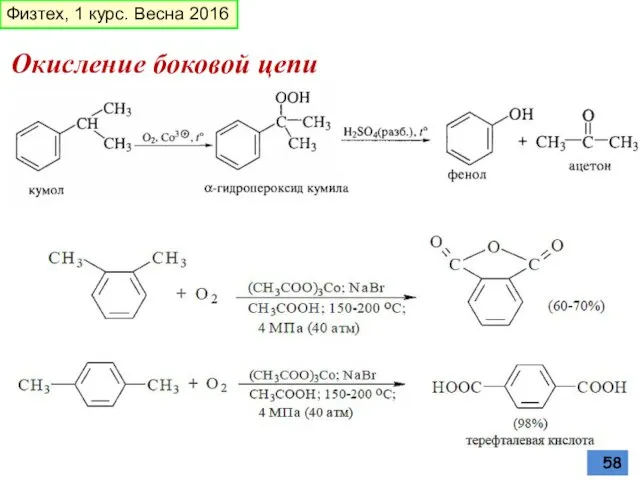
- 57. Окисление боковой цепи дихромат натрия в серной кислоте, оксид хрома (VI) в уксусной кислоте, перманганат калия
- 58. Физтех, 1 курс. Весна 2016 Окисление боковой цепи
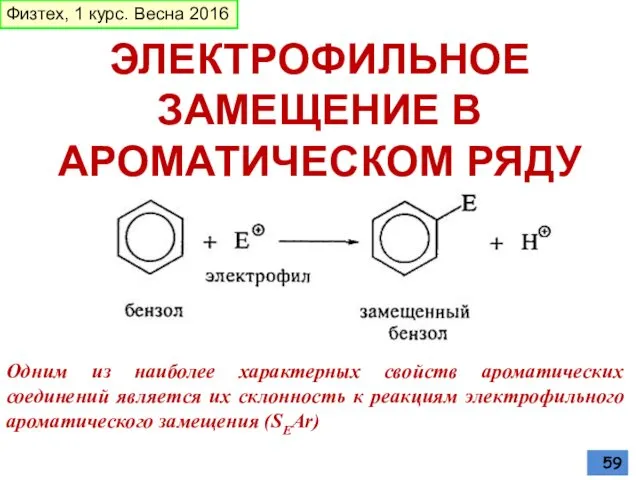
- 59. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В АРОМАТИЧЕСКОМ РЯДУ Одним из наиболее характерных свойств ароматических соединений является их склонность к
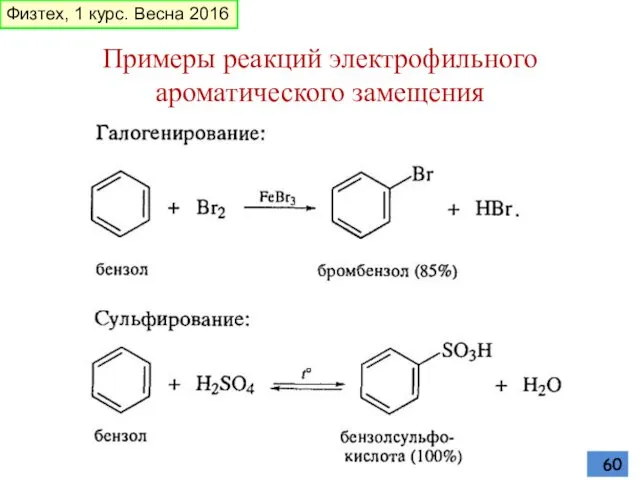
- 60. Примеры реакций электрофильного ароматического замещения Физтех, 1 курс. Весна 2016
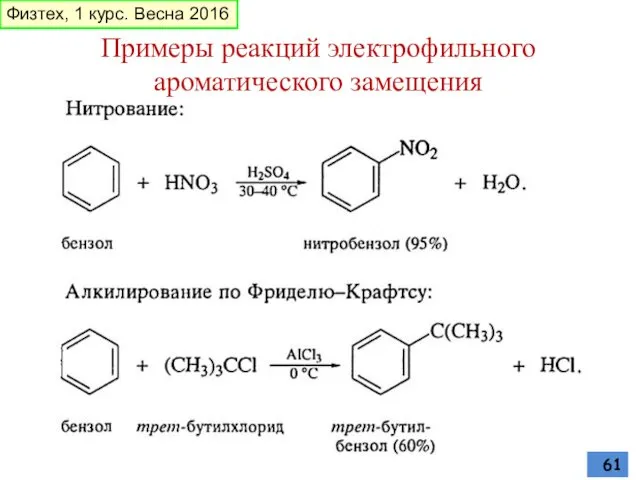
- 61. Физтех, 1 курс. Весна 2016 Примеры реакций электрофильного ароматического замещения
- 62. Физтех, 1 курс. Весна 2016
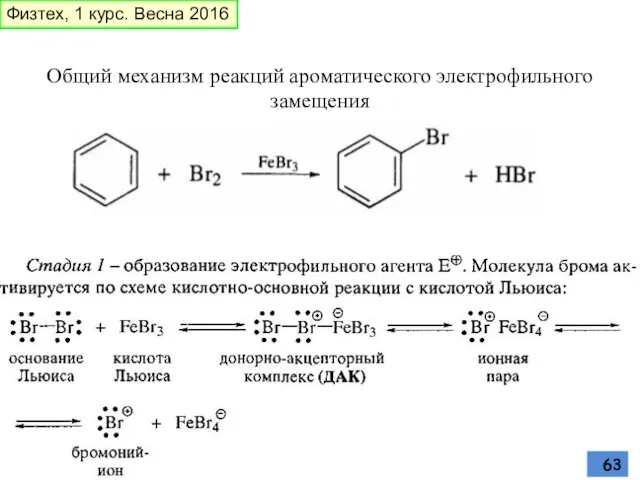
- 63. Общий механизм реакций ароматического электрофильного замещения Физтех, 1 курс. Весна 2016
- 64. нециклическая четырехэлектронная сопряженная система пентадиенильного катиона (С=С-С=С-C+) Физтех, 1 курс. Весна 2016
- 65. Физтех, 1 курс. Весна 2016
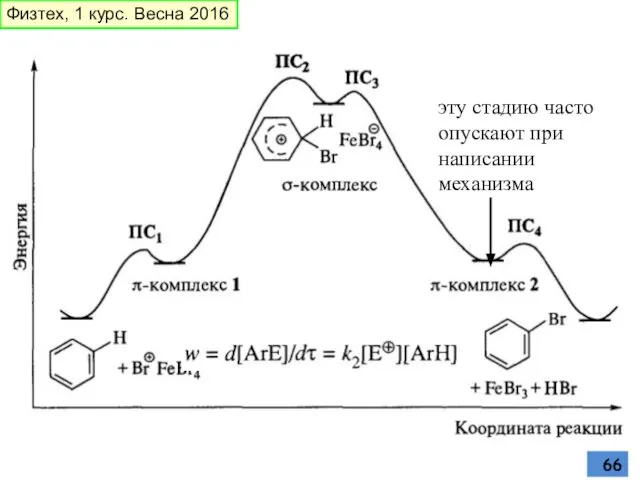
- 66. эту стадию часто опускают при написании механизма Физтех, 1 курс. Весна 2016
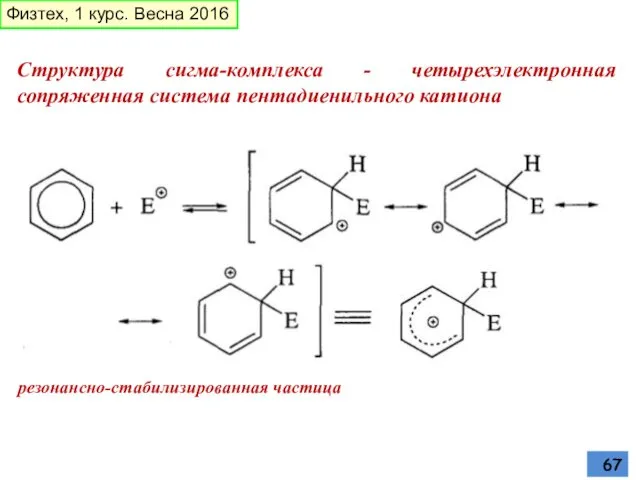
- 67. Структура сигма-комплекса - четырехэлектронная сопряженная система пентадиенильного катиона резонансно-стабилизированная частица Физтех, 1 курс. Весна 2016
- 68. При введении в раствор HCl или DCl в алкилбензолах AlCl3 или AlBr3 он начинает проводить электрический
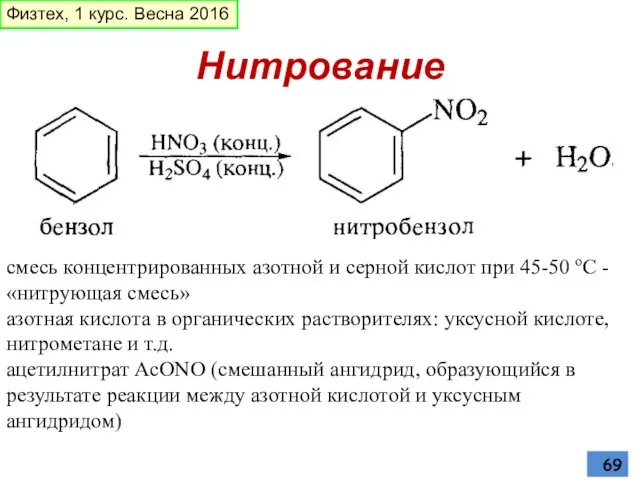
- 69. Нитрование смесь концентрированных азотной и серной кислот при 45-50 oС - «нитрующая смесь» азотная кислота в
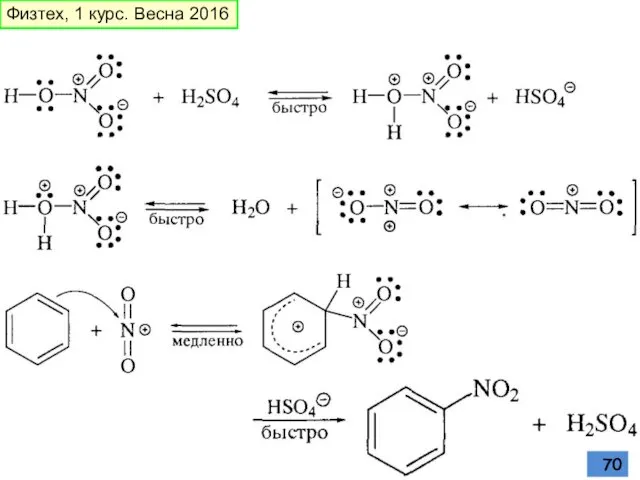
- 70. Физтех, 1 курс. Весна 2016
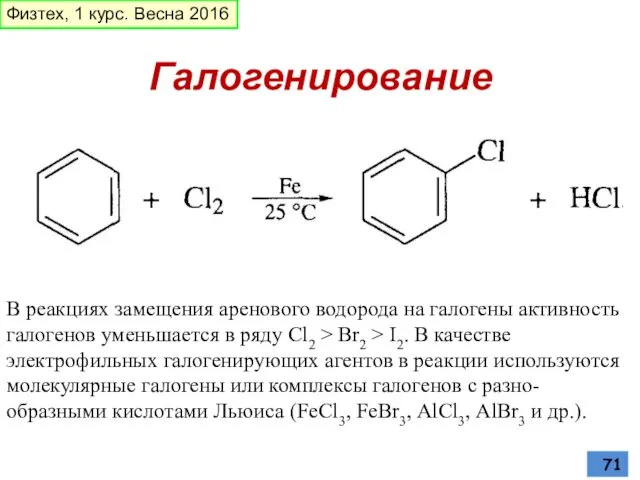
- 71. Галогенирование В реакциях замещения аренового водорода на галогены активность галогенов уменьшается в ряду Сl2 > Br2
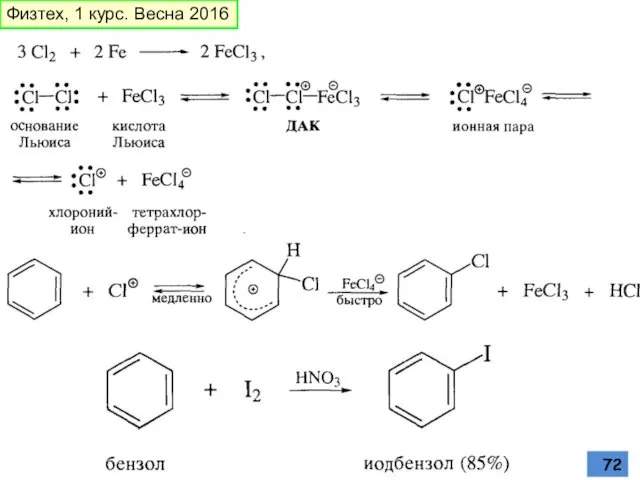
- 72. Физтех, 1 курс. Весна 2016
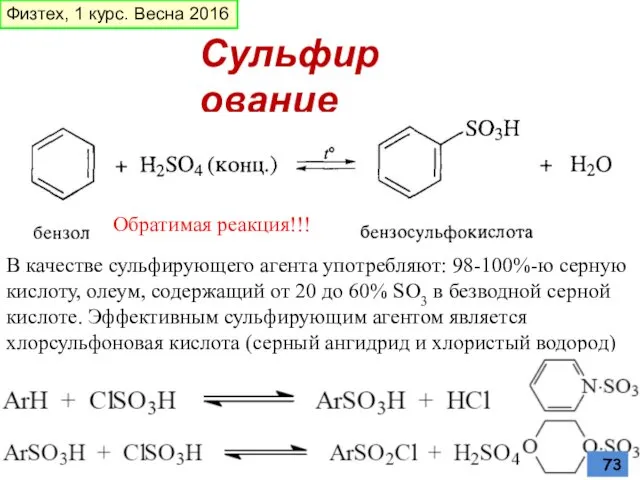
- 73. Сульфирование В качестве сульфирующего агента употребляют: 98-100%-ю серную кислоту, олеум, содержащий от 20 до 60% SO3
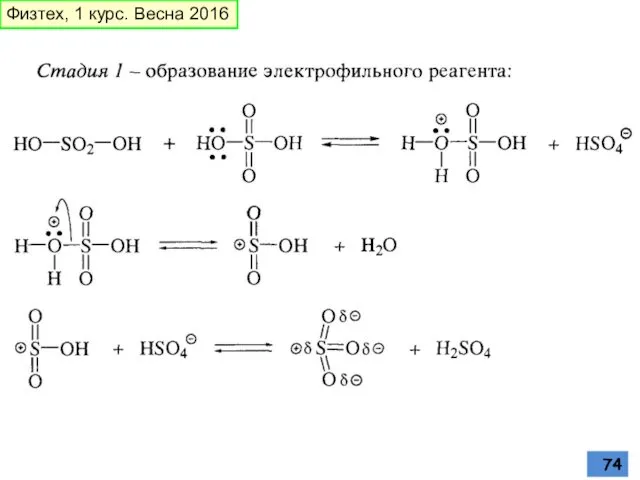
- 74. Физтех, 1 курс. Весна 2016
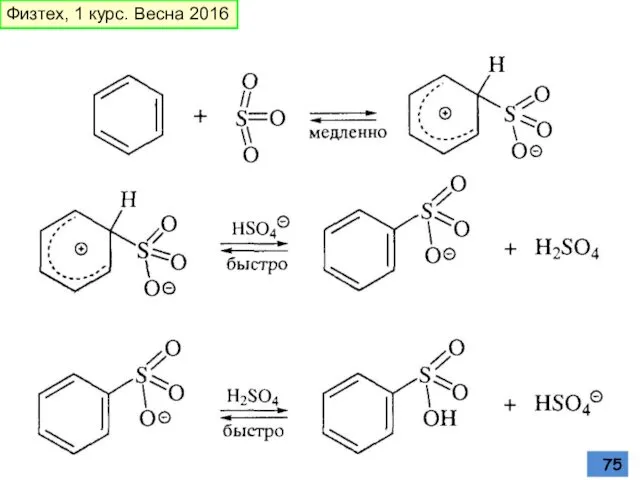
- 75. Физтех, 1 курс. Весна 2016
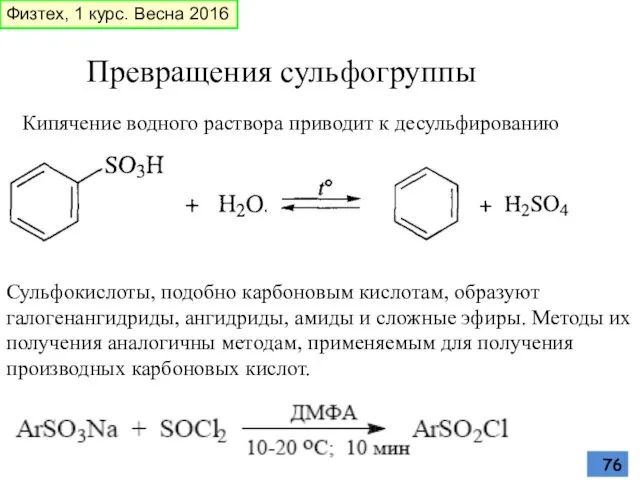
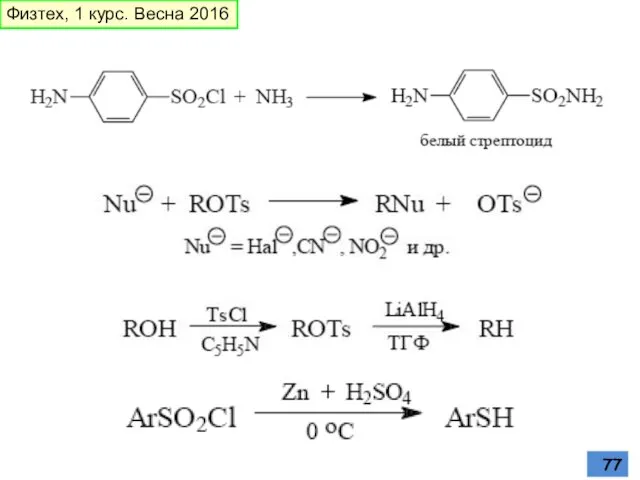
- 76. Превращения сульфогруппы Кипячение водного раствора приводит к десульфированию Сульфокислоты, подобно карбоновым кислотам, образуют галогенангидриды, ангидриды, амиды
- 77. Физтех, 1 курс. Весна 2016
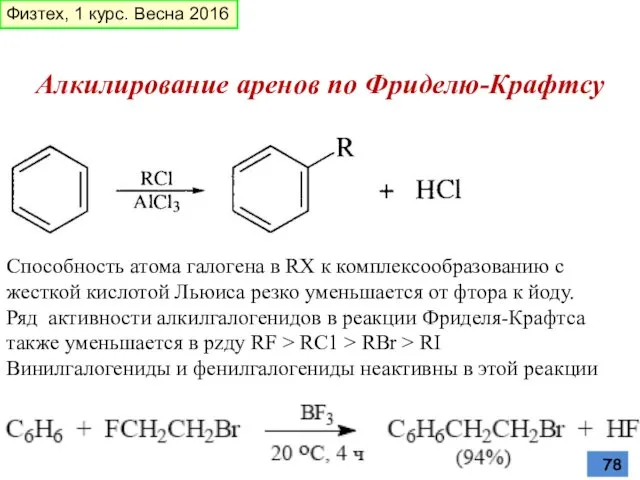
- 78. Алкилирование аренов по Фриделю-Крафтсу Способность атома галогена в RX к комплексообразованию с жесткой кислотой Льюиса резко
- 79. Физтех, 1 курс. Весна 2016
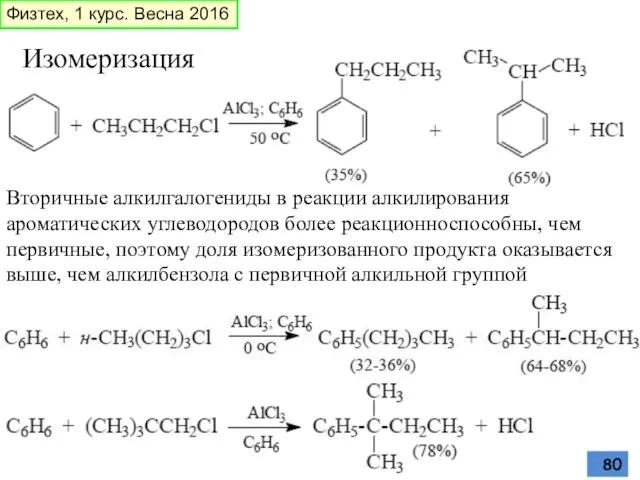
- 80. Изомеризация Вторичные алкилгалогениды в реакции алкилирования ароматических углеводородов более реакционноспособны, чем первичные, поэтому доля изомеризованного продукта
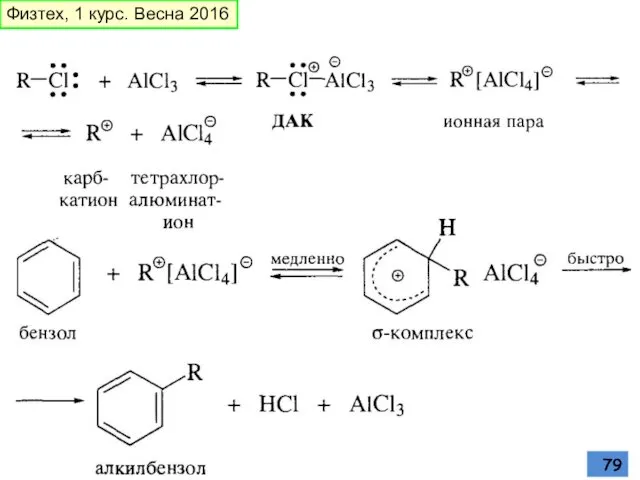
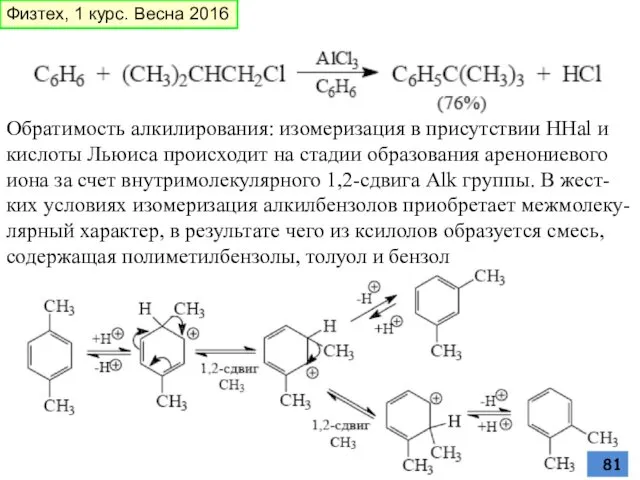
- 81. Обратимость алкилирования: изомеризация в присутствии HHal и кислоты Льюиса происходит на стадии образования аренониевого иона за
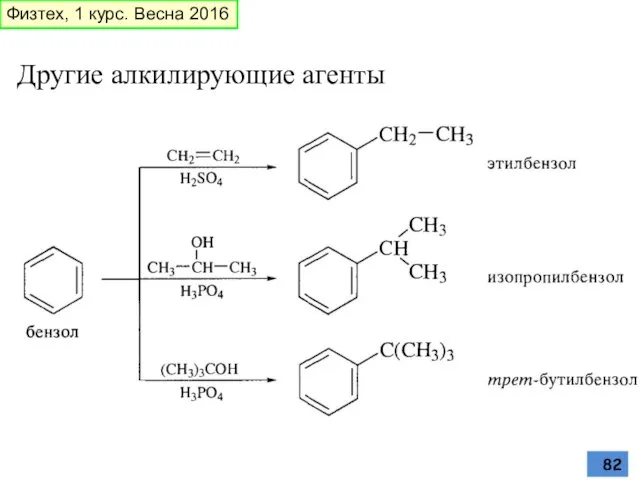
- 82. Другие алкилирующие агенты Физтех, 1 курс. Весна 2016
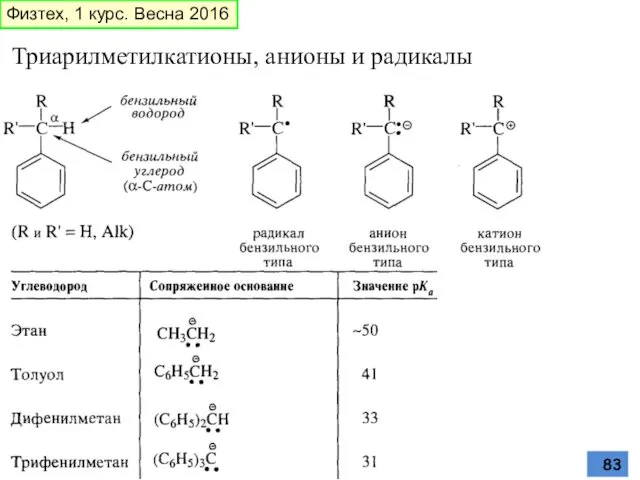
- 83. Триарилметилкатионы, анионы и радикалы Физтех, 1 курс. Весна 2016
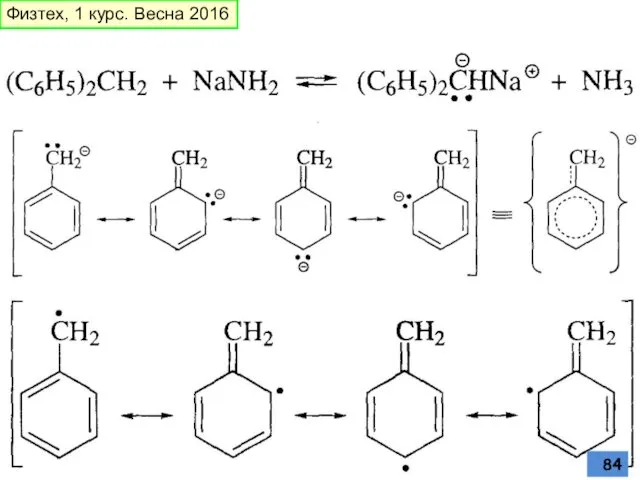
- 84. Физтех, 1 курс. Весна 2016
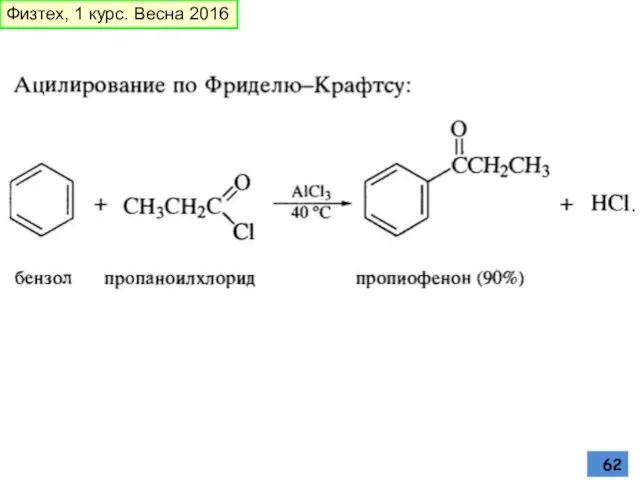
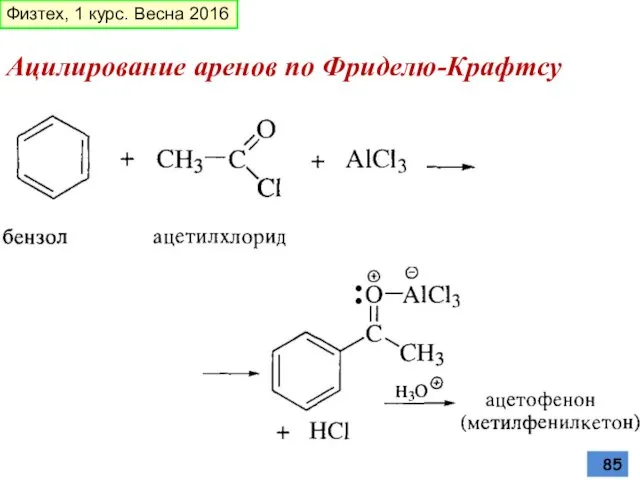
- 85. Ацилирование аренов по Фриделю-Крафтсу Физтех, 1 курс. Весна 2016
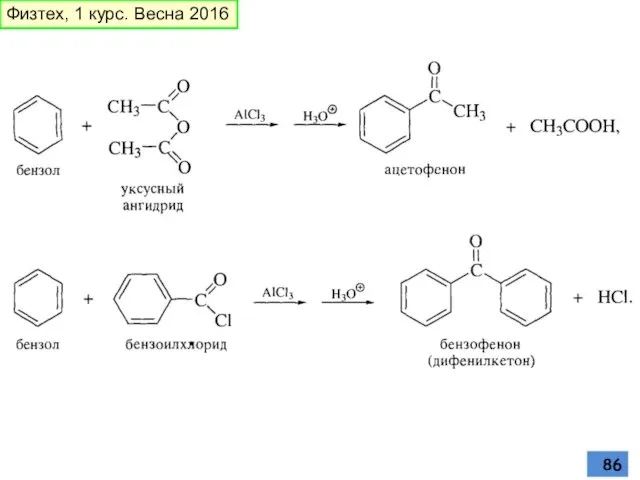
- 86. Физтех, 1 курс. Весна 2016
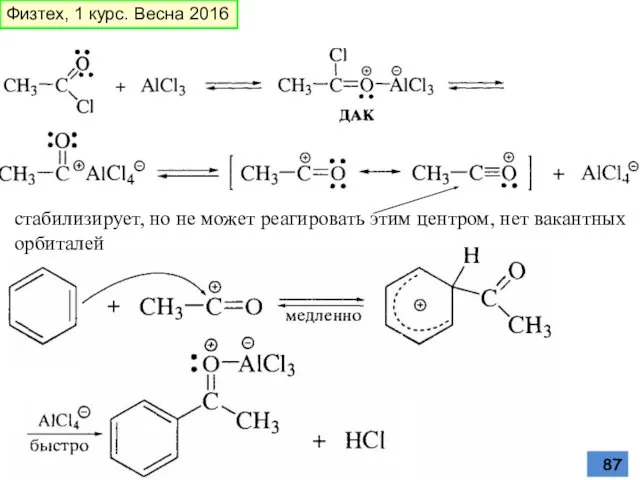
- 87. стабилизирует, но не может реагировать этим центром, нет вакантных орбиталей Физтех, 1 курс. Весна 2016
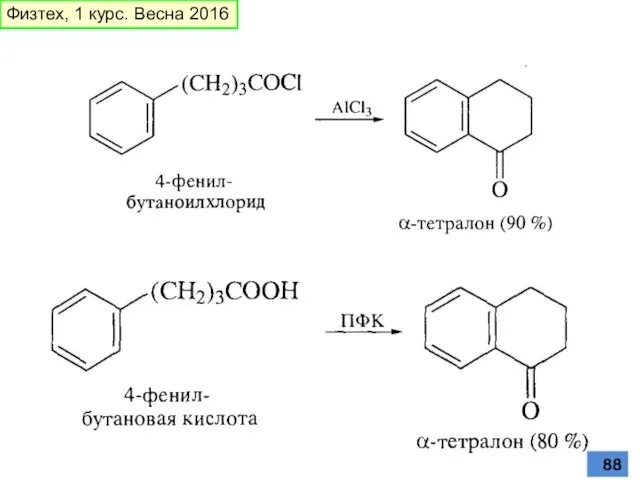
- 88. Физтех, 1 курс. Весна 2016
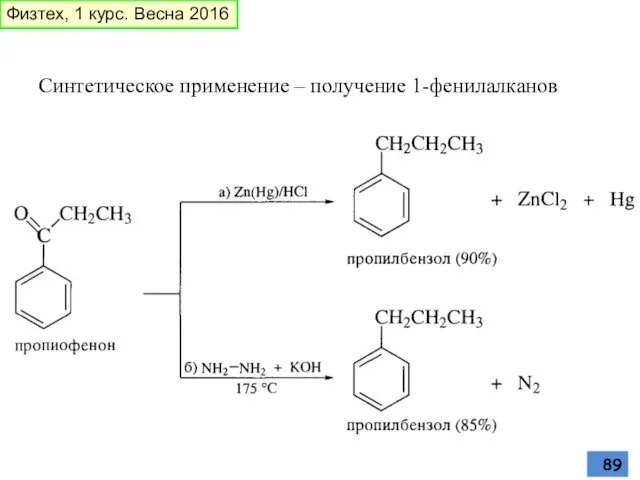
- 89. Синтетическое применение – получение 1-фенилалканов Физтех, 1 курс. Весна 2016
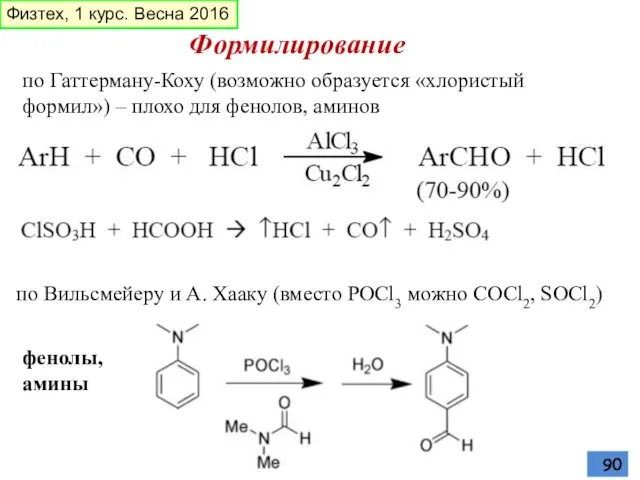
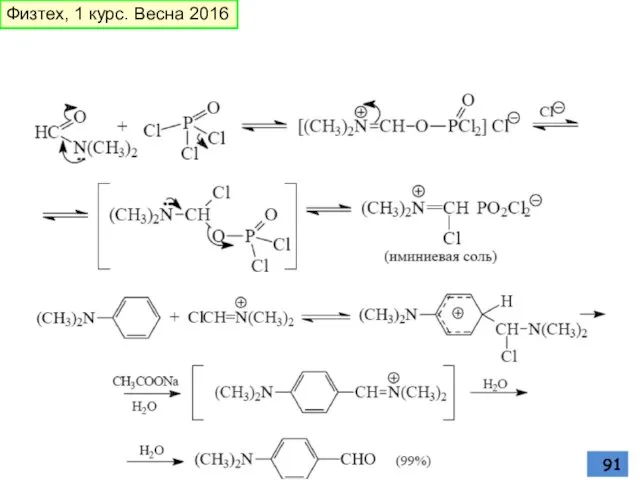
- 90. Формилирование по Гаттерману-Коху (возможно образуется «хлористый формил») – плохо для фенолов, аминов по Вильсмейеру и А.
- 91. Физтех, 1 курс. Весна 2016
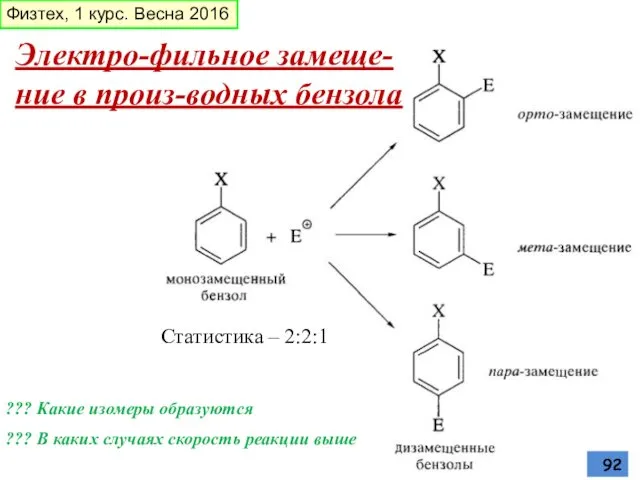
- 92. Электро-фильное замеще-ние в произ-водных бензола Статистика – 2:2:1 ??? Какие изомеры образуются ??? В каких случаях
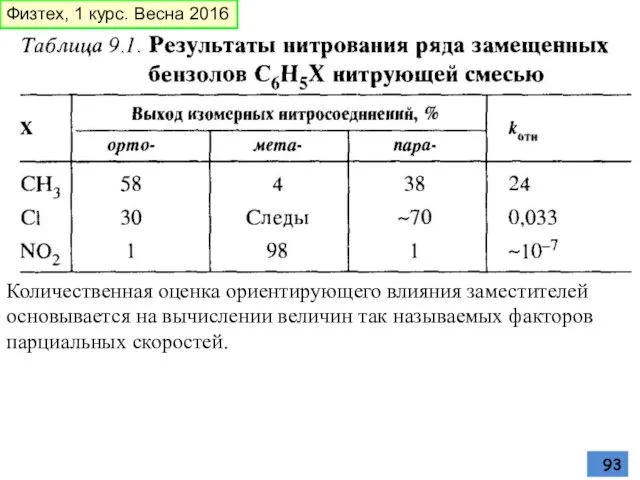
- 93. Количественная оценка ориентирующего влияния заместителей основывается на вычислении величин так называемых факторов парциальных скоростей. Физтех, 1
- 94. К ориентантам I рода относятся: OH, OR, OCOR, SH, SR, NH2, NHR, NR2, NHCOR, -N=N-, CH3,
- 95. Физтех, 1 курс. Весна 2016
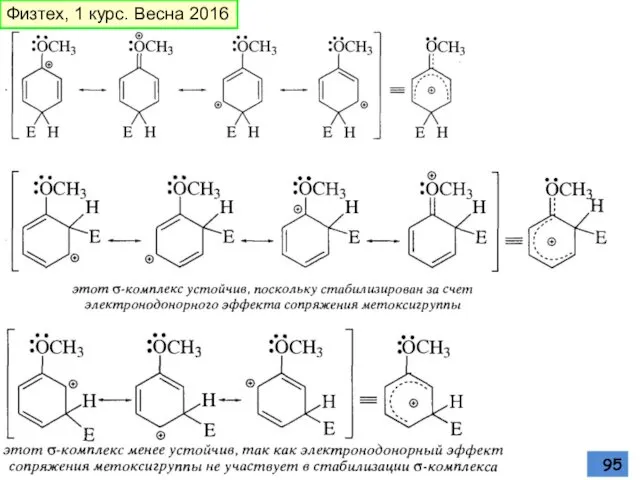
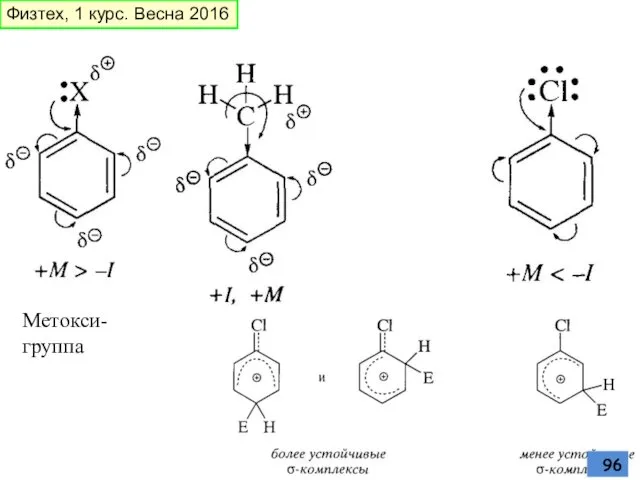
- 96. Метокси-группа Физтех, 1 курс. Весна 2016
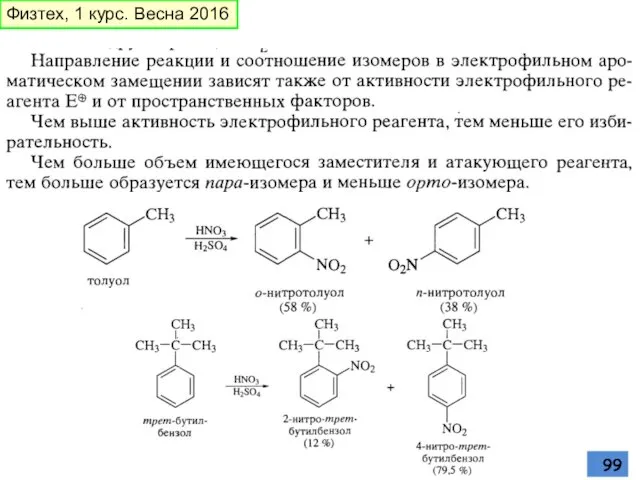
- 97. Физтех, 1 курс. Весна 2016
- 98. Физтех, 1 курс. Весна 2016
- 99. Физтех, 1 курс. Весна 2016
- 100. 1. Сильные электрофилы: NO2+, комплексы Cl2 и Br2 с кислотами Льюиса, HSO3+, H2S2O7. 2. Электрофилы средней
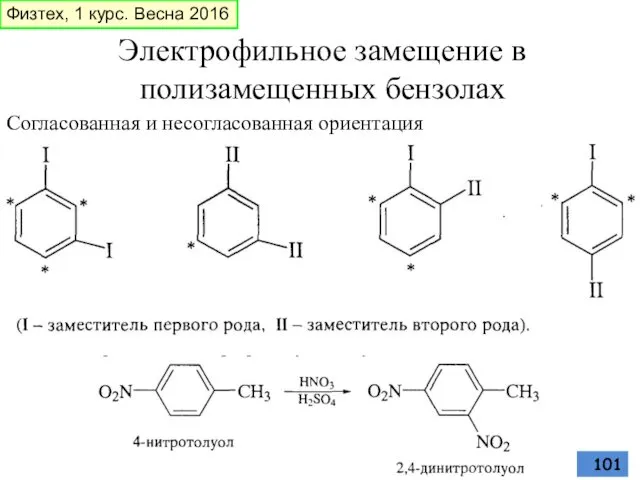
- 101. Электрофильное замещение в полизамещенных бензолах Согласованная и несогласованная ориентация Физтех, 1 курс. Весна 2016
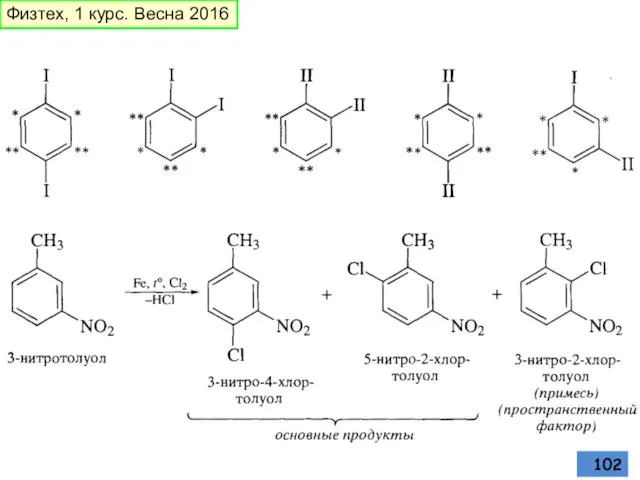
- 102. Физтех, 1 курс. Весна 2016
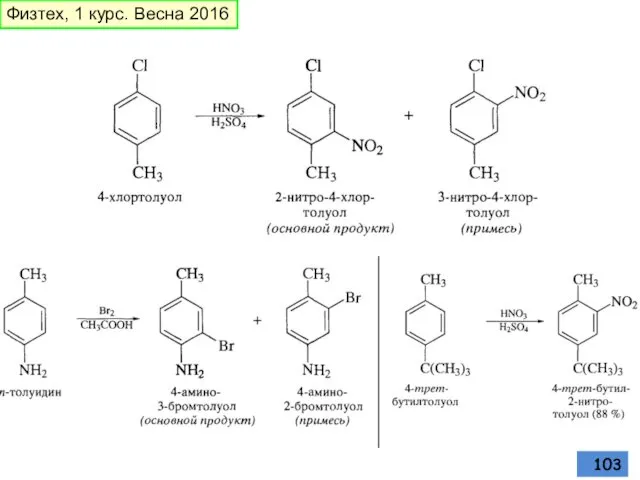
- 103. Физтех, 1 курс. Весна 2016
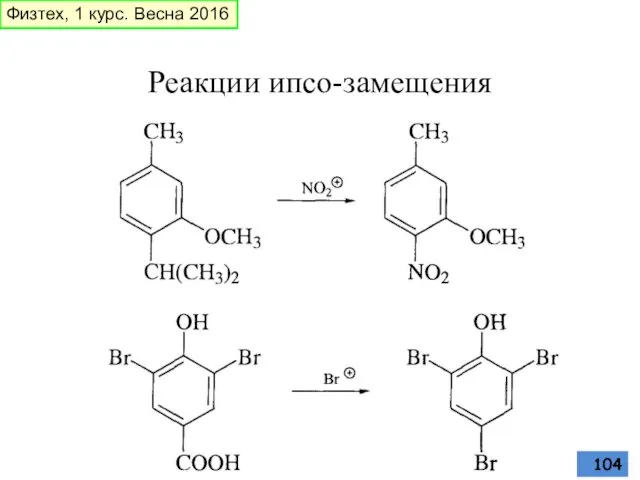
- 104. Реакции ипсо-замещения Физтех, 1 курс. Весна 2016
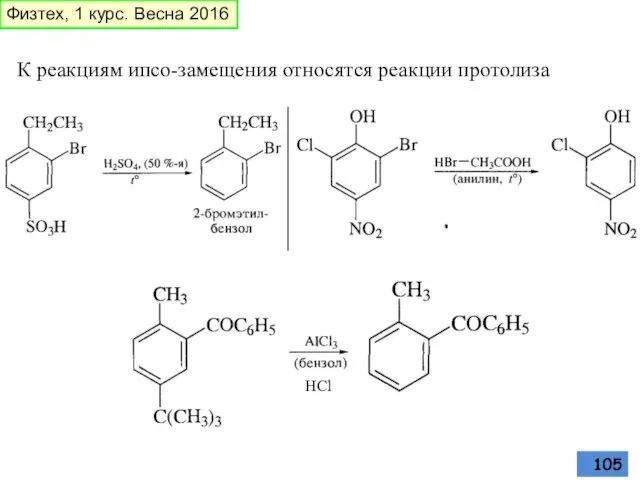
- 105. К реакциям ипсо-замещения относятся реакции протолиза HCl Физтех, 1 курс. Весна 2016
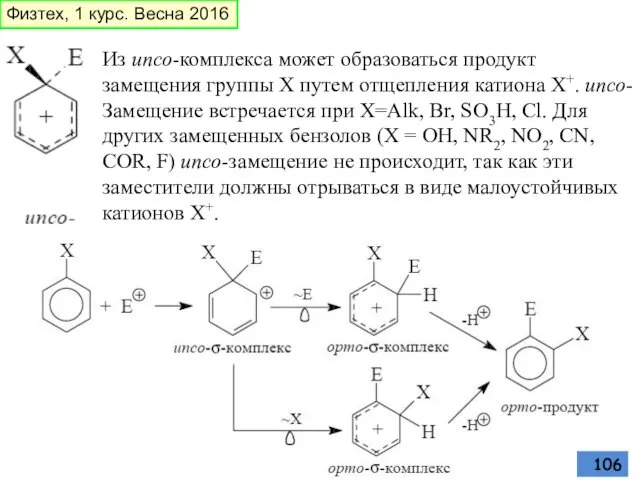
- 106. Из ипсо-комплекса может образоваться продукт замещения группы Х путем отщепления катиона Х+. ипсо-Замещение встречается при Х=Alk,
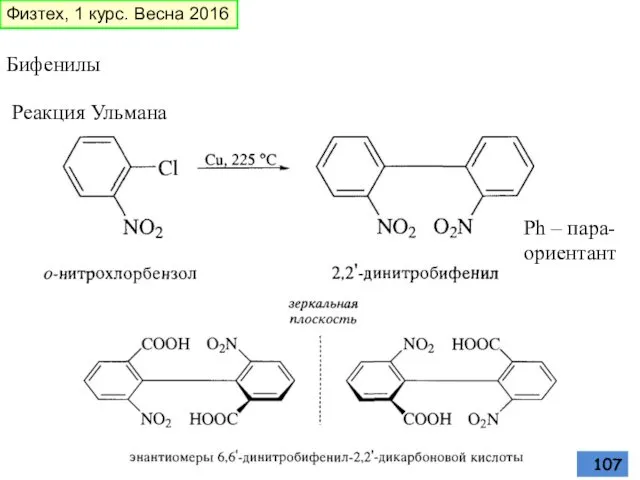
- 107. Бифенилы Реакция Ульмана Ph – пара-ориентант Физтех, 1 курс. Весна 2016
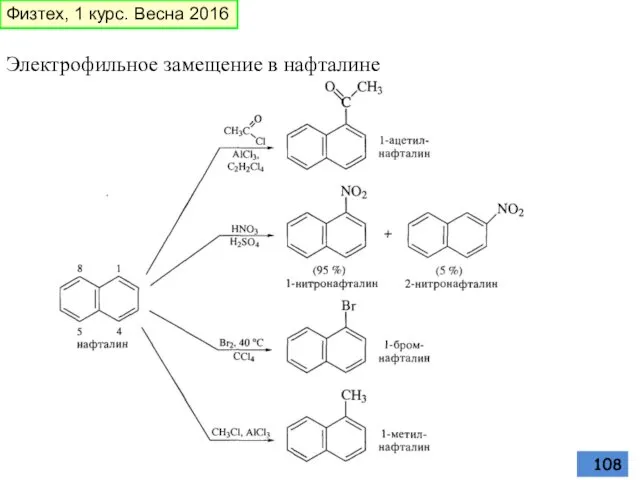
- 108. Электрофильное замещение в нафталине Физтех, 1 курс. Весна 2016
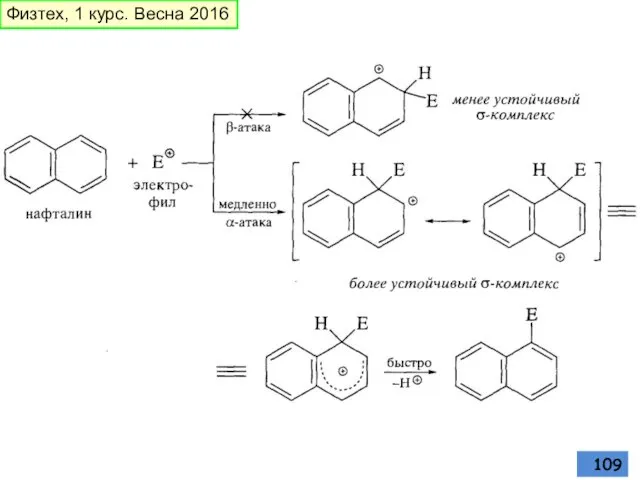
- 109. Физтех, 1 курс. Весна 2016
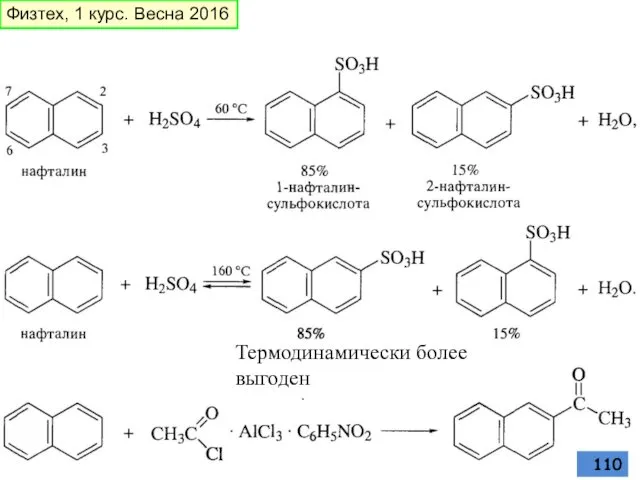
- 110. Термодинамически более выгоден Физтех, 1 курс. Весна 2016
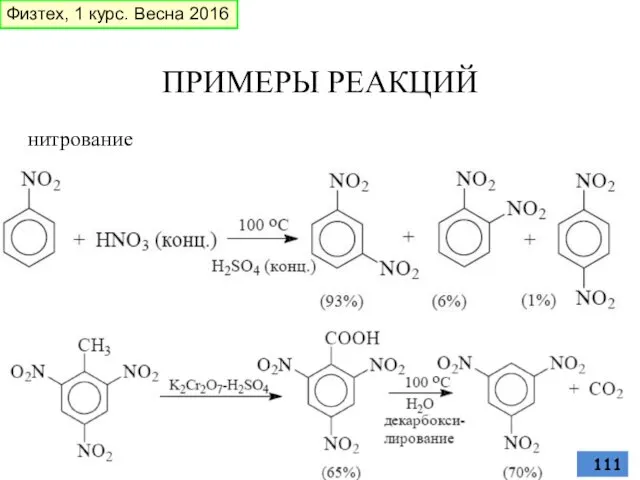
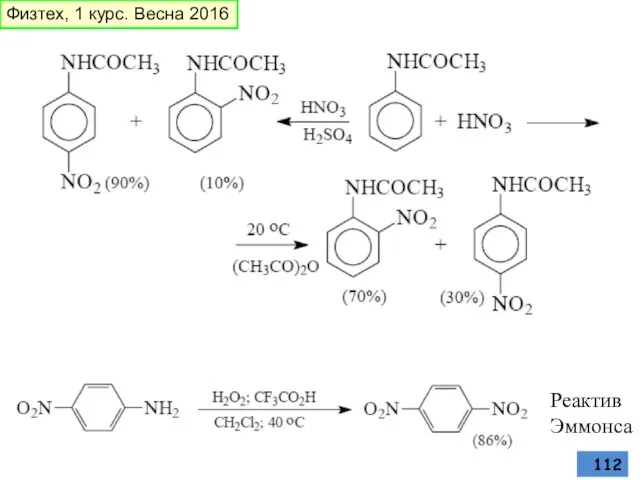
- 111. ПРИМЕРЫ РЕАКЦИЙ нитрование Физтех, 1 курс. Весна 2016
- 112. Реактив Эммонса Физтех, 1 курс. Весна 2016
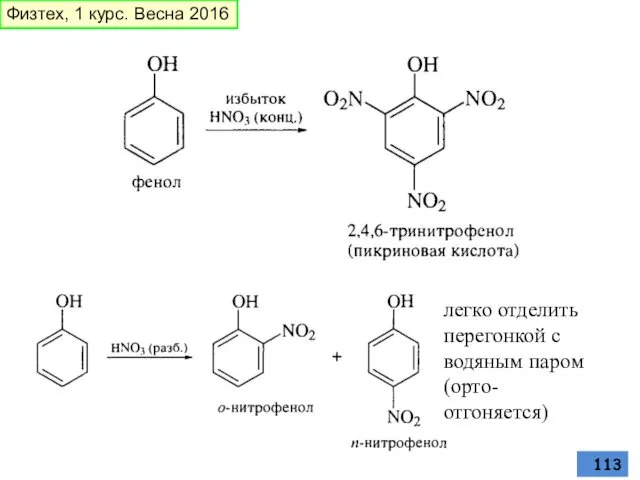
- 113. легко отделить перегонкой с водяным паром (орто- отгоняется) Физтех, 1 курс. Весна 2016
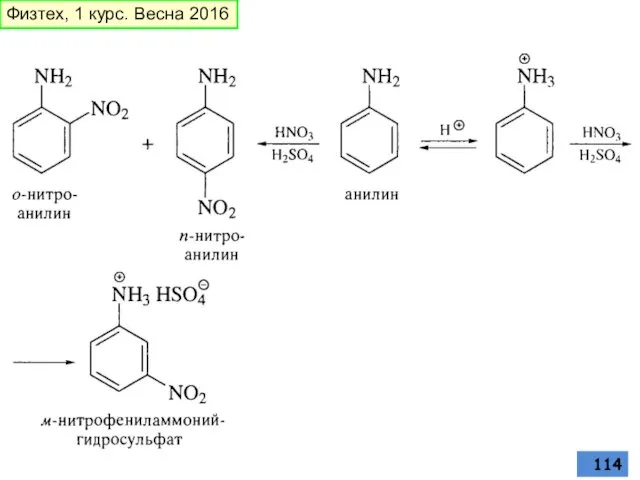
- 114. Физтех, 1 курс. Весна 2016
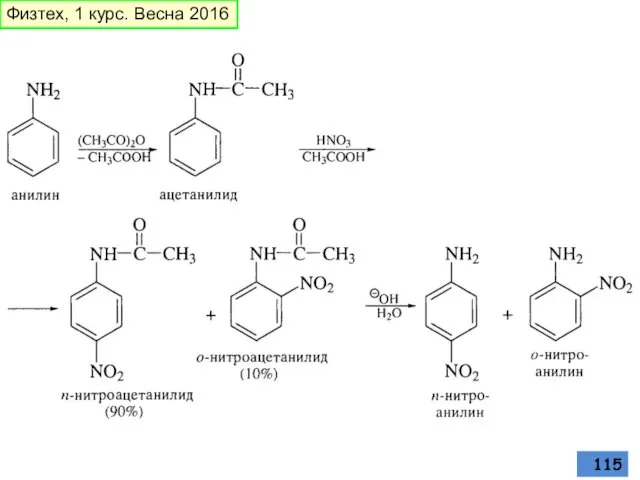
- 115. Физтех, 1 курс. Весна 2016
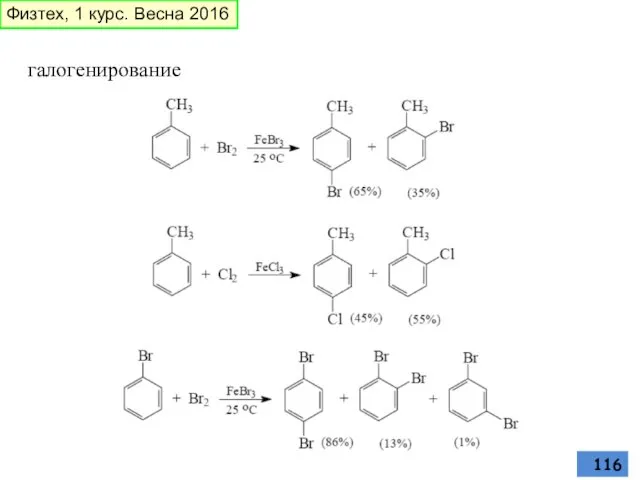
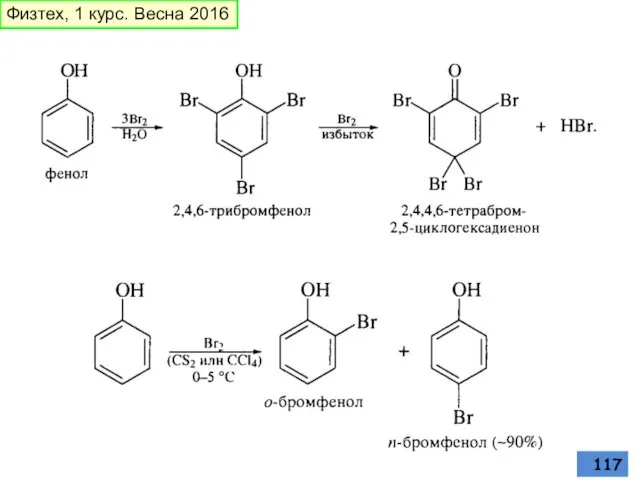
- 116. галогенирование Физтех, 1 курс. Весна 2016
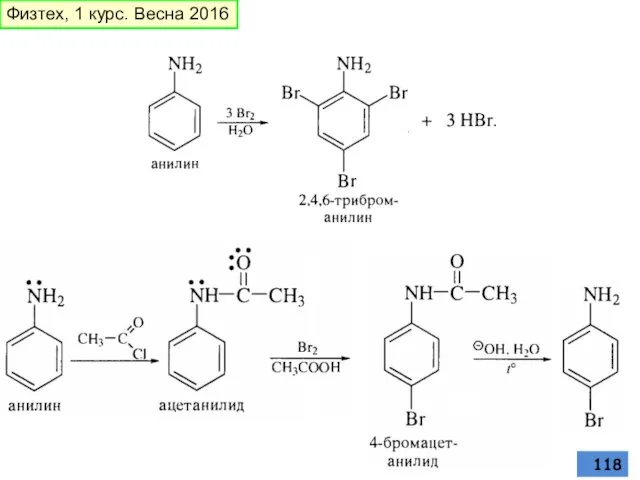
- 117. Физтех, 1 курс. Весна 2016
- 118. Физтех, 1 курс. Весна 2016
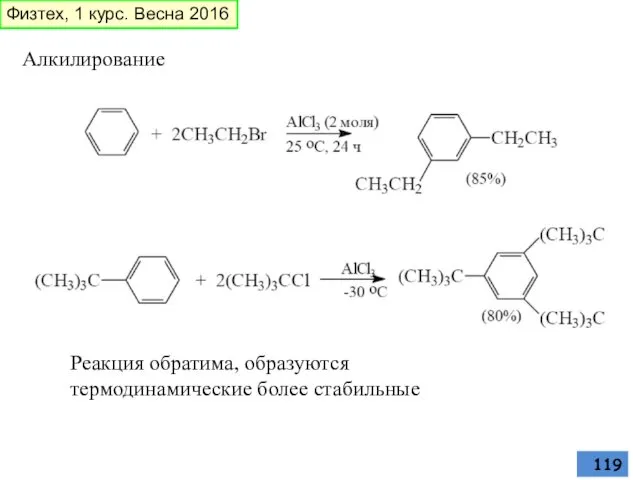
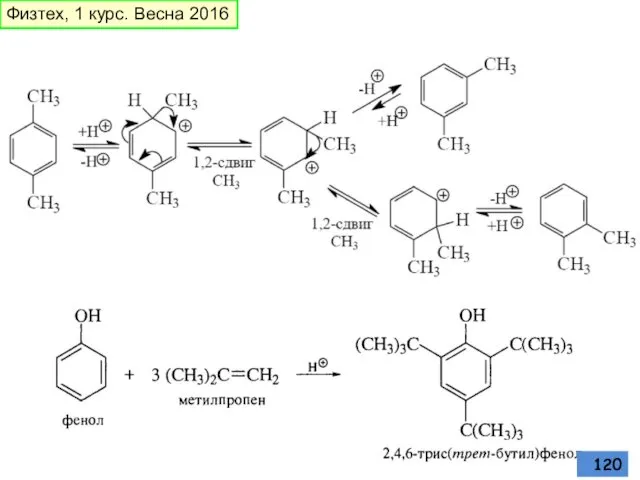
- 119. Алкилирование Реакция обратима, образуются термодинамические более стабильные Физтех, 1 курс. Весна 2016
- 120. Физтех, 1 курс. Весна 2016
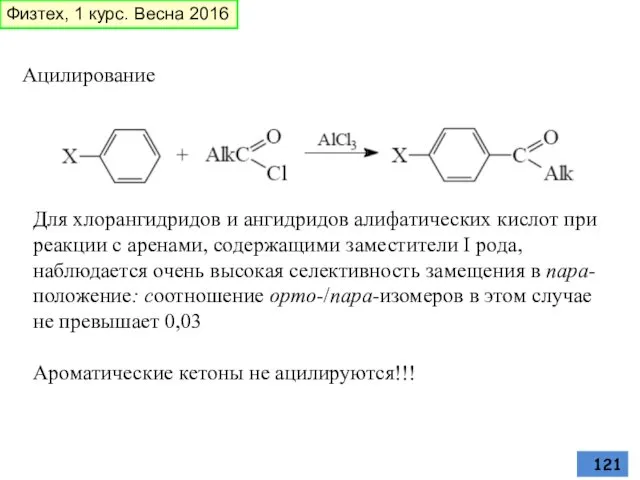
- 121. Ацилирование Для хлорангидридов и ангидридов алифатических кислот при реакции с аренами, содержащими заместители I рода, наблюдается
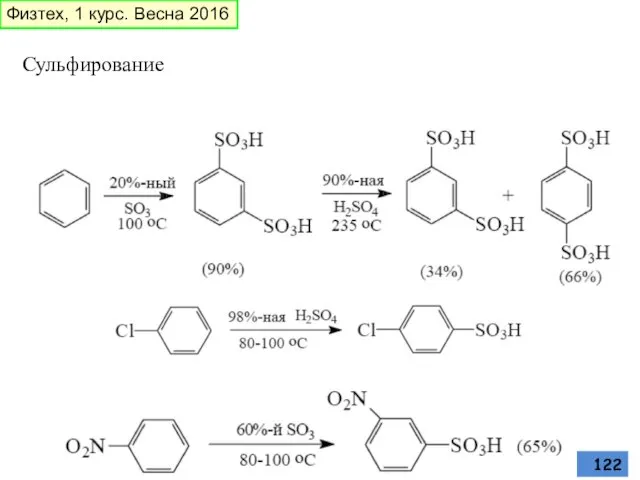
- 122. Сульфирование Физтех, 1 курс. Весна 2016
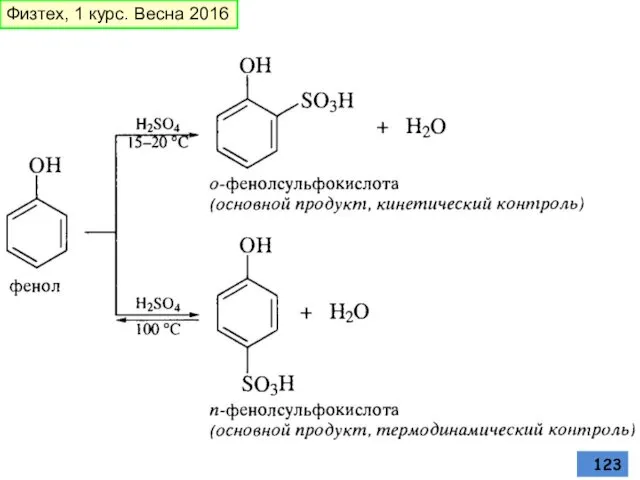
- 123. Физтех, 1 курс. Весна 2016
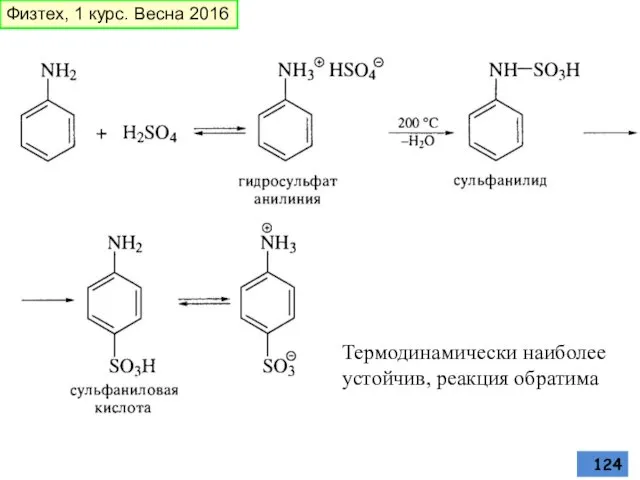
- 124. Термодинамически наиболее устойчив, реакция обратима Физтех, 1 курс. Весна 2016
- 125. Коротко о главном Химические свойства полиненасыщенных углеводородов – привязаны к «характеру-π-связи» и их взаимному влиянию. Алкины,
- 127. Скачать презентацию















 Презентация Сплавы металлов.
Презентация Сплавы металлов. N-(2-амино-3,5-дибромбензил)-N-метилциклогексанамина гидрохлорид
N-(2-амино-3,5-дибромбензил)-N-метилциклогексанамина гидрохлорид Азот
Азот Многоатомные спирты
Многоатомные спирты Фазовые диаграммы с протеканием 3-фазных реакций
Фазовые диаграммы с протеканием 3-фазных реакций Важнейшие химические понятия и законы
Важнейшие химические понятия и законы Макроэлементтер N,Cа,P
Макроэлементтер N,Cа,P Электрический ток в растворах и расплавах электролитов. Электролиз
Электрический ток в растворах и расплавах электролитов. Электролиз Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері
Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Обмен индивидуальных аминокислот
Обмен индивидуальных аминокислот Химическая термодинамика. Лекция 3
Химическая термодинамика. Лекция 3 Химия в сельском хозяйстве
Химия в сельском хозяйстве Значение химии в повседневной жизни
Значение химии в повседневной жизни Полимеры органические, неорганические
Полимеры органические, неорганические Щелочные и щелочно-земельные металлы Na K Li Cs Ba Rb Fr
Щелочные и щелочно-земельные металлы Na K Li Cs Ba Rb Fr  Углерод
Углерод Презентация по Химии "Дмитрий Иванович Менделеев - ученый с мировым именем" - скачать смотреть
Презентация по Химии "Дмитрий Иванович Менделеев - ученый с мировым именем" - скачать смотреть  Химическая связь
Химическая связь Эксперимент. Принципы теории планирования эксперимента. Классификация и виды экспериментов
Эксперимент. Принципы теории планирования эксперимента. Классификация и виды экспериментов Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные
Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные Аттестационная работа. Повышение квалификации учителей химии и биологии в организации проектно-исследовательской деятельности
Аттестационная работа. Повышение квалификации учителей химии и биологии в организации проектно-исследовательской деятельности Окисно-відновні реакції, процеси окиснення і відновлення, окисники і відновники
Окисно-відновні реакції, процеси окиснення і відновлення, окисники і відновники ОГЭ №1, вопрос 1-16
ОГЭ №1, вопрос 1-16 Хімічні добавки. Е-числа
Хімічні добавки. Е-числа  Метаболизм сложных белков. (Тема 2)
Метаболизм сложных белков. (Тема 2) Уреидтер және оның маңызы
Уреидтер және оның маңызы Презентация по Химии "Химия и сельское хозяйство. Пестициды" - скачать смотреть
Презентация по Химии "Химия и сельское хозяйство. Пестициды" - скачать смотреть