Содержание
- 2. Материалы Равновесные Неравновесные
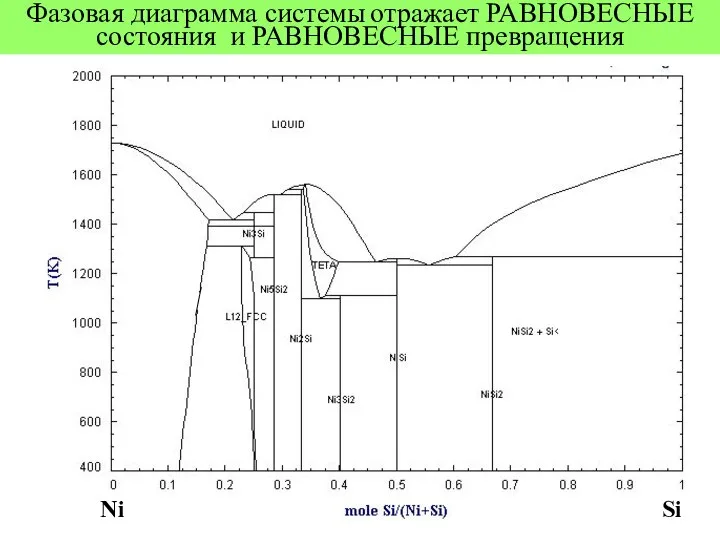
- 3. Фазовая диаграмма системы отражает РАВНОВЕСНЫЕ состояния и РАВНОВЕСНЫЕ превращения Ni Si
- 4. Правило Таммана: Диффузионные взаимодействия в твердофазных системах становятся возможными при Т ~> 0,6 Тпл
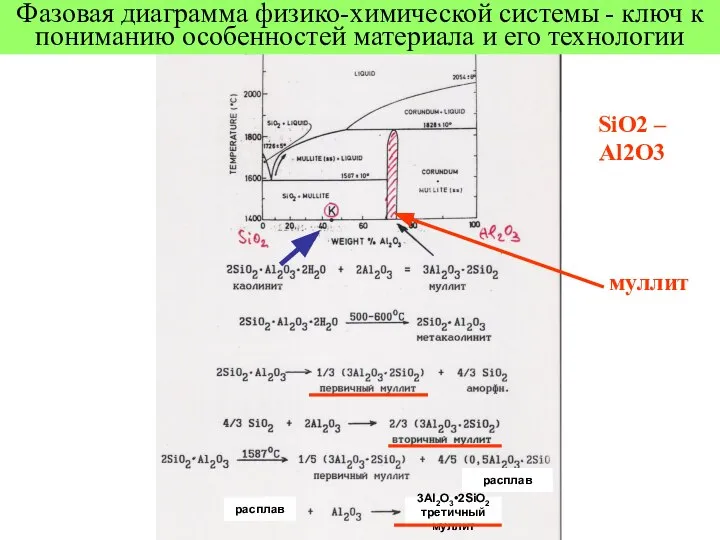
- 5. Фазовая диаграмма физико-химической системы - ключ к пониманию особенностей материала и его технологии 3Al2O3•2SiO2 третичный муллит
- 6. Физико-химическая система – совокупность выделенных из окружающей среды материальных объектов, между которыми возможен обмен энергией и
- 7. Гетерогенная система – физико-химическая система, содержащая поверхности раздела, на которых происходит скачкообразное изменение какого-либо свойства.
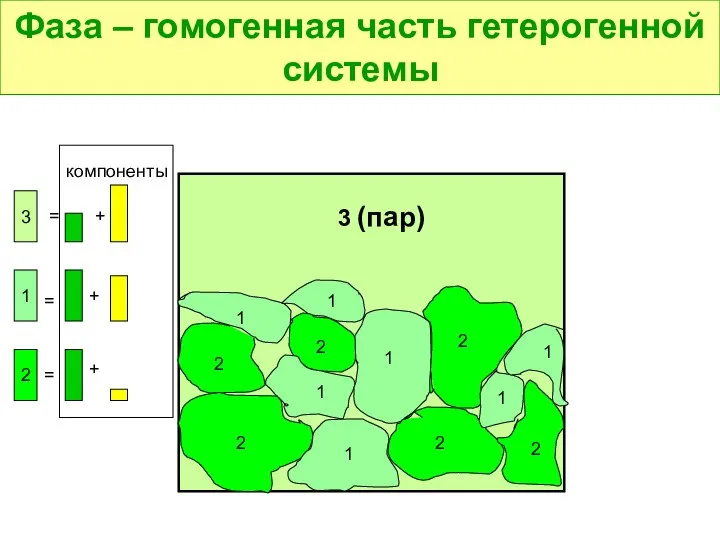
- 8. Фаза – гомогенная часть гетерогенной системы 1 1 1 1 1 1 1 2 2 2
- 9. Компоненты – индивидуальные вещества, составляющие систему. Число компонентов – минимальное число индивидуальных веществ , из которых
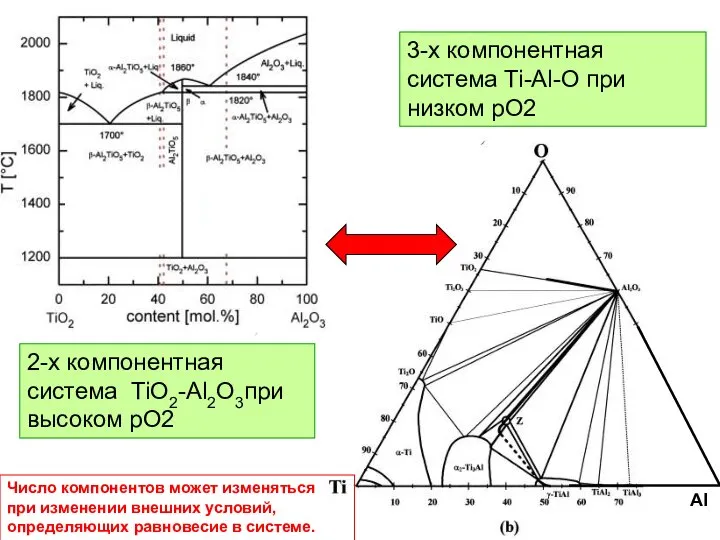
- 10. Al 2-х компонентная система TiO2-Al2O3при высоком рО2 3-х компонентная система Ti-Al-O при низком рО2 Число компонентов
- 11. Определение химического потенциала компонента μj = μjo + RTlnaj aj = γjcj Свободная энергия системы Число
- 12. Химическое равновесие гетерогенной системы достигается тогда, когда химические потенциалы каждого из компонентов равны во всех фазах
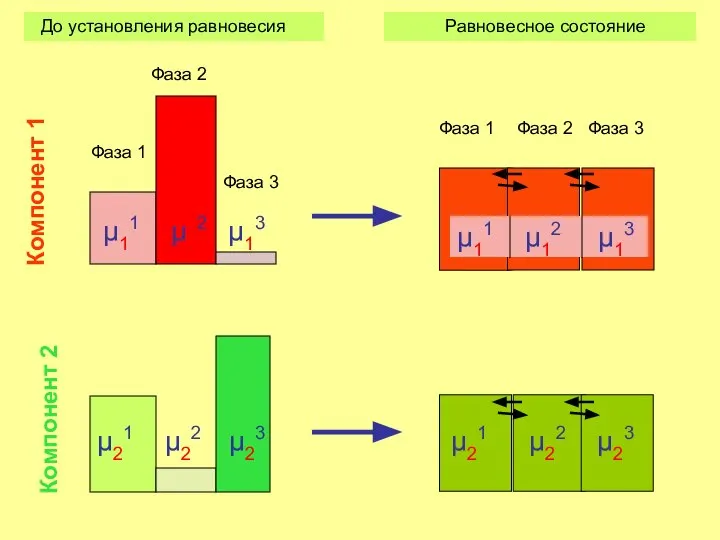
- 13. μ11 μ12 μ13 μ11 μ12 μ13 Фаза 1 Фаза 2 Фаза 3 Фаза 1 Фаза 2
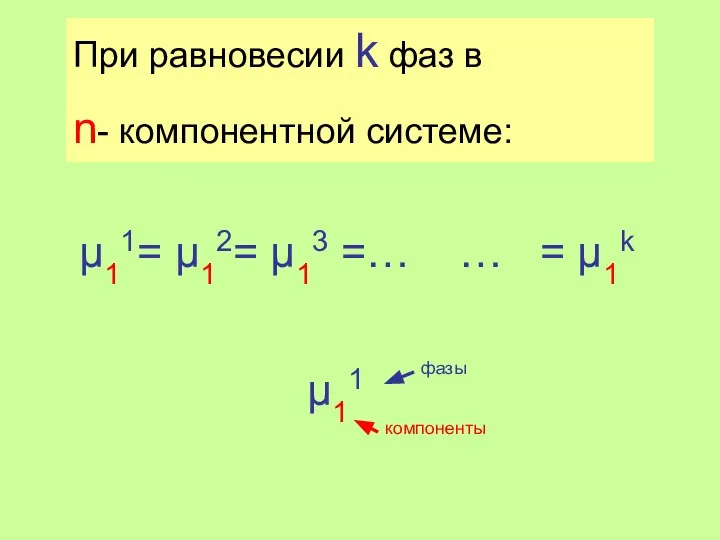
- 14. μ11= μ12= μ13 =… … = μ1k При равновесии k фаз в n- компонентной системе: μ11
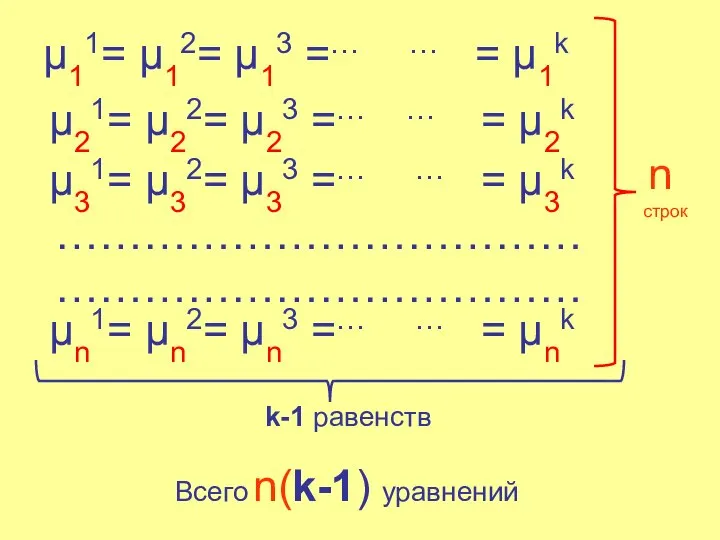
- 15. μ11= μ12= μ13 =… … = μ1k μ21= μ22= μ23 =… … = μ2k μ31= μ32=
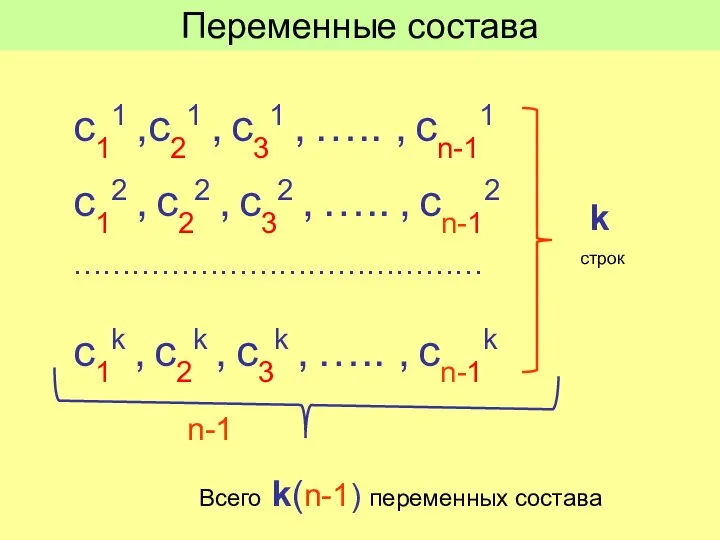
- 16. Система уравнений имеет определенное решение, если число уравнений равно числу переменных. Переменные: Состав равновесных фаз Температура
- 17. с11 ,с21 , с31 , ….. , cn-11 с12 , с22 , с32 , ….. ,
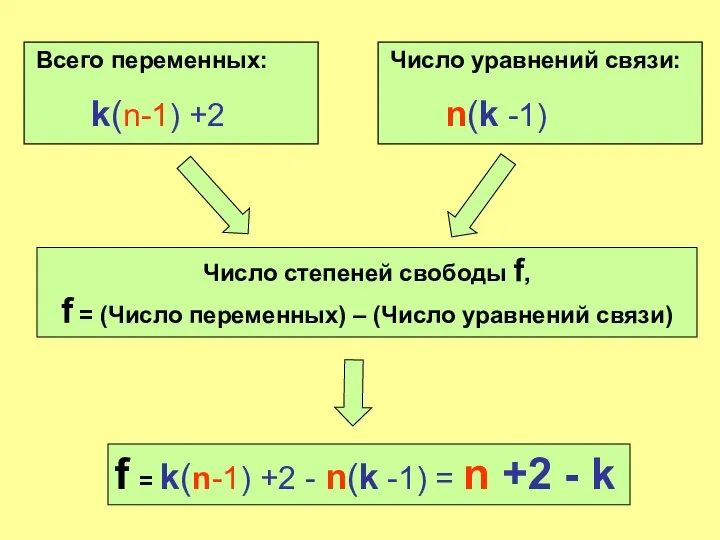
- 18. Всего переменных: k(n-1) +2 Число уравнений связи: n(k -1) Число степеней свободы f, f = (Число
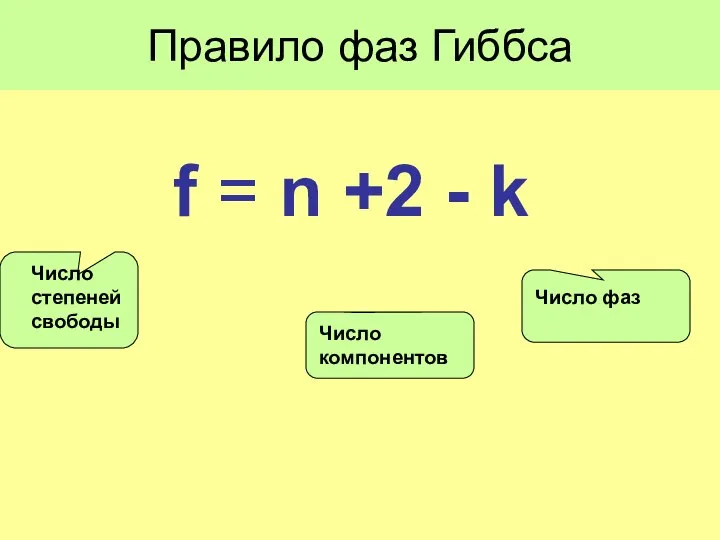
- 19. Правило фаз Гиббса f = n +2 - k Число фаз Число компонентов Число степеней свободы
- 20. Принцип соответствия Всякому комплексу фаз на диаграмме состояния соответствует свой геометрический образ, причем мерность этого образа
- 21. Фазовые диаграммы однокомпонентных систем
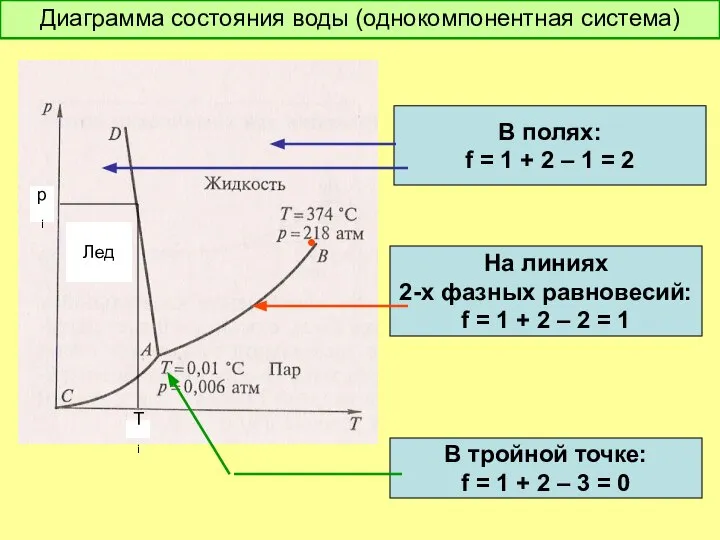
- 22. Диаграмма состояния воды (однокомпонентная система) • Лед pi Ti В полях: f = 1 + 2
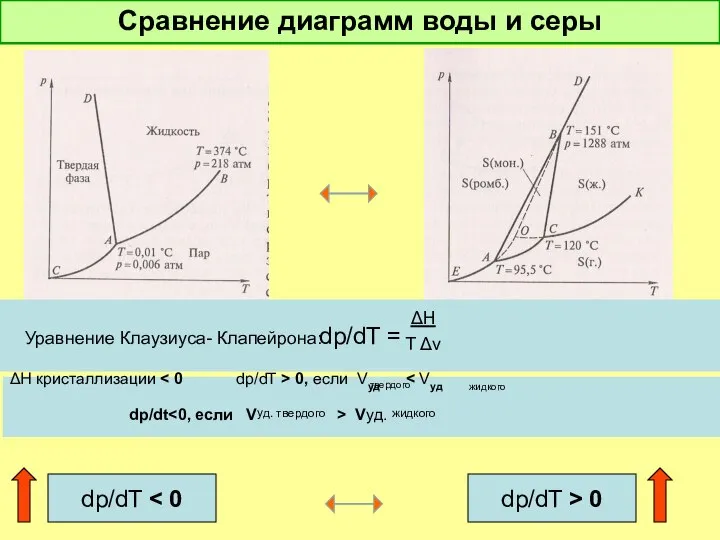
- 23. Сравнение диаграмм воды и серы dp/dT = Уравнение Клаузиуса- Клапейрона: ΔH T Δv ΔH кристаллизации 0,
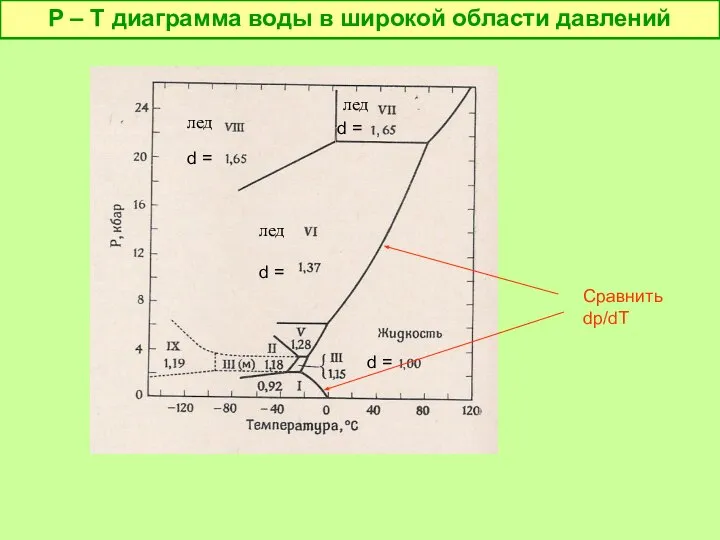
- 24. P – T диаграмма воды в широкой области давлений Сравнить dp/dT лед лед лед d =
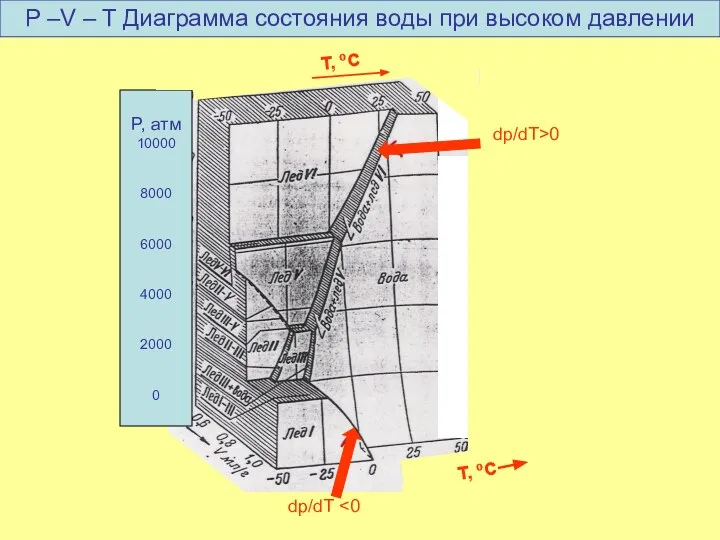
- 25. dp/dT T, oC P, атм 10000 8000 6000 4000 2000 0 T, oC dp/dT>0 P –V
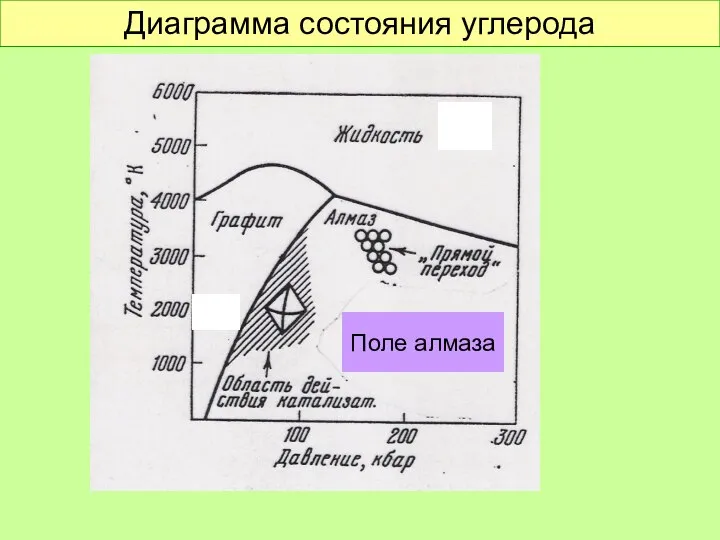
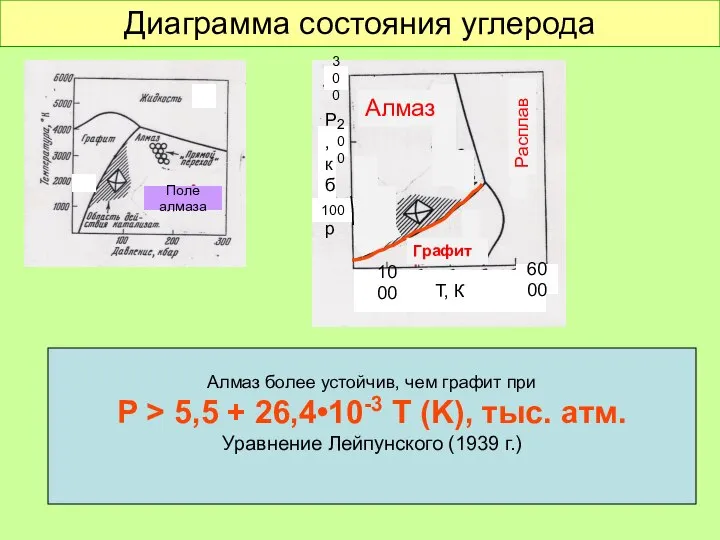
- 26. Диаграмма состояния углерода Поле алмаза
- 27. Диаграмма состояния углерода Поле алмаза Т, К 1000 6000 Р, кбар 300 200 100 Алмаз более
- 28. Цех установок роста алмазов Установка роста алмазов
- 29. Искусственные алмазы ювелирного качества
- 30. Синтетические алмазы используются в бурении горных пород, металлообработке. Алмазные полировочные пасты
- 31. Разновидности графитовых материалов
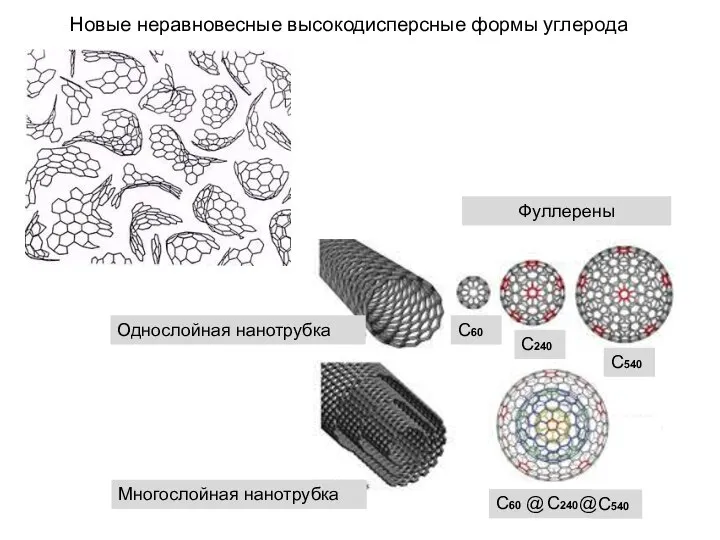
- 32. Новые неравновесные высокодисперсные формы углерода Однослойная нанотрубка Многослойная нанотрубка Фуллерены С60 С240 С540 С60 С240 С540
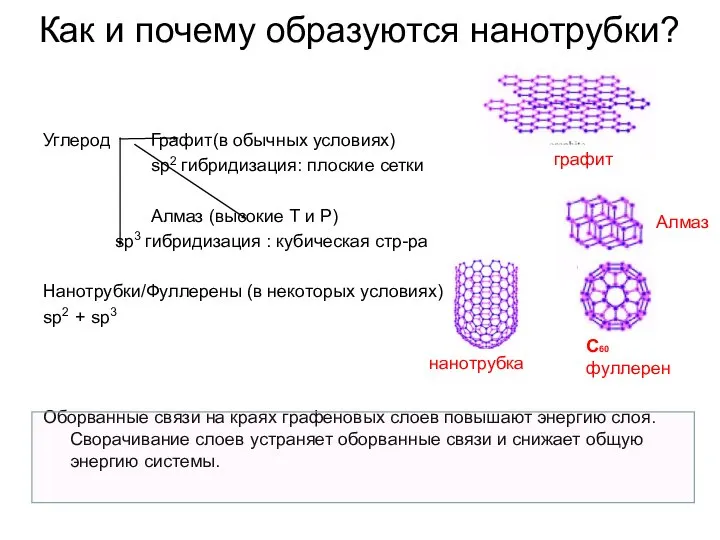
- 33. Как и почему образуются нанотрубки? Углерод Графит(в обычных условиях) sp2 гибридизация: плоские сетки Алмаз (высокие Т
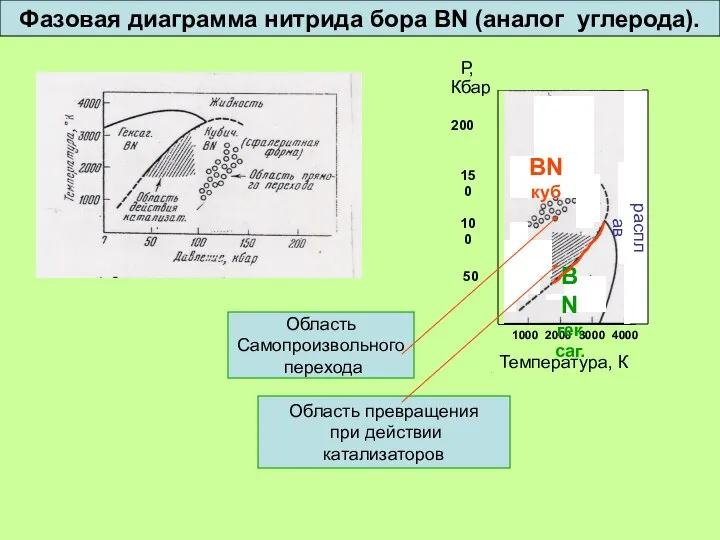
- 34. 1000 2000 3000 4000 Температура, К Р, Кбар 200 150 100 50 BN куб BN гексаг.
- 35. Кубический нитрид бора – высокотвердый материал для режущих инструментов BN, в отличие от алмаза, инертен по
- 36. Двухкомпонентные (бинарные) системы
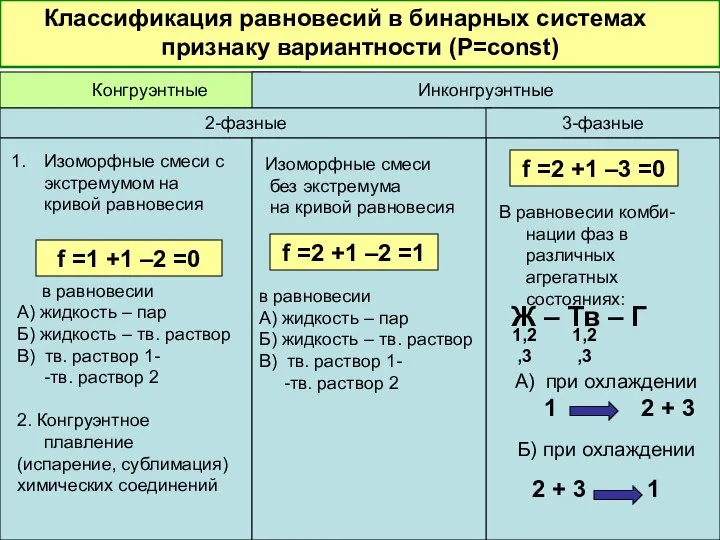
- 37. Классификация равновесий в бинарных системах по признаку вариантности (Р=const) Конгруэнтные Инконгруэнтные 2-фазные 3-фазные в равновесии А)
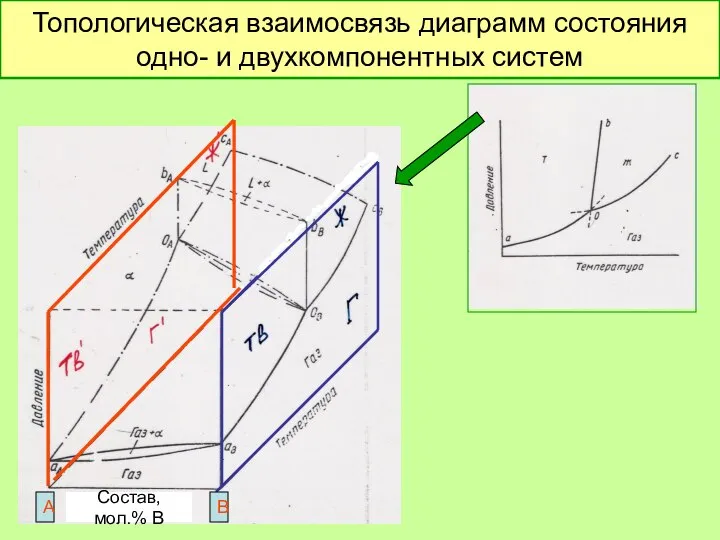
- 38. Топологическая взаимосвязь диаграмм состояния одно- и двухкомпонентных систем Состав, мол.% В А В
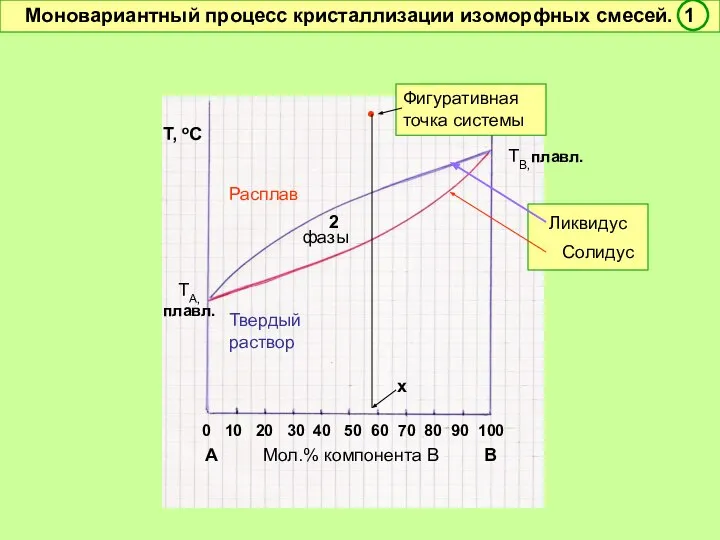
- 39. А Мол.% компонента В В Т, оС Расплав Твердый раствор А Мол.% компонента В В Т,
- 40. 0 10 20 30 40 50 60 70 80 90 100 А Мол.% компонента В В
- 41. 0 10 20 30 40 50 60 70 80 90 100 А Мол.% компонента В В
- 42. 0 10 20 30 40 50 60 70 80 90 100 А Мол.% компонента В В
- 43. 0 10 20 30 40 50 60 70 80 90 100 А Мол.% компонента В В
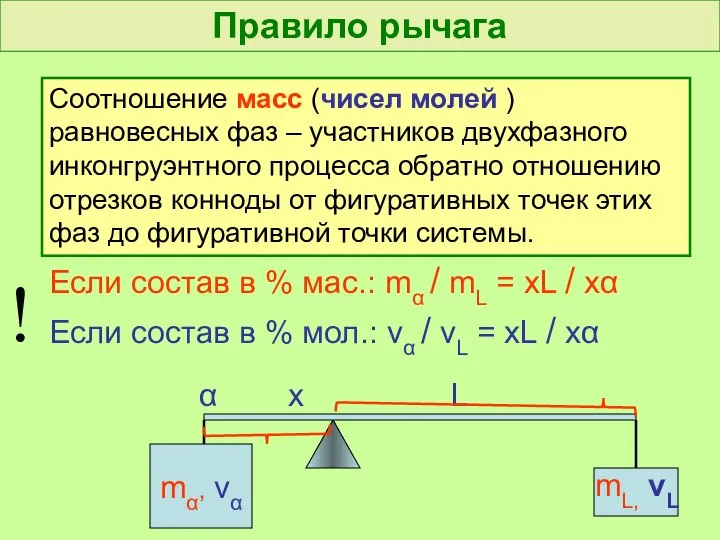
- 44. Правило рычага Соотношение масс (чисел молей ) равновесных фаз – участников двухфазного инконгруэнтного процесса обратно отношению
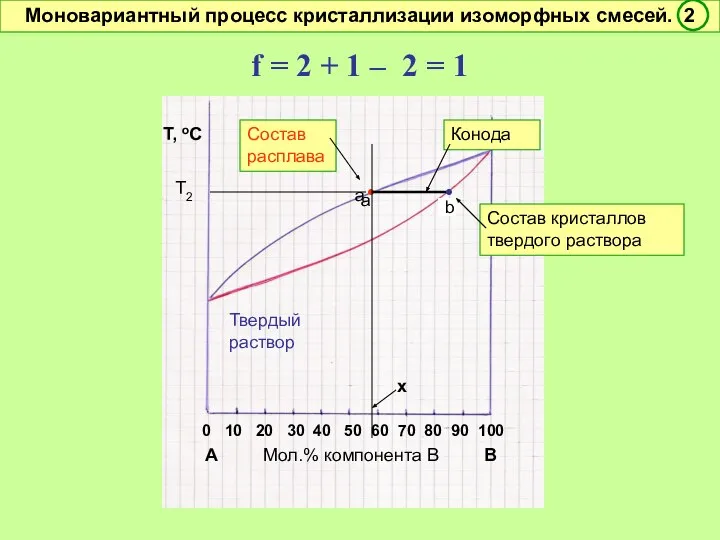
- 45. 0 10 20 30 40 50 60 70 80 90 100 А Мол.% компонента В В
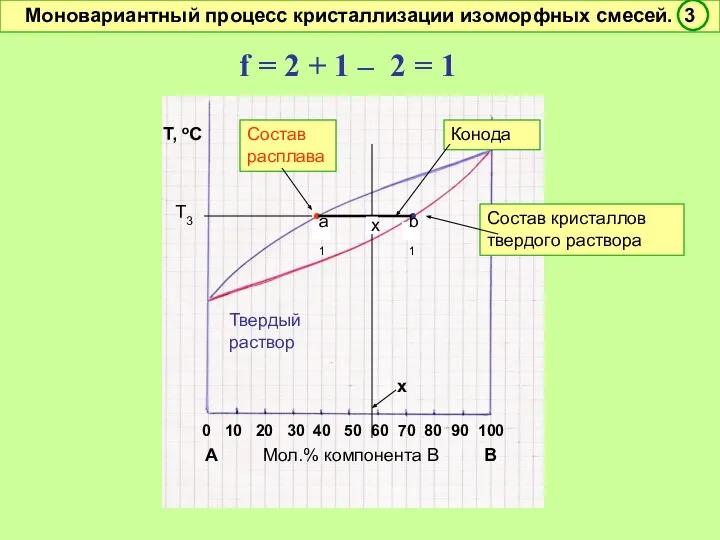
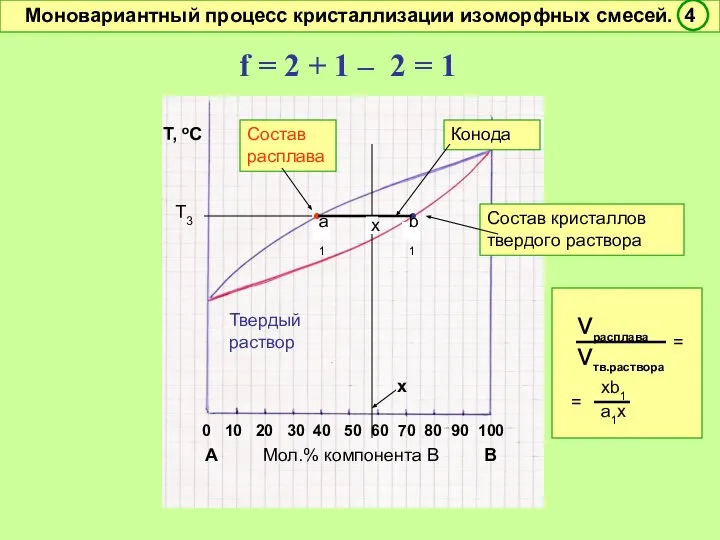
- 46. 0 10 20 30 40 50 60 70 80 90 100 А Мол.% компонента В В
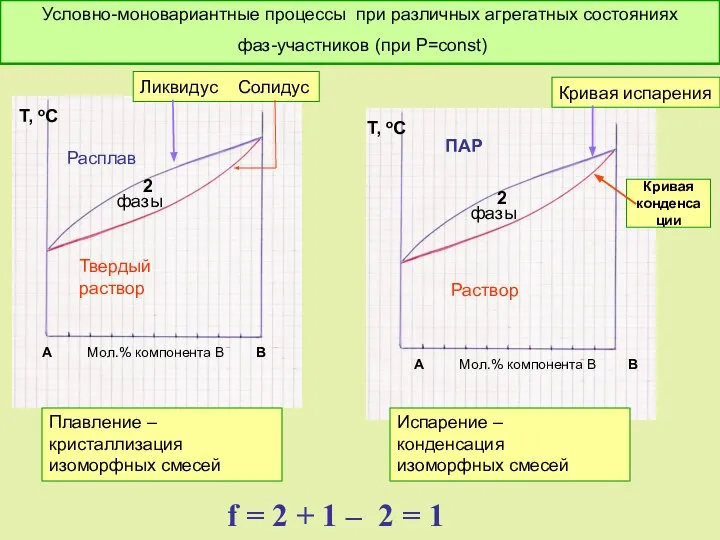
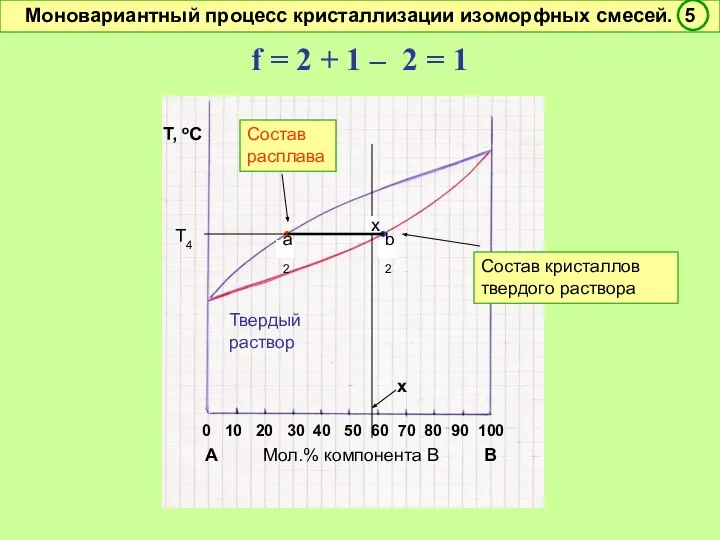
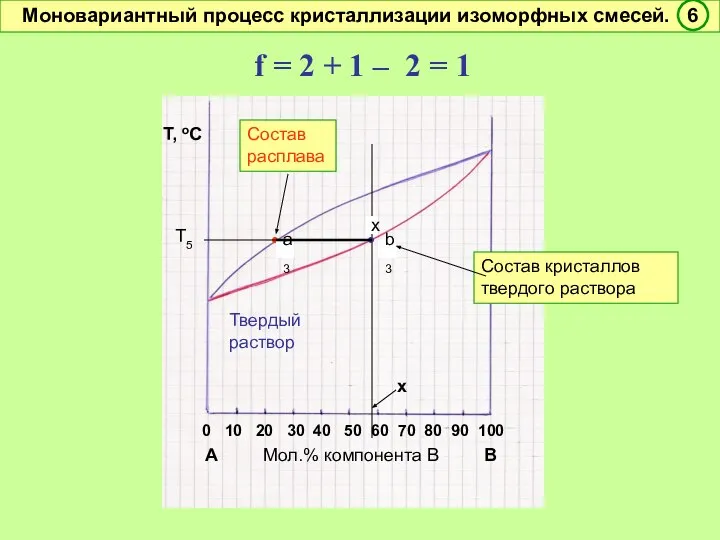
- 47. f = 2 + 1 – 2 = 1 Условно моновариантное превращение. Смысл моновариантности (f =
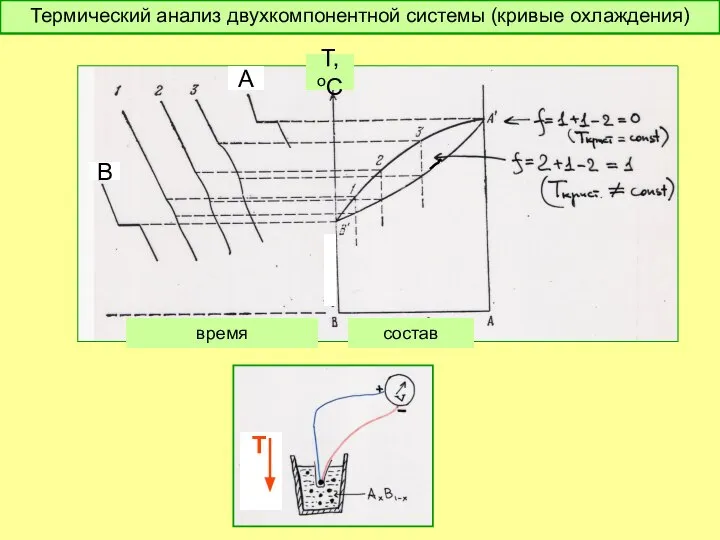
- 48. время В А состав Т,оС Термический анализ двухкомпонентной системы (кривые охлаждения) Т
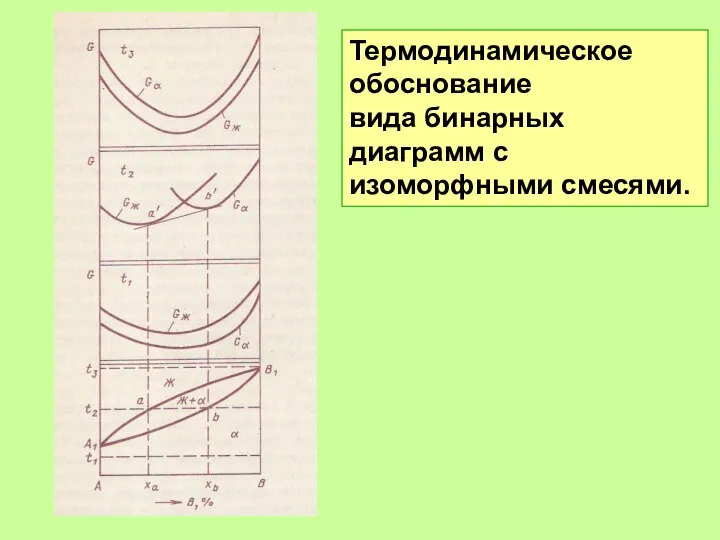
- 49. Термодинамическое обоснование вида бинарных диаграмм с изоморфными смесями.
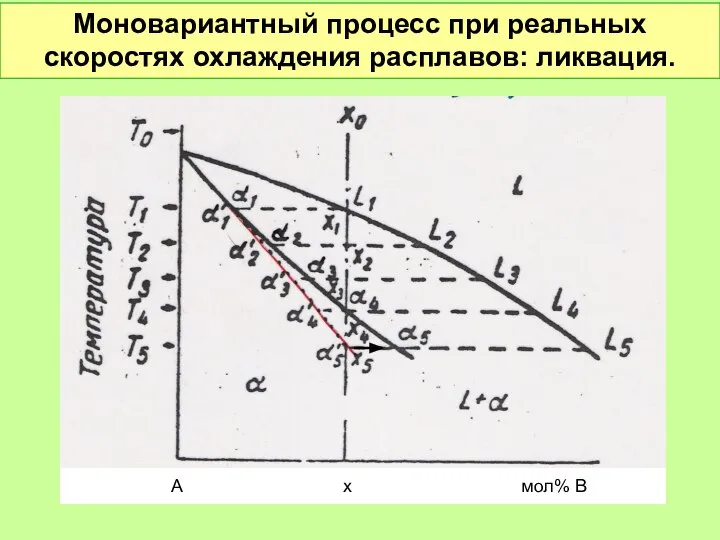
- 50. Моновариантный процесс при реальных скоростях охлаждения расплавов: ликвация. А х мол% В
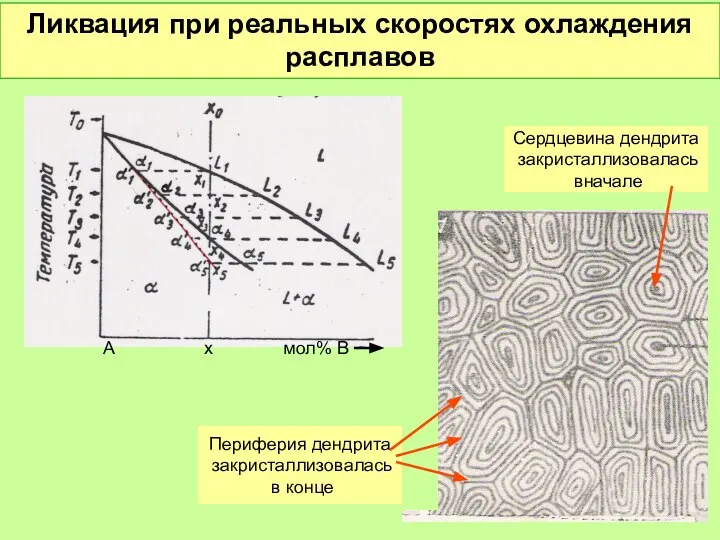
- 51. Ликвация при реальных скоростях охлаждения расплавов А х мол% В Сердцевина дендрита закристаллизовалась вначале Периферия дендрита
- 52. Диффузионный отжиг ликвидирует последствия ликвации Микроструктура сплава Ni0,7Cu0,3 . Увеличение 100 До отжига После отжига Обогащено
- 53. При ликвации остатки расплава сохраняются до T При нагреве сплавов, подвергшихся ликвации, расплав появляется при T
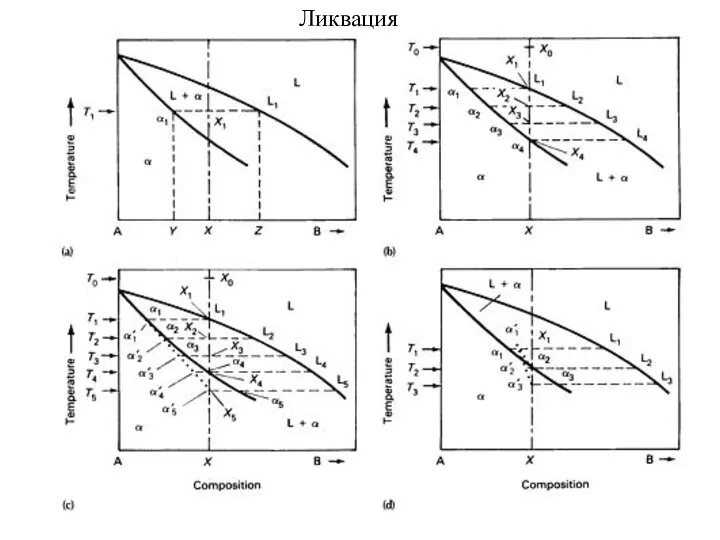
- 54. Ликвация
- 56. Скачать презентацию

















 Сероводоро́д, сернистый водород (H2S) (физические свойства)
Сероводоро́д, сернистый водород (H2S) (физические свойства) Автомобильные трансмиссионные масла
Автомобильные трансмиссионные масла Композиційні матеріали на основі функціоналізованих олігодієнів, вінілових мономерів і наповнювачів різної природи
Композиційні матеріали на основі функціоналізованих олігодієнів, вінілових мономерів і наповнювачів різної природи Теоретические основы рентгенофлуоресцентного метода анализа. (Лекция 7)
Теоретические основы рентгенофлуоресцентного метода анализа. (Лекция 7) Презентация Карбоновые кислоты и их производные
Презентация Карбоновые кислоты и их производные Происхождение жизни на Земле. Процесс химической эволюции
Происхождение жизни на Земле. Процесс химической эволюции Функциональные производные с кратной связью C=“Э”. Часть 1. Карбонильные соединения и имины
Функциональные производные с кратной связью C=“Э”. Часть 1. Карбонильные соединения и имины Органическая химия. Классификация кислот
Органическая химия. Классификация кислот Превращение веществ
Превращение веществ Аналитическая химия. Количественный анализ
Аналитическая химия. Количественный анализ Общая химия. Часть 1
Общая химия. Часть 1 Органическая химия
Органическая химия Основные классы неорганических соединений
Основные классы неорганических соединений Молекулы и атомы (часть 2)
Молекулы и атомы (часть 2) Липиды. Химия липидов. Переваривание липидов в ЖКТ. Нарушение переваривания и всасывания
Липиды. Химия липидов. Переваривание липидов в ЖКТ. Нарушение переваривания и всасывания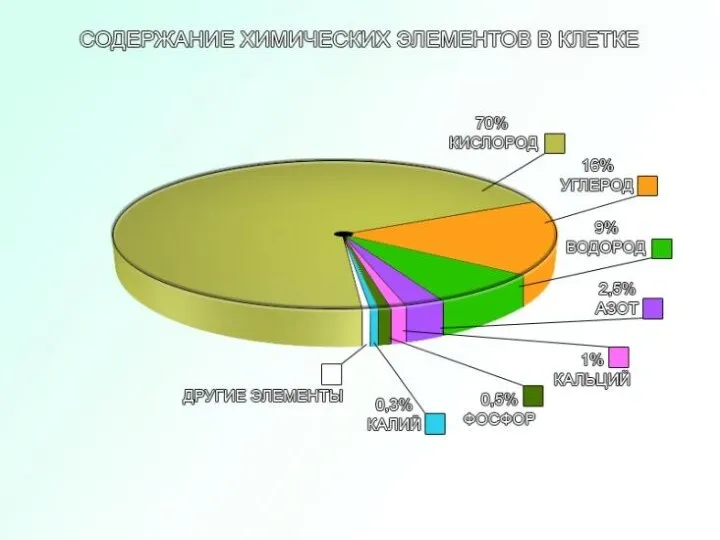 Содержание химических элементов в клетке
Содержание химических элементов в клетке Набор № 3 ВС "Щелочи"
Набор № 3 ВС "Щелочи" Обмен триацилглицеролов и жирных кислот
Обмен триацилглицеролов и жирных кислот СПИРТЫ
СПИРТЫ  Химия вокруг нас Презентация к внеклассному мероприятию Альбина Фанузовна Хамидуллина учитель химии первой квалификационно
Химия вокруг нас Презентация к внеклассному мероприятию Альбина Фанузовна Хамидуллина учитель химии первой квалификационно Жиры – биологически важные органические соединения Работа ученицы 11а класса МБОУ СОШ № 26 Ногинского района Московской облас
Жиры – биологически важные органические соединения Работа ученицы 11а класса МБОУ СОШ № 26 Ногинского района Московской облас Гидролиз солей
Гидролиз солей Резины – эластомеры
Резины – эластомеры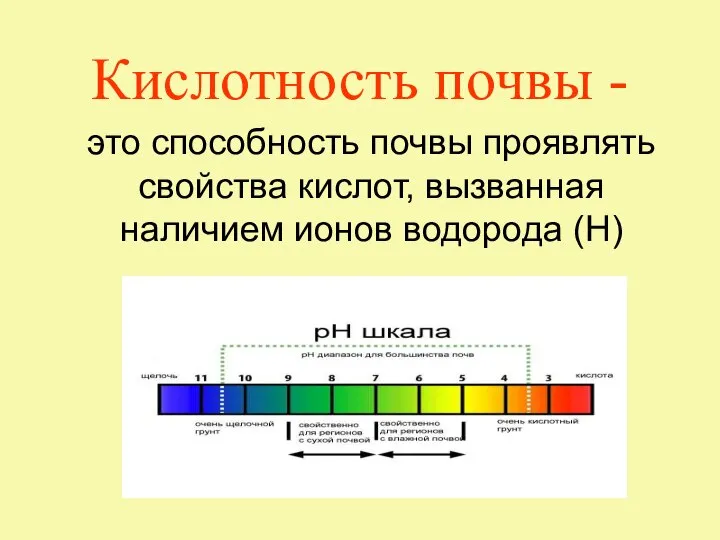 Кислотность почвы
Кислотность почвы Термодинамика. 2 закон термодинамики. Энтропия
Термодинамика. 2 закон термодинамики. Энтропия Силоксановый каучук
Силоксановый каучук Гигиеническое нормирование. Принципы гигиенического нормирования
Гигиеническое нормирование. Принципы гигиенического нормирования Теория строения органических соединений А.М. Бутлерова. Классы органических соединений. Тема 1
Теория строения органических соединений А.М. Бутлерова. Классы органических соединений. Тема 1