Содержание
- 2. Тест – экспресс 1) Электронная конфигурация атома углерода 2) Разновидности простого вещества, образованные одним и тем
- 4. КАРБОНАТЫ – СОЛИ УГОЛЬНОЙ КИСЛОТЫ СРЕДНИЕ КАРБОНАТЫ Na2CO3 КИСЛЫЕ ГИДРОКАРБОНАТЫ NaHCO3
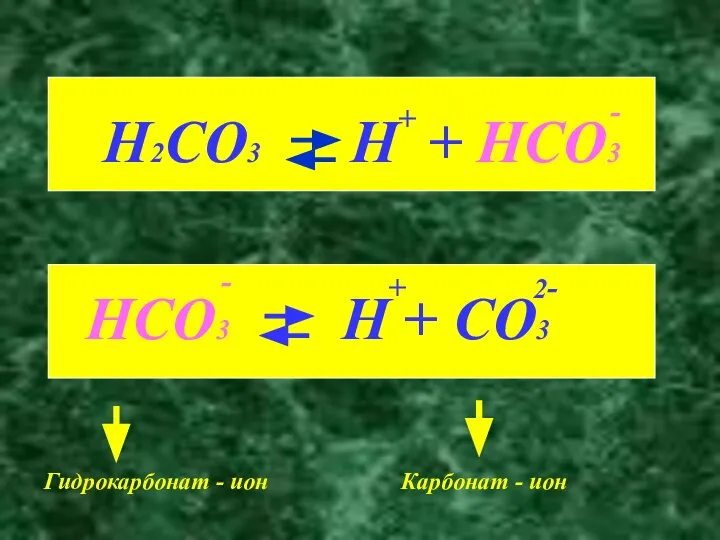
- 5. Гидрокарбонат - ион Карбонат - ион
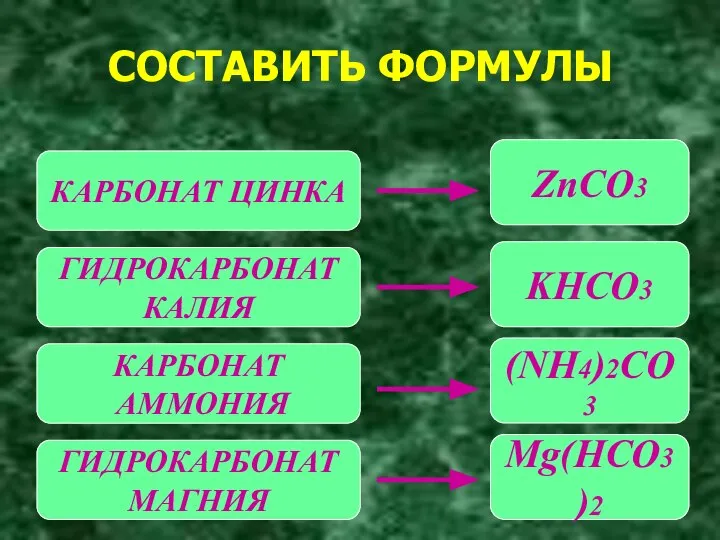
- 6. СОСТАВИТЬ ФОРМУЛЫ КАРБОНАТ ЦИНКА ГИДРОКАРБОНАТ КАЛИЯ КАРБОНАТ АММОНИЯ ГИДРОКАРБОНАТ МАГНИЯ ZnCO3 KHCO3 (NH4)2CO3 Mg(HCO3)2
- 8. Ca(OH)2+CO2 CaCO3 +H2O CaCO3+CO2+H2O Ca(HCO3)2 Получение карбонатов, гидрокарбонатов
- 9. Взаимодействие с сильными кислотами CaCO3+2HCl = CaCl2 +H2O+CO2 Качественные реакции
- 10. Превращение гидрокарбонатов в карбонаты а) при нагревании 2NaHCO3 Na2CO3 + H2O+CO2 б) при действии щёлочи NaHCO3
- 11. Na2 CO3+BaCl2 BaCO3 +2NaCl Взаимодействие с растворами солей Разложение карбонатов MgCO3 MgO + CO2
- 12. ОСУЩЕСТВИТЕ ПРЕВРАЩЕНИЕ I. Ca(OH)2 CaCO3 Ca(HCO3)2 II. NaOH Na2CO3 NaHCO3 III. Na2CO3 BaCO3 CO2
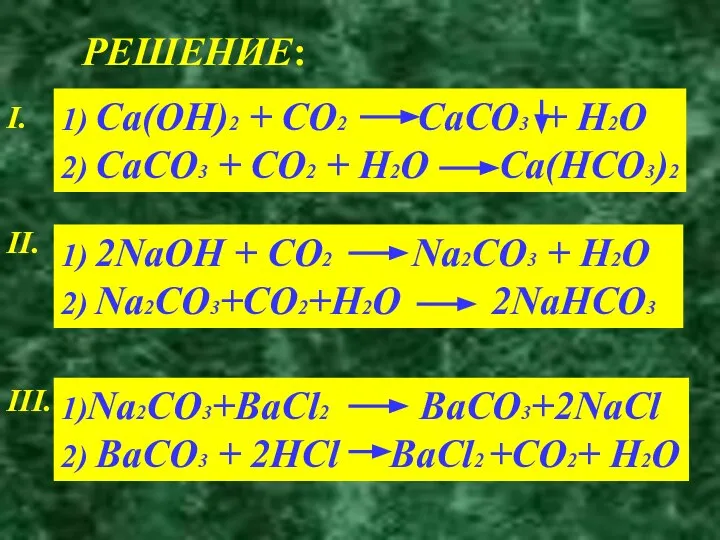
- 13. РЕШЕНИЕ: I. 1) Ca(OH)2 + CO2 CaCO3 + H2O 2) CaCO3 + CO2 + H2O Ca(HCO3)2
- 14. 1,7% земной коры – карбонатные породы
- 15. КОРАЛЛОВЫЕ ПОЛИПЫ – CaCO3
- 16. CaCO3+CO2+H2O Ca(HCO3)2 Ca(HCO3)2 CaCO3 + H2O +CO2
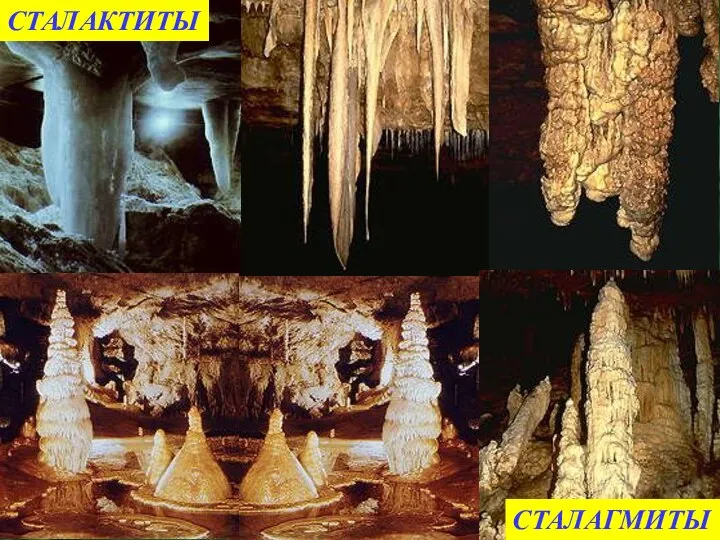
- 17. СТАЛАКТИТЫ СТАЛАГМИТЫ
- 18. Применение
- 19. ИЗВЕСТНЯК – CaCO3
- 20. Малахит Cu2(ОН)2CO3 – хрупкий, цвет ярко-зеленый, темно-зеленый, блестит. Из него изготовляют художественно-декоративные предметы,используют для получения меди.
- 22. Кальцинированная сода Na2CO3– белый порошок, используется в производстве стекла, мыла, бумаги, моющих средств.
- 23. Na HCO3 – ПИТЬЕВАЯ СОДА NaHCO3 + HCl = NaCl + CO2 + H2O
- 25. 1)Какие минералы содержат кальций карбонат? Мрамор, известняк, мел. 2) Зачем хозяйки добавляют питьевую соду в тесто?
- 26. 3) Что такое сталактиты? Каменные сосульки в пещерах состоящие из карбоната кальция. 4) Как химическим путем
- 28. Скачать презентацию





















 Сложные эфиры
Сложные эфиры Лекция 6 Нарушения кислотнощелочного равновесия ацидозы, алкалозы
Лекция 6 Нарушения кислотнощелочного равновесия ацидозы, алкалозы Тұздар. Құрамы және химиялық қасиеттері
Тұздар. Құрамы және химиялық қасиеттері Научные принципы химического производства. Производство аммиака
Научные принципы химического производства. Производство аммиака Углерод и 4 группа
Углерод и 4 группа Способы количественного определения белка
Способы количественного определения белка Поверхневі явища. Адсорбція
Поверхневі явища. Адсорбція Теория строения химических соединений А. М. Бутлерова
Теория строения химических соединений А. М. Бутлерова МИР ИНДИКАТОРОВ
МИР ИНДИКАТОРОВ Презентация по Химии "Органічні сполуки і здоров’я людини." - скачать смотреть бесплатно
Презентация по Химии "Органічні сполуки і здоров’я людини." - скачать смотреть бесплатно Ионная, металлическая, водородная связь
Ионная, металлическая, водородная связь Растворы
Растворы Презентация по Химии "Карбоновые кислоты 10 класс" - скачать смотреть
Презентация по Химии "Карбоновые кислоты 10 класс" - скачать смотреть  Скорость химической реакции. Порядок и молекулярность реакции. Катализ
Скорость химической реакции. Порядок и молекулярность реакции. Катализ Пиролиз углеводородного сырья
Пиролиз углеводородного сырья Свойства химических элементов
Свойства химических элементов ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»
ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»  Химия, как наука. Основные понятия и законы
Химия, как наука. Основные понятия и законы Изотопы. Химические и физические свойства
Изотопы. Химические и физические свойства Фізичні методи дослідження хімічних сполук
Фізичні методи дослідження хімічних сполук Растворы электролитов
Растворы электролитов Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Химический элемент водород
Химический элемент водород Химия гетероциклических соединений
Химия гетероциклических соединений Мұнай құрамындағы тұздың мөлшерін анықтау
Мұнай құрамындағы тұздың мөлшерін анықтау Гидролиз солей
Гидролиз солей Дослідження на тему: Історія назви міста За проектом “Екологічна ситуація у рідному місті”
Дослідження на тему: Історія назви міста За проектом “Екологічна ситуація у рідному місті” Сульфиды. Лекция 8
Сульфиды. Лекция 8