Содержание
- 2. Катионы IV аналитической группы Al+3 Cr+3 Zn+2
- 3. Общая характеристика катионов В состав IV аналитической группы входят катионы р-элементов главной подгруппы III ( Al+3)
- 4. Применение в медицине: ZnSO4 x 7H2О – применяют как антисептическое и вяжущее средство в виде глазных
- 5. Качественные реакции на катионы IV аналитической группы
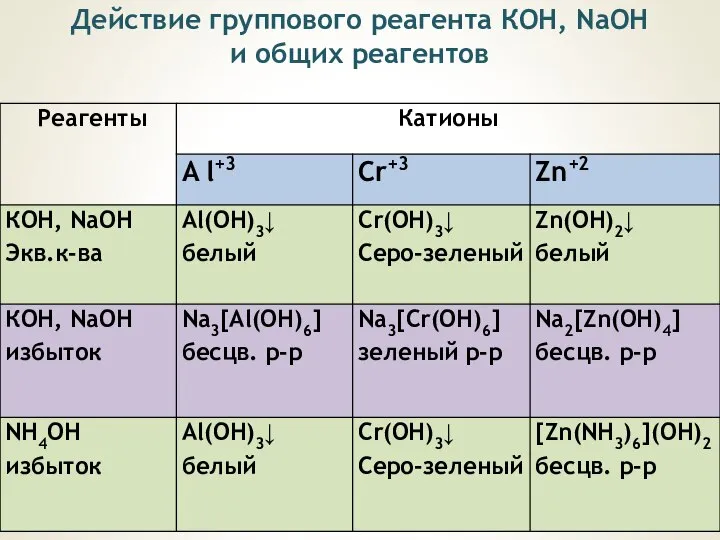
- 6. Действие группового реагента КОН, NаОН и общих реагентов
- 7. Гидроксиды алюминия и цинка растворяются в соляной кислоте с образованием растворов солей: Al(OH)3 + 3HCl =
- 8. ХАРАКТЕРНЫЕ РЕАКЦИИ НА КАТИОН Al3+
- 9. 1.Реакция с ализарином: AlCl3 + 3NН4ОН + С14Н6О2(ОН)2 = Al(OH)2С14Н6О2(ОН)↓ + 3NН4Cl + H2O С14Н6(ОН)2 –
- 10. 2. Реакция с нитратом кобальта: пирохимический метод (полоску фильтровальной бумаги смачивают растворами Al2 (SO4)3 и Co(NO3)2,
- 11. 3. Реакция с ацетатом натрия: AlCl3+3СН3СООNа+H2O= Al(OH)2СН3СОО↓ + 3NаCl + 2СН3СООН При кипячении раствора солей алюминия
- 12. ХАРАКТЕРНЫЕ РЕАКЦИИ НА КАТИОН Zn2+
- 13. 1. Реакция с аммиаком: ZnCl2+2NH4OH=Zn(OH)2↓+2NH4Cl Белый осадок, растворяется в избытке аммиака Zn(OH)2+4NH4OHизб.=[Zn(NH3)4](OH)2+ 4H2O
- 14. 2. Реакция с гексоцианоферратом (II) калия(желтой кровяной солью): ZnSO4 + K4[Fe(CN)6] = К2Zn[Fe(CN)6]↓ + K2SO4 -
- 15. 3. Реакция с нитратом кобальта: пирохимический метод (полоску фильтровальной бумаги смачивают растворами Zn(NO3)2 и Co(NO3)2, подсушивают
- 16. 4. Реакция микрокристаллоскопическая с тетратиоцианомеркуратом аммония (NН4)2[Нg(SCN)4 ]: ZnСl2 + (NН4)2[Нg(SCN)4]= Zn[Нg(SCN)4]↓ + 2NН4Сl - с
- 17. Качественные реакции на катионы V аналитической группы Fe+3 Fe+2 Mg+2 Mn+2
- 18. Общая характеристика катионов В состав V аналитической группы входят катионы s-и d- элементов. Mg+2 – s-
- 19. Применение в медицине: MgSO4 – как слабительное средство, как спазмолитическое средство при гипертонической болезни, в качестве
- 20. Действие группового реагента NaОН и общих реагентов
- 21. Характерные реакции на катионы V аналитической группы
- 22. Характерные реакции на катион Fe+2
- 23. Действие гексацианоферрата (III) калия K3[Fe(CN)6]. (красная кровяная соль, фармакопейная): 3FeCl2 + 3K3[Fe(CN)6] = Fe3[Fe(CN)6] 2↓+ 6KCl
- 24. 2. С водным раствором аммиака FeSO4 +2NH4OH=Fe(OH)2↓ + (NH4)2SO4 Зеленый осадок, буреет
- 25. 4. Реакция с перманганатом калия КМnО4 в кислой среде: 10FeSО4 + 2КМnО4 + 8Н2SО4 = 2МnSО4
- 26. На катион Fe +3 1. Действие гексацианоферрата (II) калия K4[Fe(CN)6] (жёлтая кровяная соль, фармакопейная): 4FeCl3 +
- 27. Действие роданидом аммония NH4CNS (фармакопейная): Для достижения положительного результата необходим избыток реактива. Образуется роданид железа (III)
- 28. 3. Реакция окисления- восстановления с иодидом калия КJ: 2 FeCl3 +2KJ = 2 FeCl2 + 2KCl
- 29. Характерные реакции на катион Mn 2+
- 30. 1. Окисление пероксидом свинца PbO2 2MnSO4 + 5PbO2 + 6HNO3 = 2HMnO4 + 2PbSO4 + 3Pb(NO3)2
- 31. Характерные реакции на катион Mg2+
- 32. 1. Реакция с гидрофосфатом натрия Na2HPO4, реакция фармакопейная: MgСl2 + Na2HPO4 + NH4ОН = MgNH4PO4↓ +
- 33. 2. Реакция с гидроксидом натрия и йодом: MgSO4 + 2NaOH+I2 = [Mg(OH)2]I2 + Na2SO4 Происходит обесцвечивание,
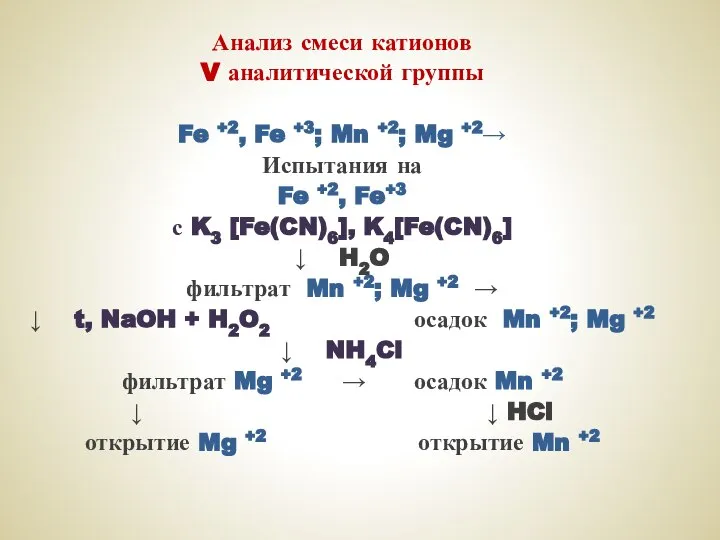
- 34. Анализ смеси катионов V аналитической группы Fe +2, Fe +3; Mn +2; Mg +2→ Испытания на
- 35. Качественные реакции на катионы VI аналитической группы Cu+2 Hg+2
- 36. Общая характеристика катионов Hg+2, Cu+2 Все катионы VI аналитической группы являются простыми катионами d –элементов, которые
- 37. Применение в медицине CuSO4 ٠ 5 H2O – рвотное средство HgCl2 – сулема очень ядовита, поэтому
- 38. Качественные реакции на катион Cu+2
- 39. Катион Cu2+ 1. Действие группового реагента гидроксида аммония 2CuSO4 +2NH4OH =( CuOH)2SO4↓ + (NH4)2SO4 при недостатке
- 40. CuSO4 +4NH4OH =[Cu(NH3)4]SO4 + 4H2O - при добавлении избытка раствора аммиака наблюдается темно-синее окрашивание раствора в
- 41. Характерные реакции на катион Cu+ 2
- 42. 1. Действие гексоцианоферрата (II) калия K4Fe(CN)6 (жёлтая кровяная соль) 2CuSO4 + K4[Fe(CN)6] = Cu2[Fe(CN)6]↓ + 2K2SO4
- 43. 2. Действие недостатком тиосульфата натрия: 2 СuSO4 + Na2S2O3(недостаток) = Na2SO4 + СuS2O3 СuS2O3 +Н2О =
- 44. 3. Реакция с избытком тиосульфатом натрия Na2S2O3: CuSO4 +4Na2S2O3(избыток) = 3Na2SO4 + Na2S4O6 + Cu2S↓ +
- 45. 4. Восстановление иона Cu2+ до металлической меди (фармакопейная): CuSO4 + Fe = Cu + FeSO4 Cu2+
- 46. 5. Реакция с гидроксидом натрия NаОН: CuSO4 + NаОН = Cu(OH)2↓ + Na2SO4 – образуется голубой
- 47. 6. Реакция пирохимическая: В присутствии солей меди бесцветное пламя окрашивается в зеленый цвет
- 48. 7. Реакция с сульфидом натрия: CuSO4+Na2S =CuS↓+Na 2SO4 образуется осадок черного цвета.
- 49. 2 Cu+2 + 2 e-→ 2 Cu+1 (восстановле́ние) 2 I-I - 2 e- → 2 I0
- 50. Качественные реакции на катион Hg+2
- 51. 1. Действие группового реагента гидроксида аммония HgCl2 + 2NH4OH = [HgNH2]Cl↓ + NH4Cl + 2H2O -
- 52. HgCl2 + 4NH4OH = [Hg(NH3)4]Cl + 4H2O - при добавлении избытка аммиака образуется комплексное бесцветное соединение
- 53. Характерные реакции на кХарактерные реакции на катион Hg2+ н
- 54. 1. Реакция с иодидом калия (фармакопейная) Hg(NO3)2 + 2KJ = Hg2J↓ + 2 KNO3 - при
- 55. 2. Реакция с гидроксидом натрия NаОН: 2NаОН + Hg(NO3)2 = Hg(ОН)2↓ + 2Nа NO3 – образуется
- 56. 3. Реакция с тиосульфатом натрия Na2S2O3: HgCl2 + Na2S2O3 + Н2О= HgS↓ + Na2SO4 + 2НСl
- 57. 4.Реакция с сульфидом натрия Na2S: HgCl2 + Na2S = HgS↓ + 2NaCl – образуется черный осадок,
- 58. 5.Реакция с хроматом калия К2СrО4: HgCl2 + К2СrО4 = HgСrО4↓ + 2КCl – образуется желтый осадок
- 59. 7.Реакция с дифенилкарбазидом - образуется фиолетовый или синий осадок комплексного соединения
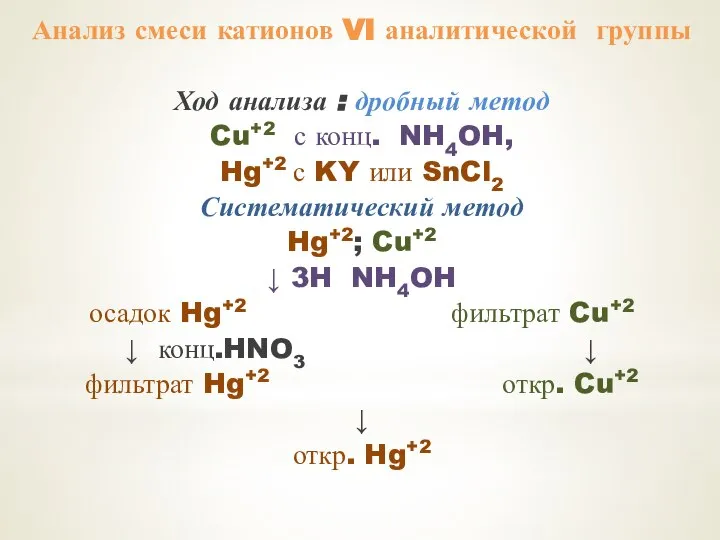
- 60. Анализ смеси катионов VI аналитической группы Ход анализа : дробный метод Cu+2 с конц. NH4OH, Hg+2
- 62. Скачать презентацию










2+ 4H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-12.jpg)
![2. Реакция с гексоцианоферратом (II) калия(желтой кровяной солью): ZnSO4 + K4[Fe(CN)6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-13.jpg)

![4. Реакция микрокристаллоскопическая с тетратиоцианомеркуратом аммония (NН4)2[Нg(SCN)4 ]: ZnСl2 + (NН4)2[Нg(SCN)4]=](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-15.jpg)






![Действие гексацианоферрата (III) калия K3[Fe(CN)6]. (красная кровяная соль, фармакопейная): 3FeCl2 +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-22.jpg)


![На катион Fe +3 1. Действие гексацианоферрата (II) калия K4[Fe(CN)6] (жёлтая](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-25.jpg)












![CuSO4 +4NH4OH =[Cu(NH3)4]SO4 + 4H2O - при добавлении избытка раствора аммиака](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-39.jpg)










![1. Действие группового реагента гидроксида аммония HgCl2 + 2NH4OH = [HgNH2]Cl↓](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-50.jpg)
![HgCl2 + 4NH4OH = [Hg(NH3)4]Cl + 4H2O - при добавлении избытка](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1351748/slide-51.jpg)







 Мұнайлардың жіктелуі
Мұнайлардың жіктелуі Типы химических реакций в органической химии. Типы реакций в органике
Типы химических реакций в органической химии. Типы реакций в органике Синтез полимерных комплексонов на основе аминокислот
Синтез полимерных комплексонов на основе аминокислот Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010
Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010 Деление ядер урана
Деление ядер урана  Физические и химические явления
Физические и химические явления Моделирование электронной структуры и сенсорных свойств наноструктурированных смешанных оксидов
Моделирование электронной структуры и сенсорных свойств наноструктурированных смешанных оксидов Отношение масс элементов в веществе. Массовые доли элементов в веществе
Отношение масс элементов в веществе. Массовые доли элементов в веществе Витамины и коферменты
Витамины и коферменты Түймедақ гүлімен құрғақ теріге арналған ылғалдандырушы крем дайындау
Түймедақ гүлімен құрғақ теріге арналған ылғалдандырушы крем дайындау Алкены
Алкены Моносахариды
Моносахариды Предмет химии. Вещества
Предмет химии. Вещества Карбоновые кислоты и их производные
Карбоновые кислоты и их производные Моделирование химико-технологической системы. Эмпирические, физические, математические методы моделирования
Моделирование химико-технологической системы. Эмпирические, физические, математические методы моделирования Метод изолирования Васильевой
Метод изолирования Васильевой Галогены
Галогены Хімія в побуті
Хімія в побуті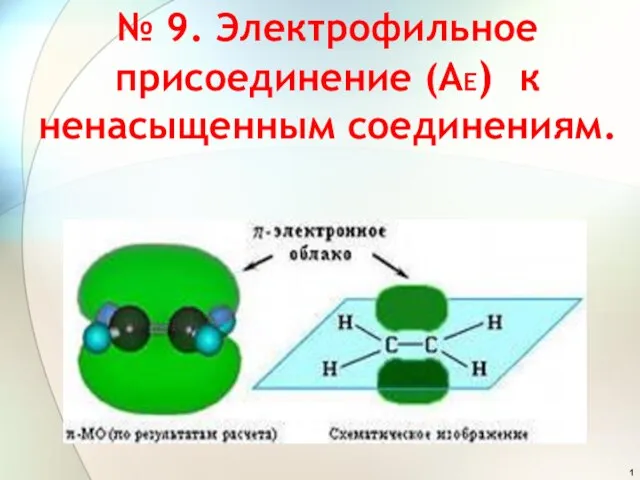 Презентация по химии Электрофильное присоединение (АЕ) к ненасыщенным соединениям.
Презентация по химии Электрофильное присоединение (АЕ) к ненасыщенным соединениям.  Электрохимические анализаторы медицинского назначения
Электрохимические анализаторы медицинского назначения Изопроцессы в идеальном газе
Изопроцессы в идеальном газе Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Получение и применение порфиринов и их аналогов
Получение и применение порфиринов и их аналогов Використання вуглеводнів
Використання вуглеводнів Дәрілік препараттардың синтезі мен олардың классификациясы
Дәрілік препараттардың синтезі мен олардың классификациясы Гетерофункциональные органические соединения
Гетерофункциональные органические соединения Алканы: изомерия и номенклатура
Алканы: изомерия и номенклатура Презентация по Химии "Закон збереження маси" - скачать смотреть
Презентация по Химии "Закон збереження маси" - скачать смотреть