Содержание
- 2. Основоположники химической кинетики Якоб Хендрик Вант-Гофф (нидерл. Jacobus Henricus (Henry) van 't Hoff; 1852, — 1911,
- 3. Э́ЙРИНГ (Eyring) Генри (1901-1981), американский физикохимик. Область изучения - квантовая химиия и химическая кинетика. Один из
- 4. Введение в кинетику Стехиометрия. Химическую реакцию принято записывать в форме стехиометрического уравнения. Последнее представляет собой простейшее
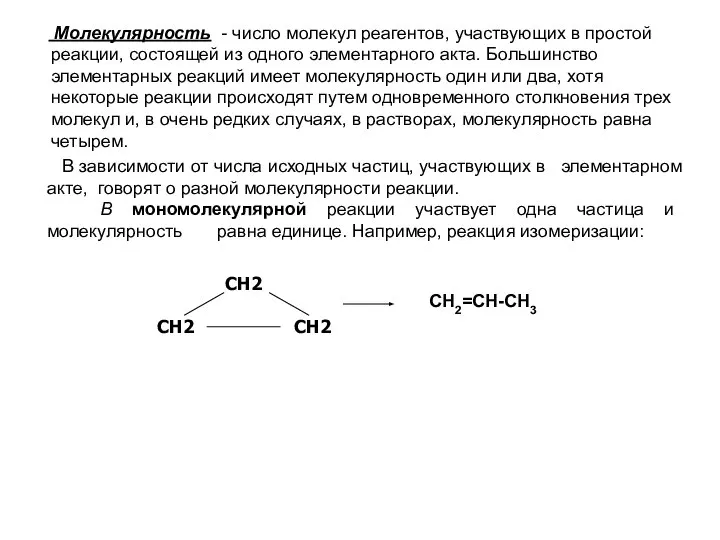
- 5. Молекулярность - число молекул реагентов, участвующих в простой реакции, состоящей из одного элементарного акта. Большинство элементарных
- 6. В бимолекулярной реакции взаимодействуют две одинаковые или неодинаковые молекулы реагентов с образованием одной или нескольких молекул
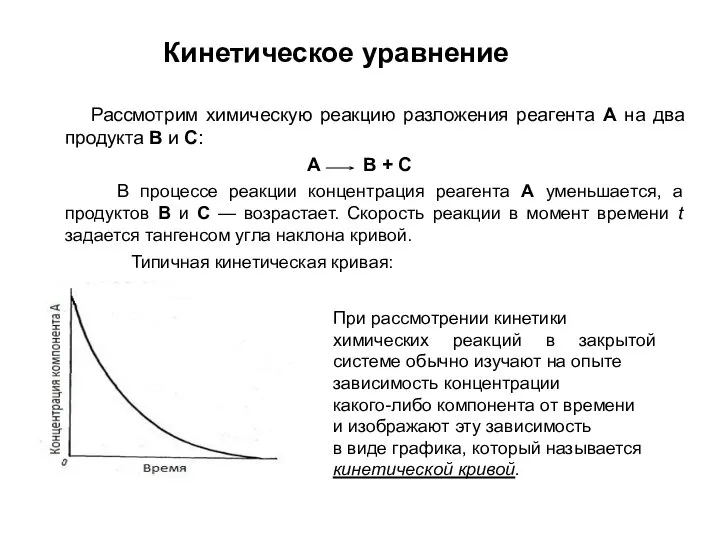
- 7. Кинетическое уравнение Рассмотрим химическую реакцию разложения реагента A на два продукта В и С: А В
- 8. ; Скорость реакции равна скорости уменьшения концентрации реагента А во времени. Кроме того, скорость реакции определяется
- 9. Порядок реакции Если зависимость скорости скорости реакции от концентрации реагирующих веществ записывается в виде: , то
- 10. Константа скорости Константа скорости химического процесса – это множитель в кинетическом уравнении, показывающий, с какой скоростью
- 11. Кинетические уравнения первого порядка Рассмотрим реакцию: А Продукты. Пусть а — начальная концентрация реагента А; x
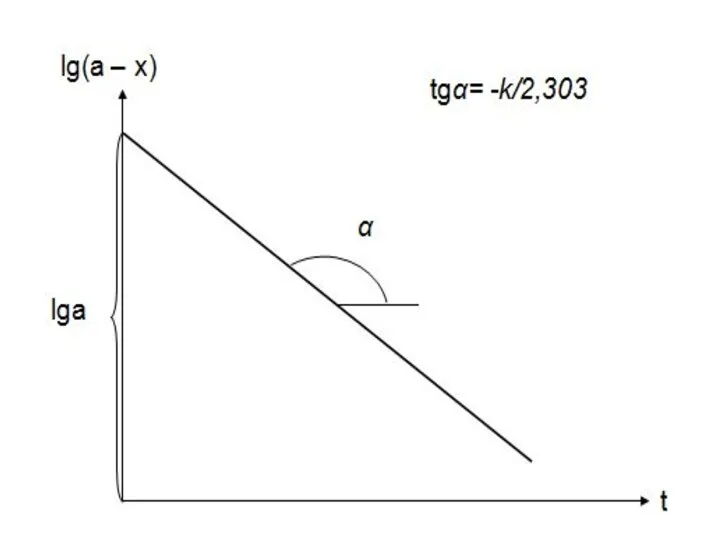
- 12. Определение константы скорости реакции первого порядка Выразим константу скорости реакции из уравнения(2): 3 Или используя десятичный
- 13. Метод подстановки Зная значения а – х, то есть текущие концентрации реагента А в разные моменты
- 15. Кинетические уравнения второго порядка Рассмотрим реакцию: А + В Продукты. Пусть начальные концентрации реагентов А и
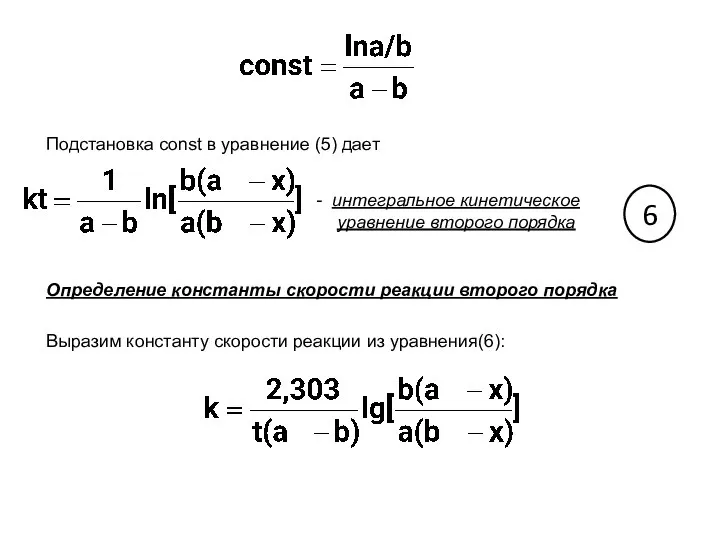
- 16. Подстановка const в уравнение (5) дает интегральное кинетическое уравнение второго порядка 6 Определение константы скорости реакции
- 17. Метод подстановки Константу скорости рассчитывают путем подстановки экспериментальных значений а - х и b - х,
- 19. Кинетические уравнения третьего порядка Рассмотрим в общем виде реакцию третьего порядка А + В + С
- 20. Подстановка const в уравнение (8) дает интегральное кинетическое уравнение третьего порядка Константу скорости можно определить подстановкой
- 21. Кинетика сложных реакций Большинство реакций являются сложными и состоят из нескольких элементарных стадий при этом все
- 22. Пусть а — начальная концентрация реагента А, х — уменьшение концентрации А за время t и
- 23. Интегрирование кинетического уравнения (10) при начальных условиях СА=СА,0 и t=0 приводит к следующему выражению Полученное соотношение
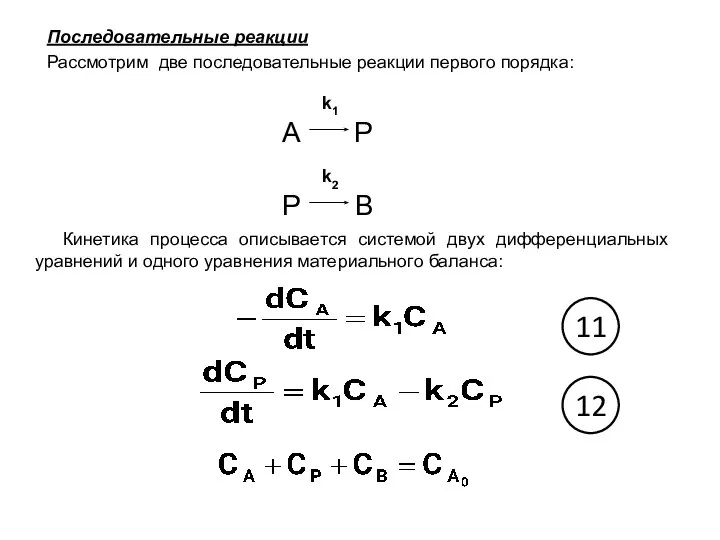
- 24. Последовательные реакции Рассмотрим две последовательные реакции первого порядка: k1 A Р k2 Р В Кинетика процесса
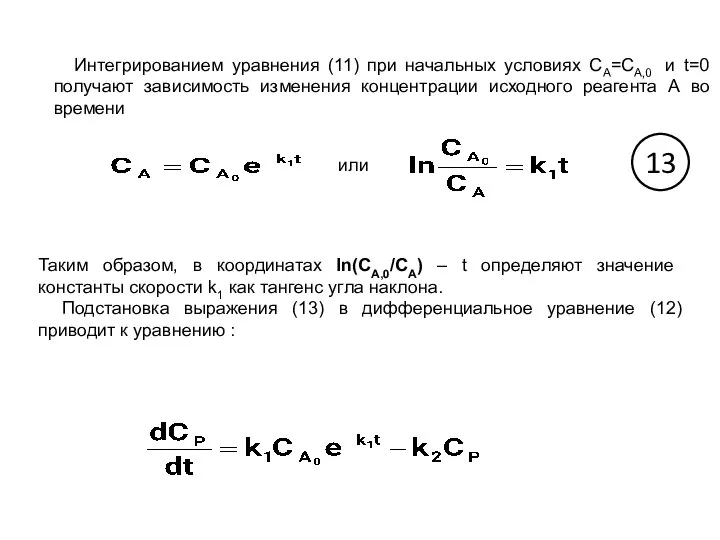
- 25. Интегрированием уравнения (11) при начальных условиях СА=СА,0 и t=0 получают зависимость изменения концентрации исходного реагента А
- 26. При интегрировании полученного дифференциального уравнения при начальных условиях: СР=0, СА=СА,0 и t=0, получают зависимость накопления промежуточного
- 27. Параллельные реакции Рассмотрим две параллельные реакции первого порядка, в которых вещество А одновременно превращается по двум
- 28. Дифференциальные уравнения для продуктов В1 и В2 имеют следующий вид: Интегрирование этих уравнений соответственно при начальных
- 29. Таким образом, для химического процесса, протекающего по схеме параллельных реакций, соотношения концентраций продуктов реакции СВ1 и
- 30. Цепные реакции многие гомогенные реакции имеют особенности: 1) реакции не подчиняются уравнению первого, второго и высших
- 31. Представляют интерес цепные реакции в некоторых важнейших промышленных процессах. Так, для хлорирования органических соединений цепная реакция
- 32. Метод стационарных концентраций Для описания кинетики многостадийных реакций можно использовать приближенный метод стационарных концентраций Боденштейна. В
- 34. Скачать презентацию

























 Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура
Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура Викторина по химии
Викторина по химии Алканы. Гомологический ряд
Алканы. Гомологический ряд Презентация по химии Химические уравнения Реакции обмена
Презентация по химии Химические уравнения Реакции обмена  Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Минералы и горные породы
Минералы и горные породы Сложные вещества Выполнил ученик 8 класса КГООУ «Железногорская санаторно-лесная школа» Москальчук Павел Учитель химии и биол
Сложные вещества Выполнил ученик 8 класса КГООУ «Железногорская санаторно-лесная школа» Москальчук Павел Учитель химии и биол История возникновения химии
История возникновения химии Основные понятия, классификация, структура и свойства полимеров. (Лекция 1)
Основные понятия, классификация, структура и свойства полимеров. (Лекция 1) Мыло ручной работы Подготовила ученицы 11 класса Хахалева Юлия
Мыло ручной работы Подготовила ученицы 11 класса Хахалева Юлия  Урок в 8 классе
Урок в 8 классе Белки. Свойства белков. (Тема 2)
Белки. Свойства белков. (Тема 2) Металлы в живой приподе
Металлы в живой приподе Основы электрохимии
Основы электрохимии Разработка реактора для отопления домов путем извлечения водорода из воды
Разработка реактора для отопления домов путем извлечения водорода из воды Химия нефти и газа
Химия нефти и газа Основные характеристики клеев
Основные характеристики клеев Гетероциклдік қосылыстар
Гетероциклдік қосылыстар Профилактика интоксикаций медьсодержащими веществами
Профилактика интоксикаций медьсодержащими веществами Процесс электролиза
Процесс электролиза Гетероциклічні ароматичні сполуки
Гетероциклічні ароматичні сполуки Коррозия металлов
Коррозия металлов Кислоты. Классификация. Способы получения
Кислоты. Классификация. Способы получения Симметрия кристаллических решеток
Симметрия кристаллических решеток Липиды омыляемые и неомыляемые
Липиды омыляемые и неомыляемые Химия функциональных материалов. Адсорбционные материалы. Цеолиты
Химия функциональных материалов. Адсорбционные материалы. Цеолиты Классификация методов аналитической химии
Классификация методов аналитической химии Амфотерность. Амфотерные соединения
Амфотерность. Амфотерные соединения