Содержание
- 2. ВЕК ЖИВИ- ВЕК УЧИСЬ «Сами трудясь, вы многое сделаете для себя и для близких, а если
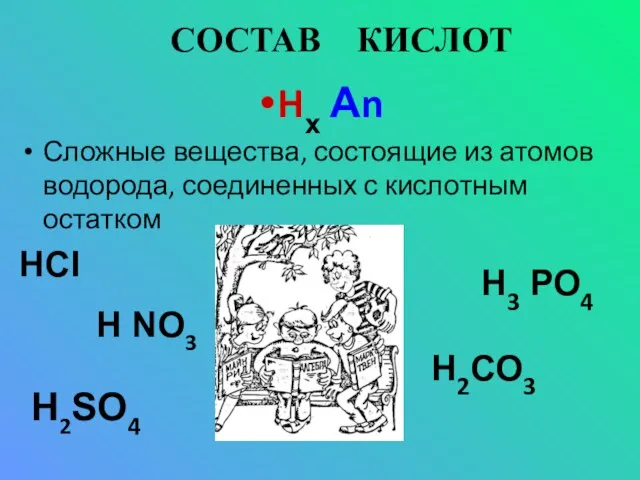
- 3. СОСТАВ КИСЛОТ Hх Аn Сложные вещества, состоящие из атомов водорода, соединенных с кислотным остатком НСI Н2SО4
- 4. КИСЛОТЫ - это вкусно
- 5. КИСЛОТЫ – это важно Объём продукции желудочного сока В сутки в желудке взрослого человека вырабатывается около
- 6. КИСЛОТЫ – это опасно КИСЛОТЫ — едкие вещества, при попадании на кожу вызывает сильные химические ожоги.
- 7. КЛАССИФИКАЦИЯ
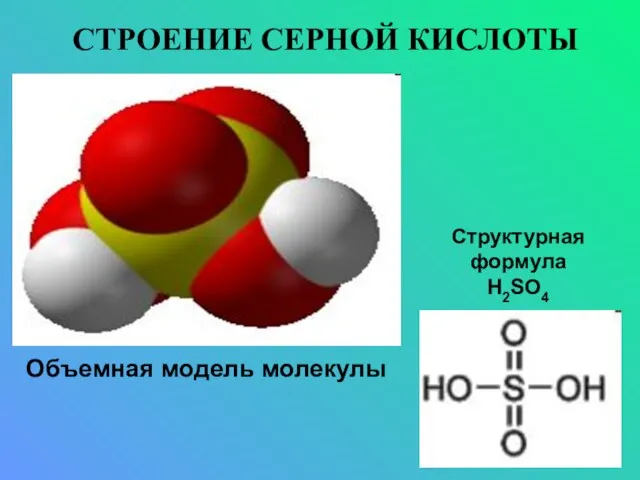
- 8. СТРОЕНИЕ СЕРНОЙ КИСЛОТЫ Объемная модель молекулы Структурная формула H2SO4
- 9. ХИМИЧЕСКИЕ СВОЙСВА 1. кислота + металл (стоящий до водорода в ЭХР напряжений) 2HCl + Mg →MgCl2
- 10. Взаимодействие кислот с индикаторами
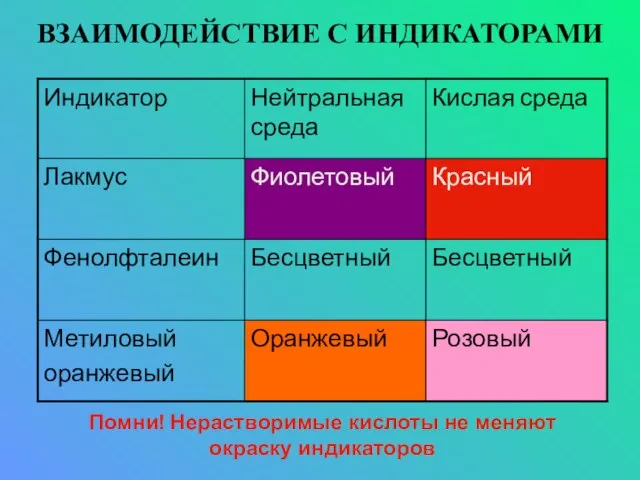
- 11. ВЗАИМОДЕЙСТВИЕ С ИНДИКАТОРАМИ Помни! Нерастворимые кислоты не меняют окраску индикаторов
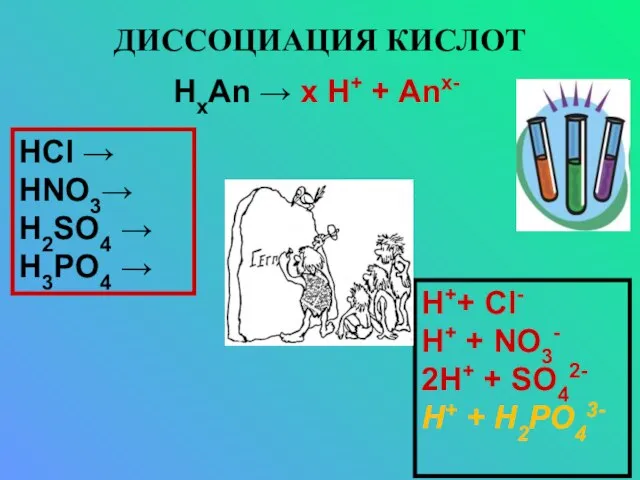
- 12. ДИССОЦИАЦИЯ КИСЛОТ HCl → HNO3→ H2SO4 → H3PO4 → НxAn → x Н+ + Anx- H++
- 13. ВЗАИМОДЕЙСТВИЕ КИСЛОТ С Ме МЕТАЛЛ + КИСЛОТА→СОЛЬ + ВОДОРОД левее Pb + H2SO4 →Х ???
- 14. ВЗАИМОДЕЙСТВИЕ С ОСНОВНЫМИ ОКСИДАМИ ОСНОВНЫЙ ОКСИД + КИСЛОТА → СОЛЬ + ВОДА
- 15. ВЗАИМОДЕЙСТВИЕ С ОСНОВАНИЯМИ ОСНОВАНИЕ + КИСЛОТА → СОЛЬ + ВОДА Реакция между основанием и кислотой с
- 16. ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ СОЛЬ + КИСЛОТА → НОВАЯ КИСЛОТА + НОВАЯ СОЛЬ Реакция возможна, ЕСЛИ образуется
- 17. ХИМИЧЕСКИЕ СВОЙСТВА
- 18. О КИСЛОТНЫХ ДОЖДЯХ Оксиды азота, серы содержатся в выхлопных газах реактивных двигателей и двигателей внутреннего сгорания,
- 19. Кислотные дожди виноваты в исчезновении рыбы во многих реках и озёрах, так как рыба не выдерживает
- 20. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ Диссоциация Взаимодействие с индикаторами Взаимодействие с металлами Взаимодействие с основными оксидами Взаимодействие с
- 21. Какое свойство кислот? Кислота, когда здорова, Угостить друзей готова Тем, что ей дала природа - Катионом
- 22. ОТ ПЕРЕМЕНЫ МЕСТ СЛАГАЕМЫХ…?
- 23. 1. Узнал много нового. 2. Мне это пригодится в жизни. 3. Было над чем подумать. 4.
- 25. Скачать презентацию


















 Презентация Лепиды
Презентация Лепиды  Железо 9 класс - Презентация по Химии_
Железо 9 класс - Презентация по Химии_ Ступенчатые процессы получения полимеров: полиприсоединение, поликонденсация
Ступенчатые процессы получения полимеров: полиприсоединение, поликонденсация Аттестационная работа. Методическая разработка исследователького урока «Строение вещества. Молекулы и атомы»
Аттестационная работа. Методическая разработка исследователького урока «Строение вещества. Молекулы и атомы» Материя и цвет. Свет
Материя и цвет. Свет Фуллерендер құрылымдары және олардың түрлерi
Фуллерендер құрылымдары және олардың түрлерi Соединения азота. Оксиды азота
Соединения азота. Оксиды азота Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Органическая химия. Фенолы
Органическая химия. Фенолы Презентация по Химии "Сходства и различия в теориях разбавленных растворов Аррениуса и Менделеева" - скачать смотреть
Презентация по Химии "Сходства и различия в теориях разбавленных растворов Аррениуса и Менделеева" - скачать смотреть  Свойства алкадиенов и их получение
Свойства алкадиенов и их получение Новітні досягнення в хімії (9 клас)
Новітні досягнення в хімії (9 клас) Химия и производство
Химия и производство 11 хб
11 хб  Празеодим
Празеодим Презентация по Химии "Симметрия в мире химии: кристаллы" - скачать смотреть
Презентация по Химии "Симметрия в мире химии: кристаллы" - скачать смотреть  Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Классификация химических реакций по тепловому эффекту
Классификация химических реакций по тепловому эффекту Карбоновые кислоты
Карбоновые кислоты Второй закон термодинамики
Второй закон термодинамики Простые вещества – металлы. Общие физические свойства металлов.
Простые вещества – металлы. Общие физические свойства металлов.  УГЛЕВОДЫ И ЛИПИДЫ. ИХ РОЛЬ В ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТКИ Презентация учителя химии, биологии и экологии МОУ СОШ п.Алексеевка Беша
УГЛЕВОДЫ И ЛИПИДЫ. ИХ РОЛЬ В ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТКИ Презентация учителя химии, биологии и экологии МОУ СОШ п.Алексеевка Беша Вода – основа жизни на Земле
Вода – основа жизни на Земле Презентация по Химии "Полимеры" 10 класс
Презентация по Химии "Полимеры" 10 класс Гидролиз солей
Гидролиз солей Презентация по Химии "Силікатні матеріали: скло, кераміка, цемент" - скачать смотреть бесплатно
Презентация по Химии "Силікатні матеріали: скло, кераміка, цемент" - скачать смотреть бесплатно Вуглеводи
Вуглеводи Ерітінділер түрлері. Идеал ертітінділер және реал ерітінділер. Ерітіндінің пайыздық концентрациясына eсептер
Ерітінділер түрлері. Идеал ертітінділер және реал ерітінділер. Ерітіндінің пайыздық концентрациясына eсептер