Содержание
- 2. План лекции Общие понятия Строение комплексных соединений Характер химической связи Номенклатура Классификация
- 3. Диссоциация солей Наряду с соединениями обычного типа (KCI, Al2(SO4)3), встречаются и более сложные соединения – двойные,
- 4. Комплексные соединения Молекулярные соединения, содержащие в своем составе комплексные ионы, способные к существованию как в растворе,
- 5. Основные положения теории Центральное место в комплексном соединении занимает комплексообразователь Fe3+ С комплексообразователем координированы лиганды CN-
- 6. Комплексообразователь Положительно заряженный ион (чаще всего металл) Нейтральный атом Неметалл (редко) Является акцептором электронных пар, предоставляя
- 7. Наибольшей способностью к комплексообразованию обладают атомы f и d-элементов f > d > p >> s
- 8. Лиганды Ионы противоположного знака CN-, NO2-, NO3-, CI-, Br-, J-, OH-, CO32- Нейтральные полярные молекулы NH3,
- 9. Характеристики лигандов Дентантность – количество мест, которые занимает лиганд вокруг центрального атома Монодентантные H2O, NH3, CO,
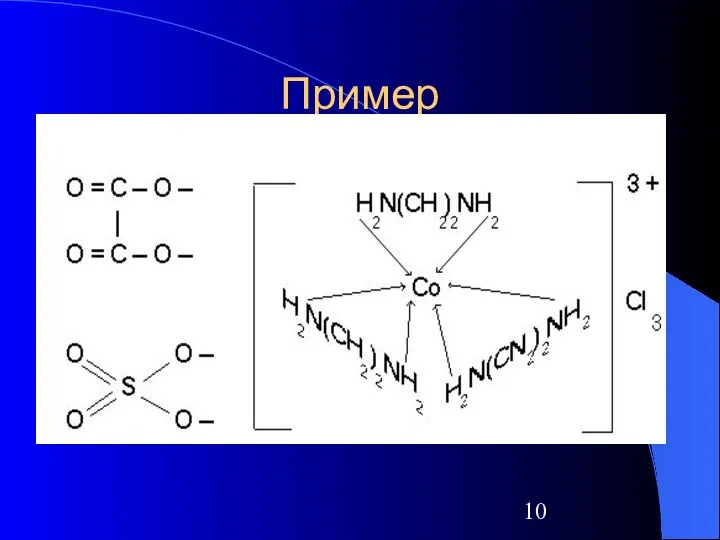
- 10. Пример
- 11. Внутренняя сфера Заключается в квадратные скобки [ ]. Остается стабильной при растворении В соответствии с зарядом
- 12. Внешняя сфера Состоит из: Положительно заряженных ионов, если комплексный ион заряжен отрицательно K31+[Fe3+(CN)6]3- Отрицательно заряженных ионов,
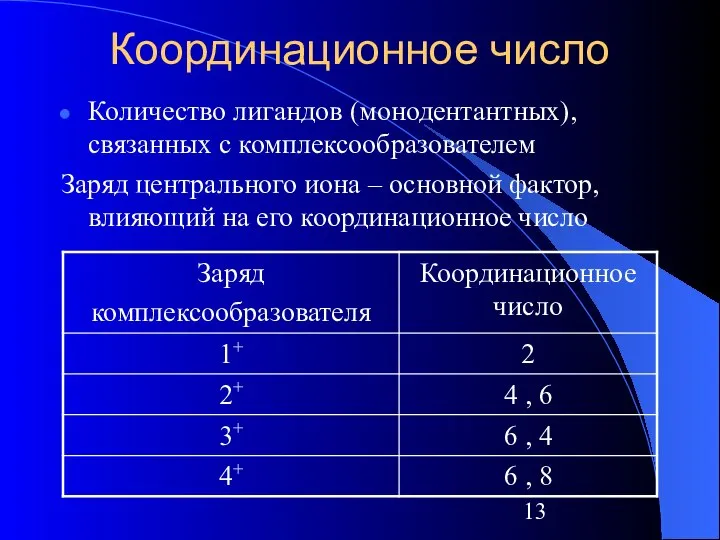
- 13. Координационное число Количество лигандов (монодентантных), связанных с комплексообразователем Заряд центрального иона – основной фактор, влияющий на
- 14. Формулу комплексного соединения определяют Заряд (степень окисления) комплексообразователя Заряд лигандов Координационное число Ионы внешней сферы Заряд
- 15. Пространственное строение комплексного иона К.число = 2 – линейное К.число = 4 – квадрат, тетраэдр К.число
- 16. Характер химической связи Образование комплексных соединений происходит в том случае, когда один из компонентов представляет неподеленную
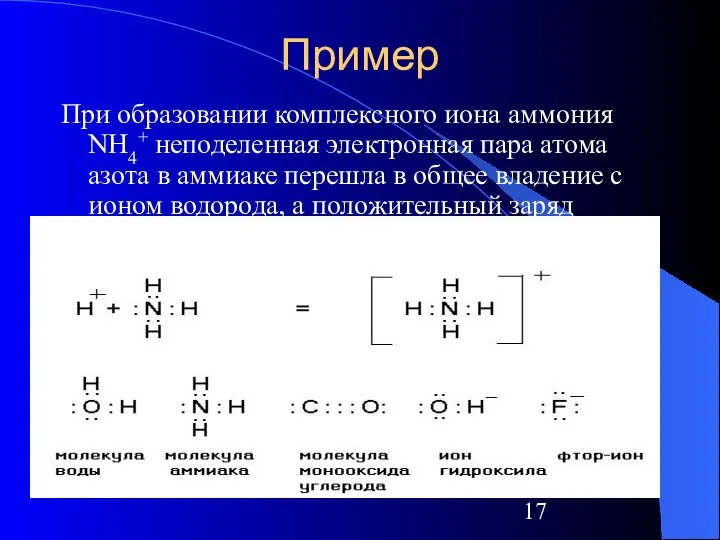
- 17. Пример При образовании комплексного иона аммония NH4+ неподеленная электронная пара атома азота в аммиаке перешла в
- 18. Диссоциация КС Первичная – практически нацело на комплексный ион и ионы внешней сферы [Ag(NH3)2]CI → [Ag(NH3)2]+
- 19. Константа нестойкости (КН) Применяя закон действующих масс к обратимым процессам, можно получить выражение КН комплексного иона:
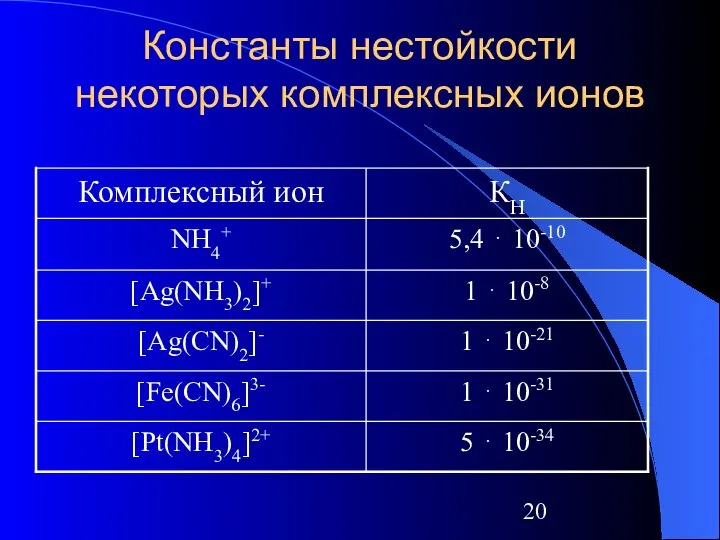
- 20. Константы нестойкости некоторых комплексных ионов
- 21. Константа устойчивости В растворах имеет место ступенчатая диссоциация комплексов; между КН имеется соотношение КН1 > КН2
- 22. Номенклатура Вначале называют катион, затем анион Отрицательно заряженные ионы с окончанием «о»: CN- – циано OH-
- 23. Перед названием лигандов ставится их число (греческие числительные би, тетра, пента, гекса) В комплексном анионе комплексообразователь
- 24. Примеры K[Al(OH)4(H2O)2] – калия тетрагидроксодиакваалюминат (III) K3[Fe(CN)6] – калия гексацианоферрат (III) [Co(NH3)5CI]SO4 – хлоропентааминкобальта (III) сульфат
- 25. Классификация А. По составу Ацидокомплексы: лигандами являются отрицательно заряженные анионы кислот Гидроксокомплексы Аммиакаты, аквакомплексы, карбонилы –
- 26. Б. По строению Многоядерные: [(NH3)5Co – NH2 – Co(NH3)5]5+ цитохромоксидаза Циклические (хелатные): устойчивые комплексные соединения металлов
- 27. Внутрикомплексные соединения – одна из разновидностей циклических комплексных соединений, отличающаяся тем, что один из концевых атомов
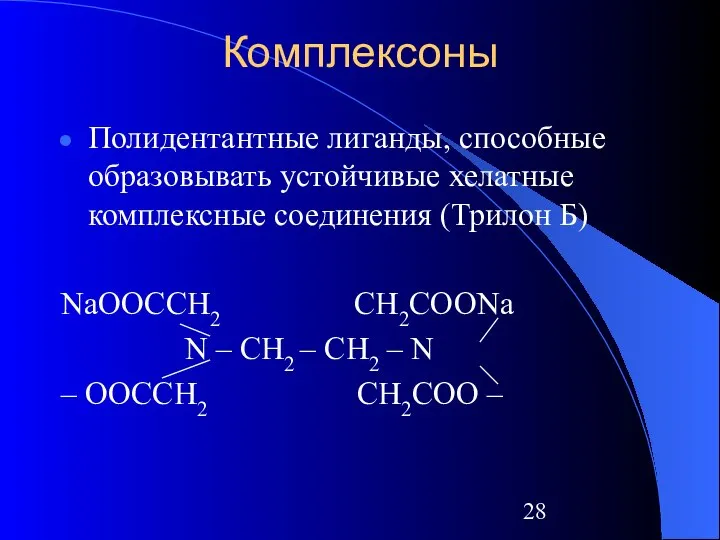
- 28. Комплексоны Полидентантные лиганды, способные образовывать устойчивые хелатные комплексные соединения (Трилон Б) NaOOCCH2 CH2COONa N – CH2
- 29. Применение комплексонов Трилон Б – в аналитической химии для титриметрического (количественного) определения многих катионов и анионов
- 30. В лакокрасочной и кинофотопромышленности Для разделения редкоземельных элементов Для лечения болезней растений В медицине для лечения
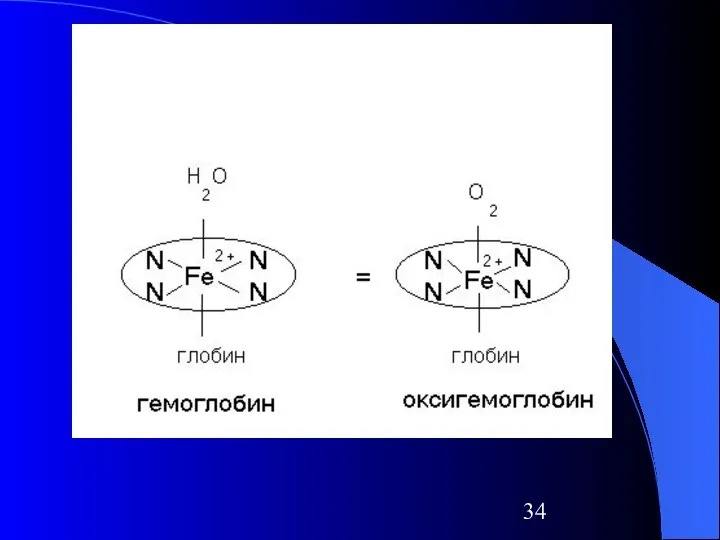
- 31. Природные комплексные соединения Железо находится в центре плоской порфириновой системы в таких белках, как: Гемоглобин Миоглобин
- 32. Кобальт как комплексообразователь содержится в витамине В12 Цинк – в ферментах: Карбоксипептидаза Карбоангидраза Магний – в
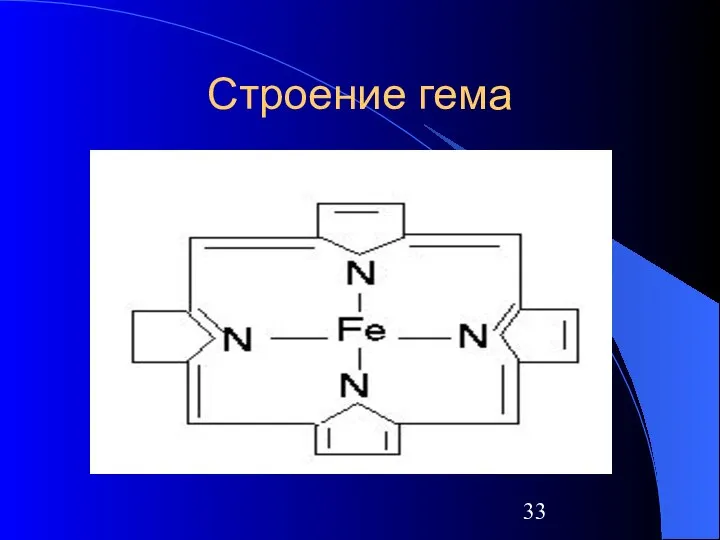
- 33. Строение гема 2 +
- 36. Скачать презентацию








![Внутренняя сфера Заключается в квадратные скобки [ ]. Остается стабильной при](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407476/slide-10.jpg)









![Примеры K[Al(OH)4(H2O)2] – калия тетрагидроксодиакваалюминат (III) K3[Fe(CN)6] – калия гексацианоферрат (III)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407476/slide-23.jpg)

![Б. По строению Многоядерные: [(NH3)5Co – NH2 – Co(NH3)5]5+ цитохромоксидаза Циклические](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1407476/slide-25.jpg)





 Химические свойства предельных одноатомных спиртов
Химические свойства предельных одноатомных спиртов Химия – наука о веществах, их свойствах и превращениях Урок №1
Химия – наука о веществах, их свойствах и превращениях Урок №1 Химическая связь
Химическая связь Углерод и кремний
Углерод и кремний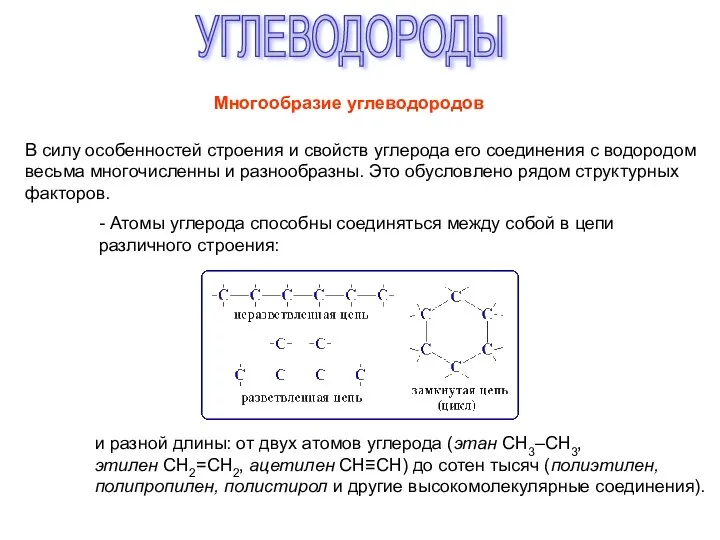 Углеводороды. Многообразие углеводородов
Углеводороды. Многообразие углеводородов Гетерофункциональные соединения
Гетерофункциональные соединения Магматические формации
Магматические формации Полисахариды. Крахмал
Полисахариды. Крахмал Нефть Михеева Анастасия 11-П
Нефть Михеева Анастасия 11-П  Вуглеводні. Підсумковий урок 9 клас
Вуглеводні. Підсумковий урок 9 клас Презентация по Химии "Химическая посуда и оборудование" - скачать смотреть
Презентация по Химии "Химическая посуда и оборудование" - скачать смотреть  Липиды
Липиды Кинетика сложных реакций
Кинетика сложных реакций Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства Chemistry
Chemistry Строение кристаллов
Строение кристаллов Углерод, аллотропные модификации
Углерод, аллотропные модификации Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7)
Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7) Көміртекті материалдар
Көміртекті материалдар Атомы. Нахождение в природе
Атомы. Нахождение в природе Количества вещества
Количества вещества Презентация Электрохимический ряд напряжений металлов
Презентация Электрохимический ряд напряжений металлов Биосинтез триацилглицеролов и глицерофосфолипидов. Обмен холестерола
Биосинтез триацилглицеролов и глицерофосфолипидов. Обмен холестерола Раздел: «Гетероциклические соединения» Раздел: «Гетероциклические соединения» Лекция №32-33 Тема: «6-ти членные ГЦС» План: 1. О
Раздел: «Гетероциклические соединения» Раздел: «Гетероциклические соединения» Лекция №32-33 Тема: «6-ти членные ГЦС» План: 1. О Оружие массового поражения. Биологическое оружие
Оружие массового поражения. Биологическое оружие  Консистентные смазки для легковых автомобилей
Консистентные смазки для легковых автомобилей Нуклеиновые кислоты
Нуклеиновые кислоты Классификация химических реакций
Классификация химических реакций