Содержание
- 2. Химическое равновесие Химическое равновесие характерно для реакций, способных протекать в прямом и обратном направлениях, т.е. из
- 3. Химическое равновесие В случае изменения условий протекания реакции, в силу вступает принцип Ле Шателье: «При изменении
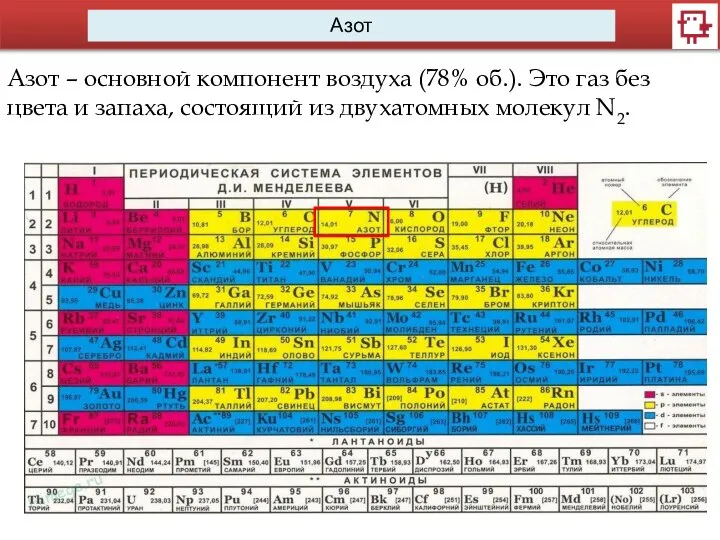
- 4. Азот Азот – основной компонент воздуха (78% об.). Это газ без цвета и запаха, состоящий из
- 5. Азот Азот является важным элементом белков. Растения синтезируют белки, используя нитраты из почвы. Нитраты там образуются
- 6. Азот Азот может иметь степени окисления от -3 до +5. Что бы N2 вступил в реакцию
- 7. Азот Только в «жестких» условиях реагирует с О2: N2 + O2 2NO – Q C Н2,
- 8. Азот Нитриды легко взаимодействуют с водой: Ca3N2 + 6H2O = 3Ca(OH)2 + 2NH3 И с кислотами:
- 9. Азот Получение: В лабораторных условиях: (NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O NH4NO2 = N2 +
- 10. Азот Аммиак. NH3. В обычных условиях газ, с резким запахом. В жидком состоянии молекулы связан водородными
- 12. Скачать презентацию








 Двовимірний ямр. Типи двовимірних спектрів
Двовимірний ямр. Типи двовимірних спектрів Стероиды. Дицетин-холестерин-ацилтрансферазная реакция
Стероиды. Дицетин-холестерин-ацилтрансферазная реакция Атом. Изотопы
Атом. Изотопы Redox reactions
Redox reactions The way to prepare gold clusters - Every atom makes a difference
The way to prepare gold clusters - Every atom makes a difference Основания
Основания Общая радиохимия. Свойства радиоколлоидов
Общая радиохимия. Свойства радиоколлоидов Оксикислоты (гидроксикислоты)
Оксикислоты (гидроксикислоты) Вода. Физические и химические свойства
Вода. Физические и химические свойства Химия в пище (нитраты и пищевые добавки)
Химия в пище (нитраты и пищевые добавки) Таблица взаимодействия с металлами
Таблица взаимодействия с металлами Направление окислительно-восстановительного процесса
Направление окислительно-восстановительного процесса Кристаллы и их свойства. Понятие о симметрии кристаллов и элементах симметрии. Сингония
Кристаллы и их свойства. Понятие о симметрии кристаллов и элементах симметрии. Сингония Тест по теме «Альдегиды и кетоны»
Тест по теме «Альдегиды и кетоны» Валентность связи и локальный баланс валентности
Валентность связи и локальный баланс валентности Флавоноидтар
Флавоноидтар Хлориды. Получение
Хлориды. Получение Презентация по Химии "Вещества и их превращения. Роль химии в нашей жизни" - скачать смотреть
Презентация по Химии "Вещества и их превращения. Роль химии в нашей жизни" - скачать смотреть  Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Кислоты – кислотные гидроксиды
Кислоты – кислотные гидроксиды Идеал газ. Молекулалы-кинетикалық теорияның негізгі теңдеуі. Молекулалық орташа квадраттық жылдамдығына есептер шығару
Идеал газ. Молекулалы-кинетикалық теорияның негізгі теңдеуі. Молекулалық орташа квадраттық жылдамдығына есептер шығару Управління якістю у фармацевтичній галузі. Державна система забезпечення якості лікарських засобів в Україні
Управління якістю у фармацевтичній галузі. Державна система забезпечення якості лікарських засобів в Україні Основания и соли
Основания и соли Презентация "Соль"
Презентация "Соль" Składniki odżywcze
Składniki odżywcze Презентация по Химии "Природні І синтетичні Органічні речовини" - скачать смотреть бесплатно
Презентация по Химии "Природні І синтетичні Органічні речовини" - скачать смотреть бесплатно Применение нитратов
Применение нитратов  Предельные одноатомные спирты Герасимова Н.Ф. – учитель химии ГОУ СОШ №639 ЮАО г.Москва
Предельные одноатомные спирты Герасимова Н.Ф. – учитель химии ГОУ СОШ №639 ЮАО г.Москва