Содержание
- 2. Глинка Н.Л. Общая химия. – М., КНОРУС, 2009. Коровин Н.В. Общая химия. – М., ВШ, 2006.
- 3. Тема: Строение атома и Периодический закон Д.И. Менделеева 1. Современные квантово-механические представления о строении атома. 2.
- 4. 1. Современные квантово-механические представления о строении атома Учение о строении вещества является основным в системе знаний
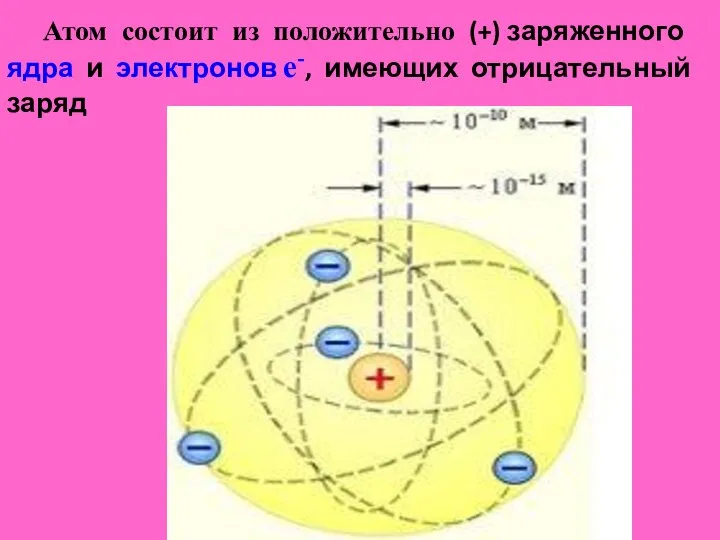
- 5. Атом состоит из положительно (+) заряженного ядра и электронов е-, имеющих отрицательный заряд
- 6. Вся масса атома сосредоточена в ядре, образован-ного протонами p+ (частицы с зарядом +1,60 ∙ 10-19 Кл
- 8. Данная модель не укладывалась в рамки класси-ческой физики, т.к. вращающийся по орбите электрон должен терять энергию.
- 10. В химических превращениях масса и заряд ядра не меняются, поэтому на них базируется электронная структура атома.
- 11. Пространство вокруг ядра, в котором может нахо-диться е- , называется орбиталью. В соответствии с дискретностью энергии
- 12. В реально существующих атомах электронами могут быть заполнены 6 уровней, 7-ой заполнен частично (табл.). Орбитальное квантовое
- 14. 3. Магнитное квантовое число ml. Подуровни также делятся на атомные орбитали АО, обозначаемые квантовым числом ml.
- 15. 3 первых квантовых числа характеризуют вращение электронов вокруг ядра атома (отсюда название Планетарная модель атома Резерфорда),
- 16. 2. Правила квантовой механики Состояние е- в атоме определяется набором 4-х квантовых чисел. Подобно любой системе,
- 17. На одной АО по принципу Паули не может быть больше 2-х электронов (е- на одной АО
- 18. 2) Правило Гунда. Заполнение электронами АО одного подуровня происходит таким образом, чтобы суммарный спин (по модулю)
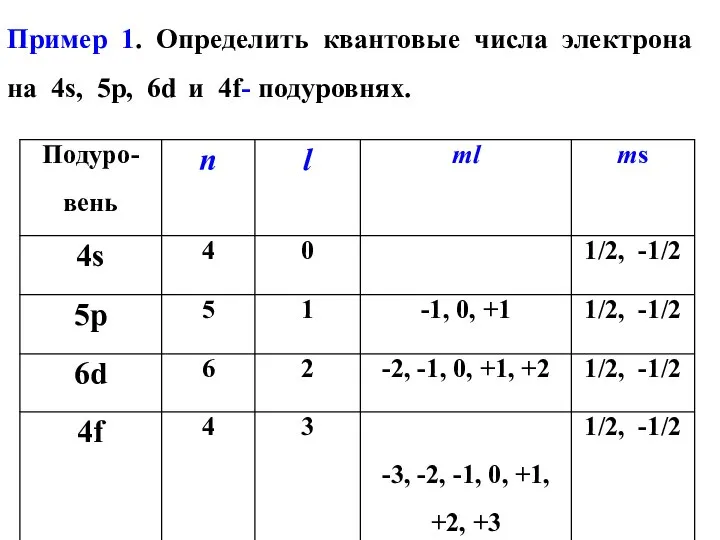
- 19. Пример 1. Определить квантовые числа электрона на 4s, 5р, 6d и 4f- подуровнях.
- 20. Электронную структуру атома принято записывать двумя квантовыми числами в виде nl. Число электронов на подуровне обозначается
- 21. 3) Правила Клечковского (принцип наименьшей энергии атома) устанавливают последовательность заполнения электронами энергетических подуров-ней в зависимости от
- 22. (n – 1)d4 ns2 → (n – 1)d5 ns1 (n – 1)d9 ns2 → (n –
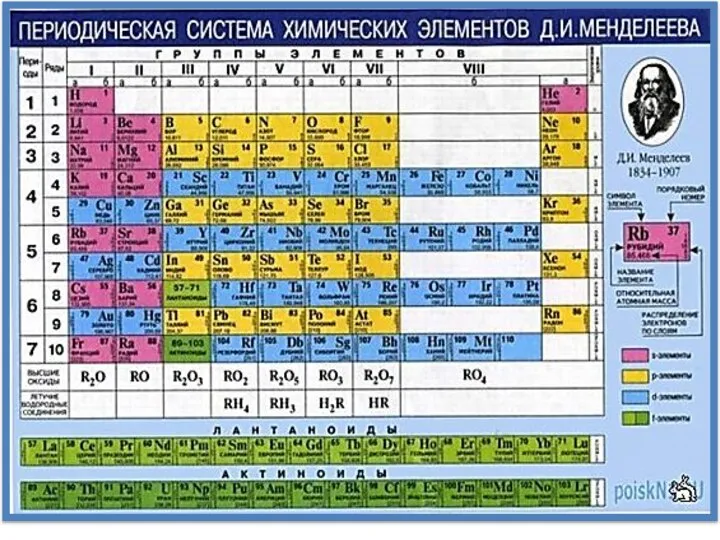
- 24. Номер периода совпадает со значением главного квантового числа n внешнего уровня. Каждый период начинается с s-
- 25. Количество элементов в периоде: χчетн = (N + 2)2/2; χнечетн = (N + 1)2/2, N –
- 26. Из электронной формулы атома легко определить валентные электроны и орбитали: им соответству-ют подуровни с максимальным значением
- 27. Металлы - это элементы, способные отдавать электроны, превращаясь в положительно (+) заряженный ион, проявляют восстановительные свойства.
- 28. Потенциал ионизации I - наименьшее значение энергии, необходимое для отрыва одного электрона от атома. Эта энергия
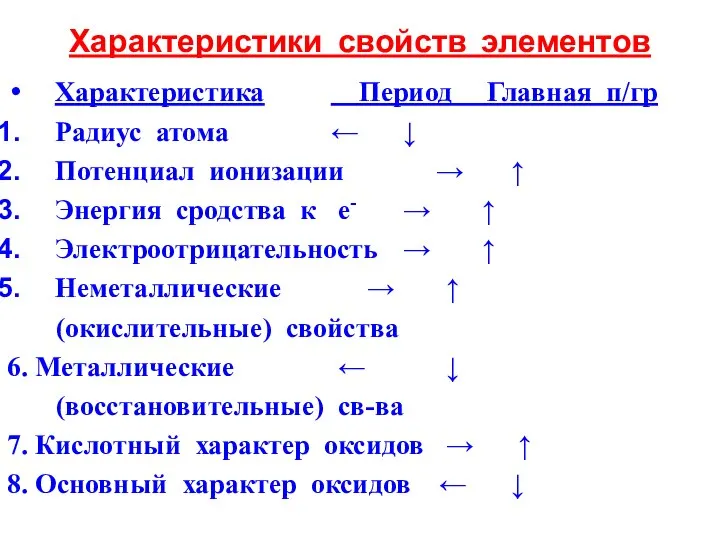
- 29. Характеристики свойств элементов Характеристика Период Главная п/гр Радиус атома ← ↓ Потенциал ионизации → ↑ Энергия
- 30. Изменение кислотно-основных свойств гидроксидов: (3-ий период): NaOH (щел) → Mg(OH)2 (осн) → Al(OH)3 (амфот. гидроксид) →
- 32. Скачать презентацию

























 Неравновесные электрохимические методы. Полярография постоянного тока. Вольтамперометрия. Лекция 2
Неравновесные электрохимические методы. Полярография постоянного тока. Вольтамперометрия. Лекция 2 Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии
Разработка и внедрение метода измерений массовых концентраций сульфид-ионов в водах методом ионной хроматографии Метаболизм этанола
Метаболизм этанола Вода Підготувала Учениця 10-Б класу Брикова Ганна
Вода Підготувала Учениця 10-Б класу Брикова Ганна  Репликация ДНК
Репликация ДНК Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона
Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона Презентация по Химии "Застосування жирів" - скачать смотреть бесплатно
Презентация по Химии "Застосування жирів" - скачать смотреть бесплатно Хімія для ремонту Лисенко Демид ; Понура Назар
Хімія для ремонту Лисенко Демид ; Понура Назар  Три элемента таблицы Менделеева
Три элемента таблицы Менделеева Органическая химия. Жиры
Органическая химия. Жиры Ионы. Определение кислотности раствора
Ионы. Определение кислотности раствора Полимер. Использование и вред
Полимер. Использование и вред Химия Соли. Свойства солей.
Химия Соли. Свойства солей. Биологическое окисление 2. Оксигеназные, пероксидазные и радикальные пути использования кислорода. (Лекция 5)
Биологическое окисление 2. Оксигеназные, пероксидазные и радикальные пути использования кислорода. (Лекция 5) Ферменты в пищевой промышленности
Ферменты в пищевой промышленности Строение газообразных, жидких, твердых тел
Строение газообразных, жидких, твердых тел Синтез лоратадина
Синтез лоратадина Презентация по Химии "Презентация ОСНОВАНИЯ" - скачать смотреть
Презентация по Химии "Презентация ОСНОВАНИЯ" - скачать смотреть  Электронные конфигурации атомов
Электронные конфигурации атомов ВИКТОРИНА: «ПОЛЕЗНАЯ ХИМИЯ ВО ФРУКТАХ И ОВОЩАХ»
ВИКТОРИНА: «ПОЛЕЗНАЯ ХИМИЯ ВО ФРУКТАХ И ОВОЩАХ» Аренкарбонільні комплекси металів у реакціях перфлюороалкілювання та деароматизації
Аренкарбонільні комплекси металів у реакціях перфлюороалкілювання та деароматизації Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть
Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть  Алхимический период
Алхимический период Эфиры. Жиры
Эфиры. Жиры ЙОД
ЙОД  Синтез реакционноспособных олигомеров и полимеров на их основе. Лекция 1
Синтез реакционноспособных олигомеров и полимеров на их основе. Лекция 1 Основные классы неорганических соединений
Основные классы неорганических соединений Презентация по Химии "СПИРТЫ" - скачать смотреть бесплатно
Презентация по Химии "СПИРТЫ" - скачать смотреть бесплатно