Содержание
- 2. по схеме: Ме0 – nē → Меn+ Меn+ + nē → Ме0 Двойной электрический слой. Электродные
- 3. С течением времени устанавливается равновесие: Ме0 + mH2O ⇄ Me(H2O)mn+ + nē Ме0 ⇄ Меn++ nē
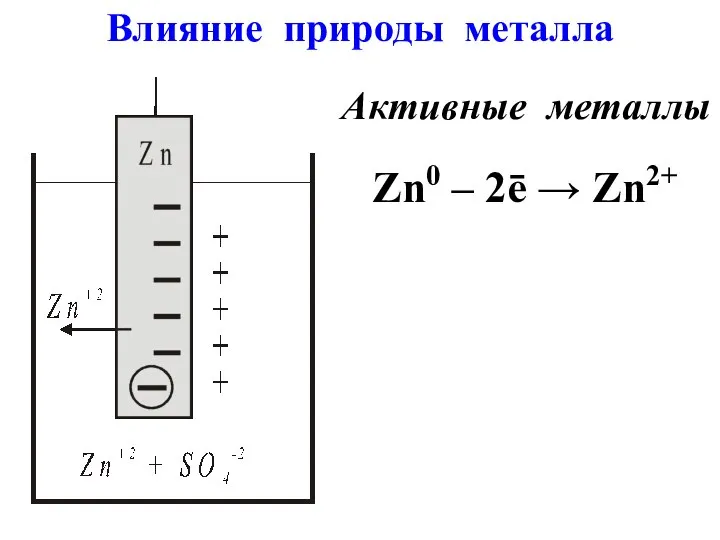
- 4. Активные металлы Zn0 – 2ē → Zn2+ Влияние природы металла
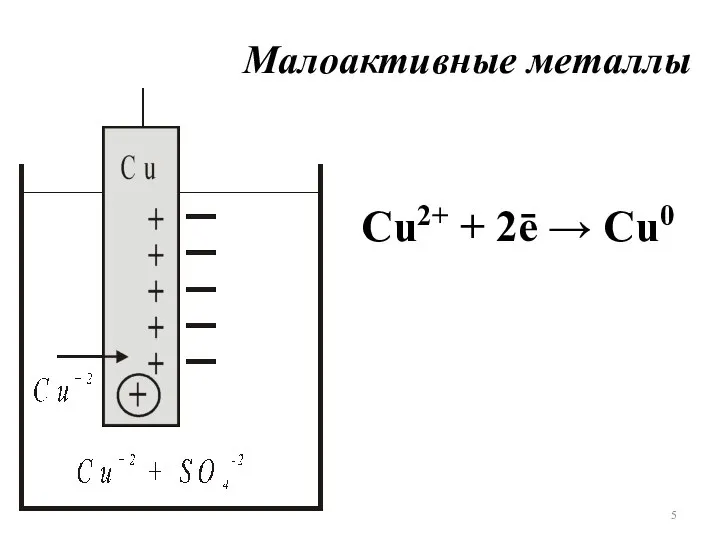
- 5. Малоактивные металлы Сu2+ + 2ē → Cu0
- 6. Электродный потенциал (Е, ϕ, [В]) Если концентрация ионов равна 1 моль/л при температуре 25оС, то электродный
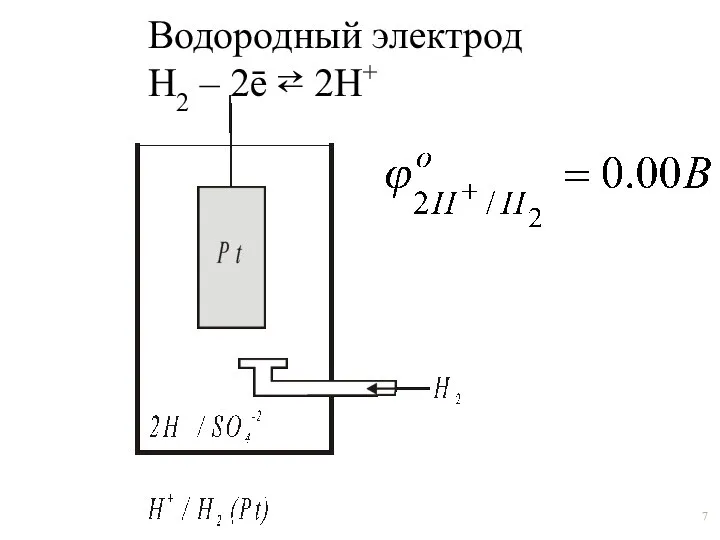
- 7. Водородный электрод Н2 – 2ē ⇄ 2Н+
- 8. Пример: Fe + CuCl2 = FeCl2 +Cu Cu + Hg(NO3)2 = Hg + Cu(NO3)2 Zn+2HCl=ZnCl2+H2
- 9. Таблица стандартных электродных потенциалов характеризует химическую активность металлов. 1. чем меньше электродный потенциал металла, тем больше
- 10. формула Нернста: ϕо – стандартный электродный потенциал (В); F – постоянная Фарадея (96500 Кл/экв);
- 11. R – универсальная газовая постоянная (8,314 Дж/моль); T – фактическая температура (298 К); n – число
- 12. Цинковая пластинка погружена в 0,01 М раствор её соли
- 13. Гальванические элементы (ГЭ)
- 14. Элемент Даниэля-Якоби (К) (А)
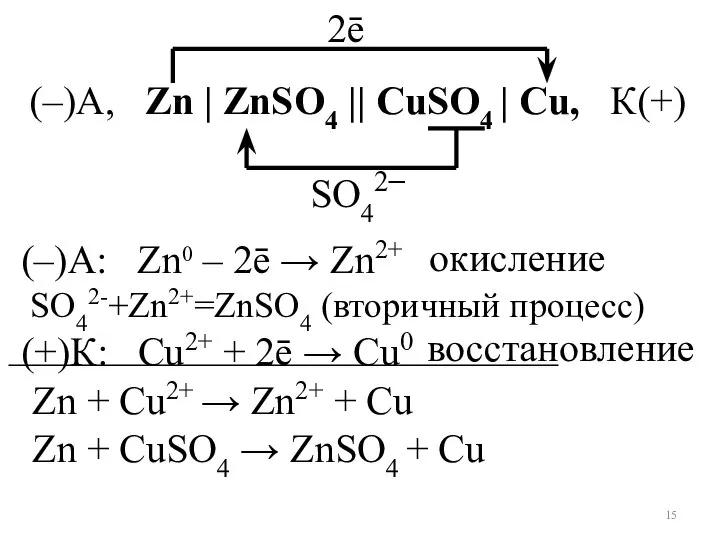
- 15. (–)А, Zn | ZnSO4 || CuSO4 | Cu, К(+) Zn + Сu2+ → Zn2+ + Cu
- 16. ЭДС = – Для элемента Даниэля-Якоби: ЭДС = – = 0,34 + 0,76 = 1,1 В
- 17. Формула Нернста ϕо – стандартный электродный потенциал (В); n – число отданных или принятых электронов; –
- 18. Пример: Цинковая пластинка погружена в 0,01 м раствор её соли.
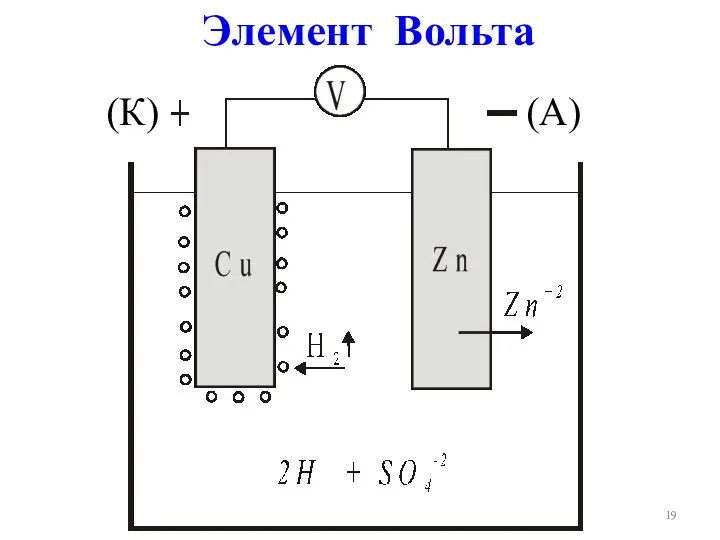
- 19. Элемент Вольта (К) (А)
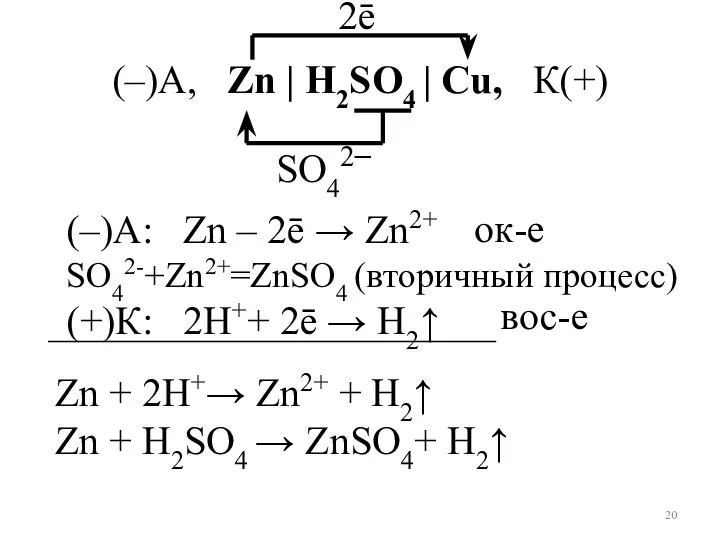
- 20. (–)А: Zn – 2ē → Zn2+ SO42-+Zn2+=ZnSO4 (вторичный процесс) (+)К: 2Н++ 2ē → Н2↑ Zn +
- 21. ЭДС = – = 0,34 + 0,76 = 1,1 В =
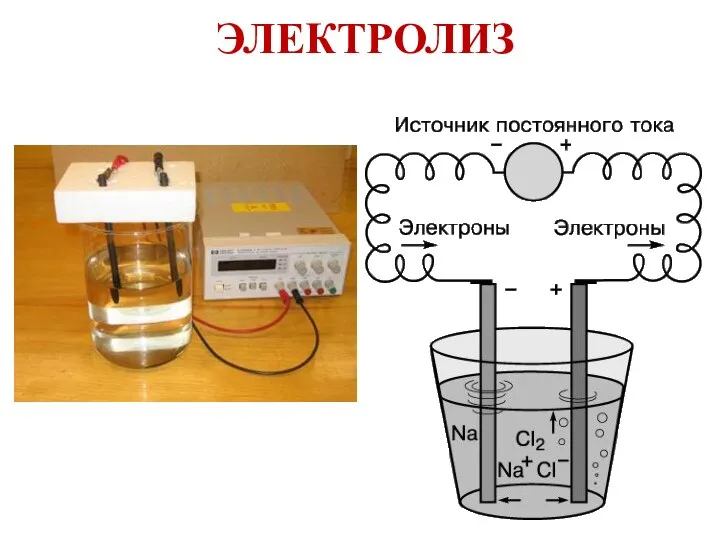
- 22. ЭЛЕКТРОЛИЗ
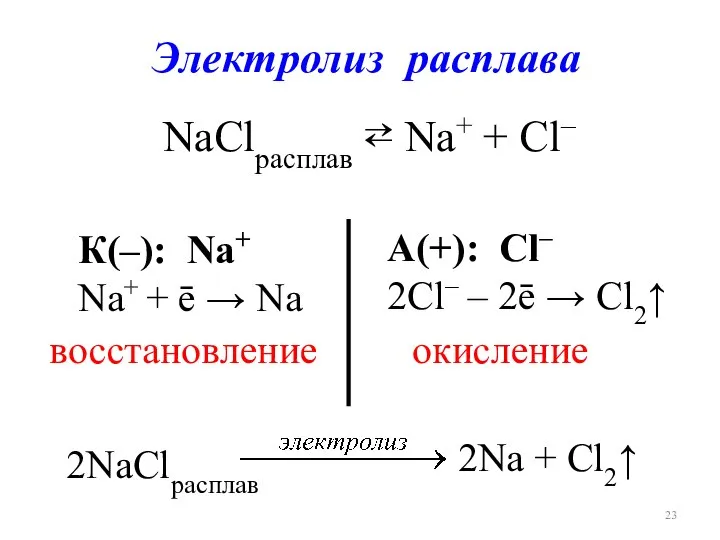
- 23. Электролиз расплава NaClрасплав ⇄ Na+ + Cl– К(–): Na+ Na+ + ē → Na А(+): Cl–
- 24. Na2SO4 расплав ⇄ 2Na+ + SO4–2 К (–): Na+ Na++ ē→Na А (+): SO4–2 SO4–2– 2ē
- 25. Электролиз водных растворов
- 26. Последовательность разрядки ионов и молекул на электродах 1) На катоде: в первую очередь разряжается (восстанавливается) ион
- 28. 2) На аноде: окисляются более сильные восстановители – вещества, имеющие меньшее значение потенциала. SO42– OH– (H2O)
- 30. Электролиз водного раствора йодида калия с инертными электродами KI ⇄ K+ + I– К(–): K+; H+(H2O)
- 31. Электролиз водного раствора иодида калия с инертными электродами KI ⇄ K+ + I– Суммарный процесс (сокращенный
- 32. Na2SO4 ⇄ 2Na+ + SO42– К(–): Na+, H+(H2O) –3 А(+): SO42–, OH–(H2O) +2.05 > +1.4 ϕо
- 33. Na2SO4 ⇄ 2Na+ + SO42– Электролиз водного раствора Na2SO4 с инертными электродами H2O ⇄ H+ +
- 34. NiSO4 ⇄ Ni2+ + SO42– К(–): Ni2+, H+(H2O) –0,25 > -0,41 А(+): SO42–, OH–(H2O) +2.05 >
- 35. NiSO4 ⇄ Ni2+ + SO42– К(–): Ni2+, H+(H2O) –0,25 А(+): SO42–, OH–, Ni0 +2.05>+1.4>–0,25 ϕо 2H2O
- 36. Законы электролиза I закон Фарадея m = kQ m – количество вещества, г; k – электрохимический
- 37. Q = Iτ I – сила тока, А; τ – время, с. m = kIτ
- 38. Мэ – молярная масса эквивалента металла, г/моль; I – сила тока, А; F – число Фарадея
- 39. для газов: VЭ(O2) = 5,6 л/моль VЭ(H2,Cl2) = 11,2 л/моль
- 40. II закон Фарадея m1 : m2 : … : mn = ЭМ1 : ЭМ2 : …
- 41. Пример: ZnCl2 ⇄ Zn2++ 2Cl– К (–): Zn2+, H2O –0.76 А (+): Cl–, H2O 1.36 >
- 42. mZn = ⇒
- 44. Скачать презентацию


![Электродный потенциал (Е, ϕ, [В]) Если концентрация ионов равна 1 моль/л](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/746537/slide-5.jpg)




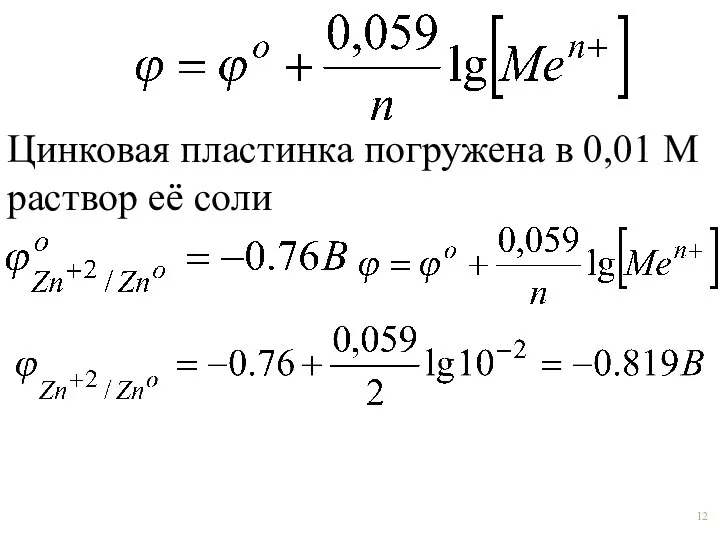





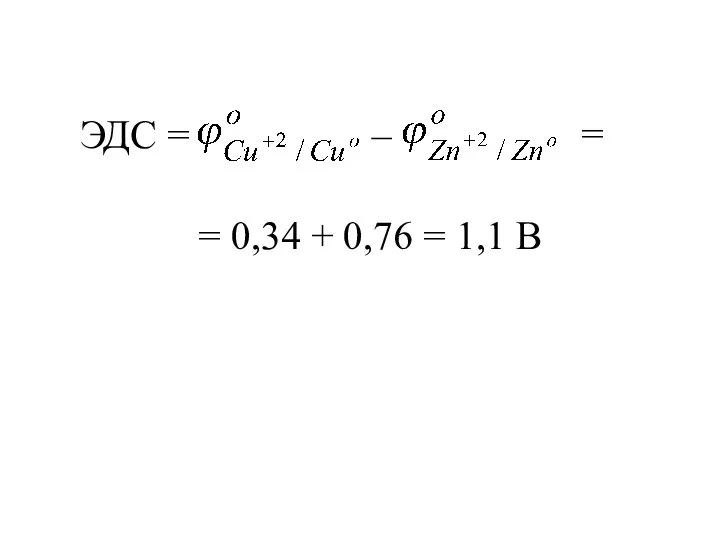















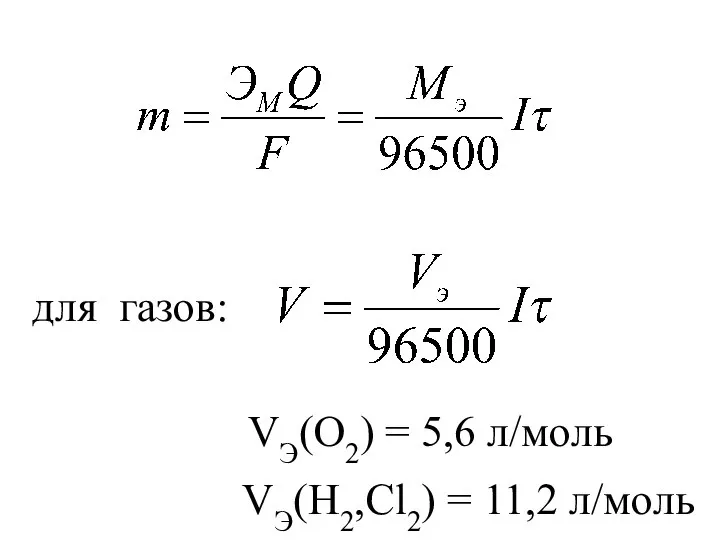



 Масла и функциональные жидкости
Масла и функциональные жидкости Структура и функции биомакромолекул. Лекция 1
Структура и функции биомакромолекул. Лекция 1 Контроль качества эфирных масел
Контроль качества эфирных масел Фармацевтические эмульсии
Фармацевтические эмульсии Протолитические равновесия в растворах электролитов
Протолитические равновесия в растворах электролитов Нечаев 18
Нечаев 18 Окислительно-восстановитительные реакции Выполнили ученики 9 А класса МОУ-СОШ №4 Никитин Андрей Афонин Николай
Окислительно-восстановитительные реакции Выполнили ученики 9 А класса МОУ-СОШ №4 Никитин Андрей Афонин Николай Презентация по Химии "Оксиды и их свойства (8 класс)" - скачать смотреть бесплатно
Презентация по Химии "Оксиды и их свойства (8 класс)" - скачать смотреть бесплатно Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Ցեմենտի արտադրություն
Ցեմենտի արտադրություն Энзимология. Структура и механизм действия ферментов. (Лекция 2)
Энзимология. Структура и механизм действия ферментов. (Лекция 2) Химические свойства неорганических веществ (повторение)
Химические свойства неорганических веществ (повторение) Электрофильные реакции
Электрофильные реакции Смазывающие вещества
Смазывающие вещества Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Применение ацетилена
Применение ацетилена Физико-химический процесс элелктролиз. (11 класс)
Физико-химический процесс элелктролиз. (11 класс) Вода
Вода Органічні сполуки в побуті Виконала Учениця 11-Б класу Панчоха Вероніка
Органічні сполуки в побуті Виконала Учениця 11-Б класу Панчоха Вероніка  Химические волокна (7 класс)
Химические волокна (7 класс) Элементы VI группы главной подгруппы Халькогены
Элементы VI группы главной подгруппы Халькогены Безазотистые вторичные метаболиты минорных групп в фармации. Биохимия, функциональное значение в царстве растений
Безазотистые вторичные метаболиты минорных групп в фармации. Биохимия, функциональное значение в царстве растений Семинар на тему Природные источники углеводородов и их переработка
Семинар на тему Природные источники углеводородов и их переработка Общие химические свойства металлов
Общие химические свойства металлов Презентация по Химии "Силикатная промышленность" - скачать смотреть
Презентация по Химии "Силикатная промышленность" - скачать смотреть  Закон сохранения массы веществ Омельянчук Т.Е. учитель химии МАОУ ДСОШ №2 г. Домодедово
Закон сохранения массы веществ Омельянчук Т.Е. учитель химии МАОУ ДСОШ №2 г. Домодедово Аттестационная работа. Программа элективного курса Исследовательская проектная деятельность при изучении химии
Аттестационная работа. Программа элективного курса Исследовательская проектная деятельность при изучении химии Коррозия материалов
Коррозия материалов