Содержание
- 2. С органическими соединениями человек знаком с глубокой древности. Растительный и животный мир состоит из соединений, которые
- 3. Наиболее часто встречающиеся в органических соединениях элементы Периодической системы Д.И. Менделеева
- 4. Дми́трий Ива́нович Менделе́ев (1834 - 1907)- великий русский учёный: химик, физикохимик, физик, метролог, экономист, технолог, геолог,
- 5. Органическая химия как наука в историческом плане сформировалась к началу XIX века. Понятие «органическая химия» ввел
- 6. Йёнс Якоб Берце́лиус (1779-1848) — химик и минералог. Член Шведской академии наук, с 1810 года —
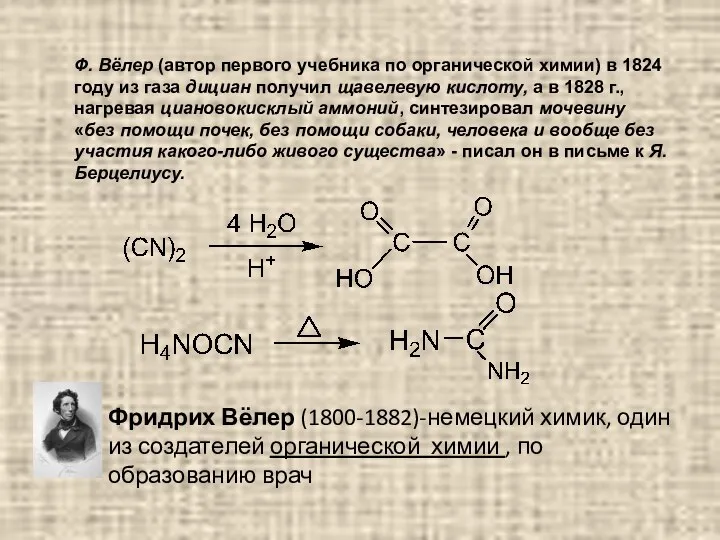
- 7. Ф. Вёлер (автор первого учебника по органической химии) в 1824 году из газа дициан получил щавелевую
- 8. Атомно-молекулярная теория: Все вещества состоят из молекул – наименьших частиц вещества, обладающих их свойствами. Молекулы состоят
- 9. Химия - язык природы. Химия имеет свой алфавит – Периодическую систему химических элементов. Элементы являются разновидностями
- 10. Алекса́ндр Миха́йлович Бу́тлеров (1828-1886) - русский химик, создатель теории химического строения органических веществ, родоначальник «бутлеровской школы
- 11. В начале XX столетия Г.Н. Льюис развил теорию ковалентной связи и предложил правило «октета», согласно которому
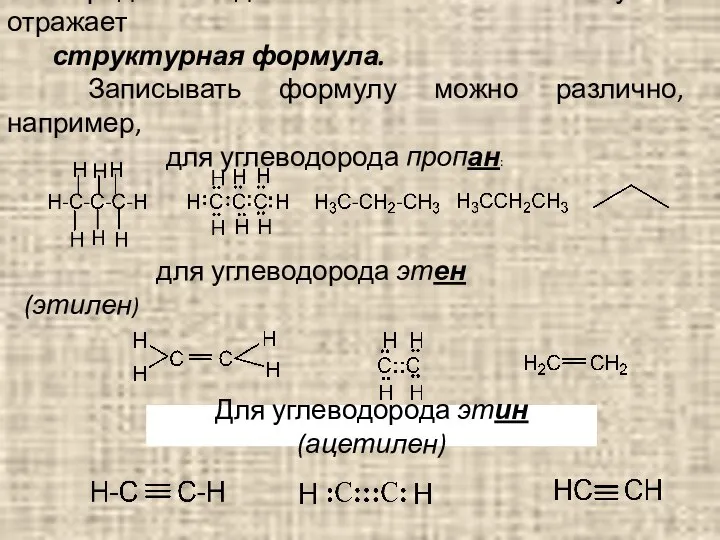
- 12. Порядок соединения атомов в молекулах отражает структурная формула. Записывать формулу можно различно, например, для углеводорода пропан:
- 13. Ла́йнус Карл По́линг (1901-1994) —американский химик, кристаллограф – лауреат двух Нобелевских премий: по химии (1954) и
- 14. Перекрывание гибридных АО атомов углерода в молекулах углеводородов приводит к образованию σ-связей С–С. В молекуле метана
- 15. Якоб Хендрик Вант-Гофф (1852 - 1911) — Голландский химик, один из основателей стереохимии и химической кинетики,
- 16. В настоящее время насчитывается свыше 60.000.000 органических соединений. Их многообразие определяется: возможностью углерода объединяться в цепочки
- 17. Классификация органических соединений Ациклические углеводороды (А означает «нет» цикла) Алканы СnH2n+2 или СnH2n+1H ↔ R-H Предельные
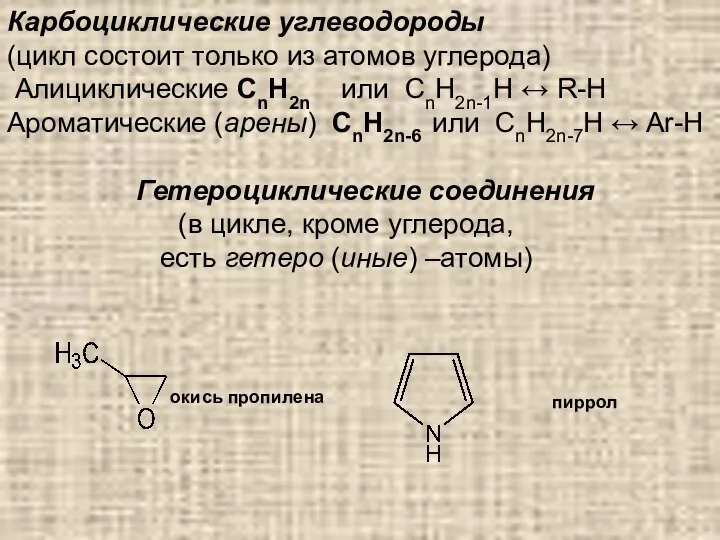
- 18. Карбоциклические углеводороды (цикл состоит только из атомов углерода) Алициклические СnH2n или СnH2n-1H ↔ R-H Ароматические (арены)
- 19. Производные углеводородов (при действии водорода в присутствии катализатора превращаются в углеводороды) 1. галогенопроизводные R-X (Х=F, Cl,
- 20. 7. Производные кислот (при действии подкисленной воды превращаются в кислоты) 7.1. Соли R-C(O)OМ (М – металлы
- 21. Подавляющее большинство органических реакций протекает с первоначальным образованием активной частички за счёт распада ковалентной связи. Ковалентная
- 22. А : Б А∙ + ∙Б – гомолитический распад ковалентной связи (частички похожи по строению –
- 23. А : Б А+ + :Б– – гетеролитический распад образуются различные частички – одна – заряд
- 24. Устойчивость промежуточных частиц Химическая реакция протекает таким образом, чтобы конечный продукт, либо промежуточная частица, образующаяся в
- 25. Устойчивость карбокатионов (карбо – от «карбоникум» – углерод): карбокатион плоский - углерод в состоянии sp2– гибридизации.
- 26. Устойчивость карбанионов: Карбанион имеет форму тетраэдра. Устойчивость карбанионов обратна устойчивости карбокатионов. метил этил изопропил трет.-бутил
- 27. Некоторые понятия Среди химиков, работающих в области органической химии, распространена практика использования сокращений вместо структурных формул
- 28. Классификация реакций по направлению Реакции замещения – образование новых ковалентных связей при замещении атома (или группы
- 29. Классификация реакций по направлению Реакции изомеризации (перегруппировки) – происходит структурная перегруппировка атомов в молекуле. Реакции распада
- 30. Индукционный эффект - смещение электронов по системе σ-связей, обусловлено различной электроотрицательностью атомов (электроотрицательность - склонность к
- 31. Некоторые термины Гидрирование – присоединение водорода. Дегидрирование – отщепление водорода. Гидратация – присоединение воды. Дегидратация –
- 32. Гомологи – соединения, сходные по строению и химическим свойствам, имеют одну и ту же функциональную группу;
- 33. Как составлять структурные формулы: – вначале записать углеродный скелет (наиболее длинную цепочку заданного углеводорода); например, 2,2-диметил-4-этил-5-хлор-гептана:
- 34. Гомологический ряд алканов и образуемых ими радикалов.
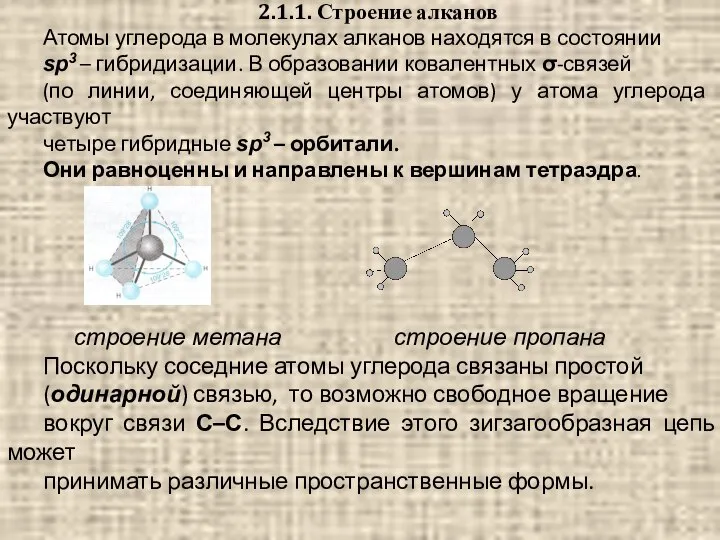
- 35. 2.1.1. Строение алканов Атомы углерода в молекулах алканов находятся в состоянии sp3 – гибридизации. В образовании
- 36. 2.1.2. Природные источники углеводородов Природный газ – на 98% состоит из метана. Метан СН4 – газ
- 37. Уголь состоит из углерода и примесей. При нагревании угля без доступа воздуха происходит его термическое разложение
- 38. Некоторые продукты переработки нефти Бензин – смесь углеводородов различного строения С5-С12, жидкость. Получают перегонкой (дистилляцией) нефти
- 39. Некоторые продукты переработки нефти Керосин – смесь углеводородов С9-С16, жидкость, т. кип. 200-300 0С. Содержит: 23-60%
- 40. Некоторые продукты переработки нефти Реактивное топливо – смесь алканов (20-60%), циклопарафинов (20-60%), аренов (18,5-20%), алкенов (0,3-1%);
- 41. 2.1.3. Получение алканов в лаборатории гидрирование алкенов (р –давление, t - температура): реакция Вюрца: 2.1.4. Химические
- 42. Топливо Одно из основных направлений использования углеводородов – топливо. Эталоном качества моторного топлива выбран изооктан –
- 43. 2.2. АЛКЕНЫ CnH2n Этот раздел будет подробно рассматриваться в Модуле 3 Алкены – это углеводороды, в
- 44. 2.2.1. Строение алкенов Атомы углерода, связанные двойной связью, находятся в состоянии sp2 – гибридизации. Три sp2
- 45. 2.2.2. Типы изомерии алкенов Изомерия углеродного скелета для соединений, содержащих 4 и более атомов углерода. 2-пентен
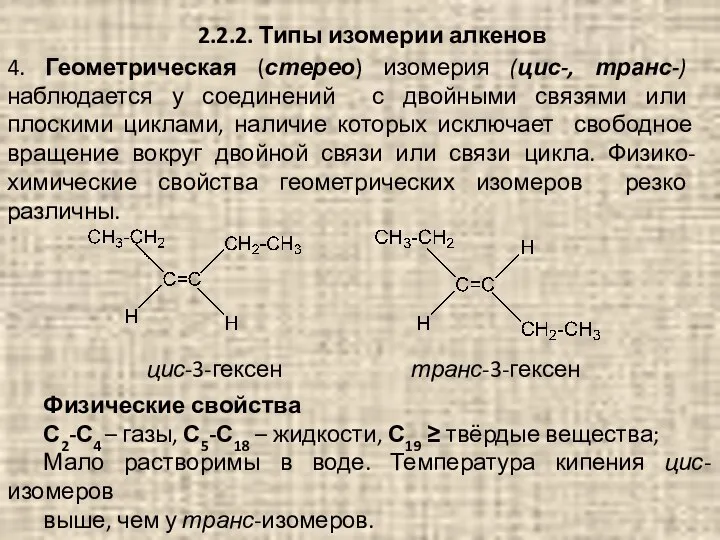
- 46. 2.2.2. Типы изомерии алкенов 4. Геометрическая (стерео) изомерия (цис-, транс-) наблюдается у соединений с двойными связями
- 47. 2.2.4. Получение алкенов Крекинг нефтепродуктов (высокая температура): С16Н34 → С8Н18 алкан + С8Н16 алкен Дегидрирование алканов
- 48. 2.2.5. Химические свойства алкенов 1) Электрофильное присоединение (АdЕ к С sp2). В случае несимметричных алкенов электрофильное
- 49. 2. Радикальное присоединение к алкенам (только в случае HBr) протекает против правила Марковникова (образующийся промежуточный радикал
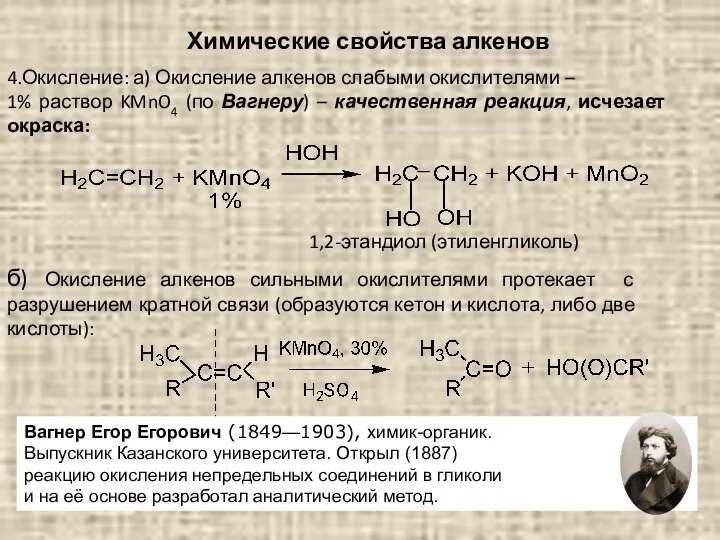
- 50. Химические свойства алкенов 4.Окисление: а) Окисление алкенов слабыми окислителями – 1% раствор KMnO4 (по Вагнеру) –
- 51. Полимеризация алкенов (подробно будет рассмотрена в модуле 3) Полимеризация – получение высокомолекулярного соединения (ВМС) (полимера) из
- 52. 2.3. АЛКИНЫ CnH2n-2 При названии по IUPAС тройная связь - окончание ин. НС≡СН этин (ацетилен); СН3С≡СН
- 53. Методы получения ацетилена Получение в промышленности: Из карбида кальция (высокая температура): CaCO3 → CaO + CO2;
- 54. Химические свойства ацетилена 1.Реакции по подвижному водороду (С-Н кислотность) 2НС≡СН + 2Na → NaС≡СNa + 2H2
- 55. а) гидратация (реакция М.Г. Кучерова) – первоначально образующийся этенол (виниловый спирт) неустойчив и перегруппировывается в этаналь
- 56. в) присоединение кислот (в присутствии солей, например, в случае уксусной – катализ натриевой солью уксусной кислоты
- 57. Нобелевская премия по химии за 2000 г. присуждена американским исследователям Алану Хигеру и Алану Мак-Диармиду и
- 58. 2.4. АЛКАДИЕНЫ CnH2n-2 Изомеры ацетиленовых углеводородов. Они классифицируются по взаимному расположению двойных связей. Кумулированные двойные связи
- 59. Сопряжённые диены: бутадиен, изопрен – мономеры для производства синтетического каучука (СК) Методы получения бутадиена и изопрена:
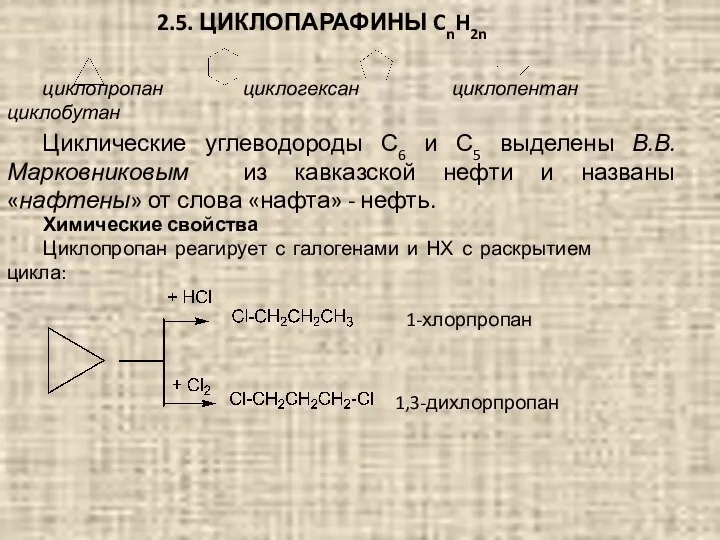
- 60. 2.5. ЦИКЛОПАРАФИНЫ CnH2n циклопропан циклогексан циклопентан циклобутан Циклические углеводороды С6 и С5 выделены В.В. Марковниковым из
- 61. Химические свойства циклопарафинов Циклобутан частично реагирует с галогенами раскрытием цикла, частично – по типу реакции замещения.
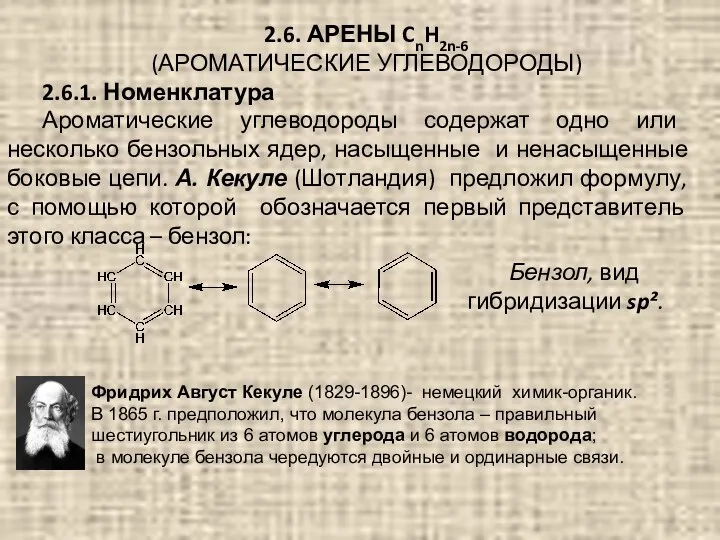
- 62. 2.6. АРЕНЫ CnH2n-6 (АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ) 2.6.1. Номенклатура Ароматические углеводороды содержат одно или несколько бензольных ядер, насыщенные
- 63. Гомологи бензола
- 64. Радикалы аренов – арилы (Ar): C6H5 – (Ph-) – фенил, С6Н2СН2- (Bz-) - бензил Примите к
- 65. Методы получения бензола и его гомологов дегидрирование циклоалканов (нагревание над соответствующим катализатором): Алкилирование по реакции Фриделя
- 66. Методы получения бензола и его гомологов Алкилированием по реакции Вюрца – Фиттига получают алкилбензолы с нормальной
- 67. 2.6.3. Химические свойства аренов Реакции присоединения На свету к бензолу присоединяются 3 моля хлора и образуется
- 68. Химические свойства аренов Реакции окисления Бензол устойчив к окислению. Все гомологи бензола, не зависимо от величины
- 69. Электрофильное замещение в ароматическом кольце Алкилирование б) алкенами (протон из катализатора присоединяется к алкену по правилу
- 70. Реакции галогенирования и нитрования толуола: фенилхлорметан фенилдихлорметан фенилтрихлорметан Нитрование толуола проводят нитрующей смесью (смесью конц. азотной
- 71. Глава 3. ПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ 3.1. Галогенопроизводные углеводородов R – X, где Х = F, Cl, Br,
- 72. Методы получения галогенопроизводных углеводородов Радикальное галогенирование алканов протекает в первую очередь по третичному атому углерода: 2-бром-2-метилбутан
- 73. Химические свойства галогенопроизводных Галогенопроизводные предельных углеводородов вступают в реакции нуклеофильного замещения (атом галогена замещается на отрицательно
- 74. Галогенопроизводные непредельных углеводородов Галоген, находящийся у атома углерода кратной связи (например, в винилхлориде), мало подвижен и
- 75. 3.2. Гидроксильные производные углеводородов 3.2.1. R-OH (спирты) Классификация спиртов По радикалу: предельные, непредельные, циклические, ароматические спирты.
- 76. Свойства спиртов Многоатомные спирты - номенклатура Двухатомные спирты (гликоли): НО-СН2-СН2-ОН 1,2-этандиол (этиленгликоль). НО-СН2-СН(ОН)-СН3 1,2-пропандиол (пропиленгликоль). НО-СН2-СН2-СН2-ОН
- 77. Методы получения спиртов Промышленные способы: а) ферментативный гидролиз крахмала с последующим брожением образующейся глюкозы под действием
- 78. Лабораторные методы получения спиртов: а) гидролиз галогенопроизводных углеводородов: R-CH2-X + HOH (NaOH) → R-CH2-OH + NaX
- 79. Химические свойства спиртов Спирты – слабые кислоты. Если изобразить кислоту Н+А-, то константа кислотности Ка (а-acid
- 80. Взаимодействие спирта с кислотой называют реакцией этерификации: этилацетат Эта реакция обратима (гидролиз образующегося сложного эфира называют
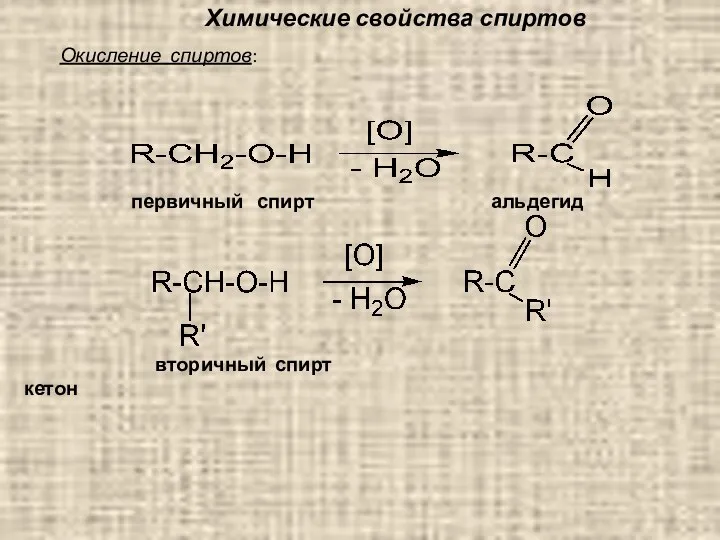
- 81. Химические свойства спиртов Окисление спиртов: вторичный спирт кетон первичный спирт альдегид
- 82. 3.2.2. Фенолы Фенол (карболовая кислота); сильный антисептик (обеззараживающее средство). Ка = 10-10 Ка = 10-18 Фенол
- 83. Методы получения фенолов 1) Из хлорбензола нагреванием со щёлочью. 2)Из ароматических сульфокислот (серную кислоту берут в
- 84. Свойства фенолов Фенол – бесцветное, кристаллическое вещество, с резким запахом, на воздухе окисляется (появляется малиновая окраска).
- 85. Свойства фенолов 2) Электрофильное замещение : Гидроксильная группа – сильный электронодонор и направляет электрофил в орто-
- 86. 3.3. Карбонильные производные углеводородов Функциональная группа >С=О называется карбонильной 3.3.1. Альдегиды Альдегиды классифицируют – по углеводородному
- 87. 3.3.1.1. Методы получения карбонильных соединений 1) Окисление или дегидрирование спиртов – первичные спирты образуют альдегиды, вторичные
- 88. 3.3.1.2. Химические свойства альдегидов Альдегиды легко окисляются, образуя кислоты с тем же числом атомов углерода. На
- 89. 5) Полимеризация формальдегида приводит к параформу, тримеризация формальдегида – к триоксиметилену, ацетальдегида – к паральдегиду :
- 90. 3.3.2. Кетоны Ацетон – бесцветная жидкость со специфическим запахом; смешивается с водой и органическими растворителями; т.
- 91. 3.4. Карбоксильные производные углеводородов Карбоксильные производные – карбоновые кислоты – содержат карбоксильную группу -С(=О)-ОН. По количеству
- 92. Муравьиная (метановая) кислота – подвижная бесцветная жидкость с резким запахом; т. кип. 101 0C. Смешивается с
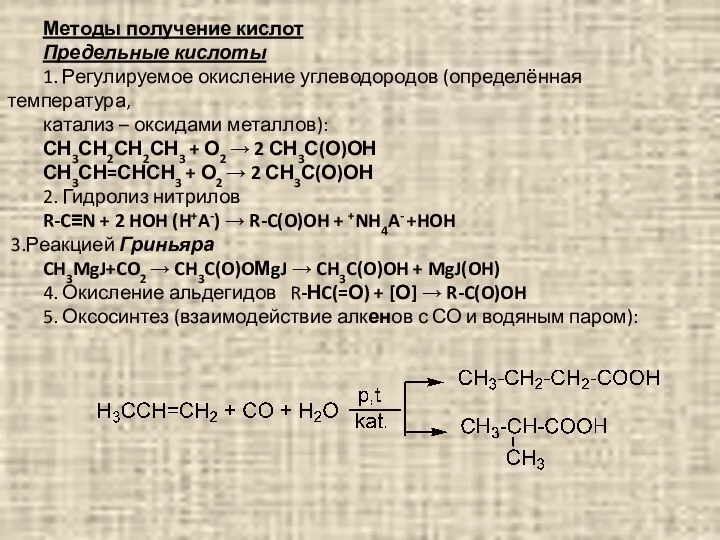
- 93. Методы получение кислот Предельные кислоты 1. Регулируемое окисление углеводородов (определённая температура, катализ – оксидами металлов): СН3СН2СН2СН3
- 94. Получение непредельных кислот: 1) Из алкенов: 2) Из глагогенозамещённых кислот: Получение ароматических кислот: Окисление гомологов бензола
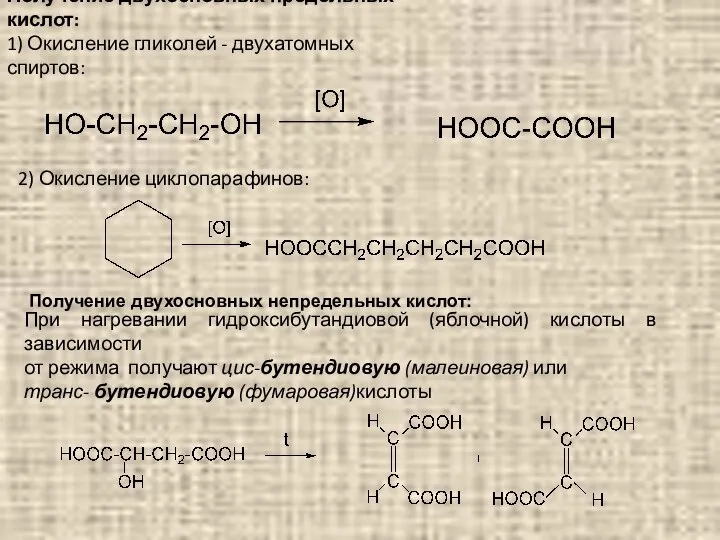
- 95. Получение двухосновных предельных кислот: 1) Окисление гликолей - двухатомных спиртов: 2) Окисление циклопарафинов: Получение двухосновных непредельных
- 96. Оствальд и Аррениус (1890): кислоты - источник протонов (ионов Н+), а основание – источник ионов гидроксила
- 97. Брёнстед и Лоури (1923): кислоты – доноры протонов (отдают протон – положительно заряженный атом водорода), основания
- 98. Льюис (1923): кислоты – акцепторы электронной пары (в их внешней электронной оболочке недостаёт двух электронов), а
- 99. 3.5. Углеводы Соединения общей формулы Cn(H2O)m растительного происхождения. По отношению к гидролизу их подразделяют на: моносахариды
- 100. Моносахариды В природе чаще встречаются гексозы (6 атомов углерода) и пентозы (5 атомов углерода). По функциональной
- 102. Скачать презентацию
























































































 Комплексные соединения. Природа химической связи: метод молекулярных орбиталей
Комплексные соединения. Природа химической связи: метод молекулярных орбиталей Реакции ионного обмена
Реакции ионного обмена Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.
Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.  Лекция 3. Протолитические равновесия и процессы
Лекция 3. Протолитические равновесия и процессы Химия. Введение
Химия. Введение Железо Fe. Строение атома
Железо Fe. Строение атома Халькогены. Кислород в природе
Халькогены. Кислород в природе Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б
Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б Презентация по Химии "Биогенные элементы" - скачать смотреть бесплатно
Презентация по Химии "Биогенные элементы" - скачать смотреть бесплатно Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Э.М. Спиридонов. Эволюция минералов олова в зоне гипергенеза
Э.М. Спиридонов. Эволюция минералов олова в зоне гипергенеза Углерод и 4 группа
Углерод и 4 группа Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) Регуляция и интеграция обмена веществ
Регуляция и интеграция обмена веществ Урок у 8 класі на тему: «Класифікація неорганічних сполук» Учитель хімії Верхівцевського НВК Кукса Наталія Миколаї
Урок у 8 класі на тему: «Класифікація неорганічних сполук» Учитель хімії Верхівцевського НВК Кукса Наталія Миколаї Воздух. Состав воздуха. Реакция горения
Воздух. Состав воздуха. Реакция горения Взаимосвязь неорганических веществ
Взаимосвязь неорганических веществ Волокна підготував учень 11 класу :
Волокна підготував учень 11 класу :  Железо и его соединения
Железо и его соединения Коэффициент концентрации меди
Коэффициент концентрации меди Карбонат натрия
Карбонат натрия Гетерофункционалды органикалық қосылыстар
Гетерофункционалды органикалық қосылыстар Структура и текстура магматических пород
Структура и текстура магматических пород Electron Structure
Electron Structure Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би
Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би Альдегиды. Кетоны
Альдегиды. Кетоны Свойство воды, устранение жесткости воды и очистка воды
Свойство воды, устранение жесткости воды и очистка воды Сурьма, Sb
Сурьма, Sb