Содержание
- 2. УМОВИ УСПІШНОЇ ЗДАЧІ ІСПИТУ З МАТЕРІАЛОЗНАВСТВА ВІДВІДУВАННЯ ЗАНЯТЬ (лекцій та лабораторних) 10 лекцій та 6 занять
- 3. 1.Молекулярна будова, типи зв'язків у твердих тілах. 2. Агрегатний стан речовин, вплив на властивості. Будова твердих
- 4. 3.Поняття про кристалічні та аморфні тіла. 4.Градація структури твердих тіл. Дефекти структури, методи їх дослідження. Будова
- 5. ЛІТЕРАТУРА НМП для самостійного вивчення дисципліни «МОТВ ТНС» за КМСОНП для студентів за напрямом 6.050310 “Товарознавство
- 6. 1. Молекулярна будова, типи зв'язків у твердих тілах.
- 7. Знання складу та будови вихідної сировини необхідне для: засвоєння закономірностей формування структури матеріалів розуміння закономірностей формування
- 8. Знання складу та будови вихідної сировини необхідне для: особливостей зміни властивостей під впливом різних факторів під
- 9. Знання складу та будови вихідної сировини необхідне для: вибору найбільш раціональної конструкції виробу визначення оптимального режиму
- 10. ВЛАСТИВОСТІ МАТЕРІАЛІВ ОБУМОВЛЕНІ: Природою атомів Характером з'єднання атомів між собою Типом і ступінню досконалості структури
- 11. РОЗРІЗНЯЮТЬ: БУДОВУ МАТЕРІАЛІВ СТРУКТУРУ МАТЕРІАЛІВ
- 12. БУДОВА (хімічна) - характер зв'язку та послідовність з'єднання атомів у молекулі, як первинної структурної одиниці речовини
- 13. СТРУКТУРА - просторове розміщення структурних одиниць (молекул), характер їх об'єднання у більш великі структурні елементи
- 14. Хімічний зв'язок між атомами в молекулах обумовлений Взаємодією електричних зарядів електронів Взаємодією атомних ядер Перерозподі лом
- 15. Які типи зв'язків атомів в молекулах Вам відомі: ковалентний електровалентний (іонний) координаційний (донорно-акцепторний) металічний
- 16. ІНДИВІДУАЛЬНЕ ЗАВДАННЯ №1 ДАТИ ХАРАКТЕРИСТИКУ ОСНОВНИХ ВИДІВ ЗВ'ЯЗКІВ У ТВЕРДИХ ТІЛАХ ЗА СХЕМОЮ: в яких молекулах
- 17. Тип міжатомного зв'язку залежить від Розміру молекул Форми молекул
- 18. Геометрична конфігурація молекули визначається лінійне; у вигляді зиґзаґу тощо. Довжиною зв'язку між атомами Довжиною зв'язку між
- 19. ВПЛИВ ТИПУ ЗВ'ЯЗКУ НА БУДОВУ ТА ВЛАСТИВОСТІ МАТЕРІАЛІВ ТА ВИРОБІВ КЛАСИЧНИЙ ПРИКЛАД - ДВІ КРИСТАЛІЧНІ ФОРМИ
- 21. АЛМАЗ БЕЗКОЛЬОРОВИЙ ПРОЗОРИЙ НЕ ПРОВОДИТЬ ЕЛЕКТРИЧНИЙ СТРУМ МАЄ ЗНАЧНУ ТВЕРДІСТЬ ГУСТИНА 3,5 Г/СМ
- 22. БАЛАСИ – АЛМАЗИ ІЗ ВКРАПЛЕННЯМИ, НАПІВПРОЗОРІ ТА НЕПРОЗОРІ
- 23. АЛМАЗ КОВАЛЕНТНА КРИСТАЛІЧНА ГРАТКА З ОДНАКОВОЮ МІЖАТОМНОЮ ВІДСТАННЮ 1,5 А° У НАПРЯМКУ ВСІХ ЧОТИРЬОХ ЗВ'ЯЗКІВ
- 24. http://ru.wikipedia.org/wiki/Файл:Diamant_tropfen.jpg ОБРОБЛЕНИЙ АЛМАЗ
- 25. http://ru.wikipedia.org/wiki/Файл:SyntheticDiamonds.jpg ЗОБРАЖЕННЯ СИНТЕТИЧНИХ АЛМАЗІВ, ОТРИМАНЕ НА РАСТРОВОМУ ЕЛЕКТРОННОМУ МІКРОСКОПІ
- 26. ГРАФІТ характерна "мастильна" властивість жирний на дотик сіро-чорного кольору з металічним блиском з густиною 2,2 -
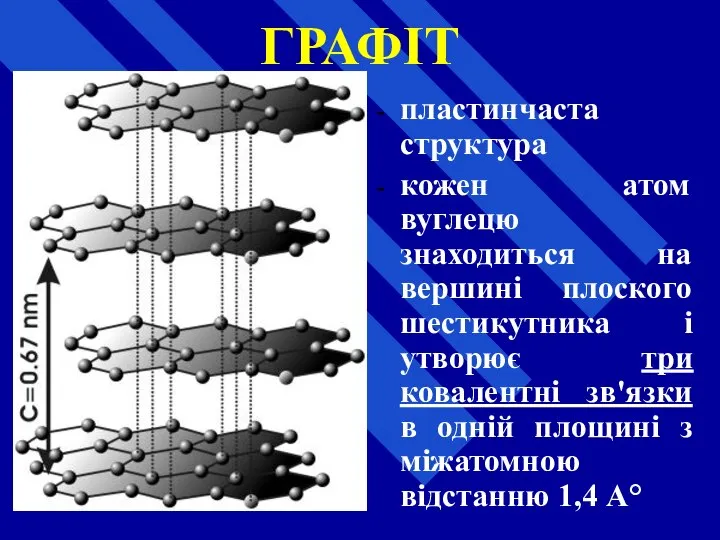
- 27. ГРАФІТ пластинчаста структура кожен атом вуглецю знаходиться на вершині плоского шестикутника і утворює три ковалентні зв'язки
- 28. ГРАФІТ четвертий валентний електрон атома вуглецю локалізований та рухливий площині шестикутника, утворюючи зв'язок типу металічного, що
- 29. ГРАФІТ паралельні площини із шестикутників знаходиться на відстані 3,35 А° один від одного і пов'язані слабкими
- 30. http://ru.wikipedia.org/wiki/Файл:Diamond_animation.gif СХЕМАТИЧНЕ ЗОБРАЖЕННЯ КРИСТАЛІЧНОЇ ГРАТКИ АЛМАЗУ
- 31. http://en.wikipedia.org/wiki/File:Graphite_stereo_animation.gif СХЕМАТИЧНЕ ЗОБРАЖЕННЯ КРИСТАЛІЧНОЇ ГРАТКИ ГРАФІТУ
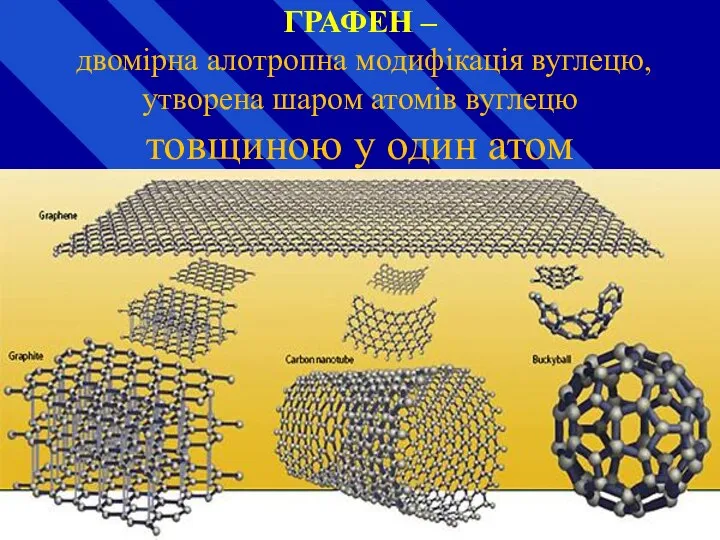
- 32. ГРАФЕН – двомірна алотропна модифікація вуглецю, утворена шаром атомів вуглецю товщиною у один атом
- 33. ЗАГАЛЬНИЙ ВИГЛЯД БАКІБОЛА C60, ЩО ОБЕРТАЄТЬСЯ молекула із 60 атомів вуглецю, що утворюють замкнену сфричну поверхню,
- 34. http://commons.wikimedia.org/wiki/File:Kohlenstoffnanoroehre_Animation.gif ВУГЛЕЦЕВА НАНОТРУБКА
- 35. 2.Агрегатний стан речовин, його вплив на властивості.
- 36. Агрегатний стан речовин Стани однієї і тієї речовини, перехід між якими супроводжується стрибкоподібною зміною цілого ряду
- 37. Агрегатний стан речовин Визначається силами взаємодії між молекулами (вандерваальсовими), які: мають електростатичну природу ( так як
- 38. ВАНДЕРВААЛЬСОВІ СИЛИ: ЕЛЕКТРО СТАТИЧНІ ДИСПЕРСІЙНІ ІНДУКЦІЙНІ
- 39. ЕЛЕКТРОСТАТИЧНІ виникають між протилежними зарядами полярних молекул.
- 40. ІНДУКЦІЙНІ проявляються під час утворення диполя, наведеного іншою полярною молекулою,яка має постійний дипольний момент.
- 41. ДИ́ПОЛЬ СУКУПНІСТЬ ДВОХ РІВНИХ ЗА АБСОЛЮТНОЮ ВЕЛИЧИНОЮ РІЗНОЙМЕННИХ ЗАРЯДІВ, ЯКІ ЗНАХОДЯТЬСЯ НА ПЕВНІЙ ВІДСТАНІ ОДИН ВІД
- 42. ДИСПЕРСІЙНІ виникають незалежно від полярності молекул, внаслідок поляризації сусідніх частинок в результаті узгодження руху їх електронів.
- 43. РЕЧОВИНИ У ПРИРОДІ газоподібному рідкому твердому у вигляді плазми
- 44. ВЛАСТИВОСТІ ГАЗОПОДІБНОГО СТАНУ частинки речовини практично не пов'язані одна із одною, знаходяться на відстані, яка значно
- 45. ВЛАСТИВОСТІ РІДИНИ: немає власної форми, але є власний об'єм виникає слабо фіксована структура речовини, бо сили
- 46. ВЛАСТИВОСТІ РІДИНИ: в рідинах існує ближній порядок, тобто упорядкованість спостерігається у розташуванні сусідніх молекул, які розміщуються
- 47. ВЛАСТИВОСТІ РІДИНИ: рідина стискається мало; щільність близька до щільності твердих тіл; при коливаннях температури змінюється сильніше
- 48. ВЛАСТИВОСТІ ТВЕРДОГО СТАНУ спостерігається формування значної упорядкованості структури , обумовленої тим, що сили притягання значно перевищують
- 49. ВЛАСТИВОСТІ ТВЕРДОГО СТАНУ частинки не можуть переміщуватися, вони лише коливаються з обмеженою амплітудою і можуть обертатися
- 50. ВЛАСТИВОСТІ ТВЕРДОГО СТАНУ спостерігається досить стійка рівновага, яка вище у низькомолекулярних речовин і нище у високомолекулярних;
- 51. ПЛАЗМА утворюється з іонізованих атомів і електронів, при яких загальний заряд дорівнює нулю. СКЛАДАЄТЬСЯ З: ЕЛЕКТРОНІВ
- 52. Плазма: ХОЛОДНА ТА ГАРЯЧА ІДЕАЛЬНА ТА НЕІДЕАЛЬНА НИЗЬКОТЕМПЕРАТУРНА ТА ВИСОКОТЕМПЕРАТУРНА РІВНОВАЖНА ТА НЕ РІВНОВАЖНА
- 54. 3.Поняття про кристалічні та аморфні тверді тіла.
- 55. АМОРФНИЙ СТАН у термодинамічному відношенні не є стійким; у звичайних умовах відбувається довільний перехід твердої речовини
- 56. КРИСТАЛІЧНИЙ СТАН найбільш стійкий у термодинамічному відношенні. перехід із аморфного стану у кристалічний завжди супроводжується підвищенням
- 57. ПОНЯТТЯ ПРО КРИСТАЛІЧНІ АМОРФНІ ТВЕРДІ ТІЛА. ВЛАСТИВОСТІ: АМОРФНІ - геометрично вірна форма - анізотропія індивідуальних кристалів
- 58. 4.Градація структури твердих тіл.
- 59. ГРАДАЦІЯ СТРУКТУРИ макроструктура мікроструктура тонка (внутрішня) структура пориста
- 60. МАКРОСТРУКТУРА - це сполучення відносно великих структурних елементів (ниток, шарів, пучків) матеріалу видимих неозброєним оком або
- 61. МІКРОСТРУКТУРА - сполучення структурних елементів видимих за допомогою оптичного мікроскопу (із збільшенням у 10 та 100
- 62. ТОНКА ВНУТРІШНЯ СТРУКТУРА - це сполучення атомів, іонів та молекул,або більш великих утворень, які вивчаються під
- 63. МЕТОДИ ВИВЧЕННЯ ТОНКОЇ СТРУКТУРИ рентгено структурний електронної мікроскопії електроно графії нейтроно графії рентгенівського просвічування ртутної порометрії
- 64. ДЕФЕКТИ СТРУКТУРИ порушення чіткого просторового упорядкування (періодичності) кристалічної ґратки, властивої ідеальному кристалу. Ці порушення притаманні всім
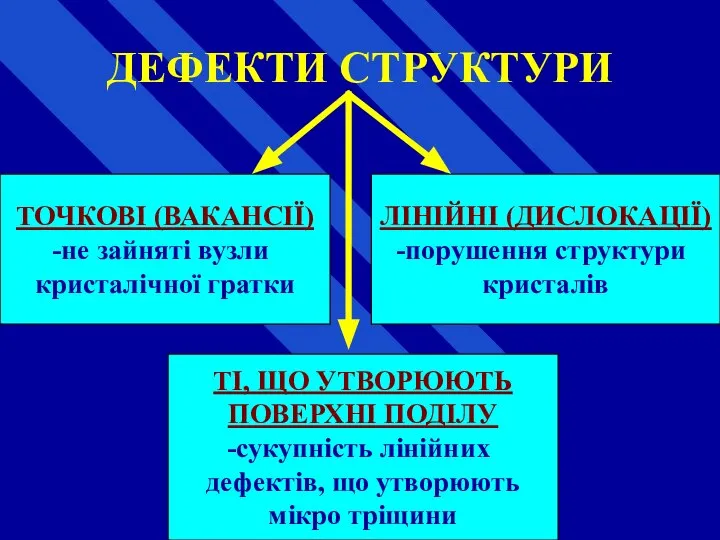
- 65. ДЕФЕКТИ СТРУКТУРИ ТОЧКОВІ (ВАКАНСІЇ) не зайняті вузли кристалічної гратки ЛІНІЙНІ (ДИСЛОКАЦІЇ) порушення структури кристалів ТІ, ЩО
- 66. МЕТОДИ ДЕФЕКТОСКОПІЇ капілярний люмінісце нтний магнітний рентге нівський гама- променевий ультра- звуковий радіаційний тіньовий резонансний
- 68. Скачать презентацию




























































 Комплексные соединения. Природа химической связи: метод молекулярных орбиталей
Комплексные соединения. Природа химической связи: метод молекулярных орбиталей Реакции ионного обмена
Реакции ионного обмена Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.
Сабақтың тақырыбы: Сутек. Сутектің табиғатта таралуы және алынуы.  Лекция 3. Протолитические равновесия и процессы
Лекция 3. Протолитические равновесия и процессы Химия. Введение
Химия. Введение Железо Fe. Строение атома
Железо Fe. Строение атома Халькогены. Кислород в природе
Халькогены. Кислород в природе Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б
Презентация по Химии "РАЗРАБОТКИ УЛЬТРАДИСПЕРСНЫХ (НАНО-) МАТЕРИАЛОВ И НАНОТЕХНОЛОГИЙ В АТОМНОЙ ОТРАСЛИ" - скачать смотреть б Презентация по Химии "Биогенные элементы" - скачать смотреть бесплатно
Презентация по Химии "Биогенные элементы" - скачать смотреть бесплатно Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Э.М. Спиридонов. Эволюция минералов олова в зоне гипергенеза
Э.М. Спиридонов. Эволюция минералов олова в зоне гипергенеза Углерод и 4 группа
Углерод и 4 группа Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) Регуляция и интеграция обмена веществ
Регуляция и интеграция обмена веществ Урок у 8 класі на тему: «Класифікація неорганічних сполук» Учитель хімії Верхівцевського НВК Кукса Наталія Миколаї
Урок у 8 класі на тему: «Класифікація неорганічних сполук» Учитель хімії Верхівцевського НВК Кукса Наталія Миколаї Воздух. Состав воздуха. Реакция горения
Воздух. Состав воздуха. Реакция горения Взаимосвязь неорганических веществ
Взаимосвязь неорганических веществ Волокна підготував учень 11 класу :
Волокна підготував учень 11 класу :  Железо и его соединения
Железо и его соединения Коэффициент концентрации меди
Коэффициент концентрации меди Карбонат натрия
Карбонат натрия Гетерофункционалды органикалық қосылыстар
Гетерофункционалды органикалық қосылыстар Структура и текстура магматических пород
Структура и текстура магматических пород Electron Structure
Electron Structure Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би
Биосинтез белков в живой клетке Продолжить формирование знаний об основных процессах метаболизма; охарактеризовать два этапа би Альдегиды. Кетоны
Альдегиды. Кетоны Свойство воды, устранение жесткости воды и очистка воды
Свойство воды, устранение жесткости воды и очистка воды Сурьма, Sb
Сурьма, Sb